文档内容
专题 01 STSE 物质的组成、性质和分类
1.下列文献记载内容涉及氧化还原反应的是
A.《旧唐书•严震传》:“梁汉之间,刀耕火耨”
B.唐代诗人刘禹锡《浪淘沙》:“美人首饰侯王印,尽是沙中浪底来”
C.葛洪《肘后备急方》:“青蒿一握,以水二升渍,绞取汁”
D.《吕氏春秋》:“金柔锡柔,合两柔则刚"
2.下列物质的用途利用其氧化性的是
A.氨气用于制备硝酸 B.二氧化硫用于葡萄酒和果酒的生产
C.FeCl 溶液用于制作简易印刷电路板 D.浓盐酸用于检查氨气运输管道是否有泄漏
3
3.下列物质混合后,因发生氧化还原反应使溶液pH减小的是
A.向浓硝酸中加入铜粉,产生红棕色气体
B.向水中加入 固体,产生无色气体
C.向碘水中通入 气体,碘水颜色变浅
D.向 溶液中通入 气体,生成黑色沉淀
4.下列变化或应用涉及氧化还原反应的有几种
①明矾净水 ②漂白粉变质 ③自然固氮 ④电解 ⑤绚丽的烟花 ⑥
风化 ⑦电离 ⑧二氧化硫使品红溶液褪色 ⑨臭氧杀菌 ⑩纳米铁粉去除污水中
的重金属离子
A.5种 B.6种 C.7种 D.8种
5.下列生产过程不涉及氧化还原反应的是
A.高炉炼铁 B.工业制硫酸
C.用 、 和饱和食盐水制备纯碱D.海水提溴
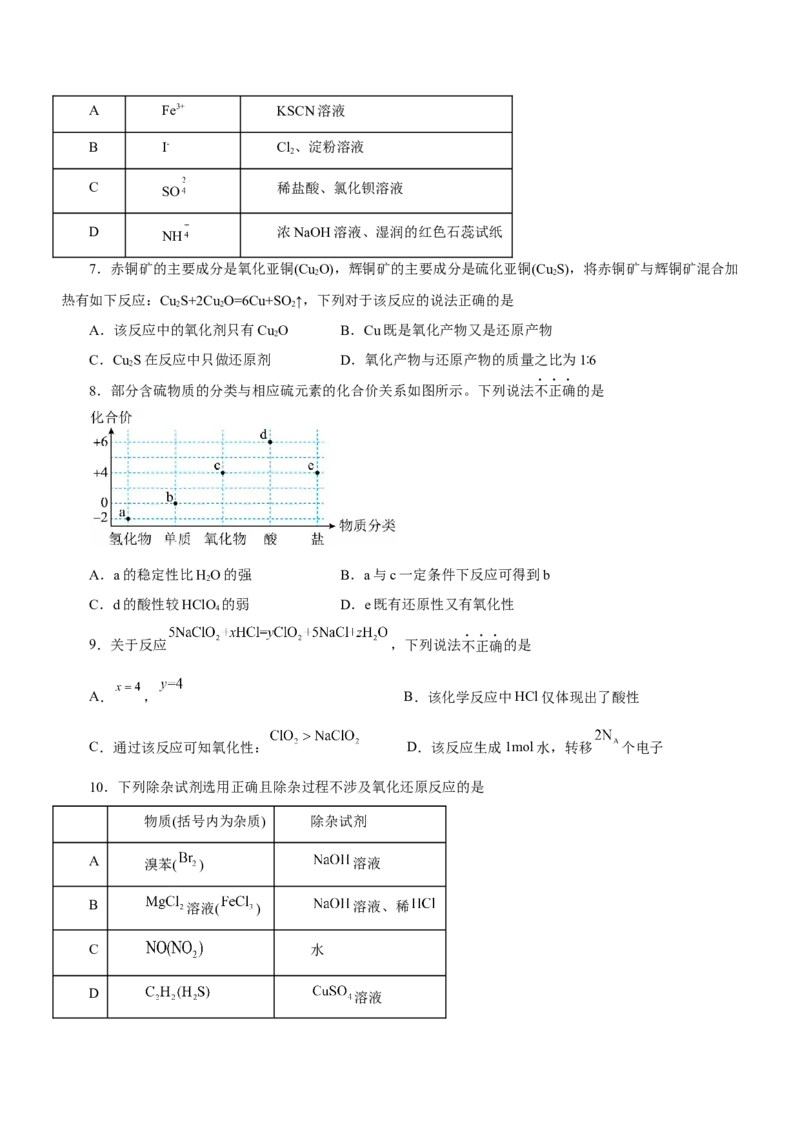
6.下列离子检验利用了氧化还原反应的是
选
待检验离子 检验试剂
项A Fe3+ KSCN溶液
B I- Cl、淀粉溶液
2
C 稀盐酸、氯化钡溶液
SO
D
NH
浓NaOH溶液、湿润的红色石蕊试纸
7.赤铜矿的主要成分是氧化亚铜(Cu O),辉铜矿的主要成分是硫化亚铜(Cu S),将赤铜矿与辉铜矿混合加
2 2
热有如下反应:Cu S+2Cu O=6Cu+SO ↑,下列对于该反应的说法正确的是
2 2 2
A.该反应中的氧化剂只有Cu O B.Cu既是氧化产物又是还原产物
2
C.Cu S在反应中只做还原剂 D.氧化产物与还原产物的质量之比为1∶6
2
8.部分含硫物质的分类与相应硫元素的化合价关系如图所示。下列说法不正确的是
A.a的稳定性比HO的强 B.a与c一定条件下反应可得到b
2
C.d的酸性较HClO 的弱 D.e既有还原性又有氧化性
4
9.关于反应 ,下列说法不正确的是
A. , B.该化学反应中HCl仅体现出了酸性
C.通过该反应可知氧化性: D.该反应生成1mol水,转移 个电子
10.下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是
物质(括号内为杂质) 除杂试剂
A 溴苯( ) 溶液
B 溶液( ) 溶液、稀
C 水
D 溶液11.高铁酸钾纯品为暗紫色有光泽粉末。在 以下干燥空气中稳定。极易溶于水而形成浅紫红色溶
液,静置后会分解放出氧气,并沉淀出水合三氧化二铁。溶液的碱性随分解而增大,在强碱性溶液中相当稳
定,是极好的氧化剂。具有高效的消毒作用,比高锰酸钾具有更强的氧化性。高铁酸钾的分子式为 ,
工业制备高铁酸钾的离子方程式为 (未配平),下列有关说法不正确
的是
A.由上述反应可知, 的氧化性强于
B.高铁酸钾中铁显+6价
C.上述反应氧化剂和还原剂的物质的量之比为
D. 处理水时,不仅能消毒杀菌,还生成 水解形成 胶体吸附水中悬浮杂质
12.三氟化溴有强氧化性和强反应活性,是一种良好的非水溶剂,遇水立即发生反应
3BrF+5H O=HBrO +Br +9HF+O↑。下列有关该反应的说法正确的是
3 2 3 2 2
A.氧化剂与还原剂的物质的量之比为3:2
B.当反应转移3mol电子时,生成的还原产物为1mol
C.当生成2.7molHF时,被BrF 还原的BrF 为0.1mol
3 3
D.当0.5molHO被氧化时,生成0.25molO
2 2
13. 是一种用途广泛的优良供氧剂,可用于鱼类养殖、农作物栽培、污水处理等多方面。某恒容密
闭容器中发生反应: 。下列说法正确的是
A.反应结束恢复到初始温度,气体压强一定变为原来的一半
B.常温常压下, 和 的摩尔体积相等
C. 既是氧化产物,也是还原产物
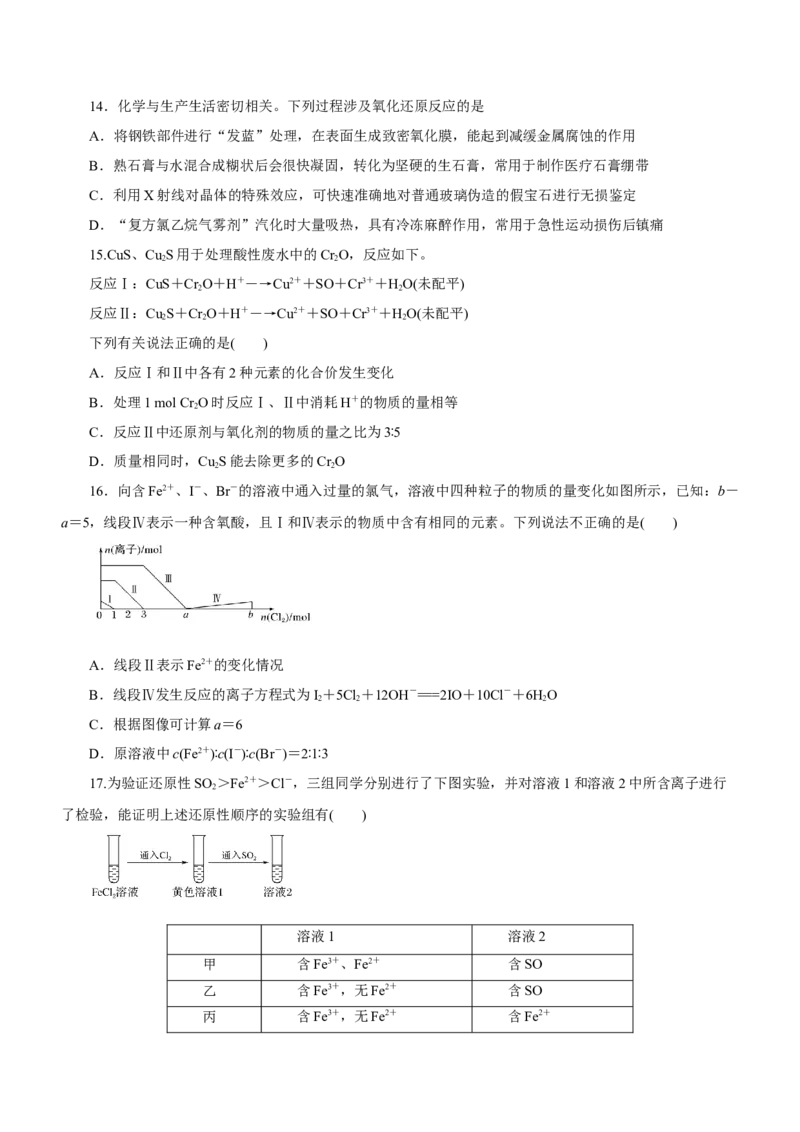
D.转移1mol电子时,生成11.2L氧气14.化学与生产生活密切相关。下列过程涉及氧化还原反应的是
A.将钢铁部件进行“发蓝”处理,在表面生成致密氧化膜,能起到减缓金属腐蚀的作用
B.熟石膏与水混合成糊状后会很快凝固,转化为坚硬的生石膏,常用于制作医疗石膏绷带
C.利用X射线对晶体的特殊效应,可快速准确地对普通玻璃伪造的假宝石进行无损鉴定
D.“复方氯乙烷气雾剂”汽化时大量吸热,具有冷冻麻醉作用,常用于急性运动损伤后镇痛
15.CuS、Cu S用于处理酸性废水中的Cr O,反应如下。
2 2
反应Ⅰ:CuS+Cr O+H+―→Cu2++SO+Cr3++HO(未配平)
2 2
反应Ⅱ:Cu S+Cr O+H+―→Cu2++SO+Cr3++HO(未配平)
2 2 2
下列有关说法正确的是( )
A.反应Ⅰ和Ⅱ中各有2种元素的化合价发生变化
B.处理1 mol Cr O时反应Ⅰ、Ⅱ中消耗H+的物质的量相等
2
C.反应Ⅱ中还原剂与氧化剂的物质的量之比为3∶5
D.质量相同时,Cu S能去除更多的Cr O
2 2
16.向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知:b-
a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素。下列说法不正确的是( )
A.线段Ⅱ表示Fe2+的变化情况
B.线段Ⅳ发生反应的离子方程式为I+5Cl+12OH-===2IO+10Cl-+6HO
2 2 2
C.根据图像可计算a=6
D.原溶液中c(Fe2+)∶c(I-)∶c(Br-)=2∶1∶3
17.为验证还原性SO >Fe2+>Cl-,三组同学分别进行了下图实验,并对溶液1和溶液2中所含离子进行
2
了检验,能证明上述还原性顺序的实验组有( )
溶液1 溶液2
甲 含Fe3+、Fe2+ 含SO
乙 含Fe3+,无Fe2+ 含SO
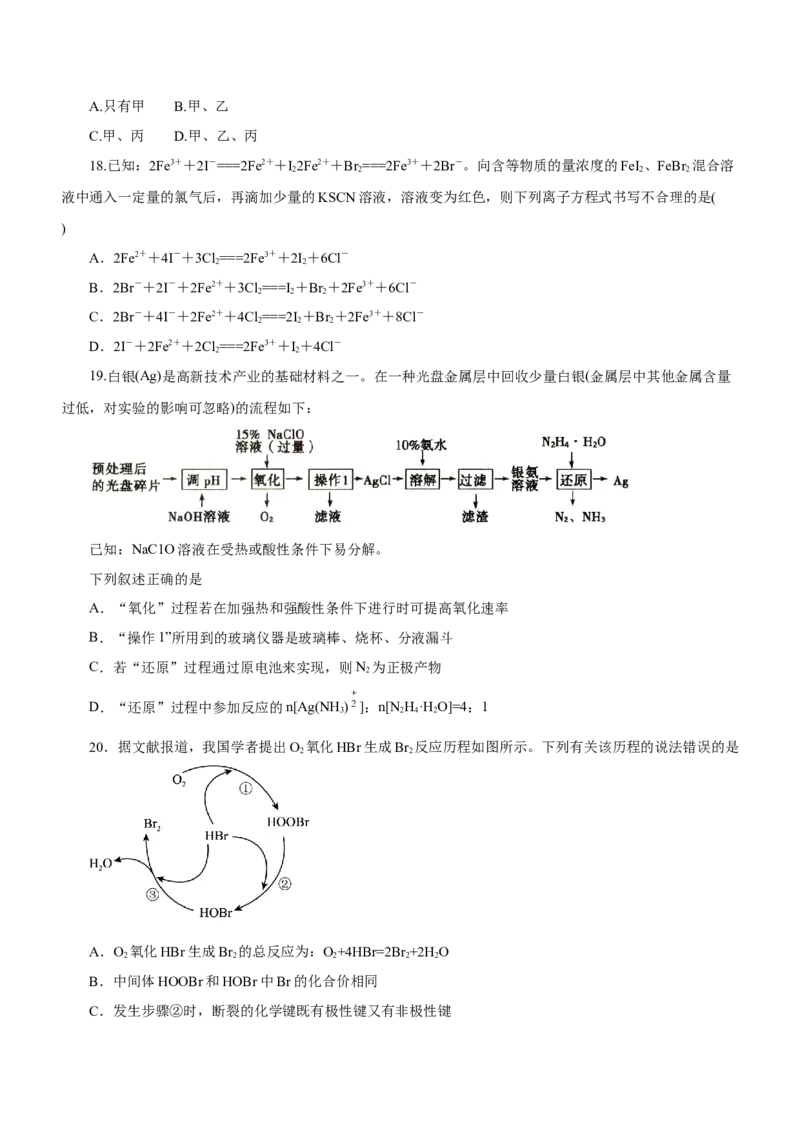
丙 含Fe3+,无Fe2+ 含Fe2+A.只有甲 B.甲、乙
C.甲、丙 D.甲、乙、丙
18.已知:2Fe3++2I-===2Fe2++I2Fe2++Br ===2Fe3++2Br-。向含等物质的量浓度的FeI、FeBr 混合溶
2 2 2 2
液中通入一定量的氯气后,再滴加少量的KSCN溶液,溶液变为红色,则下列离子方程式书写不合理的是(
)
A.2Fe2++4I-+3Cl===2Fe3++2I+6Cl-
2 2
B.2Br-+2I-+2Fe2++3Cl===I +Br +2Fe3++6Cl-
2 2 2
C.2Br-+4I-+2Fe2++4Cl===2I +Br +2Fe3++8Cl-
2 2 2
D.2I-+2Fe2++2Cl===2Fe3++I+4Cl-
2 2
19.白银(Ag)是高新技术产业的基础材料之一。在一种光盘金属层中回收少量白银(金属层中其他金属含量
过低,对实验的影响可忽略)的流程如下:
已知:NaC1O溶液在受热或酸性条件下易分解。
下列叙述正确的是
A.“氧化”过程若在加强热和强酸性条件下进行时可提高氧化速率
B.“操作1”所用到的玻璃仪器是玻璃棒、烧杯、分液漏斗
C.若“还原”过程通过原电池来实现,则N 为正极产物
2
D.“还原”过程中参加反应的n[Ag(NH) ]:n[N H·H O]=4:1
3 2 4 2
20.据文献报道,我国学者提出O 氧化HBr生成Br 反应历程如图所示。下列有关该历程的说法错误的是
2 2
A.O 氧化HBr生成Br 的总反应为:O+4HBr=2Br +2H O
2 2 2 2 2
B.中间体HOOBr和HOBr中Br的化合价相同
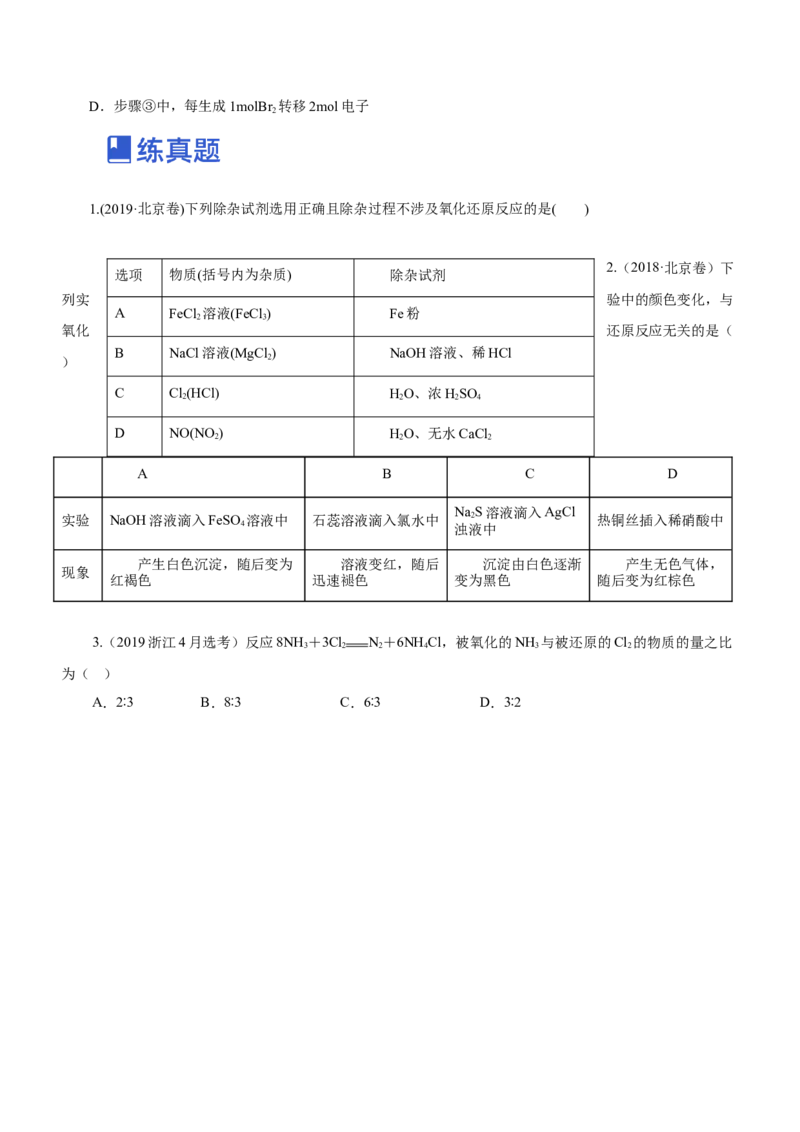
C.发生步骤②时,断裂的化学键既有极性键又有非极性键D.步骤③中,每生成1molBr 转移2mol电子
2
1.(2019·北京卷)下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是( )
2.(2018·北京卷)下
选项 物质(括号内为杂质) 除杂试剂
列实 验中的颜色变化,与
A FeCl 溶液(FeCl ) Fe粉
2 3
氧化 还原反应无关的是(
B NaCl溶液(MgCl ) NaOH溶液、稀HCl
) 2
C Cl(HCl) HO、浓HSO
2 2 2 4
D NO(NO ) HO、无水CaCl
2 2 2
A B C D
NaS溶液滴入AgCl
实验 NaOH溶液滴入FeSO 溶液中 石蕊溶液滴入氯水中 2 热铜丝插入稀硝酸中
4 浊液中
产生白色沉淀,随后变为 溶液变红,随后 沉淀由白色逐渐 产生无色气体,
现象
红褐色 迅速褪色 变为黑色 随后变为红棕色
3.(2019浙江4月选考)反应8NH +3Cl N+6NH Cl,被氧化的NH 与被还原的Cl 的物质的量之比
3 2 2 4 3 2
为( )
A.2∶3 B.8∶3 C.6∶3 D.3∶2