文档内容
专题 29 弱电解质的电离平衡
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 弱电解质的电离平衡及影响因素
考点二 电离度、电离平衡常数及计算
考点一 弱电解质的电离平衡及影响因素
1.(2023·北京东城·统考二模) 时, 的电离常数 , 的电离常数 、
。下列说法不正确的是
A. 溶液和 溶液中离子种类相同
B. 时,反应 的
C. ,物质的量浓度相同的 溶液与 溶液的 :前者小于后者
D.向氯水中加入少量 固体, 增大
2.(2023·天津河东·统考二模)常温下,下列事实能说明某一元酸 是一元强酸的是
A. 溶液的
B. 溶液
C. 溶液比 硝酸导电能力弱
D. 溶液与 溶液混合
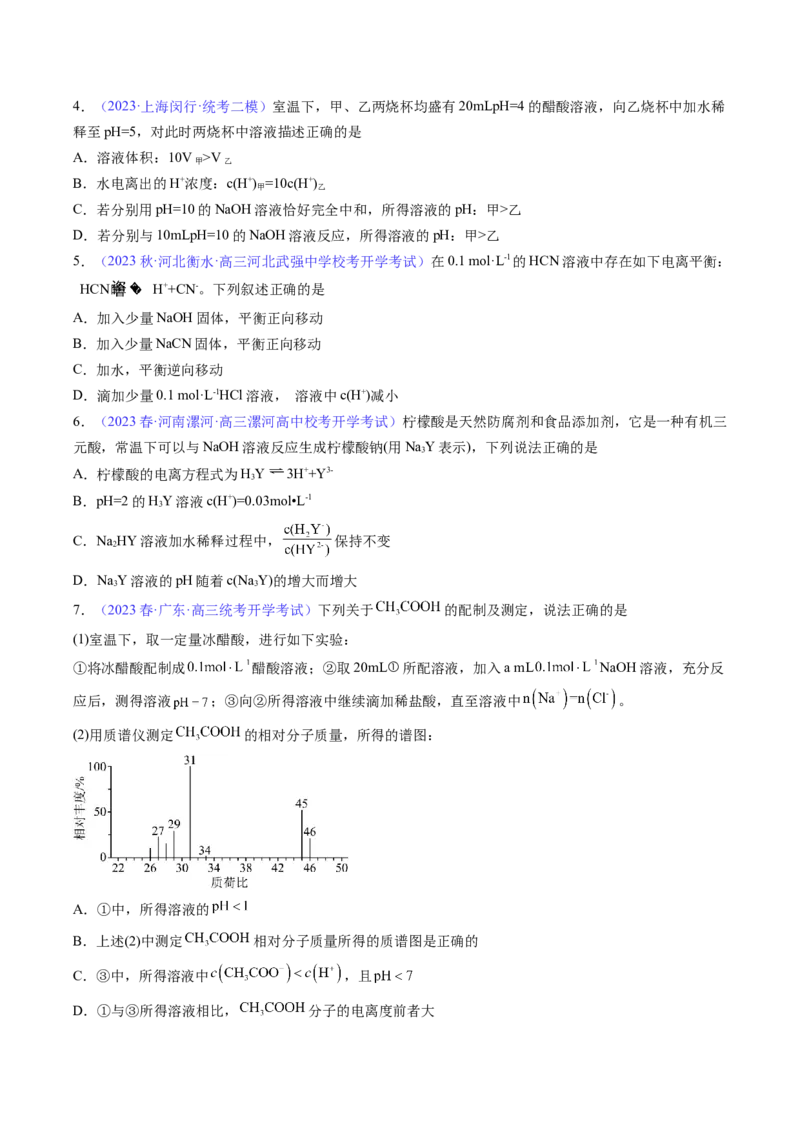
3.(2023·四川南充·统考三模)如图所示,常温下,往甲室和乙室中分别加入等体积、浓度均为0.1mol/L
的CHCOONH 溶液(pH≈7)和CHCOOH溶液(pH≈3),中间用交换膜隔开(只有未电离的CHCOOH分子可
3 4 3 3
自由通过交换膜,且不考虑溶液体积的变化),达到平衡后,下列说法错误的是
A.常温下,K(CHCOOH)≈1.0×10-5
a 3
B.平衡后,甲、乙两室pH相等
C.平衡后,甲室中:c(NH )<c(CHCOO-)
3
D.平衡前,CHCOOH分子从乙室进入甲室
3
1
原创精品资源学科网独家享有版权,侵权必究!4.(2023·上海闵行·统考二模)室温下,甲、乙两烧杯均盛有20mLpH=4的醋酸溶液,向乙烧杯中加水稀
释至pH=5,对此时两烧杯中溶液描述正确的是
A.溶液体积:10V >V
甲 乙
B.水电离出的H+浓度:c(H+) =10c(H+)
甲 乙
C.若分别用pH=10的NaOH溶液恰好完全中和,所得溶液的pH:甲>乙
D.若分别与10mLpH=10的NaOH溶液反应,所得溶液的pH:甲>乙
5.(2023秋·河北衡水·高三河北武强中学校考开学考试)在0.1 mol·L-1的HCN溶液中存在如下电离平衡:
HCN H++CN-。下列叙述正确的是
A.加入少量NaOH固体,平衡正向移动
B.加入少量NaCN固体,平衡正向移动
C.加水,平衡逆向移动
D.滴加少量0.1 mol·L-1HCl溶液, 溶液中c(H+)减小
6.(2023春·河南漯河·高三漯河高中校考开学考试)柠檬酸是天然防腐剂和食品添加剂,它是一种有机三
元酸,常温下可以与NaOH溶液反应生成柠檬酸钠(用NaY表示),下列说法正确的是
3
A.柠檬酸的电离方程式为HY 3H++Y3-
3
B.pH=2的HY溶液c(H+)=0.03mol•L-1
3
C.NaHY溶液加水稀释过程中, 保持不变
2
D.NaY溶液的pH随着c(Na Y)的增大而增大
3 3
7.(2023春·广东·高三统考开学考试)下列关于 的配制及测定,说法正确的是
(1)室温下,取一定量冰醋酸,进行如下实验:
①将冰醋酸配制成 醋酸溶液;②取20mL①所配溶液,加入a mL NaOH溶液,充分反
应后,测得溶液 ;③向②所得溶液中继续滴加稀盐酸,直至溶液中 。
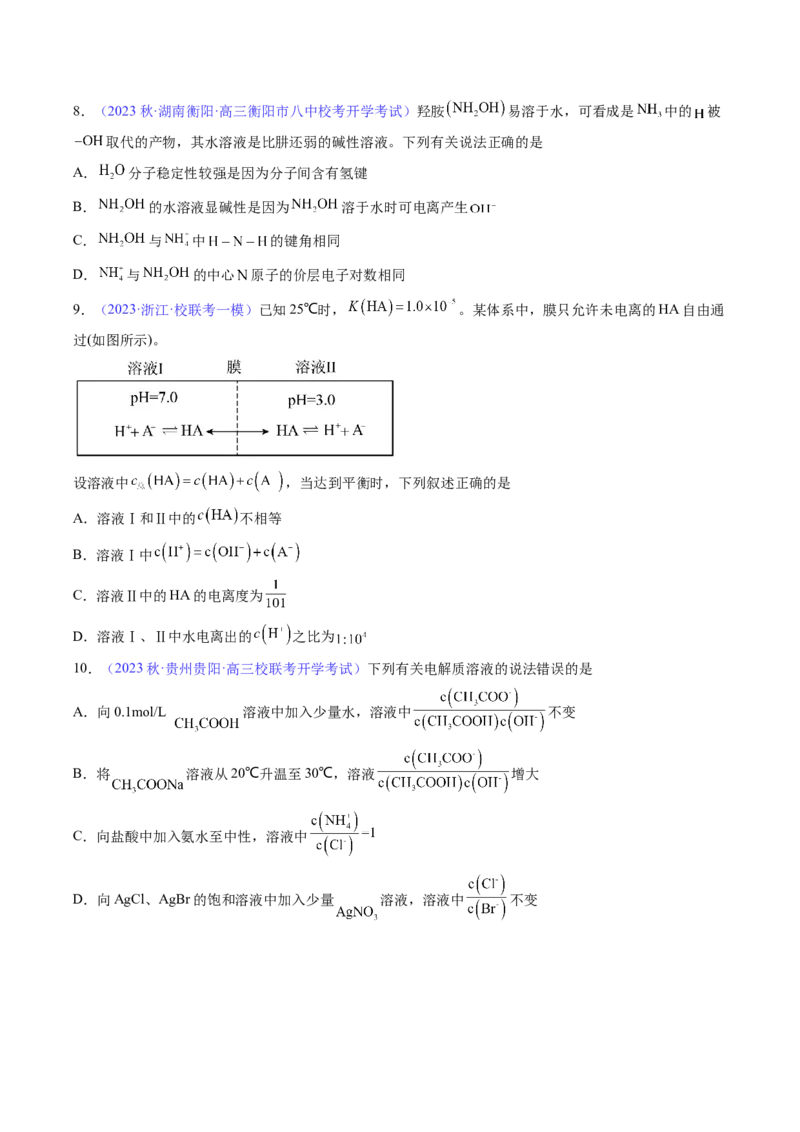
(2)用质谱仪测定 的相对分子质量,所得的谱图:
A.①中,所得溶液的
B.上述(2)中测定 相对分子质量所得的质谱图是正确的
C.③中,所得溶液中 ,且
D.①与③所得溶液相比, 分子的电离度前者大8.(2023秋·湖南衡阳·高三衡阳市八中校考开学考试)羟胺 易溶于水,可看成是 中的 被
取代的产物,其水溶液是比肼还弱的碱性溶液。下列有关说法正确的是
A. 分子稳定性较强是因为分子间含有氢键
B. 的水溶液显碱性是因为 溶于水时可电离产生
C. 与 中 的键角相同
D. 与 的中心 原子的价层电子对数相同
9.(2023·浙江·校联考一模)已知25℃时, 。某体系中,膜只允许未电离的HA自由通
过(如图所示)。
设溶液中 ,当达到平衡时,下列叙述正确的是
A.溶液Ⅰ和Ⅱ中的 不相等
B.溶液Ⅰ中
C.溶液Ⅱ中的HA的电离度为
D.溶液Ⅰ、Ⅱ中水电离出的 之比为
10.(2023秋·贵州贵阳·高三校联考开学考试)下列有关电解质溶液的说法错误的是
A.向0.1mol/L 溶液中加入少量水,溶液中 不变
B.将 溶液从20℃升温至30℃,溶液 增大
C.向盐酸中加入氨水至中性,溶液中
D.向AgCl、AgBr的饱和溶液中加入少量 溶液,溶液中 不变考点二 电离度、电离平衡常数及计算
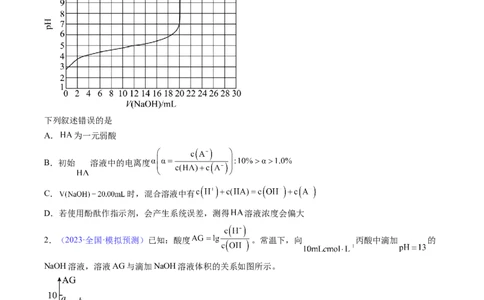
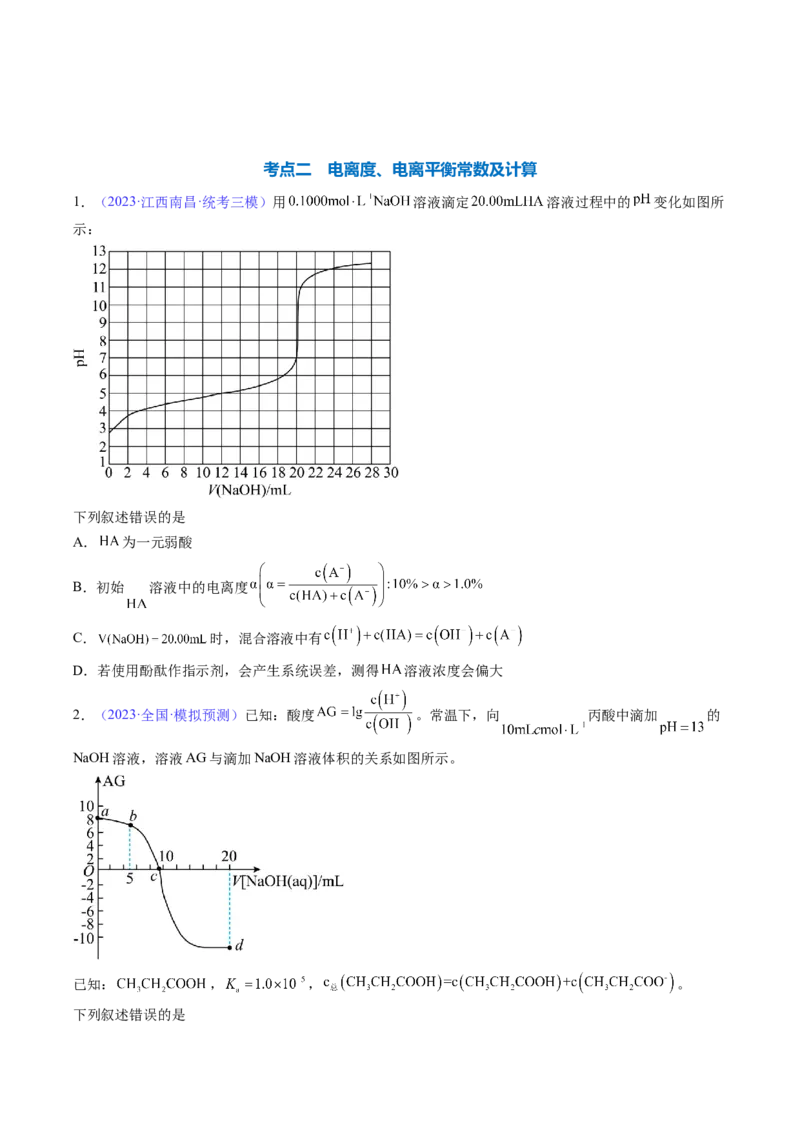
1.(2023·江西南昌·统考三模)用 溶液滴定 溶液过程中的 变化如图所
示:
下列叙述错误的是
A. 为一元弱酸
B.初始 溶液中的电离度
C. 时,混合溶液中有
D.若使用酚酞作指示剂,会产生系统误差,测得 溶液浓度会偏大
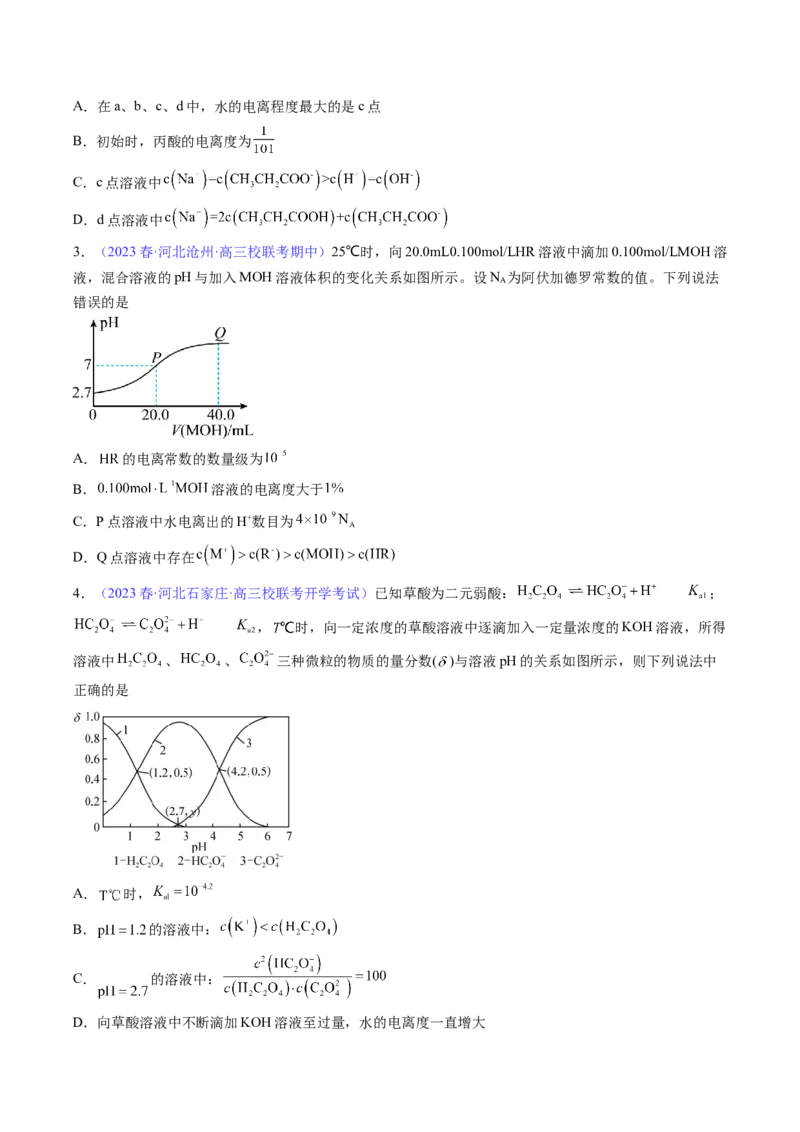
2.(2023·全国·模拟预测)已知:酸度 。常温下,向 丙酸中滴加 的
NaOH溶液,溶液AG与滴加NaOH溶液体积的关系如图所示。
已知: , , 。
下列叙述错误的是A.在a、b、c、d中,水的电离程度最大的是c点
B.初始时,丙酸的电离度为
C.c点溶液中
D.d点溶液中
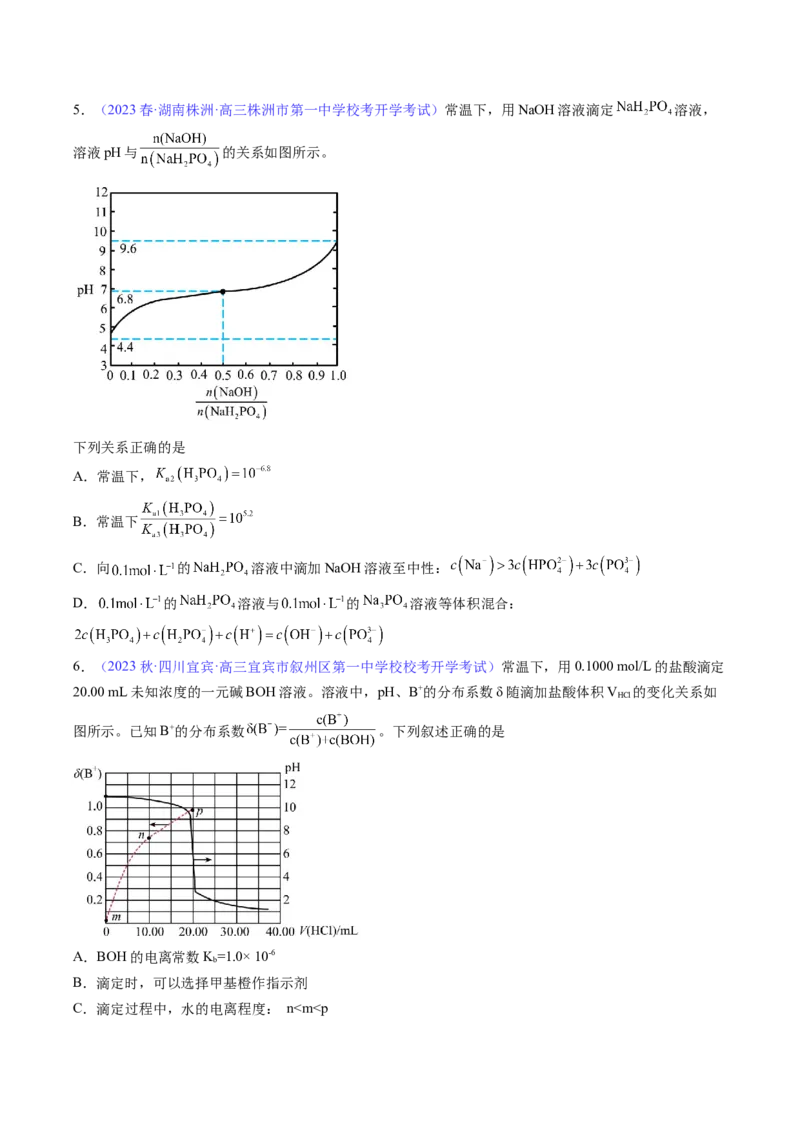
3.(2023春·河北沧州·高三校联考期中)25℃时,向20.0mL0.100mol/LHR溶液中滴加0.100mol/LMOH溶
液,混合溶液的pH与加入MOH溶液体积的变化关系如图所示。设N 为阿伏加德罗常数的值。下列说法
A
错误的是
A. 的电离常数的数量级为
B. 溶液的电离度大于
C.P点溶液中水电离出的H+数目为
D.Q点溶液中存在
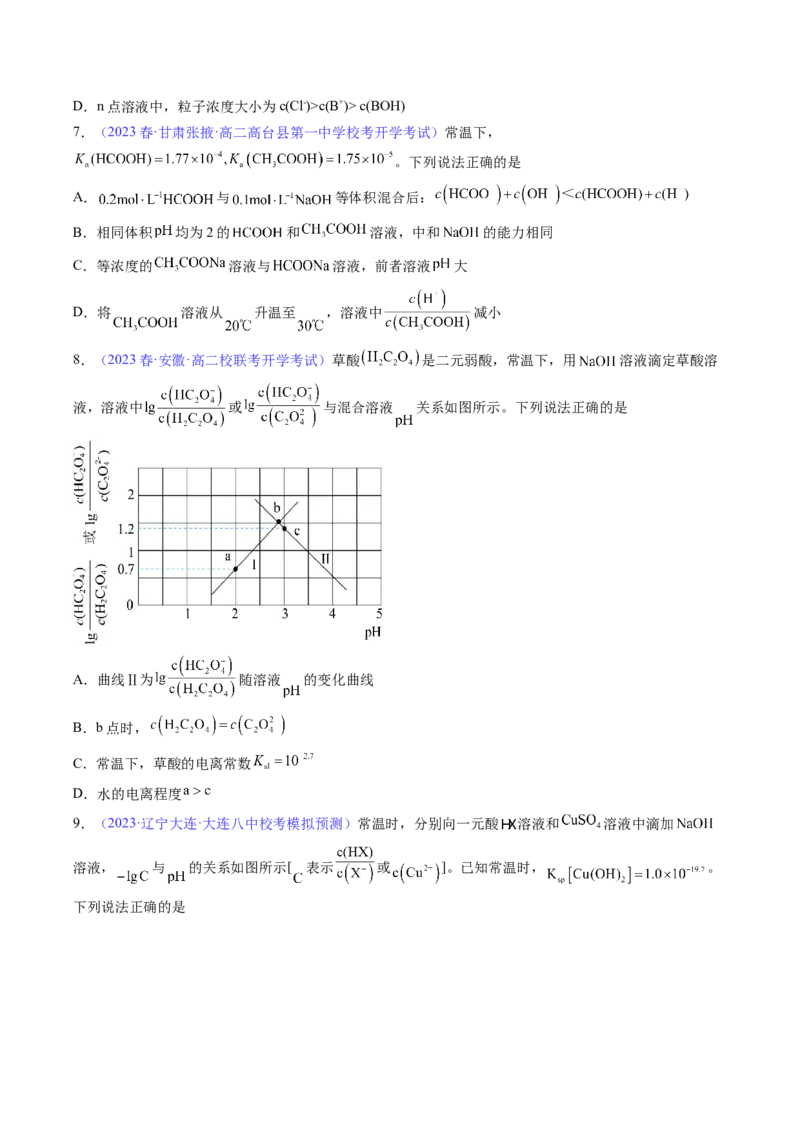
4.(2023春·河北石家庄·高三校联考开学考试)已知草酸为二元弱酸: ;
, 时,向一定浓度的草酸溶液中逐滴加入一定量浓度的KOH溶液,所得
溶液中 、 、 三种微粒的物质的量分数( )与溶液pH的关系如图所示,则下列说法中
正确的是
A. 时,
B. 的溶液中:
C. 的溶液中:
D.向草酸溶液中不断滴加KOH溶液至过量,水的电离度一直增大5.(2023春·湖南株洲·高三株洲市第一中学校考开学考试)常温下,用NaOH溶液滴定 溶液,
溶液pH与 的关系如图所示。
下列关系正确的是
A.常温下,
B.常温下
C.向 的 溶液中滴加NaOH溶液至中性:
D. 的 溶液与 的 溶液等体积混合:
6.(2023秋·四川宜宾·高三宜宾市叙州区第一中学校校考开学考试)常温下,用0.1000 mol/L的盐酸滴定
20.00 mL未知浓度的一元碱BOH溶液。溶液中,pH、B+的分布系数δ随滴加盐酸体积V 的变化关系如
HCl
图所示。已知B+的分布系数 。下列叙述正确的是
A.BOH的电离常数K=1.0× 10-6
b
B.滴定时,可以选择甲基橙作指示剂
C.滴定过程中,水的电离程度: nc(B+)> c(BOH)
7.(2023春·甘肃张掖·高二高台县第一中学校考开学考试)常温下,
。下列说法正确的是
A. 与 等体积混合后:
B.相同体积 均为2的 和 溶液,中和 的能力相同
C.等浓度的 溶液与 溶液,前者溶液 大
D.将 溶液从 升温至 ,溶液中 减小
8.(2023春·安徽·高二校联考开学考试)草酸 是二元弱酸,常温下,用 溶液滴定草酸溶
液,溶液中 或 与混合溶液 关系如图所示。下列说法正确的是
A.曲线Ⅱ为 随溶液 的变化曲线
B.b点时,
C.常温下,草酸的电离常数
D.水的电离程度
9.(2023·辽宁大连·大连八中校考模拟预测)常温时,分别向一元酸 溶液和 溶液中滴加
溶液, 与 的关系如图所示[ 表示 或 ]。已知常温时, 。
下列说法正确的是A.曲线①表示 与 的关系
B.一元酸 的电离平衡常数
C.对于曲线②的溶液,N点水的电离程度大于M点
D.M点时,对于 溶液:
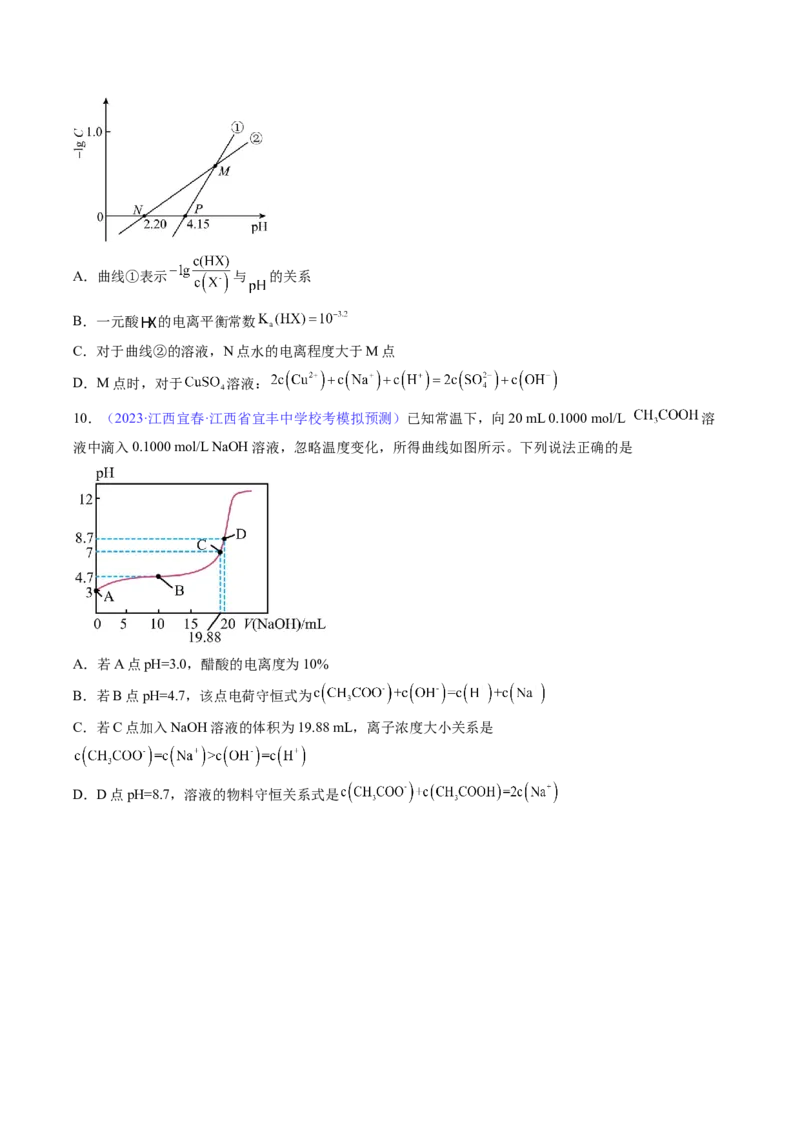
10.(2023·江西宜春·江西省宜丰中学校考模拟预测)已知常温下,向20 mL 0.1000 mol/L 溶
液中滴入0.1000 mol/L NaOH溶液,忽略温度变化,所得曲线如图所示。下列说法正确的是
A.若A点pH=3.0,醋酸的电离度为10%
B.若B点pH=4.7,该点电荷守恒式为
C.若C点加入NaOH溶液的体积为19.88 mL,离子浓度大小关系是
D.D点pH=8.7,溶液的物料守恒关系式是