文档内容
专题四 元素化合物综合应用及对环境的影响
【考情分析】
元素化合物综合应用题是高考常考的题型之一,它集元素化合物知识、基本概念
基本理论和化学计算等知识于一体,且试题结构紧凑、文字表述少、包含信息多。
因而成了高考命题中一种十分重要的命题形式,如2018·课标全国Ⅲ第26题对硫
代硫酸钠晶体的考查,2017年江苏化学18题对碱式氯化铜的考查,2016年全国
卷Ⅱ第28题对铁的化合物的性质的综合考查等。2015年全国卷Ⅱ第28题对消毒
剂ClO 的综合考查,全国卷Ⅰ第28题对碘及其化合物的综合考查等。
2
1.元素化合物综合题常见设问方向
(1)化合价:如 等。
(2)电子式:如
等。
(3)氧化还原反应离子方程式的书写
第一步得失电子守恒,配平氧化剂,还原剂,氧化产物,还原产物。
第二步电荷守恒,根据反应环境配平H+或OH-。
第三步原子守恒,根据反应前后,氢原子或氧原子配平水的系数。
(4)问题简答:常见的有反应现象叙述,基本实验操作等,如现象描述可通过下面
程序和模板加以规范,
①全面描述现象的程序——“海、陆、空”“海”——溶液有什么变化;
“陆”——固体有什么变化;
“空”——气体有什么变化。
②规范描述现象的答题模板
如a.颜色:……由……(具体颜色)变为……(具体颜色);
b.气体:溶液中产生……(颜色)的气泡,(或)在固体表面产生……(颜色)气泡;
c.沉淀:在……(颜色)溶液中产生……(颜色)的沉淀(浑浊)。
2.元素化合物综合题的解题程序
在非金属元素中,以Cl、O、S、N、P、C、Si为重点。
在金属元素中,以Na、Al、Fe、Cu为重点。其中
一、抓元素,知性质
Cl、N、S、Na、Al、Fe六种元素的单质及其化合物
性质最典型、最重要,要重点掌握
要熟悉含各元素的物质的一些特性,如含Fe3+的
溶液遇KSCN溶液变红色,含Fe2+的溶液与碱溶
二、明目的,知特性 液反应的特殊现象,Al、Al O 、Al(OH) 的两性,
2 3 3
NH 遇HCl、Cl 、HNO 产生白烟,NH 使湿润的红
3 2 3 3
色石蕊试纸变蓝,SO 的漂白性等
2
要学会将元素化合物知识与元素周期律、物质结
三、会结合 构、氧化还原反应、中和滴定、化学反应速率、化学
平衡、电化学等密切结合起来
将掌握的元素化合物知识与题目所给信息相结
四、结合题目信息作答 合,判断不同情况下框图中各字母代表的物质,进
而结合物质的性质按要求回答问题
考点指导1 信息提供型元素化合物综合题
【题型说明】
此类题目往往起点高、落点低,考查的是对信息的获取与问题解决能力,解题的
关键是理解新信息。当遇到这一类题时,第一步是读题,陌生度较高的信息应逐
字逐句地阅读,挖掘关键字,排除定势思维的影响;第二步是联想,在读题的基础
上结合题目的问题联想分析考查的知识模块,提取出已学的相关化学知识;第三
步是解题,按要求填好相应的问题答案,使化学意义顺畅。
【案例1】 Ⅰ.(6分)请回答:(1)H O 的电子式________。
2 2
(2)镁燃烧不能用CO 灭火,用化学方程式表示其理由
2
_____________________________________________________________________
。
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子
方程式__________________________________________________________。
(4)完成以下氧化还原反应的离子方程式:
( )MnO+( )C O+________===( )Mn2++( )CO ↑+________
2 2
Ⅱ.(12分)化合物甲和NaAlH 都是重要的还原剂。一定条件下金属钠和H 反应生
4 2
成甲。甲与水反应可产生H ,甲与AlCl 反应可得到NaAlH 。将4.80 g甲加热至
2 3 4
完全分解,得到金属钠和2.24 L(已折算成标准状况)的H 。
2
请推测并回答:
(1)甲的化学式________。
(2) 甲 与 AlCl 反 应 得 到 NaAlH 的 化 学 方 程 式
3 4
_____________________________________________________________________
_
_____________________________________________________________________
。
(3)NaAlH 与 水 发 生 氧 化 还 原 反 应 的 化 学 方 程 式
4
_____________________________________________________________________
_
_____________________________________________________________________
。
(4)甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe O ),脱
2 3
锈过程发生反应的化学方程式
___________________________________________________________________。
(5)某同学认为:用惰性气体赶尽反应体系中的空气,将铁和盐酸反应后的气体经
浓硫酸干燥,再与金属钠反应,得到的固体物质即为纯净的甲;取该固体物质与
水反应,若能产生H ,即可证明得到的甲一定是纯净的。
2
判断该同学设想的制备和验纯方法的合理性并说明理由_____________________________________________________________________
。
[标准答案] Ⅰ.(1) (1分)
(2)2Mg+CO 2MgO+C(2分)
2
(3)AgCl(s)+Br-(aq)===AgBr(s)+Cl-(aq)(1分)
(4)2MnO+5C O+16H+===2Mn2++10CO ↑+8H O(2分)
2 2 2
Ⅱ.(1)NaH(2分) (2)4NaH+AlCl ===NaAlH +3NaCl(2分)
3 4
(3)NaAlH +2H O===NaAlO +4H ↑(2分)
4 2 2 2
(4)3NaH+Fe O ===2Fe+3NaOH(2分)
2 3
(5)制备过程不合理,因为盐酸易挥发,H 中混有HCl,导致产物中有NaCl;(2分)
2
验纯方法不合理,如果有 Na残留,Na与水反应也产生 H ;没有考虑混入的
2
NaCl(2分)
[解题心得] 元素化合物知识是中学化学的主干知识,要学好元素化合物知识,
需注意以下几点:①回归教材,立足基础。②注重知识点之间的联系,形成知识网
络,在“融会贯通”上下功夫。③反思纠正作业、练习和考试中出现的差错。
【对点训练】
1.工业上氰化物的用途广泛,在电镀、洗注、油漆、燃料、橡胶等行业都会用到。
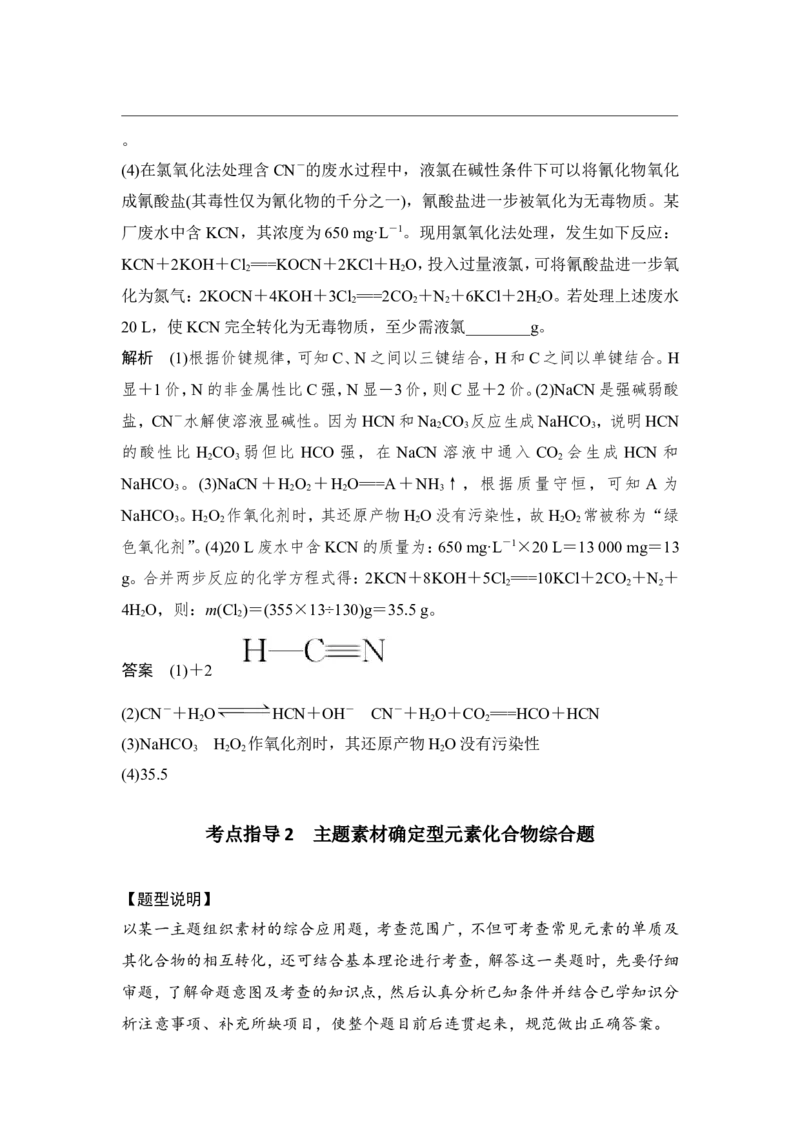
(1)氢氰酸(HCN)是一种酸性很弱的酸,其中碳元素的化合价为________,氢氰酸
分子的结构式为________。
(2) 氰 化 钠 (NaCN) 溶 液 显 强 碱 性 , 原 因 是 ( 用 离 子 方 程 式 表
示)________________________。已知 Na CO 溶液能和 HCN 反应:Na CO +
2 3 2 3
HCN===NaHCO +NaCN,则向NaCN溶液中通入少量CO 时反应的离子方程式
3 2
为_____________________________________________________________。
(3)双氧水可消除氰化物(如NaCN)污染:NaCN+H O +H O===A+NH ↑,则生
2 2 2 3
成物A的化学式为________________,H O 常被称为“绿色氧化剂”的理由是
2 2
_____________________________________________________________________
______________________________________________________________________
。
(4)在氯氧化法处理含CN-的废水过程中,液氯在碱性条件下可以将氰化物氧化
成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质。某
厂废水中含KCN,其浓度为650 mg·L-1。现用氯氧化法处理,发生如下反应:
KCN+2KOH+Cl ===KOCN+2KCl+H O,投入过量液氯,可将氰酸盐进一步氧
2 2
化为氮气:2KOCN+4KOH+3Cl ===2CO +N +6KCl+2H O。若处理上述废水
2 2 2 2
20 L,使KCN完全转化为无毒物质,至少需液氯________g。
解析 (1)根据价键规律,可知C、N之间以三键结合,H和C之间以单键结合。H
显+1价,N的非金属性比C强,N显-3价,则C显+2价。(2)NaCN是强碱弱酸
盐,CN-水解使溶液显碱性。因为HCN和Na CO 反应生成NaHCO ,说明HCN
2 3 3
的酸性比 H CO 弱但比 HCO 强,在 NaCN 溶液中通入 CO 会生成 HCN 和
2 3 2
NaHCO 。(3)NaCN+H O +H O===A+NH ↑,根据质量守恒,可知 A 为
3 2 2 2 3
NaHCO 。H O 作氧化剂时,其还原产物H O没有污染性,故H O 常被称为“绿
3 2 2 2 2 2
色氧化剂”。(4)20 L废水中含KCN的质量为:650 mg·L-1×20 L=13 000 mg=13
g。合并两步反应的化学方程式得:2KCN+8KOH+5Cl ===10KCl+2CO +N +
2 2 2
4H O,则:m(Cl )=(355×13÷130)g=35.5 g。
2 2
答案 (1)+2
(2)CN-+H O HCN+OH- CN-+H O+CO ===HCO+HCN
2 2 2
(3)NaHCO H O 作氧化剂时,其还原产物H O没有污染性
3 2 2 2
(4)35.5
考点指导2 主题素材确定型元素化合物综合题
【题型说明】
以某一主题组织素材的综合应用题,考查范围广,不但可考查常见元素的单质及
其化合物的相互转化,还可结合基本理论进行考查,解答这一类题时,先要仔细
审题,了解命题意图及考查的知识点,然后认真分析已知条件并结合已学知识分
析注意事项、补充所缺项目,使整个题目前后连贯起来,规范做出正确答案。【案例2】 铜是一种古老而又年轻的金属元素,铜及其化合物在生产生活中有着
广泛的应用。
(1)古代留下来的青铜器表面呈绿色,原因是在潮湿的空气中,铜易发生腐蚀生成
铜绿,有关反应的化学方程式为:
_____________________________________________________________________
_
_____________________________________________________________________
。
(2)现代工业主要采用高温冶炼黄铜矿(CuFeS ,也可表示为Cu S·Fe S )的方法获
2 2 2 3
得铜。火法炼铜首先要焙烧黄铜矿:2CuFeS +4O =====Cu S+3SO +2FeO,每
2 2 2 2
转移0.6 mol电子,有________ mol硫原子被氧化。
(3)CuSO 可 用 于 游 泳 池 水 的 消 毒 , 原 因 是
4
_____________________________________________________________________
_
_____________________________________________________________________
。
(4)向CuCl 和FeCl 的混合溶液中加入CuO粉末会产生新的沉淀,该沉淀的主要
2 3
成分的化学式为________(已知:Fe3+水解程度比Cu2+大)。
(5)利用Cu和FeCl 溶液的反应可制作印刷电路板,为了从含有 FeCl 、FeCl 、
3 3 2
CuCl 的废液中回收Cu,某化学兴趣小组的同学设计了以下两种实验方案:
2
方案1:向废液中加入过量铁粉,充分反应后过滤。在所得滤渣中加入足量盐酸,
充分反应后,再过滤即得到铜。方案1中涉及的四种阳离子的氧化性由强到弱的
顺序为________。
方案2:在废液中加入适量的盐酸调节溶液的pH=1,用铜和石墨作电极进行电
解。当观察到阴极上有少量气泡产生时,即停止电解,这时Cu已全部析出,在电
极上可直接回收铜。操作上比方案1简便,但方案2也有不足之处,主要表现为
________。
解析 (1)在潮湿的空气中,铜易与O 、H O、CO 发生反应生成铜锈,铜锈的主要
2 2 2
成分是Cu (OH) CO 。(2)在CuFeS 中Cu、Fe、S三种元素的化合价依次是+2、+
2 2 3 2
2、-2,2 mol CuFeS 发生反应时,转移18 mol电子,有3 mol硫原子被氧化,则每
2转移0.6 mol电子,有0.1 mol硫原子被氧化。(3)CuSO 是重金属盐,能使蛋白质
4
变性,可杀灭水中的细菌。(4)CuCl 和FeCl 水解使溶液显酸性,向混合溶液中加
2 3
入CuO时,CuO与水解生成的酸反应,使水解平衡正向移动,因Fe3+水解程度比
Cu2+大,故主要生成Fe(OH) 沉淀。(5)根据氧化还原反应中氧化剂的氧化性大于
3
氧化产物的氧化性,可知氧化性:Fe3+>Cu2+>H+>Fe2+。方案2电解时有污染
性的气体Cl 产生,且能耗大。
2
答案 (1)2Cu+O +H O+CO ===Cu (OH) CO
2 2 2 2 2 3
(2)0.1 (3)CuSO 能使蛋白质变性
4
(4)Fe(OH)
3
(5)Fe3+>Cu2+>H+>Fe2+ 有污染性气体Cl 产生,使用了电解装置,成本较高
2
【对点训练】
2.硫的化合物丰富多彩,且都有一定的用途。
(1)用作橡胶工业的硫化剂S Cl 的分子结构中每个原子均满足8电子稳定结构,
2 2
S Cl 的电子式为________。S Cl 遇水很容易发生水解反应生成一种淡黄色固体
2 2 2 2
和两种气体,其反应的化学方程式为__________________________________。
(2)用作氧化剂的过二硫酸铵[(NH ) S O ]属于离子化合物,易溶于水,其可由硫酸
4 2 2 8
铵[(NH ) SO ]为原料制备。
4 2 4
①(NH ) SO 溶液呈酸性的原因是________________________(用离子方程式表
4 2 4
示 ) , (NH ) SO 溶 液 中 各 种 离 子 的 浓 度 由 大 到 小 的 顺 序 为
4 2 4
________________________。
②若硫酸铵溶液的浓度为250 g·L-1,其物质的量浓度是________mol·L-1。
③(NH ) S O 在Ag+的催化作用下能将Mn2+氧化成MnO,其反应的离子方程式
4 2 2 8
为__________________________________________________________________。
(3)Na S O 在空气分析中常用来吸收氧气,当吸收氧气、水蒸气后发生反应时,若
2 2 4
还原剂和氧化剂的物质的量之比为1∶1,则产物为________(填化学式)。
解析 (1)S Cl 中每个原子均满足8电子稳定结构,其结构式为Cl—S—S—Cl,
2 2
则电子式为 ;由题意可知有S生成,根据氧化还原反应和水解反应的规律知有 HCl、SO 生成,则发生反应的化学方程式为
2
2S Cl +2H O===4HCl↑+SO ↑+3S↓。
2 2 2 2
(2)①(NH ) SO 溶液因 NH 水解而呈酸性,则水解方程式为 NH+H O
4 2 4 2
NH ·H O+H+;(NH ) SO 水解是一个微弱的过程,则c(NH)>c(SO)>c(H+)>
3 2 4 2 4
c(OH-)。②c=[250÷(18×2+32+16×4)] mol·L-1≈1.89 mol·L-1。③根据氧化还
原反应中得失电子守恒以及电荷守恒可得离子方程式 2Mn2++5S O+
2
8H O=====2MnO+10SO+16H+。(3)根据还原剂和氧化剂的物质的量之比为
2
1∶1以及得失电子守恒可写出反应的化学方程式Na S O +O +H O===NaHSO
2 2 4 2 2 4
+NaHSO ;产物为NaHSO 和NaHSO 。
3 4 3
答案 (1)
2S Cl +2H O===4HCl↑+SO ↑+3S↓
2 2 2 2
(2)①NH+H O NH ·H O+H+ c(NH)>c(SO)>c(H+)>c(OH-) ②1.89
2 3 2
③2Mn2++5S O+8H O=====2MnO+10SO+16H+
2 2
(3)NaHSO 和NaHSO
4 3
考点指导3 元素化合物综合题中的环境保护和绿色化学
【题型说明】
以单质及其化合物的性质,考查环境保护与绿色化学的应用是近几年高考命题的
热点;是一类与社会、生产、生活结合较为紧密的一类题目,题中一些答案的制定
经常具有一定的开放性,作答时,要联系生产、生活实际,充分利用化学语言,敢
于下笔。
【案例3】 (北京卷)研究CO 在海洋中的转移和归宿,是当今海洋科学研究的前
2
沿领域。
(1)溶于海水的CO 主要以4种无机碳形式存在,其中HCO占95%。写出CO 溶
2 2于水产生HCO的方程式:
_____________________________________________________________________
。
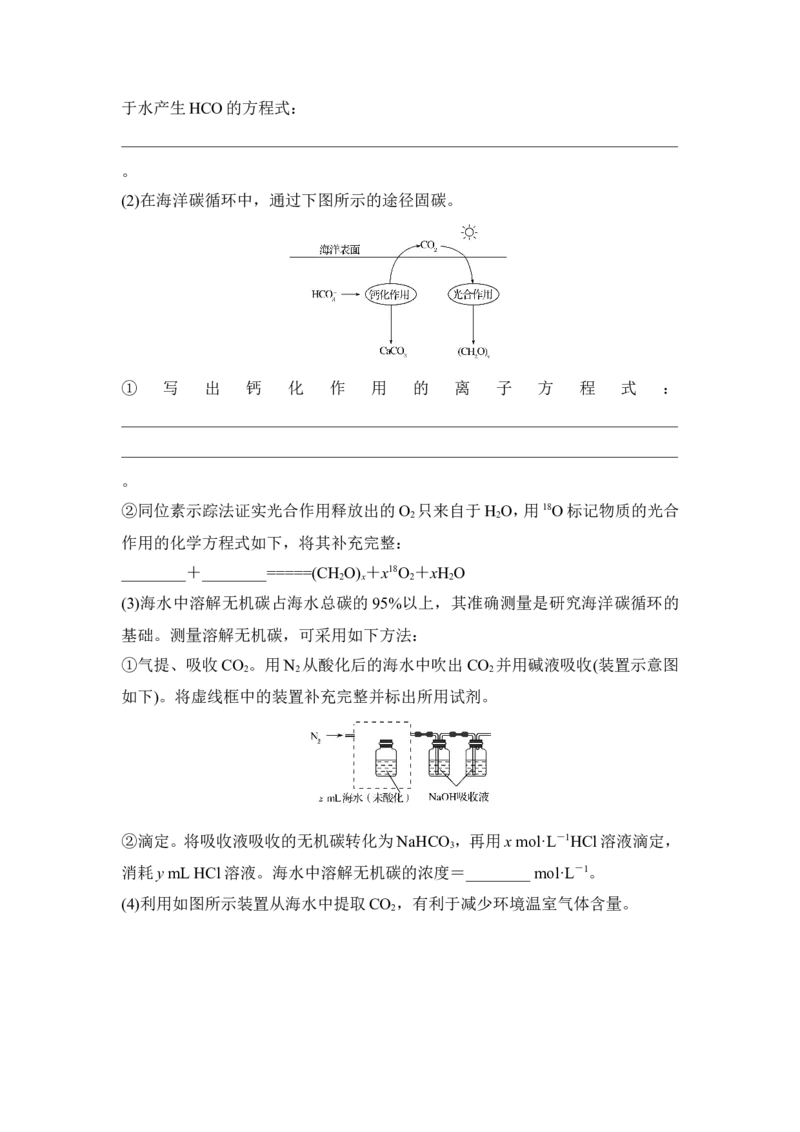
(2)在海洋碳循环中,通过下图所示的途径固碳。
① 写 出 钙 化 作 用 的 离 子 方 程 式 :
_____________________________________________________________________
_____________________________________________________________________
。
②同位素示踪法证实光合作用释放出的O 只来自于H O,用18O标记物质的光合
2 2
作用的化学方程式如下,将其补充完整:
________+________=====(CH O) +x18O +xH O
2 x 2 2
(3)海水中溶解无机碳占海水总碳的95%以上,其准确测量是研究海洋碳循环的
基础。测量溶解无机碳,可采用如下方法:
①气提、吸收CO 。用N 从酸化后的海水中吹出CO 并用碱液吸收(装置示意图
2 2 2
如下)。将虚线框中的装置补充完整并标出所用试剂。
②滴定。将吸收液吸收的无机碳转化为NaHCO ,再用x mol·L-1HCl溶液滴定,
3
消耗y mL HCl溶液。海水中溶解无机碳的浓度=________ mol·L-1。
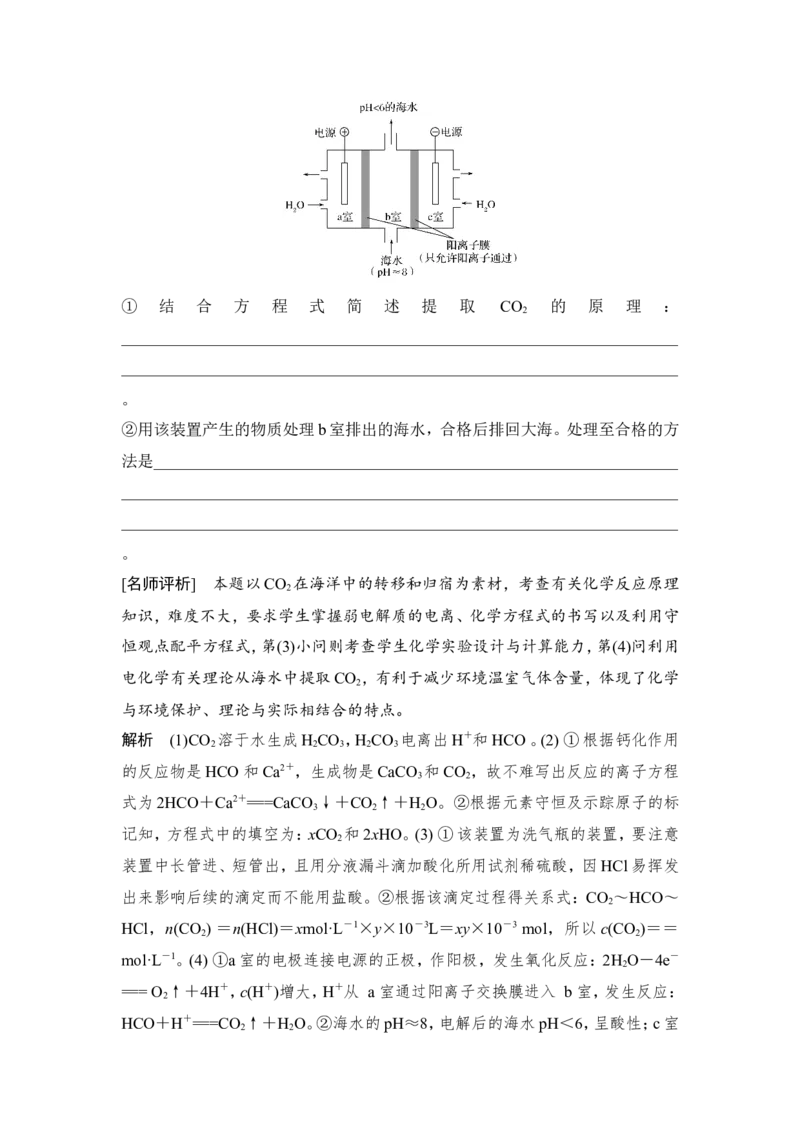
(4)利用如图所示装置从海水中提取CO ,有利于减少环境温室气体含量。
2① 结 合 方 程 式 简 述 提 取 CO 的 原 理 :
2
_____________________________________________________________________
_____________________________________________________________________
。
②用该装置产生的物质处理b室排出的海水,合格后排回大海。处理至合格的方
法是_________________________________________________________________
_____________________________________________________________________
_____________________________________________________________________
。
[名师评析] 本题以CO 在海洋中的转移和归宿为素材,考查有关化学反应原理
2
知识,难度不大,要求学生掌握弱电解质的电离、化学方程式的书写以及利用守
恒观点配平方程式,第(3)小问则考查学生化学实验设计与计算能力,第(4)问利用
电化学有关理论从海水中提取CO ,有利于减少环境温室气体含量,体现了化学
2
与环境保护、理论与实际相结合的特点。
解析 (1)CO 溶于水生成H CO ,H CO 电离出H+和HCO 。(2) ①根据钙化作用
2 2 3 2 3
的反应物是HCO 和Ca2+,生成物是CaCO 和CO ,故不难写出反应的离子方程
3 2
式为2HCO+Ca2+===CaCO ↓+CO ↑+H O。②根据元素守恒及示踪原子的标
3 2 2
记知,方程式中的填空为:xCO 和2xHO。(3) ①该装置为洗气瓶的装置,要注意
2
装置中长管进、短管出,且用分液漏斗滴加酸化所用试剂稀硫酸,因HCl易挥发
出来影响后续的滴定而不能用盐酸。②根据该滴定过程得关系式:CO ~HCO~
2
HCl,n(CO ) =n(HCl)=xmol·L-1×y×10-3L=xy×10-3 mol,所以c(CO )==
2 2
mol·L-1。(4) ①a室的电极连接电源的正极,作阳极,发生氧化反应:2H O―4e-
2
=== O ↑+4H+,c(H+)增大,H+从 a 室通过阳离子交换膜进入 b 室,发生反应:
2
HCO+H+===CO ↑+H O。②海水的pH≈8,电解后的海水pH<6,呈酸性;c室
2 2的反应:2H O+2e-=== H ↑+2OH-,可用c室排出的碱液与从b室排出的酸液
2 2
中和调至接近装置入口海水的pH,即处理合格。
答案 (1)CO +H O H CO 、
2 2 2 3
H CO H++HCO
2 3
(2)①2HCO+Ca2+===CaCO ↓+CO ↑+H O
3 2 2
②xCO 2xHO
2
(3) ①
②
(4)①a 室:2H O―4e-=== O ↑+4H+,H+通过阳离子膜进入b室,发生反应:
2 2
HCO+H+===CO ↑+H O ②c室的反应:2H O+2e-===H ↑+2OH-,用c室
2 2 2 2
排出的碱液将从b室排出的酸液调至接近装置入口海水的pH
【对点训练】
3.构建人与自然的和谐、营造安全的生态环境已成为全人类的共识。
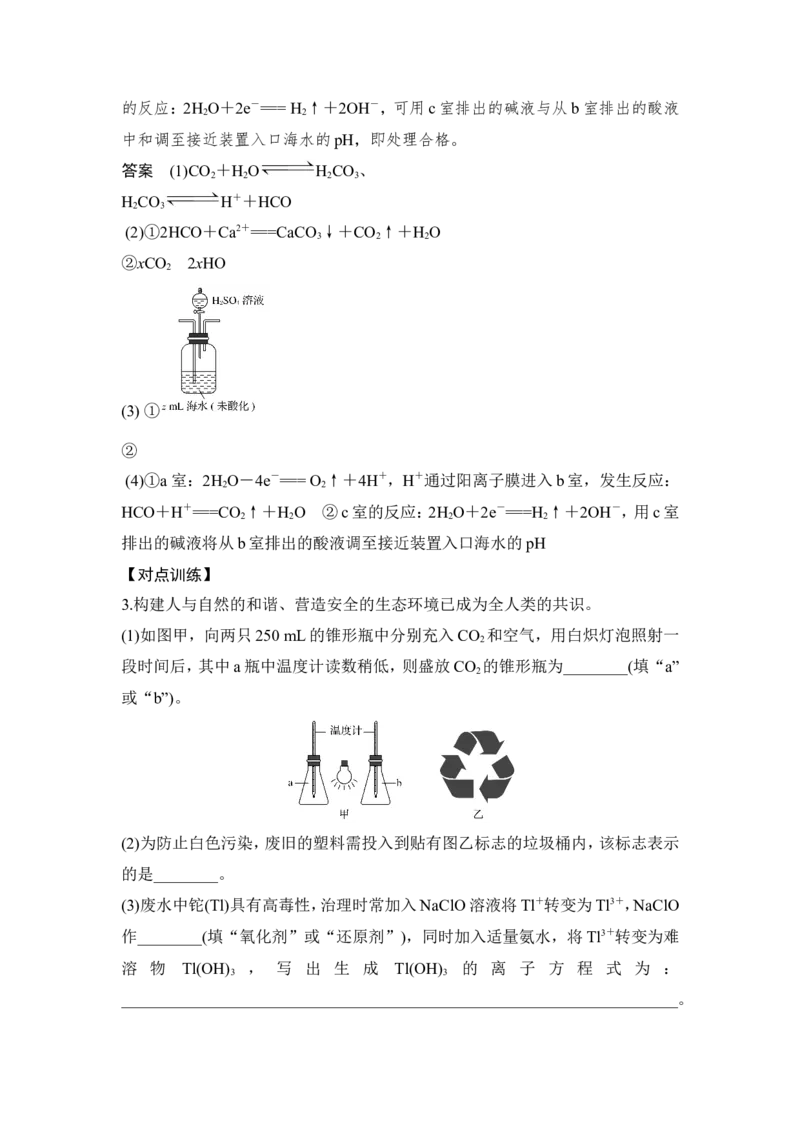
(1)如图甲,向两只250 mL的锥形瓶中分别充入CO 和空气,用白炽灯泡照射一
2
段时间后,其中a瓶中温度计读数稍低,则盛放CO 的锥形瓶为________(填“a”
2
或“b”)。
(2)为防止白色污染,废旧的塑料需投入到贴有图乙标志的垃圾桶内,该标志表示
的是________。
(3)废水中铊(Tl)具有高毒性,治理时常加入NaClO溶液将Tl+转变为Tl3+,NaClO
作________(填“氧化剂”或“还原剂”),同时加入适量氨水,将Tl3+转变为难
溶 物 Tl(OH) , 写 出 生 成 Tl(OH) 的 离 子 方 程 式 为 :
3 3
_____________________________________________________________________。解析 (1)由于CO 会产生温室效应,因此温度高的一瓶装的是CO ,即b瓶中装
2 2
的是CO 。(2)塑料属于可回收利用的垃圾,因此图乙是可回收垃圾的图标。(3)加
2
入NaClO溶液将Tl+转变为Tl3+,反应中铊元素失电子被氧化,NaClO中+1价
的氯被还原,因此NaClO是氧化剂;加入适量氨水,将Tl3+转变为难溶物Tl(OH)
3
的离子方程式见答案。
答案 (1)b (2)可回收垃圾 (3)氧化剂 Tl3++3NH ·H O===Tl(OH) ↓+3NH
3 2 3