文档内容
专题突破卷 03 金属及其化合物
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.明代《天工开物》记载“火法”冶炼锌:“每炉甘石十斤,装载入一泥罐内……然后逐层用煤炭饼垫
盛,其底铺薪,发火煅红……冷定毁罐取出……即倭铅也”(注:炉甘石的主要成分为碳酸锌,泥罐中掺有
煤炭)。下列说法不正确的是( )
A.倭铅是指金属锌和铅的混合物
B.煤炭中起作用的主要成分是C
C.冶炼Zn的化学方程式:ZnCO +2C=====Zn+3CO↑
3
D.该冶炼锌的方法属于热还原法
2.中国银行发行的中国航天普通纪念币,面额为10元,直径为27毫米,材质为双色铜合金。下列关于合
金的叙述不正确的是( )
A.铜合金和单质铜一样,具有良好的导电性、导热性和延展性
B.铜合金的硬度比单质铜大
C.铜合金的熔点比单质铜低
D.该纪念币能完全溶解于稀硫酸中
3.(2023·江苏南京期末)下列有关金属冶炼的说法不正确的是( )
A. 制Na:电解饱和NaCl溶液
B. 制Mg:电解熔融MgCl
2
C. 制Fe:用焦炭和空气反应产生的CO在高温下还原铁矿石中的铁的氧化物
D. 制Cu:熬胆矾铁釜,久之亦化为铜
4.下列铁及其化合物的性质与用途具有对应关系的是( )
A.Fe粉具有还原性,可用作抗氧化剂
B.Fe O 粉末呈红棕色,可用于制取铁盐
2 3
C.Fe (SO ) 易溶于水,可用作净水剂
2 4 3
D.FeCl 溶液呈酸性,用于蚀刻铜电路板
3
5.(2024·北京师范大学附属中学高三统练)关于离子化合物 和 ,下列说法不正确的是
A. 、 中均含有非极性共价键
B. 、 中阴、阳离子个数比均为C. 、 与水反应时水均不作氧化剂或还原剂
D.相同物质的量的 和 与足量的水反应,所得气体的物质的量
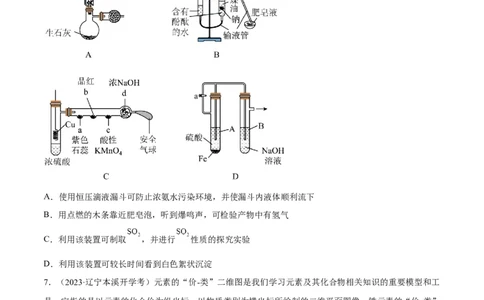
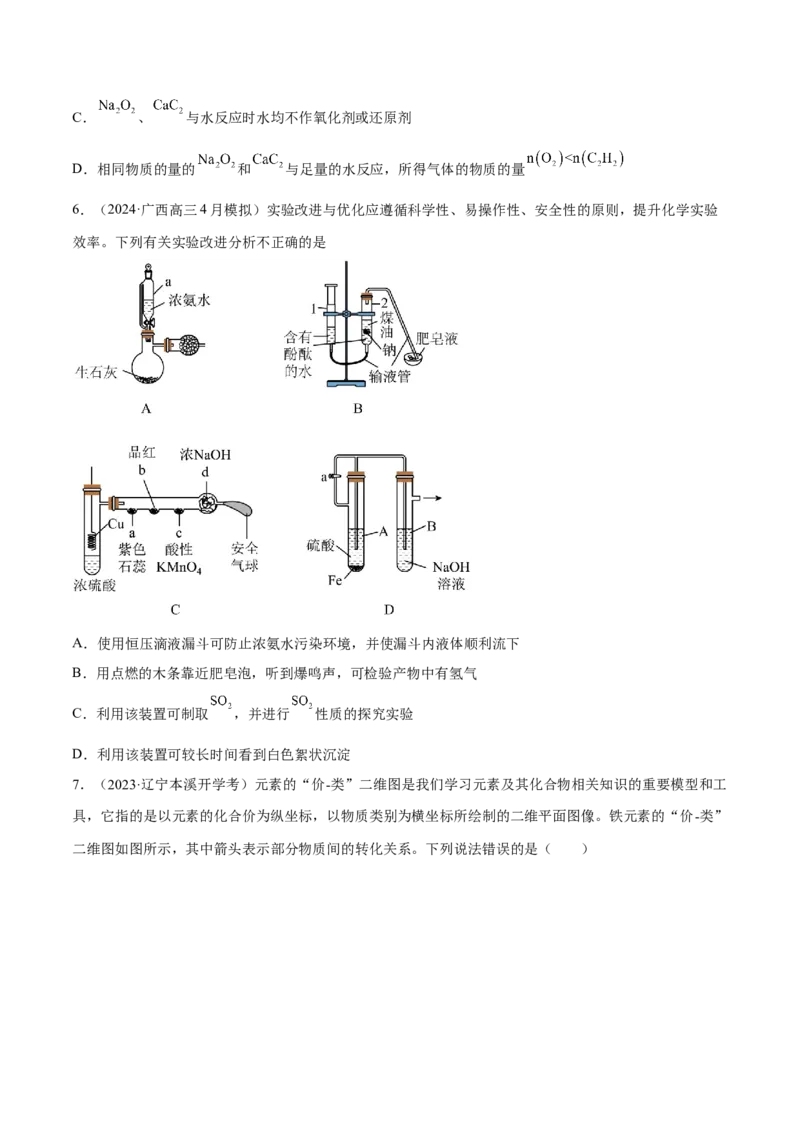
6.(2024·广西高三4月模拟)实验改进与优化应遵循科学性、易操作性、安全性的原则,提升化学实验
效率。下列有关实验改进分析不正确的是
A.使用恒压滴液漏斗可防止浓氨水污染环境,并使漏斗内液体顺利流下
B.用点燃的木条靠近肥皂泡,听到爆鸣声,可检验产物中有氢气
C.利用该装置可制取 ,并进行 性质的探究实验
D.利用该装置可较长时间看到白色絮状沉淀
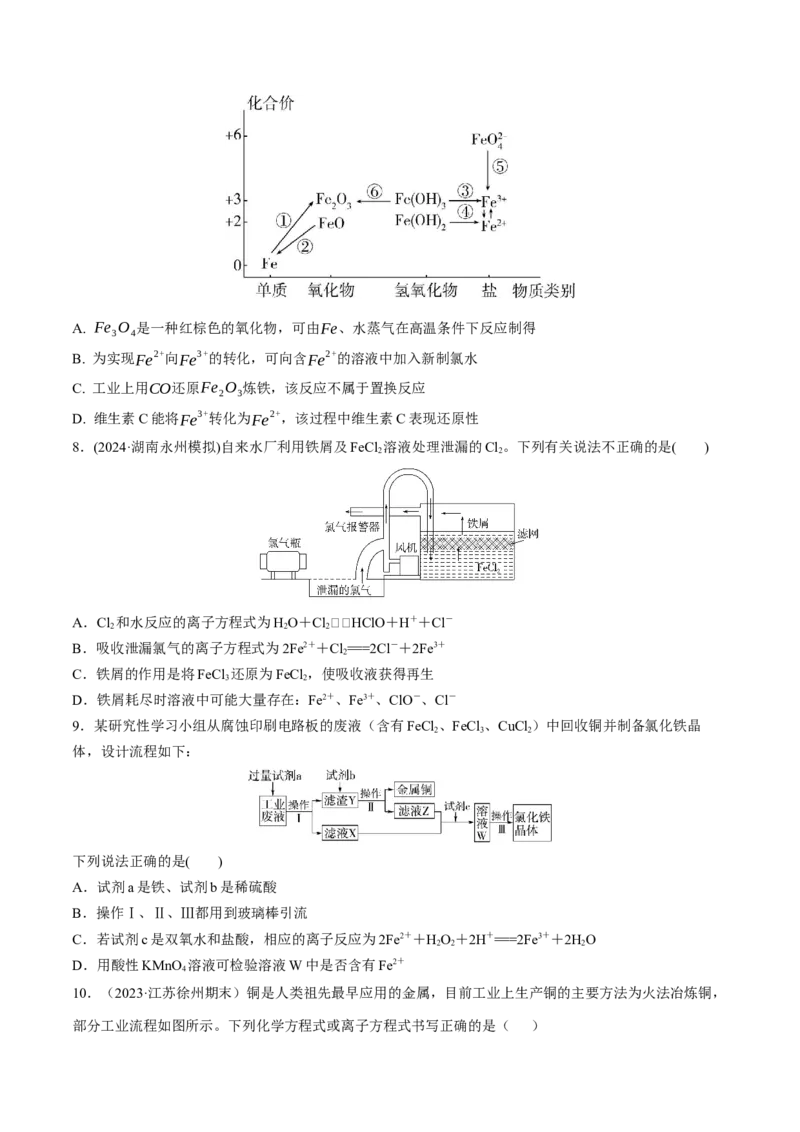
7.(2023·辽宁本溪开学考)元素的“价-类”二维图是我们学习元素及其化合物相关知识的重要模型和工
具,它指的是以元素的化合价为纵坐标,以物质类别为横坐标所绘制的二维平面图像。铁元素的“价-类”
二维图如图所示,其中箭头表示部分物质间的转化关系。下列说法错误的是( )A. Fe O 是一种红棕色的氧化物,可由Fe、水蒸气在高温条件下反应制得
3 4
B. 为实现Fe2+向Fe3+的转化,可向含Fe2+的溶液中加入新制氯水
C. 工业上用CO还原Fe O 炼铁,该反应不属于置换反应
2 3
D. 维生素C能将Fe3+转化为Fe2+,该过程中维生素C表现还原性
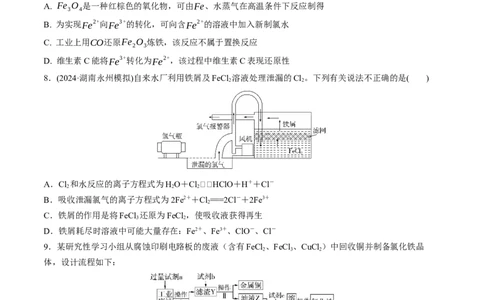
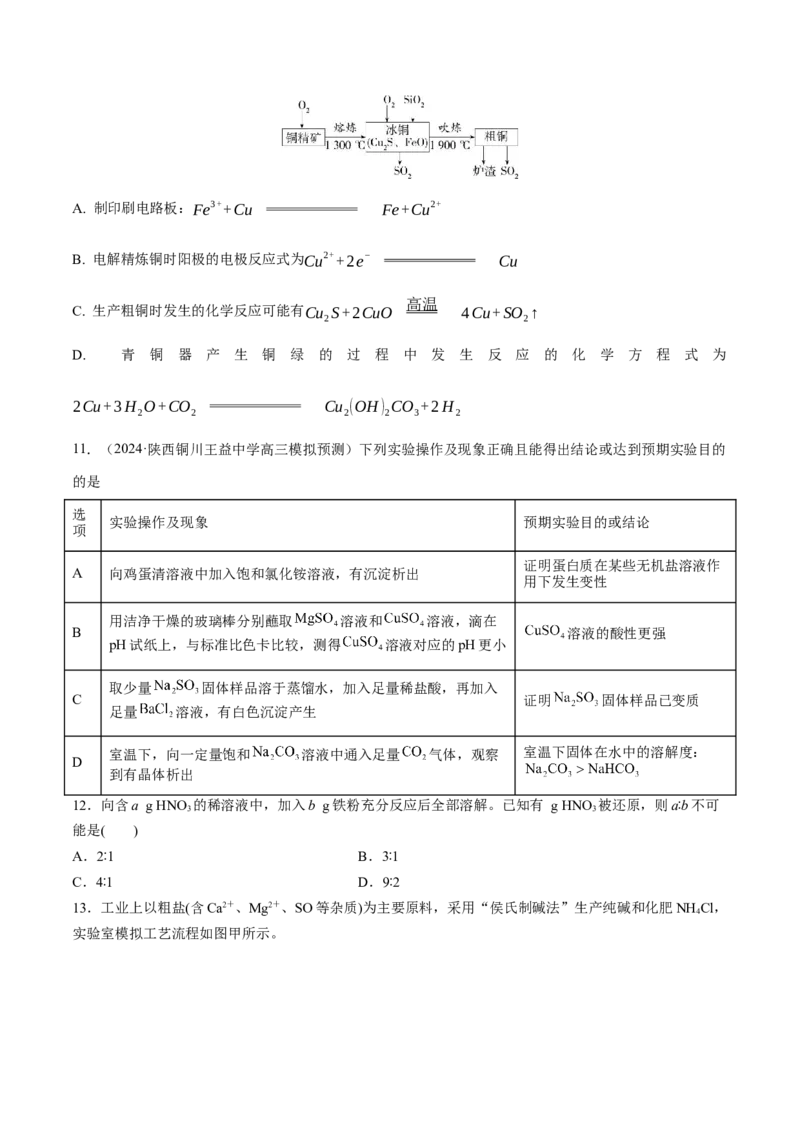
8.(2024·湖南永州模拟)自来水厂利用铁屑及FeCl 溶液处理泄漏的Cl。下列有关说法不正确的是( )
2 2
A.Cl 和水反应的离子方程式为HO+ClHClO+H++Cl-
2 2 2
B.吸收泄漏氯气的离子方程式为2Fe2++Cl===2Cl-+2Fe3+
2
C.铁屑的作用是将FeCl 还原为FeCl ,使吸收液获得再生
3 2
D.铁屑耗尽时溶液中可能大量存在:Fe2+、Fe3+、ClO-、Cl-
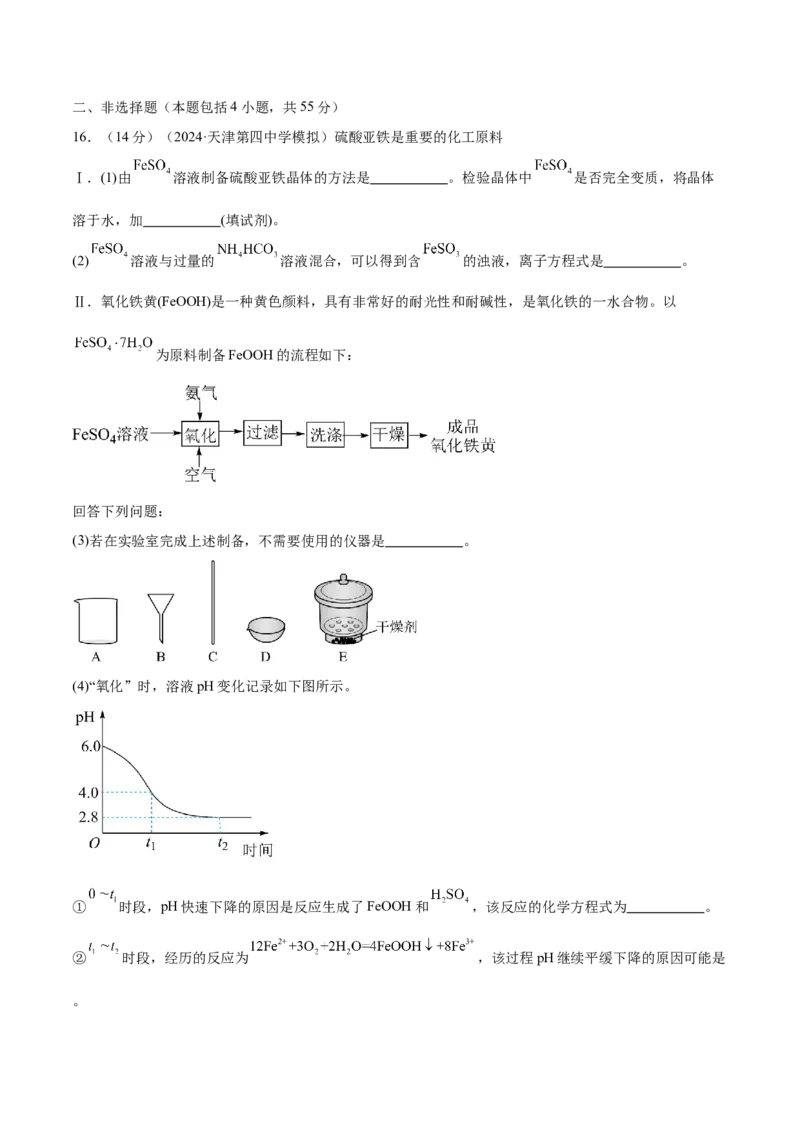
9.某研究性学习小组从腐蚀印刷电路板的废液(含有FeCl 、FeCl 、CuCl )中回收铜并制备氯化铁晶
2 3 2
体,设计流程如下:
下列说法正确的是( )
A.试剂a是铁、试剂b是稀硫酸
B.操作Ⅰ、Ⅱ、Ⅲ都用到玻璃棒引流
C.若试剂c是双氧水和盐酸,相应的离子反应为2Fe2++HO+2H+===2Fe3++2HO
2 2 2
D.用酸性KMnO 溶液可检验溶液W中是否含有Fe2+
4
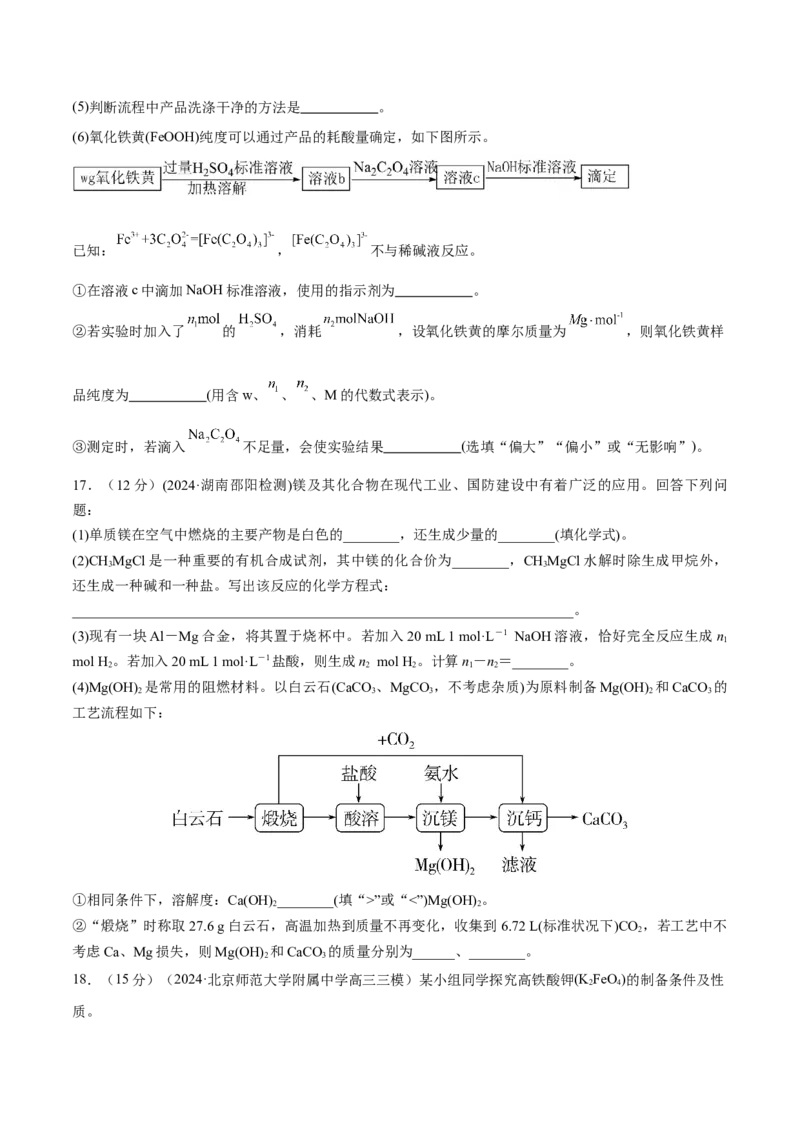
10.(2023·江苏徐州期末)铜是人类祖先最早应用的金属,目前工业上生产铜的主要方法为火法冶炼铜,
部分工业流程如图所示。下列化学方程式或离子方程式书写正确的是( )A. 制印刷电路板:Fe3++Cu Fe+Cu2+
B. 电解精炼铜时阳极的电极反应式为Cu2++2e− Cu
高温
C. 生产粗铜时发生的化学反应可能有Cu S+2CuO 4Cu+SO ↑
2 2
D. 青 铜 器 产 生 铜 绿 的 过 程 中 发 生 反 应 的 化 学 方 程 式 为
2Cu+3H O+CO Cu (OH) CO +2H
2 2 2 2 3 2
11.(2024·陕西铜川王益中学高三模拟预测)下列实验操作及现象正确且能得出结论或达到预期实验目的
的是
选
实验操作及现象 预期实验目的或结论
项
证明蛋白质在某些无机盐溶液作
A 向鸡蛋清溶液中加入饱和氯化铵溶液,有沉淀析出
用下发生变性
用洁净干燥的玻璃棒分别蘸取 溶液和 溶液,滴在
B 溶液的酸性更强
pH试纸上,与标准比色卡比较,测得 溶液对应的pH更小
取少量 固体样品溶于蒸馏水,加入足量稀盐酸,再加入
C 证明 固体样品已变质
足量 溶液,有白色沉淀产生
室温下,向一定量饱和 溶液中通入足量 气体,观察 室温下固体在水中的溶解度:
D
到有晶体析出
12.向含a g HNO 的稀溶液中,加入b g铁粉充分反应后全部溶解。已知有 g HNO 被还原,则a∶b不可
3 3
能是( )
A.2∶1 B.3∶1
C.4∶1 D.9∶2
13.工业上以粗盐(含Ca2+、Mg2+、SO等杂质)为主要原料,采用“侯氏制碱法”生产纯碱和化肥NH Cl,
4
实验室模拟工艺流程如图甲所示。下列说法正确的是( )
A.饱和食盐水中先通入的气体为CO
2
B.流程图中的“系列操作”中一定需要使用玻璃棒
C.如图乙所示装置可以比较NaCO 和NaHCO 晶体的热稳定性
2 3 3
D.对粗盐溶液除杂可依次加入过量NaOH、NaCO、BaCl 溶液,过滤后再加入盐酸调节溶液的pH
2 3 2
14.(2024·安徽安庆第一中学高三6月热身考试)软磁材料 可由阳极渣和黄铁矿 制得。阳极渣的
主要成分为 且含有少量Pb、Fe、Cu等元素的化合物。制备流程如下。
25℃时, 。下列说法错误的是
A.X可为稀硫酸
B.滤渣2成分是 和
C.“酸浸”时 中的铁元素转化为 ,该反应中氧化剂与还原剂物质的量之比为3:2
D.利用 替代CaO可优化该流程
15.(2024·辽宁省实验中学调研)一块11.0 g的铁铝合金,加入一定量的稀硫酸后合金完全溶解,然后加
HO 至溶液中无Fe2+存在,加热除去多余的HO ,当加入200 mL 6 mol·L-1NaOH溶液时沉淀量最多,且
2 2 2 2
所得沉淀质量为26.3 g,设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.该合金中铁的质量为5.6 g
B.所加稀硫酸中含1.2 mol HSO
2 4
C.合金与稀硫酸反应共生成0.45 mol H
2
D.该合金与足量氢氧化钠溶液反应,转移的电子数为0.3N
A二、非选择题(本题包括4小题,共55分)
16.(14分)(2024·天津第四中学模拟)硫酸亚铁是重要的化工原料
Ⅰ.(1)由 溶液制备硫酸亚铁晶体的方法是 。检验晶体中 是否完全变质,将晶体
溶于水,加 (填试剂)。
(2) 溶液与过量的 溶液混合,可以得到含 的浊液,离子方程式是 。
Ⅱ.氧化铁黄(FeOOH)是一种黄色颜料,具有非常好的耐光性和耐碱性,是氧化铁的一水合物。以
为原料制备FeOOH的流程如下:
回答下列问题:
(3)若在实验室完成上述制备,不需要使用的仪器是 。
(4)“氧化”时,溶液pH变化记录如下图所示。
① 时段,pH快速下降的原因是反应生成了FeOOH和 ,该反应的化学方程式为 。
② 时段,经历的反应为 ,该过程pH继续平缓下降的原因可能是
。(5)判断流程中产品洗涤干净的方法是 。
(6)氧化铁黄(FeOOH)纯度可以通过产品的耗酸量确定,如下图所示。
已知: , 不与稀碱液反应。
①在溶液c中滴加NaOH标准溶液,使用的指示剂为 。
②若实验时加入了 的 ,消耗 ,设氧化铁黄的摩尔质量为 ,则氧化铁黄样
品纯度为 (用含w、 、 、M的代数式表示)。
③测定时,若滴入 不足量,会使实验结果 (选填“偏大”“偏小”或“无影响”)。
17.(12分)(2024·湖南邵阳检测)镁及其化合物在现代工业、国防建设中有着广泛的应用。回答下列问
题:
(1)单质镁在空气中燃烧的主要产物是白色的________,还生成少量的________(填化学式)。
(2)CH MgCl是一种重要的有机合成试剂,其中镁的化合价为________,CHMgCl水解时除生成甲烷外,
3 3
还生成一种碱和一种盐。写出该反应的化学方程式:
_______________________________________________________________________。
(3)现有一块Al-Mg合金,将其置于烧杯中。若加入20 mL 1 mol·L-1 NaOH溶液,恰好完全反应生成n
1
mol H。若加入20 mL 1 mol·L-1盐酸,则生成n mol H。计算n-n=________。
2 2 2 1 2
(4)Mg(OH) 是常用的阻燃材料。以白云石(CaCO 、MgCO ,不考虑杂质)为原料制备Mg(OH) 和CaCO 的
2 3 3 2 3
工艺流程如下:
①相同条件下,溶解度:Ca(OH) ________(填“>”或“<”)Mg(OH) 。
2 2
②“煅烧”时称取27.6 g白云石,高温加热到质量不再变化,收集到 6.72 L(标准状况下)CO ,若工艺中不
2
考虑Ca、Mg损失,则Mg(OH) 和CaCO 的质量分别为______、________。
2 3
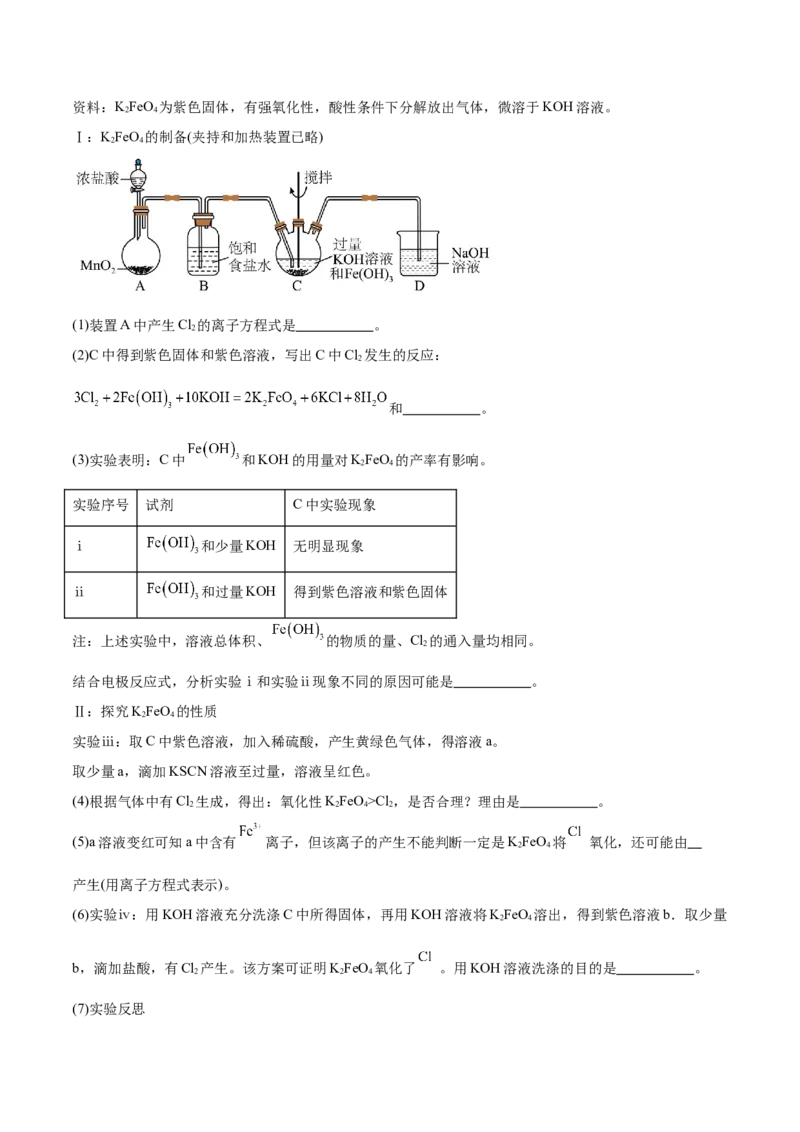
18.(15分)(2024·北京师范大学附属中学高三三模)某小组同学探究高铁酸钾(K FeO)的制备条件及性
2 4
质。资料:KFeO 为紫色固体,有强氧化性,酸性条件下分解放出气体,微溶于KOH溶液。
2 4
Ⅰ:KFeO 的制备(夹持和加热装置已略)
2 4
(1)装置A中产生Cl 的离子方程式是 。
2
(2)C中得到紫色固体和紫色溶液,写出C中Cl 发生的反应:
2
和 。
(3)实验表明:C中 和KOH的用量对KFeO 的产率有影响。
2 4
实验序号 试剂 C中实验现象
ⅰ 和少量KOH 无明显现象
ⅱ 和过量KOH 得到紫色溶液和紫色固体
注:上述实验中,溶液总体积、 的物质的量、Cl 的通入量均相同。
2
结合电极反应式,分析实验ⅰ和实验ⅱ现象不同的原因可能是 。
Ⅱ:探究KFeO 的性质
2 4
实验ⅲ:取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a。
取少量a,滴加KSCN溶液至过量,溶液呈红色。
(4)根据气体中有Cl 生成,得出:氧化性KFeO>Cl,是否合理?理由是 。
2 2 4 2
(5)a溶液变红可知a中含有 离子,但该离子的产生不能判断一定是KFeO 将 氧化,还可能由
2 4
产生(用离子方程式表示)。
(6)实验ⅳ:用KOH溶液充分洗涤C中所得固体,再用KOH溶液将KFeO 溶出,得到紫色溶液b.取少量
2 4
b,滴加盐酸,有Cl 产生。该方案可证明KFeO 氧化了 。用KOH溶液洗涤的目的是 。
2 2 4
(7)实验反思①实验一中装置B的作用是 。
②实验一中得到紫色溶液后,持续通入Cl,观察到溶液紫色变浅。解释可能原因 。
2
19.(14分)(2024·北京第十四中学高三三模).I、工业废水中的氨氮和烟气用多种方法进行处理,使
废水和烟气达标后排放。
(1)氨氮( 和 )胶水的处理过程中加 溶液,调节 至9后,升温至 ,通空气将氨赶
出并回收。
①用离子方程式表示加 溶液的作用: 。
②用化学平衡原理解释通空气的目的: 。
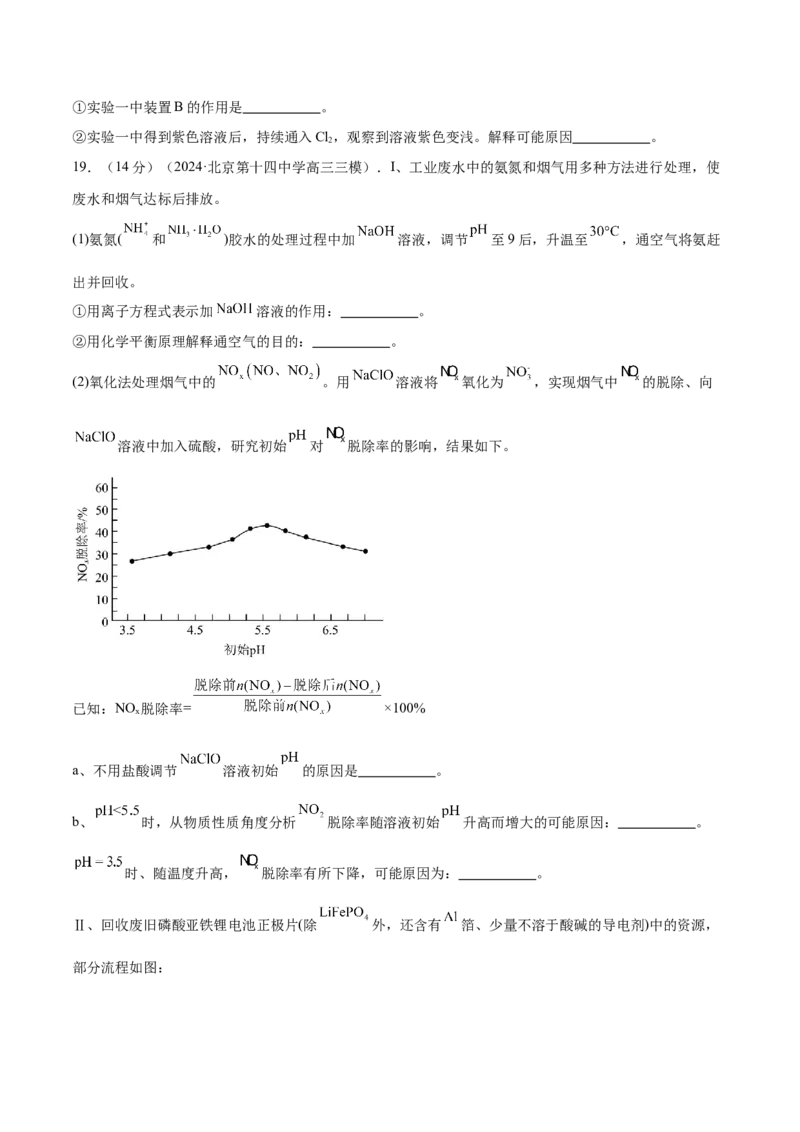
(2)氧化法处理烟气中的 。用 溶液将 氧化为 ,实现烟气中 的脱除、向
溶液中加入硫酸,研究初始 对 脱除率的影响,结果如下。
已知:NO 脱除率= ×100%
x
a、不用盐酸调节 溶液初始 的原因是 。
b、 时,从物质性质角度分析 脱除率随溶液初始 升高而增大的可能原因: 。
时、随温度升高, 脱除率有所下降,可能原因为: 。
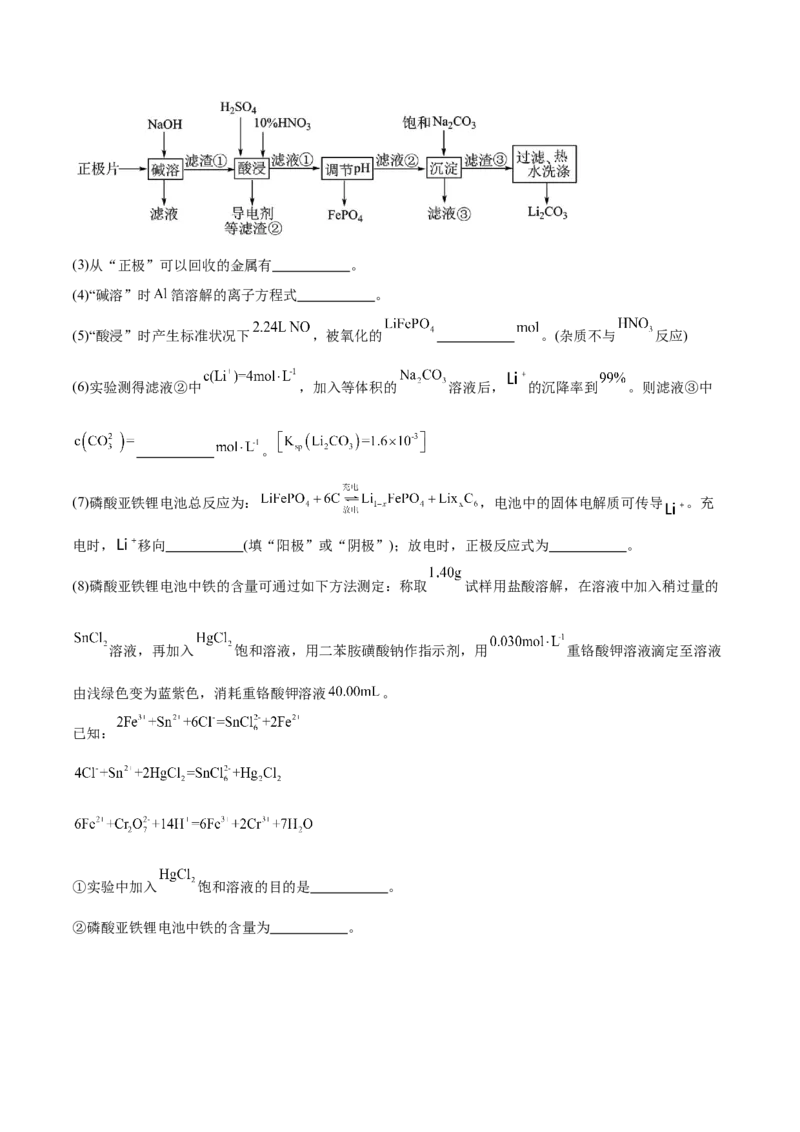
Ⅱ、回收废旧磷酸亚铁锂电池正极片(除 外,还含有 箔、少量不溶于酸碱的导电剂)中的资源,
部分流程如图:(3)从“正极”可以回收的金属有 。
(4)“碱溶”时 箔溶解的离子方程式 。
(5)“酸浸”时产生标准状况下 ,被氧化的 。(杂质不与 反应)
(6)实验测得滤液②中 ,加入等体积的 溶液后, 的沉降率到 。则滤液③中
。
(7)磷酸亚铁锂电池总反应为: ,电池中的固体电解质可传导 。充
电时, 移向 (填“阳极”或“阴极”);放电时,正极反应式为 。
(8)磷酸亚铁锂电池中铁的含量可通过如下方法测定:称取 试样用盐酸溶解,在溶液中加入稍过量的
溶液,再加入 饱和溶液,用二苯胺磺酸钠作指示剂,用 重铬酸钾溶液滴定至溶液
由浅绿色变为蓝紫色,消耗重铬酸钾溶液 。
已知:
①实验中加入 饱和溶液的目的是 。
②磷酸亚铁锂电池中铁的含量为 。