文档内容
9.电解原理及创新应用
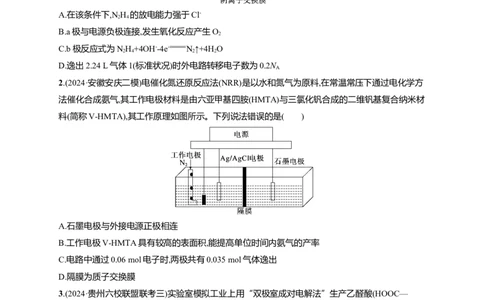
1.(2024·吉林白山二模)大连理工大学提出了一种低能耗、无阳极氯腐蚀的电解混合海水制氢新技术,
如图所示。下列叙述错误的是( )
A.在该条件下,N H 的放电能力强于Cl-
2 4
B.a极与电源负极连接,发生氧化反应产生O
2
C.b极反应式为NH+4OH--4e- N↑+4H O
2 4 2 2
D.逸出2.24 L气体1(标准状况)时外电路转移电子数为0.2N
A
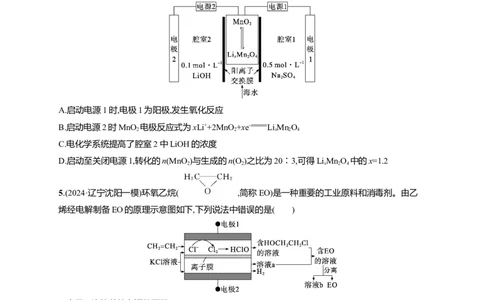
2.(2024·安徽安庆二模)电催化氮还原反应法(NRR)是以水和氮气为原料,在常温常压下通过电化学方
法催化合成氨气,其工作电极材料是由六亚甲基四胺(HMTA)与三氯化钒合成的二维钒基复合纳米材
料(简称V-HMTA),其工作原理如图所示。下列说法错误的是( )
A.石墨电极与外接电源正极相连
B.工作电极V-HMTA具有较高的表面积,能提高单位时间内氨气的产率
C.电路中通过0.06 mol电子时,两极共有0.035 mol气体逸出
D.隔膜为质子交换膜
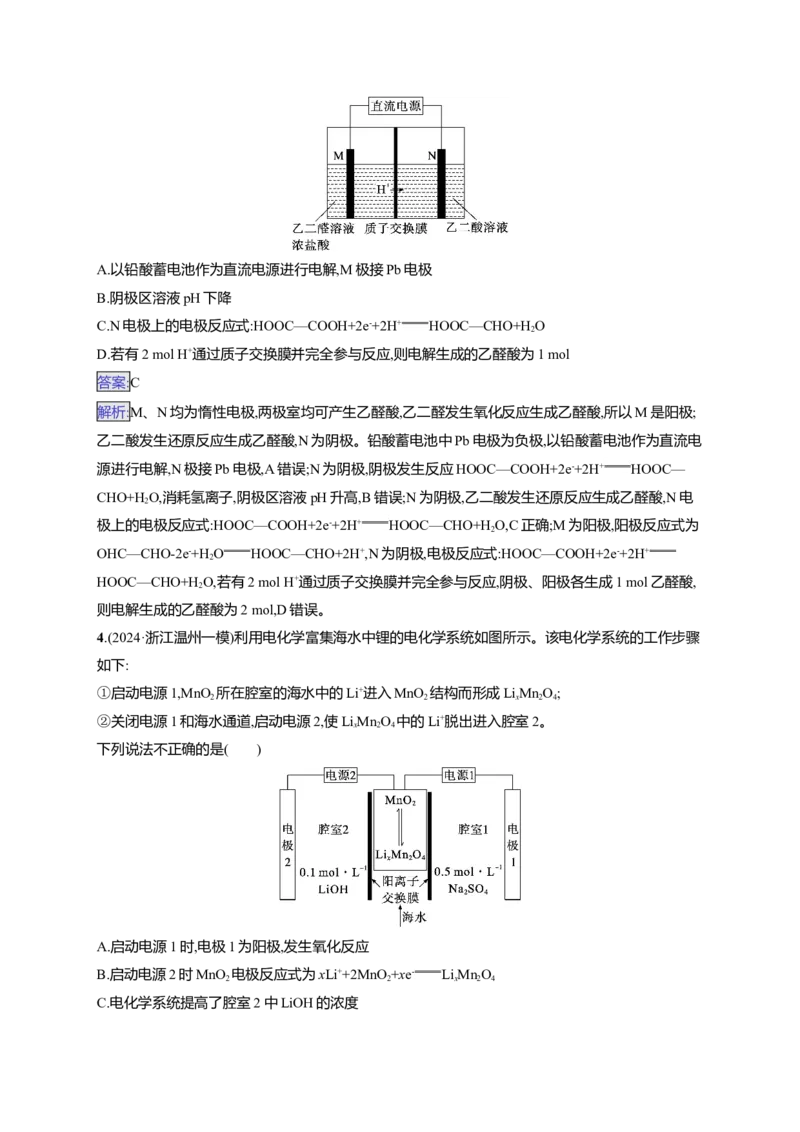
3.(2024·贵州六校联盟联考三)实验室模拟工业上用“双极室成对电解法”生产乙醛酸(HOOC—
CHO),原理如图所示,该装置中M、N均为惰性电极,两极室均可产生乙醛酸。下列说法正确的是(
)A.以铅酸蓄电池作为直流电源进行电解,M极接Pb电极
B.阴极区溶液pH下降
C.N电极上的电极反应式:HOOC—COOH+2e-+2H+ HOOC—CHO+H O
2
D.若有2 mol H+通过质子交换膜并完全参与反应,则电解生成的乙醛酸为1 mol
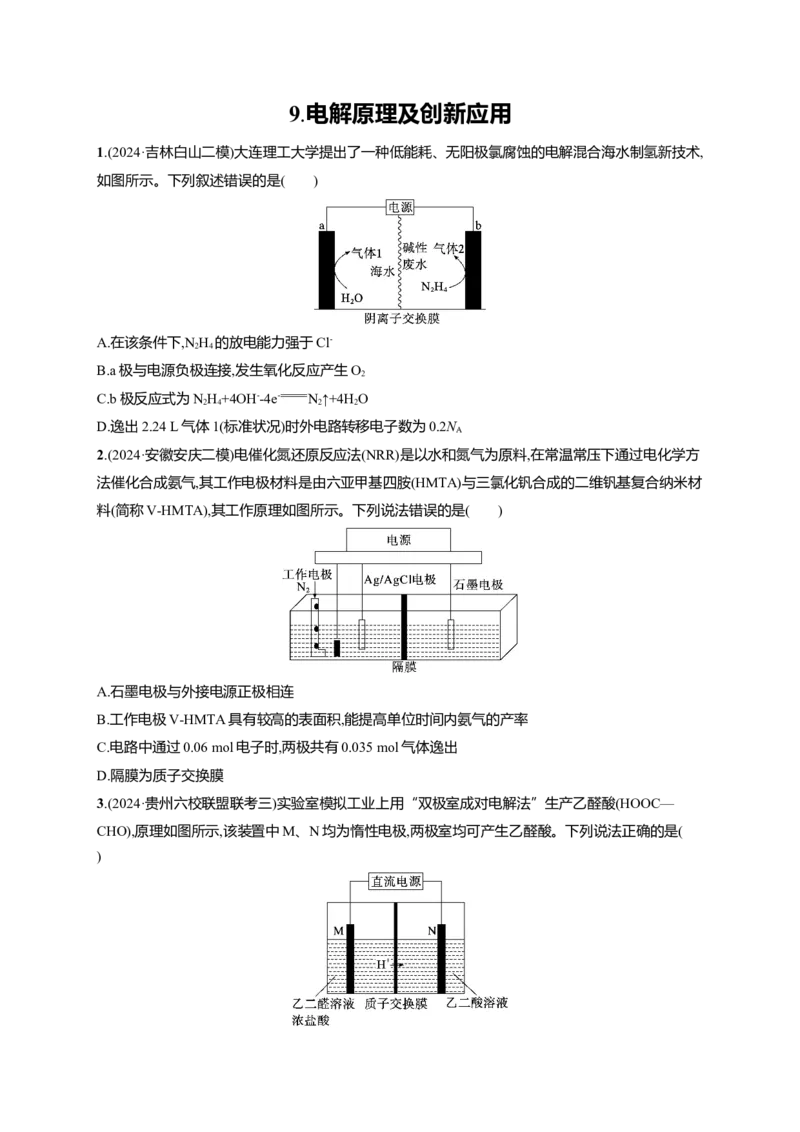
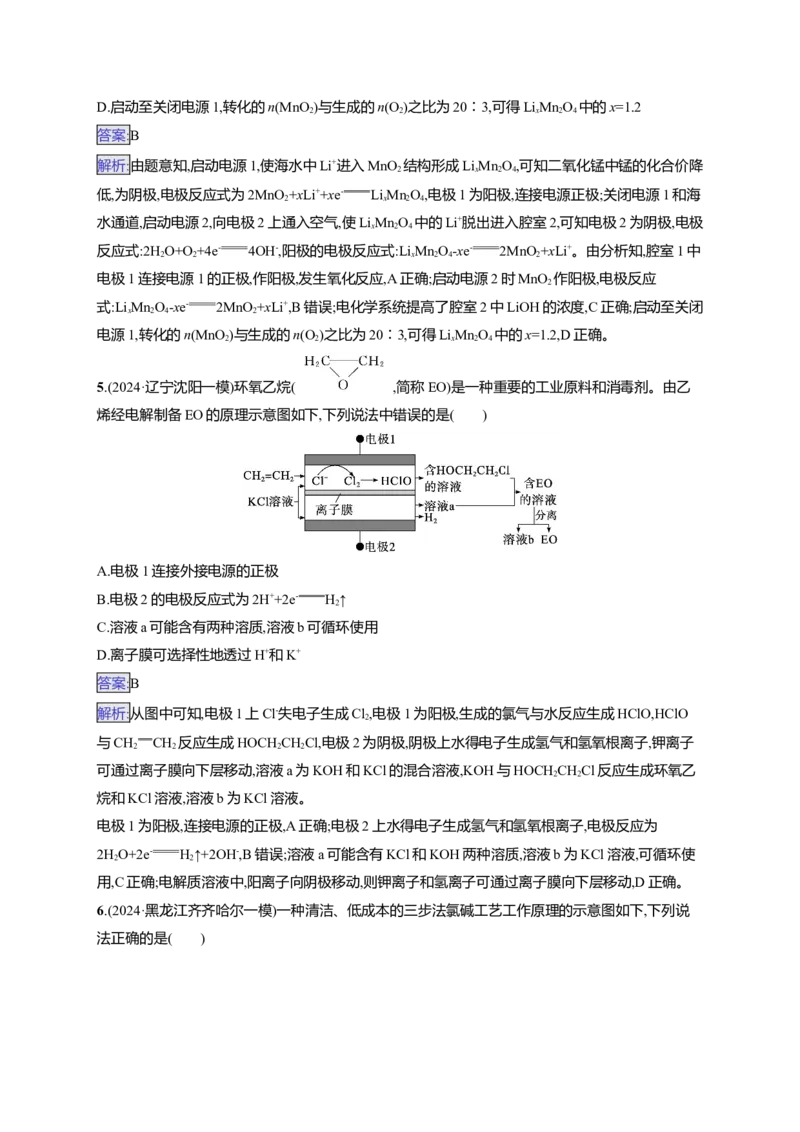
4.(2024·浙江温州一模)利用电化学富集海水中锂的电化学系统如图所示。该电化学系统的工作步骤
如下:①启动电源1,MnO 所在腔室的海水中的Li+进入MnO 结构而形成LiMnO;
2 2 x 2 4
②关闭电源1和海水通道,启动电源2,使LiMnO 中的Li+脱出进入腔室2。
x 2 4
下列说法不正确的是( )
A.启动电源1时,电极1为阳极,发生氧化反应
B.启动电源2时MnO 电极反应式为xLi++2MnO+xe- LiMnO
2 2 x 2 4
C.电化学系统提高了腔室2中LiOH的浓度
D.启动至关闭电源1,转化的n(MnO )与生成的n(O )之比为20∶3,可得LiMnO 中的x=1.2
2 2 x 2 4
5.(2024·辽宁沈阳一模)环氧乙烷( ,简称EO)是一种重要的工业原料和消毒剂。由乙
烯经电解制备EO的原理示意图如下,下列说法中错误的是( )
A.电极1连接外接电源的正极
B.电极2的电极反应式为2H++2e- H↑
2
C.溶液a可能含有两种溶质,溶液b可循环使用
D.离子膜可选择性地透过H+和K+
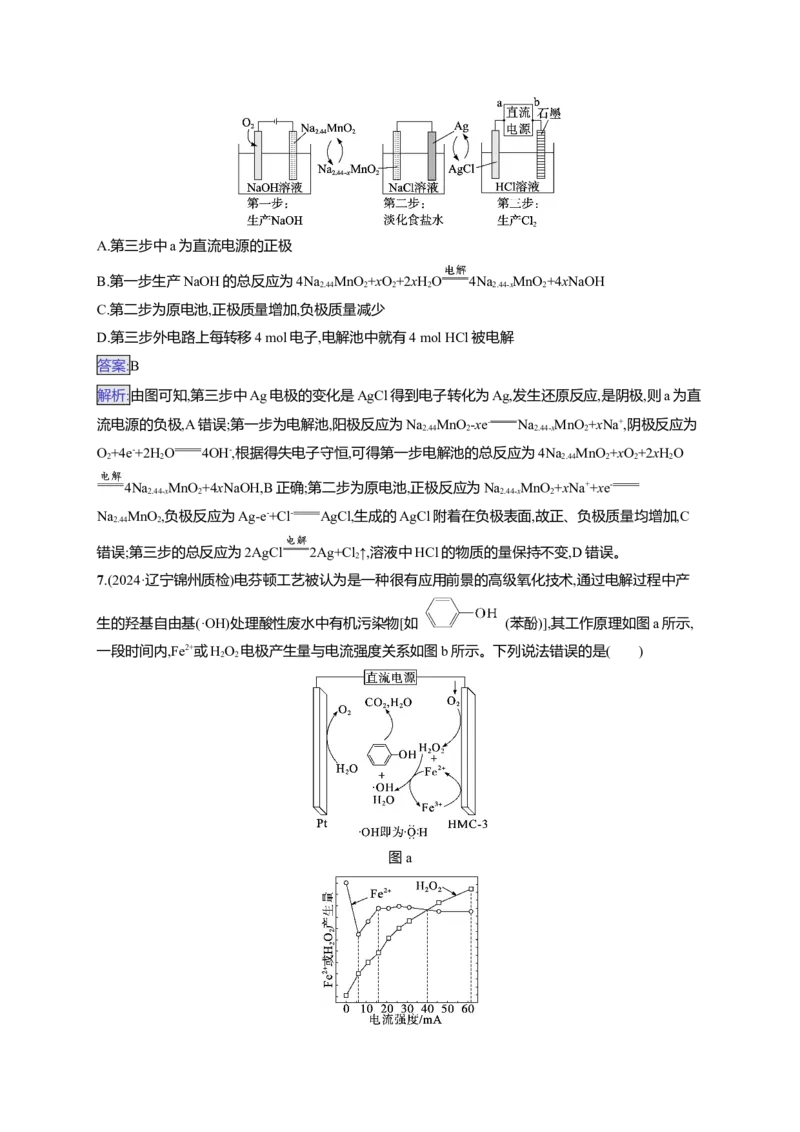
6.(2024·黑龙江齐齐哈尔一模)一种清洁、低成本的三步法氯碱工艺工作原理的示意图如下,下列说
法正确的是( )A.第三步中a为直流电源的正极
B.第一步生产NaOH的总反应为4Na MnO +xO+2xHO 4Na MnO +4xNaOH
2.44 2 2 2 2.44-x 2
C.第二步为原电池,正极质量增加,负极质量减少
D.第三步外电路上每转移4 mol电子,电解池中就有4 mol HCl被电解
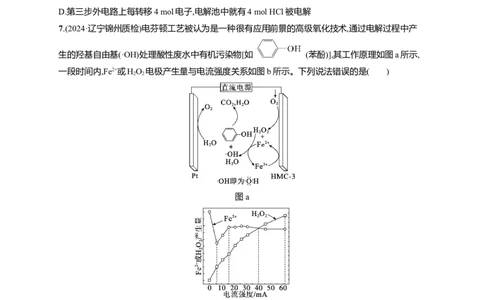
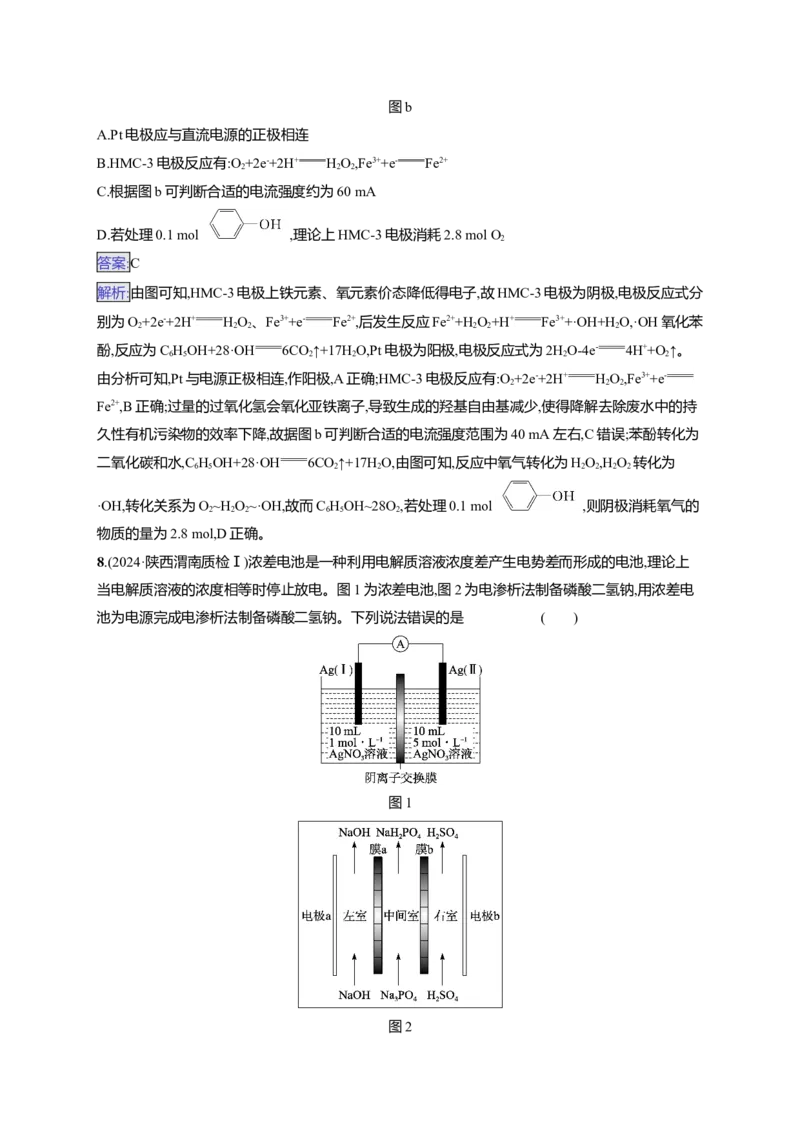
7.(2024·辽宁锦州质检)电芬顿工艺被认为是一种很有应用前景的高级氧化技术,通过电解过程中产
生的羟基自由基(·OH)处理酸性废水中有机污染物[如 (苯酚)],其工作原理如图a所示,
一段时间内,Fe2+或HO 电极产生量与电流强度关系如图b所示。下列说法错误的是( )
2 2
图a
图b
A.Pt电极应与直流电源的正极相连
B.HMC-3电极反应有:O +2e-+2H+ HO,Fe3++e- Fe2+
2 2 2
C.根据图b可判断合适的电流强度约为60 mA
D.若处理0.1 mol ,理论上HMC-3电极消耗2.8 mol O
28.(2024·陕西渭南质检Ⅰ)浓差电池是一种利用电解质溶液浓度差产生电势差而形成的电池,理论上
当电解质溶液的浓度相等时停止放电。图1为浓差电池,图2为电渗析法制备磷酸二氢钠,用浓差电
池为电源完成电渗析法制备磷酸二氢钠。下列说法错误的是 ( )
图1
图2
A.电极a应与Ag(Ⅰ)相连
B.电渗析装置中膜a为阳离子交换膜
C.电渗析过程中左、右室中NaOH和HSO 的浓度均增大
2 4
D.电池从开始到停止放电,理论上可制备1.2 g NaH PO
2 4
9.电解原理及创新应用
1.(2024·吉林白山二模)大连理工大学提出了一种低能耗、无阳极氯腐蚀的电解混合海水制氢新技术,
如图所示。下列叙述错误的是( )
A.在该条件下,N H 的放电能力强于Cl-
2 4
B.a极与电源负极连接,发生氧化反应产生O
2
C.b极反应式为NH+4OH--4e- N↑+4H O
2 4 2 2D.逸出2.24 L气体1(标准状况)时外电路转移电子数为0.2N
A
答案:B
解析:由题干信息可知,无阳极氯腐蚀,故在该条件下,N H 的放电能力强于Cl-,不是氯离子失电子得氯
2 4
气,而是NH 失电子生成N,A正确;该电解池采用电解制氢新技术,结合A选项中分析,b极失电子为
2 4 2
阳极,则a极为阴极,与电源负极连接,气体1为H,发生还原反应:2H O+2e- 2OH-+H ↑,B错误;b极
2 2 2
为阳极,发生氧化反应,N H 失电子生成N,电极反应式正确,C正确;a极反应式为2HO+2e- 2OH-
2 4 2 2
+H ↑,根据电极反应式知,标准状况下,产生0.1 mol H 时外电路转移电子数为0.2N ,D正确。
2 2 A
2.(2024·安徽安庆二模)电催化氮还原反应法(NRR)是以水和氮气为原料,在常温常压下通过电化学方
法催化合成氨气,其工作电极材料是由六亚甲基四胺(HMTA)与三氯化钒合成的二维钒基复合纳米材
料(简称V-HMTA),其工作原理如图所示。下列说法错误的是( )
A.石墨电极与外接电源正极相连
B.工作电极V-HMTA具有较高的表面积,能提高单位时间内氨气的产率
C.电路中通过0.06 mol电子时,两极共有0.035 mol气体逸出
D.隔膜为质子交换膜
答案:D
解析:由题意可知该原理是用电解法将氮气合成氨气,故左侧工作电极为阴极,电极反应式为N+6e-
2
+6H O 2NH +6OH-,右侧石墨电极为阳极,电极反应式为4OH--4e- O↑+2H O。由分析可知工
2 3 2 2
作电极为阴极,石墨电极为阳极,则石墨电极与外接电源正极相连,A正确;工作电极V-HMTA具有较
高的表面积,能吸附氮气,加快反应速率,从而提高单位时间内氨气的产率,B正确;阴极电极反应式为
N+6e-+6H O 2NH +6OH-,阳极电极反应式为4OH--4e- O↑+2H O,电路中通过0.06 mol电子时,
2 2 3 2 2
阴极产生0.02 mol气体,阳极产生0.015 mol气体,两极共产生0.035 mol气体,C正确;结合电极反应式
可知隔膜为允许氢氧根离子通过的阴离子交换膜,D错误。
3.(2024·贵州六校联盟联考三)实验室模拟工业上用“双极室成对电解法”生产乙醛酸(HOOC—
CHO),原理如图所示,该装置中M、N均为惰性电极,两极室均可产生乙醛酸。下列说法正确的是(
)A.以铅酸蓄电池作为直流电源进行电解,M极接Pb电极
B.阴极区溶液pH下降
C.N电极上的电极反应式:HOOC—COOH+2e-+2H+ HOOC—CHO+H O
2
D.若有2 mol H+通过质子交换膜并完全参与反应,则电解生成的乙醛酸为1 mol
答案:C
解析:M、N均为惰性电极,两极室均可产生乙醛酸,乙二醛发生氧化反应生成乙醛酸,所以M是阳极;
乙二酸发生还原反应生成乙醛酸,N为阴极。铅酸蓄电池中Pb电极为负极,以铅酸蓄电池作为直流电
源进行电解,N极接Pb电极,A错误;N为阴极,阴极发生反应HOOC—COOH+2e-+2H+ HOOC—
CHO+H O,消耗氢离子,阴极区溶液pH升高,B错误;N为阴极,乙二酸发生还原反应生成乙醛酸,N电
2
极上的电极反应式:HOOC—COOH+2e-+2H+ HOOC—CHO+H O,C正确;M为阳极,阳极反应式为
2
OHC—CHO-2e-+H O HOOC—CHO+2H+,N为阴极,电极反应式:HOOC—COOH+2e-+2H+
2
HOOC—CHO+H O,若有2 mol H+通过质子交换膜并完全参与反应,阴极、阳极各生成1 mol乙醛酸,
2
则电解生成的乙醛酸为2 mol,D错误。
4.(2024·浙江温州一模)利用电化学富集海水中锂的电化学系统如图所示。该电化学系统的工作步骤
如下:
①启动电源1,MnO 所在腔室的海水中的Li+进入MnO 结构而形成LiMnO;
2 2 x 2 4
②关闭电源1和海水通道,启动电源2,使LiMnO 中的Li+脱出进入腔室2。
x 2 4
下列说法不正确的是( )
A.启动电源1时,电极1为阳极,发生氧化反应
B.启动电源2时MnO 电极反应式为xLi++2MnO+xe- LiMnO
2 2 x 2 4
C.电化学系统提高了腔室2中LiOH的浓度D.启动至关闭电源1,转化的n(MnO )与生成的n(O )之比为20∶3,可得LiMnO 中的x=1.2
2 2 x 2 4
答案:B
解析:由题意知,启动电源1,使海水中Li+进入MnO 结构形成LiMnO,可知二氧化锰中锰的化合价降
2 x 2 4
低,为阴极,电极反应式为2MnO +xLi++xe- LiMnO,电极1为阳极,连接电源正极;关闭电源1和海
2 x 2 4
水通道,启动电源2,向电极2上通入空气,使LiMnO 中的Li+脱出进入腔室2,可知电极2为阴极,电极
x 2 4
反应式:2H O+O+4e- 4OH-,阳极的电极反应式:LiMnO-xe- 2MnO +xLi+。由分析知,腔室1中
2 2 x 2 4 2
电极1连接电源1的正极,作阳极,发生氧化反应,A正确;启动电源2时MnO 作阳极,电极反应
2
式:LiMnO-xe- 2MnO +xLi+,B错误;电化学系统提高了腔室2中LiOH的浓度,C正确;启动至关闭
x 2 4 2
电源1,转化的n(MnO )与生成的n(O )之比为20∶3,可得LiMnO 中的x=1.2,D正确。
2 2 x 2 4
5.(2024·辽宁沈阳一模)环氧乙烷( ,简称EO)是一种重要的工业原料和消毒剂。由乙
烯经电解制备EO的原理示意图如下,下列说法中错误的是( )
A.电极1连接外接电源的正极
B.电极2的电极反应式为2H++2e- H↑
2
C.溶液a可能含有两种溶质,溶液b可循环使用
D.离子膜可选择性地透过H+和K+
答案:B
解析:从图中可知,电极1上Cl-失电子生成Cl,电极1为阳极,生成的氯气与水反应生成HClO,HClO
2
与CH CH 反应生成HOCH CHCl,电极2为阴极,阴极上水得电子生成氢气和氢氧根离子,钾离子
2 2 2 2
可通过离子膜向下层移动,溶液a为KOH和KCl的混合溶液,KOH与HOCH CHCl反应生成环氧乙
2 2
烷和KCl溶液,溶液b为KCl溶液。
电极1为阳极,连接电源的正极,A正确;电极2上水得电子生成氢气和氢氧根离子,电极反应为
2HO+2e- H↑+2OH-,B错误;溶液a可能含有KCl和KOH两种溶质,溶液b为KCl溶液,可循环使
2 2
用,C正确;电解质溶液中,阳离子向阴极移动,则钾离子和氢离子可通过离子膜向下层移动,D正确。
6.(2024·黑龙江齐齐哈尔一模)一种清洁、低成本的三步法氯碱工艺工作原理的示意图如下,下列说
法正确的是( )A.第三步中a为直流电源的正极
B.第一步生产NaOH的总反应为4Na MnO +xO+2xHO 4Na MnO +4xNaOH
2.44 2 2 2 2.44-x 2
C.第二步为原电池,正极质量增加,负极质量减少
D.第三步外电路上每转移4 mol电子,电解池中就有4 mol HCl被电解
答案:B
解析:由图可知,第三步中Ag电极的变化是AgCl得到电子转化为Ag,发生还原反应,是阴极,则a为直
流电源的负极,A错误;第一步为电解池,阳极反应为Na MnO -xe- Na MnO +xNa+,阴极反应为
2.44 2 2.44-x 2
O+4e-+2H O 4OH-,根据得失电子守恒,可得第一步电解池的总反应为4Na MnO +xO+2xHO
2 2 2.44 2 2 2
4Na MnO +4xNaOH,B正确;第二步为原电池,正极反应为Na MnO +xNa++xe-
2.44-x 2 2.44-x 2
Na MnO ,负极反应为Ag-e-+Cl- AgCl,生成的AgCl附着在负极表面,故正、负极质量均增加,C
2.44 2
错误;第三步的总反应为2AgCl 2Ag+Cl ↑,溶液中HCl的物质的量保持不变,D错误。
2
7.(2024·辽宁锦州质检)电芬顿工艺被认为是一种很有应用前景的高级氧化技术,通过电解过程中产
生的羟基自由基(·OH)处理酸性废水中有机污染物[如 (苯酚)],其工作原理如图a所示,
一段时间内,Fe2+或HO 电极产生量与电流强度关系如图b所示。下列说法错误的是( )
2 2
图a图b
A.Pt电极应与直流电源的正极相连
B.HMC-3电极反应有:O +2e-+2H+ HO,Fe3++e- Fe2+
2 2 2
C.根据图b可判断合适的电流强度约为60 mA
D.若处理0.1 mol ,理论上HMC-3电极消耗2.8 mol O
2
答案:C
解析:由图可知,HMC-3电极上铁元素、氧元素价态降低得电子,故HMC-3电极为阴极,电极反应式分
别为O+2e-+2H+ HO、Fe3++e- Fe2+,后发生反应Fe2++H O+H+ Fe3++·OH+HO,·OH氧化苯
2 2 2 2 2 2
酚,反应为C HOH+28·OH 6CO↑+17H O,Pt电极为阳极,电极反应式为2HO-4e- 4H++O ↑。
6 5 2 2 2 2
由分析可知,Pt与电源正极相连,作阳极,A正确;HMC-3电极反应有:O +2e-+2H+ HO,Fe3++e-
2 2 2
Fe2+,B正确;过量的过氧化氢会氧化亚铁离子,导致生成的羟基自由基减少,使得降解去除废水中的持
久性有机污染物的效率下降,故据图b可判断合适的电流强度范围为40 mA左右,C错误;苯酚转化为
二氧化碳和水,C HOH+28·OH 6CO↑+17H O,由图可知,反应中氧气转化为HO,H O 转化为
6 5 2 2 2 2 2 2
·OH,转化关系为O~H O~·OH,故而C HOH~28O ,若处理0.1 mol ,则阴极消耗氧气的
2 2 2 6 5 2
物质的量为2.8 mol,D正确。
8.(2024·陕西渭南质检Ⅰ)浓差电池是一种利用电解质溶液浓度差产生电势差而形成的电池,理论上
当电解质溶液的浓度相等时停止放电。图1为浓差电池,图2为电渗析法制备磷酸二氢钠,用浓差电
池为电源完成电渗析法制备磷酸二氢钠。下列说法错误的是 ( )
图1
图2A.电极a应与Ag(Ⅰ)相连
B.电渗析装置中膜a为阳离子交换膜
C.电渗析过程中左、右室中NaOH和HSO 的浓度均增大
2 4
D.电池从开始到停止放电,理论上可制备1.2 g NaH PO
2 4
答案:D
解析:浓差电池是一种利用电解质溶液浓度差产生电势差而形成的电池,由于右侧AgNO 浓度大,则
3
Ag(Ⅰ)为负极,Ag(Ⅱ)正极;电渗析法制备磷酸二氢钠,右室中的氢离子通过膜b进入中间室,中间室中
的钠离子通过膜a进入左室,则电极a为阴极,电极b为阳极。电极a应与Ag(Ⅰ)相连,A正确。中间
室中的钠离子通过膜a进入左室,膜a为阳离子交换膜,B正确。阳极中的水失电子电解生成氧气和
氢离子,氢离子通过膜b进入中间室,消耗水,硫酸的浓度增大;阴极水得电子电解生成氢气,中间室中
的钠离子通过膜a进入左室,左室NaOH的浓度增大,C正确。电池从开始到停止放电时,浓差电池两
边AgNO 浓度相等,所以正极析出0.025 mol银,电路中转移0.025 mol电子,电渗析装置生成0.012 5
3
mol NaHPO ,质量为1.5 g,D错误。
2 4