文档内容
第 19 讲 硫及其氧化物
[复习目标] 1.了解硫的存在及其单质的性质和用途。2.掌握硫的氧化物的主要性质及应用。
3.了解空气中SO 的测定及治理。
2
考点一 硫单质的性质
1.硫元素的存在形态
2.硫单质的物理性质
溶解性
俗称 颜色状态
水 酒精 CS
2
硫黄 ______晶体 微溶
思考 (1)硫有S 、S 、S 、S 等多种单质,它们的关系是什么?加热时,S 转化为S 、
2 4 6 8 8 6
S、S 属于什么变化?
4 2
_______________________________________________________________________________
(2)硫单质难溶于水,易溶于CS,其原因是什么?
2
_______________________________________________________________________________
_______________________________________________________________________________
3.从化合价的角度认识硫单质的化学性质
S ←―――――→S1.硫在空气中燃烧的产物是SO ,在纯氧中燃烧的产物是SO ( )
2 3
2.硫与铁粉和铜粉分别反应,都可生成二价金属硫化物( )
硫及多硫化物的性质
1.在下列反应中硫元素只表现氧化性的是( )
A.2Al+3S=====Al S
2 3
B.S+2HSO (浓)=====2HO+3SO ↑
2 4 2 2
C.HS=====H+S
2 2
D.3S+6NaOH=====2NaS+NaSO +3HO
2 2 3 2
2.硫元素最常见和最稳定的一种同素异形体是黄色的正交 α-型,1912年E.Beckmann由硫
在碘中的冰点降低法测得它含有S 分子。1891年,M.R.Engel用浓盐酸和硫代硫酸盐的饱和
8
溶液在0 ℃下作用首次制得了一种菱形的ε-硫,后来证明含有S 分子。下列说法正确的是(
6
)
A.S 和S 分子都是由S原子组成,所以它们是一种物质
6 8
B.S 和S 分子分别与铁粉反应,所得产物不同
6 8
C.S 和S 分子分别与过量的氧气反应可以得到SO
6 8 3
D.等质量的S 和S 分子分别与足量的KOH溶液反应,消耗KOH的物质的量相同
6 8
3.单质硫与可溶性硫化物溶液作用生成多硫化物,如NaS(aq)+(x-1)S===NaS(x一般为2
2 2 x
~6);多硫化物在酸性溶液中不稳定,易歧化;As S +2NaS(aq)===As S +2NaS。下列说
2 3 2 2 2 5 2
法错误的是( )
A.As S (其中As显+3价)是多硫化物
2 3
B.As S 是氧化产物
2 5
C.NaS 中阴、阳离子个数比为1∶2
2 2
D.久置NaS溶液遇酸可能变浑浊
2
考点二 二氧化硫和三氧化硫
1.二氧化硫
(1)物理性质
色、味、态 密度 溶解性
____色、______________气味 ____溶于水,通常状况下,1体
比空气的____
的____________ 积的水溶解约____体积的SO
2(2)化学性质
按要求完成下列化学方程式:
SO
2
(3)实验室制法
①固体NaSO 与较浓HSO 反应,化学方程式为___________________________________。
2 3 2 4
②铜与浓HSO 混合加热,化学方程式为___________________________________________。
2 4
2.三氧化硫
(1)物理性质
熔点:16.8 ℃,沸点:44.8 ℃,常温常压下为____态,标准状况下为____态。
(2)化学性质
三氧化硫具有酸性氧化物的通性,主要反应如下:
3.硫的氧化物对环境的影响
(1)硫的氧化物的来源、危害及治理
(2)硫酸型酸雨的形成过程
4.三类漂白剂的比较
类型 原理 举例 特点
将有机色质内部“生色团”破 次氯酸及盐、过氧
氧化型 不可逆、持久
坏掉 化物、O 等
2
与有色物质内部“生色团”
加合型 SO 可逆、不持久
2
“化合”成无色物质
吸附型 将有色物质吸附而褪色 活性炭 物理变化1.标准状况下,2.24 L SO 中含有硫原子数为N ( )
3 A
2.将SO 通入紫色石蕊溶液中,紫色石蕊溶液先变红后褪色( )
2
3.SO 使滴有酚酞的NaOH溶液褪色,体现了SO 的漂白性( )
2 2
4.SO 和Cl 等物质的量混合后通入装有湿润的有色布条的集气瓶中,漂白效果更好( )
2 2
5.SO 、漂白粉、活性炭、NaO 都能使红墨水褪色,其原理相同( )
2 2 2
一、SO 的制取与性质探究
2
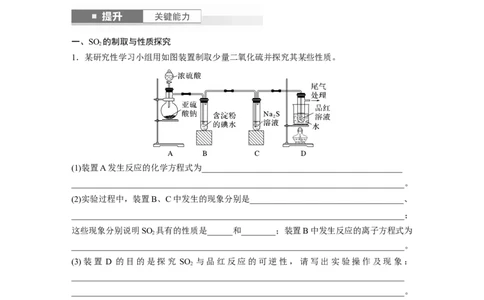
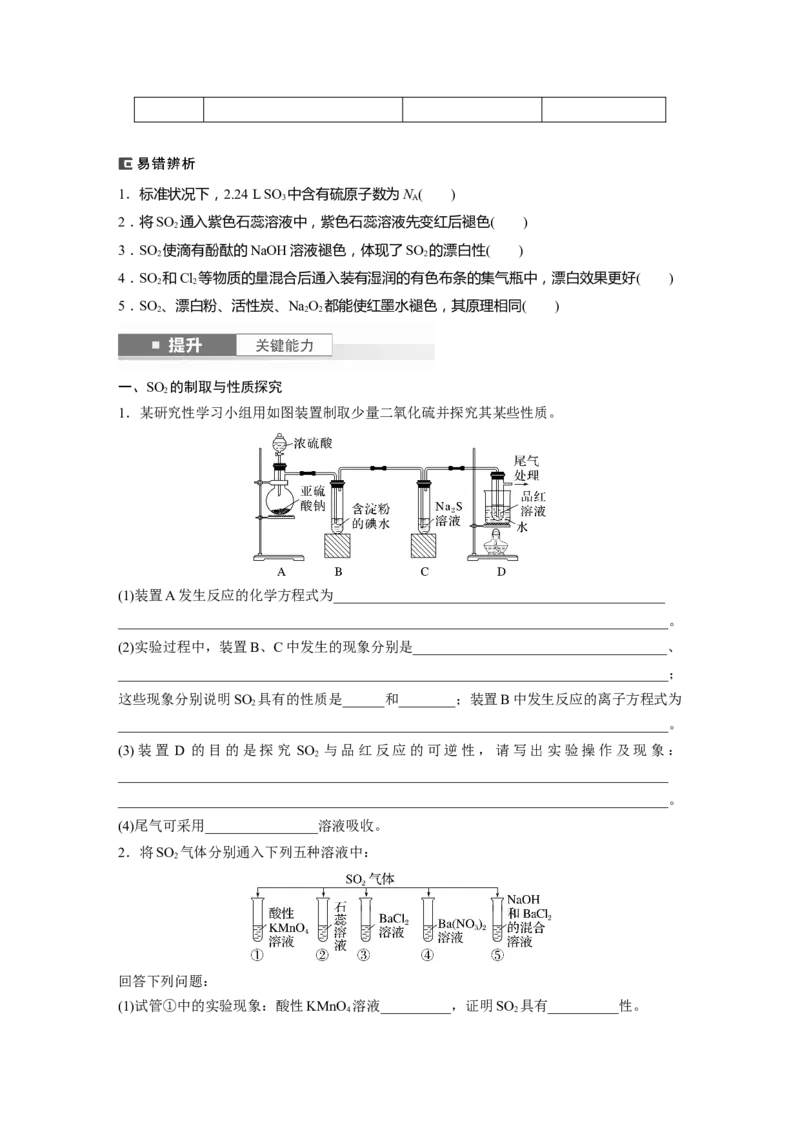
1.某研究性学习小组用如图装置制取少量二氧化硫并探究其某些性质。
(1)装置A发生反应的化学方程式为_______________________________________________
______________________________________________________________________________。
(2)实验过程中,装置B、C中发生的现象分别是____________________________________、
______________________________________________________________________________;
这些现象分别说明SO 具有的性质是______和________;装置B中发生反应的离子方程式为
2
______________________________________________________________________________。
(3)装置 D 的目的是探究 SO 与品红反应的可逆性,请写出实验操作及现象:
2
______________________________________________________________________________
______________________________________________________________________________。
(4)尾气可采用________________溶液吸收。
2.将SO 气体分别通入下列五种溶液中:
2
回答下列问题:
(1)试管①中的实验现象:酸性KMnO 溶液__________,证明SO 具有__________性。
4 2(2)试管②中的实验现象:石蕊溶液________________________________________________。
(3) 试 管 ③ 中 ______________________________________________________________( 填
“能”或“否”)观察到
沉淀。
(4)试管④中能产生白色沉淀,该沉淀是______(填化学式,下同)。
(5)试管⑤中能产生白色沉淀,该沉淀是____________________________________________,
用离子方程式表示产生沉淀的过程:_______________________________________________
______________________________________________________________________________。
二、CO、SO 混合气体中各成分的检验
2 2
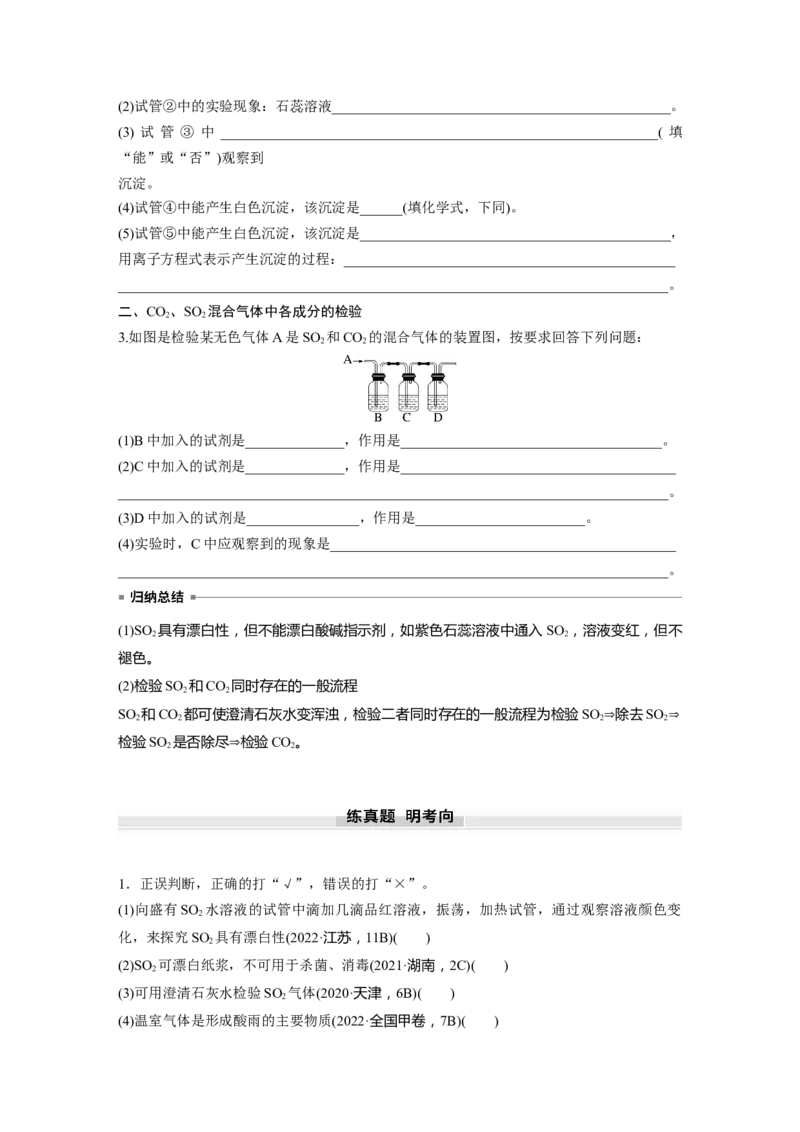
3.如图是检验某无色气体A是SO 和CO 的混合气体的装置图,按要求回答下列问题:
2 2
(1)B中加入的试剂是______________,作用是_____________________________________。
(2)C中加入的试剂是______________,作用是_______________________________________
______________________________________________________________________________。
(3)D中加入的试剂是________________,作用是________________________。
(4)实验时,C中应观察到的现象是_________________________________________________
______________________________________________________________________________。
(1)SO 具有漂白性,但不能漂白酸碱指示剂,如紫色石蕊溶液中通入SO ,溶液变红,但不
2 2
褪色。
(2)检验SO 和CO 同时存在的一般流程
2 2
SO 和CO 都可使澄清石灰水变浑浊,检验二者同时存在的一般流程为检验SO ⇒除去SO ⇒
2 2 2 2
检验SO 是否除尽⇒检验CO。
2 2
1.正误判断,正确的打“√”,错误的打“×”。
(1)向盛有SO 水溶液的试管中滴加几滴品红溶液,振荡,加热试管,通过观察溶液颜色变
2
化,来探究SO 具有漂白性(2022·江苏,11B)( )
2
(2)SO 可漂白纸浆,不可用于杀菌、消毒(2021·湖南,2C)( )
2
(3)可用澄清石灰水检验SO 气体(2020·天津,6B)( )
2
(4)温室气体是形成酸雨的主要物质(2022·全国甲卷,7B)( )(5)用石灰石-石膏法对燃煤烟气进行脱硫,同时可得到石膏(2022·浙江6月选考,8D)( )
(6)燃煤中加入CaO可以减少酸雨的形成及温室气体的排放(2017·全国卷Ⅲ,7C)( )
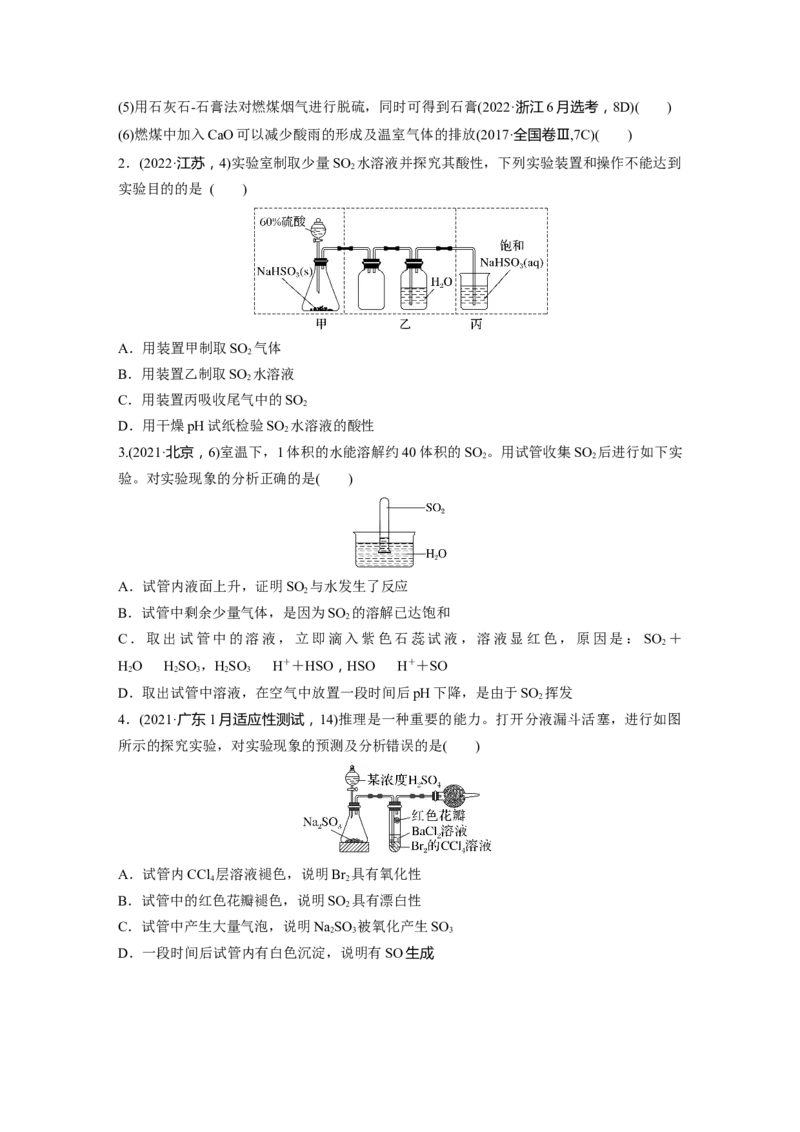
2.(2022·江苏,4)实验室制取少量SO 水溶液并探究其酸性,下列实验装置和操作不能达到
2
实验目的的是 ( )
A.用装置甲制取SO 气体
2
B.用装置乙制取SO 水溶液
2
C.用装置丙吸收尾气中的SO
2
D.用干燥pH试纸检验SO 水溶液的酸性
2
3.(2021·北京,6)室温下,1体积的水能溶解约40体积的SO 。用试管收集SO 后进行如下实
2 2
验。对实验现象的分析正确的是( )
A.试管内液面上升,证明SO 与水发生了反应
2
B.试管中剩余少量气体,是因为SO 的溶解已达饱和
2
C.取出试管中的溶液,立即滴入紫色石蕊试液,溶液显红色,原因是:SO +
2
HOHSO ,HSO H++HSO,HSOH++SO
2 2 3 2 3
D.取出试管中溶液,在空气中放置一段时间后pH下降,是由于SO 挥发
2
4.(2021·广东1月适应性测试,14)推理是一种重要的能力。打开分液漏斗活塞,进行如图
所示的探究实验,对实验现象的预测及分析错误的是( )
A.试管内CCl 层溶液褪色,说明Br 具有氧化性
4 2
B.试管中的红色花瓣褪色,说明SO 具有漂白性
2
C.试管中产生大量气泡,说明NaSO 被氧化产生SO
2 3 3
D.一段时间后试管内有白色沉淀,说明有SO生成