文档内容
微专题突破6 无机化工流程题透视一
1.(2023·江苏)VO -WO/TiO 催化剂能催化NH 脱除烟气中的NO,反应为4NH (g)+O(g)
2 5 3 2 3 3 2
+4NO(g)=4N(g)+6HO(g) ΔH=-1 632.4 kJ·mol-1。
2 2
废催化剂的回收。回收VO-WO/TiO 废催化剂并制备NH VO 的过程可表示为:
2 5 3 2 4 3
①酸浸时,加料完成后,以一定速率搅拌反应。提高钒元素浸出率的方法还有
____________________________________________________________________________。
【答案】适当增加酸的浓度、升高温度、延长酸浸时间等
【解析】提高钒元素浸出率的方法还有适当增加酸的浓度、升高温度、延长酸浸时间等。
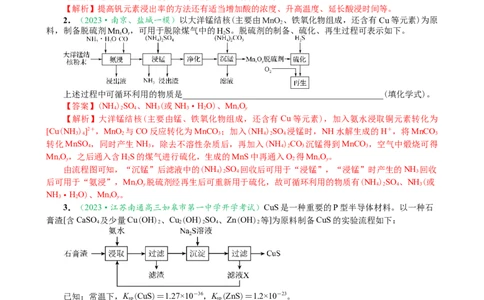
2.(2023·南京、盐城一模)以大洋锰结核(主要由MnO 、铁氧化物组成,还含有Cu等元素)为原
2
料,制备脱硫剂MnO,可用于脱除煤气中的HS。脱硫剂的制备、硫化、再生过程可表示如下。
x y 2
上述过程中可循环利用的物质是_______________________________________________(填化学式)。
【答案】(NH )SO 、NH (或NH ·HO)、MnO
4 2 4 3 3 2 x y
【解析】大洋锰结核(主要由锰、铁氧化物组成,还含有Cu等元素),加入氨水浸取铜元素转化为
[Cu(NH )]2+,MnO 与CO反应转化为MnCO ;加入(NH )SO 浸锰时,NH水解生成的H+,将MnCO
3 4 2 3 4 2 4 3
转化MnSO ,同时产生NH ,除去不溶性杂质后,再加入(NH )CO 沉锰得到MnCO ,空气中煅烧可得
4 3 4 2 3 3
MnO,之后通入含HS的煤气进行硫化,生成的MnS中再通入O 得MnO。
x y 2 2 x y
由流程图可知,“沉锰”后滤液中的(NH )SO 回收后可用于“浸锰”,“浸锰”时产生的NH 回收
4 2 4 3
后可用于“氨浸”,MnO 脱硫剂经再生后可重新用于硫化,故可循环利用的物质有(NH )SO 、NH (或
x y 4 2 4 3
NH ·HO)、MnO。
3 2 x y
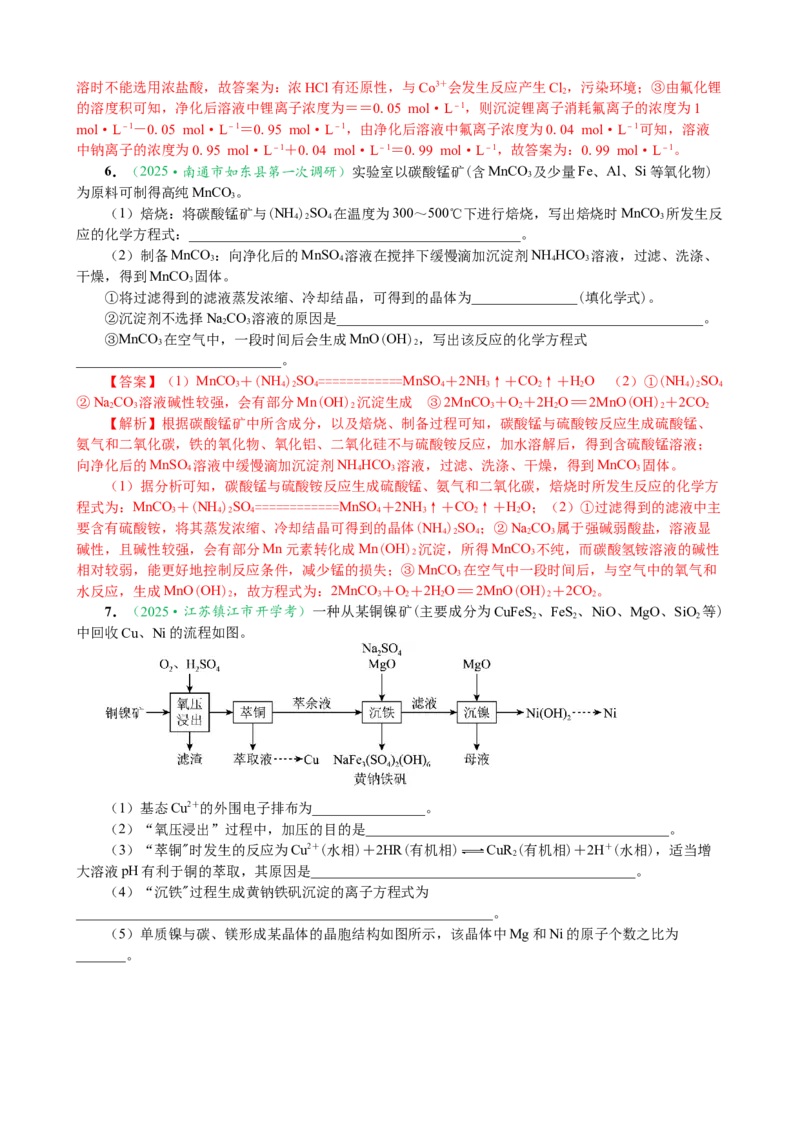
3.(2023·江苏南通高三如皋市第一中学开学考试)CuS是一种重要的P型半导体材料。以一种石
膏渣[含CaSO 及少量Cu(OH)、Cu (OH)SO 、Zn(OH) 等]为原料制备CuS的实验流程如下:
4 2 2 2 4 2
已知:常温下,K (CuS)=1.27×10-36,K (ZnS)=1.2×10-23。
sp sp
(1)“浸取”时,生成[Cu(NH )]2+与[Zn(NH )]2+等。Cu (OH)SO 参加反应的离子方程式为
3 4 3 4 2 2 4
_____________________________________________________________。
(2)“沉淀”时NaS溶液的用量不宜过多,其原因是
2
____________________________________________________________。
(3)循环“浸取”多次后,“滤液X”中浓度增大的阳离子主要有________________________。
【答案】(1)Cu (OH)SO +8NH =2[Cu(NH )]2++SO 2-+2OH- (2)生成的CuS沉淀中会混
2 2 4 3 3 4 4
有ZnS沉淀 (3)[Cu(NH )]2+和Na+
3 4
【解析】以一种石膏渣[含CaSO 及少量Cu(OH)、Cu (OH)SO 、Zn(OH) 等]为原料制备CuS,石
4 2 2 2 4 2
膏渣加入过量氨水浸取,Cu(OH)、Cu (OH)SO 、Zn(OH)“浸取”时生成[Cu(NH )]2+与[Zn(NH )]2+
2 2 2 4 2 3 4 3 4
等,同时生成氢氧化钙,过滤除去氢氧化钙,滤液加入NaS溶液,使Cu2+生成CuS沉淀,过滤得到
2
CuS,滤液可以循环利用,据此解答。微专题突破6 无机化工流程题透一
(1)Cu (OH) SO 反应生成[Cu(NH )]2+,离子方程式为Cu (OH)SO +8NH =2[Cu(NH )]2++
2 2 4 3 4 2 2 4 3 3 4
SO 2-+2OH-;(2)常温下,K (CuS)=1.27×10-36,K (ZnS)=1.2×10-23,“沉淀”时NaS溶液的用
4 sp sp 2
量不宜过多,硫离子浓度过大会生成ZnS沉淀,故其原因是生成的CuS沉淀中会混有ZnS沉淀;(3)结
合制备流程,[Zn(NH )]2+在滤液X中,且加入了NaS,引入了钠离子,故循环“浸取”多次后,“滤
3 4 2
液X”中浓度增大的阳离子主要有[Zn(NH )]2+和Na+。
3 4
4.(2024·江苏卷)回收磁性合金钕铁硼(Nd Fe B)可制备半导体材料铁酸铋和光学材料氧化钕。
2 14
含铁滤渣用硫酸溶解,经萃取、反萃取提纯后,用于制备铁酸铋。
①用含有机胺(R N)的有机溶剂作为萃取剂提纯一定浓度的Fe (SO ) 溶液,原理为:
3 2 4 3
(R NH)SO +Fe3++SO 2-+HO H++(R NH)Fe(OH)(SO )(有机层)
3 2 4 4 2 3 2 4 2
已知:(R NH)SO +H++HSO - 2(R NH•HSO )
3 2 4 4 3 4
其他条件不变,水层初始pH在0.2~0.8范围内,随水层pH增大,有机层中Fe元素含量迅速增多
的原因是___________________________________________________________________________________
___________________________________________________________________________________________
___________________________________________________________________________________________
_________________________________________________________________________________________。
【答案】①随水层pH增大,H+的浓度减小,(R NH)SO +Fe3++SO 2-+HO H++
3 2 4 4 2
(R NH)Fe(OH)(SO ) 的化学平衡向正反应方向移动,(R NH)SO +H++HSO - 2(R NH•HSO )的
3 2 4 2 3 2 4 4 3 4
化学平衡逆向移动,该平衡逆向移动引起(R NH)SO 浓度的增大,进一步促进萃取平衡向萃取方向移动,
3 2 4
导致(R NH)Fe(OH)(SO ) 的浓度增大,因此,有机层中Fe元素含量迅速增多
3 2 4 2
【解析】①减小生成物浓度,化学平衡向正反应方向移动,因此,其他条件不变,水层初始pH在
0.2~0.8范围内,随水层pH增大,H+的浓度减小,(R NH)SO +Fe3++SO 2-+HO H++
3 2 4 4 2
(R NH)Fe(OH)(SO ) 的化学平衡向正反应方向移动,又H+的浓度减小使平衡(R NH)SO +H++HSO
3 2 4 2 3 2 4 4
- 2(R NH•HSO )逆向移动,引起(R NH)SO 浓度的增大,进一步促进平衡(R NH)SO +Fe3++SO 2
3 4 3 2 4 3 2 4 4
-+HO H++(R NH)Fe(OH)(SO ) 向萃取方向移动,导致(R NH)Fe(OH)(SO ) 的浓度增大,因
2 3 2 4 2 3 2 4 2
此,有机层中Fe元素含量迅速增多。
5.(2024·镇江市丹阳市上学期开学考)钴及其化合物在工业生产中有着广阔的应用前景。已知:
Co2+不易被氧化,Co3+具有强氧化性,[Co(NH )]2+具有较强还原性,[Co(NH )]3+性质稳定。
3 6 3 6
(1)从锂钴废料(主要成分为LiCoO)分离Co2+。
2
①Co2+的电子排布式为___________________。
②“酸溶”时不选择浓HCl的理由是:___________________________________________________。
③“净化”时,加NaF固体是将Li+转化为沉淀,“净化”后溶液中c(F-)=4.0×10-2 mol·L-1,若
“过滤1”后溶液中Li+浓度为1.0 mol·L-1,则“净化”后c(Na+)=_____________________。[溶液体积
变化忽略不计,不考虑其他离子影响。25℃时K (LiF)=2.0×10-3]
sp
【答案】(1)①[Ar]3d7或1s22s22p63s23p63d7 ②浓HCl有还原性,与Co3+会发生反应产生Cl,污
2
染环境 ③0.99 mol·L-1
【解析】由题给流程可知,锂钴废料酸溶、过滤得到酸溶渣和含有锂离子、亚钴离子的滤液;向滤
液中加入氟化钠溶液,将锂离子转化为氟化锂沉淀,过滤得到氟化锂溶渣和含有亚钴离子的溶液。
①钴元素的原子序数为27,基态亚钴离子的电子排布式为[Ar]3d7或1s22s22p63s23p63d7,故答案为:
[Ar]3d7或1s22s22p63s23p63d7;②钴酸锂中钴元素的化合价为+3价,由题意可知,+3价钴元素具有强氧
化性,若酸溶时加入具有还原性的浓盐酸,钴酸锂会与浓盐酸反应生成有毒的氯气,污染空气,所以酸
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找溶时不能选用浓盐酸,故答案为:浓HCl有还原性,与Co3+会发生反应产生Cl,污染环境;③由氟化锂
2
的溶度积可知,净化后溶液中锂离子浓度为==0.05 mol·L-1,则沉淀锂离子消耗氟离子的浓度为1
mol·L-1-0.05 mol·L-1=0.95 mol·L-1,由净化后溶液中氟离子浓度为0.04 mol·L-1可知,溶液
中钠离子的浓度为0.95 mol·L-1+0.04 mol·L-1=0.99 mol·L-1,故答案为:0.99 mol·L-1。
6.(2025·南通市如东县第一次调研)实验室以碳酸锰矿(含MnCO 及少量Fe、Al、Si等氧化物)
3
为原料可制得高纯MnCO。
3
(1)焙烧:将碳酸锰矿与(NH )SO 在温度为300~500℃下进行焙烧,写出焙烧时MnCO 所发生反
4 2 4 3
应的化学方程式:_______________________________________________。
(2)制备MnCO:向净化后的MnSO 溶液在搅拌下缓慢滴加沉淀剂NH HCO 溶液,过滤、洗涤、
3 4 4 3
干燥,得到MnCO 固体。
3
①将过滤得到的滤液蒸发浓缩、冷却结晶,可得到的晶体为_______________(填化学式)。
②沉淀剂不选择NaCO 溶液的原因是____________________________________________________。
2 3
③MnCO 在空气中,一段时间后会生成MnO(OH),写出该反应的化学方程式
3 2
_____________________________。
【答案】(1)MnCO+(NH )SO ============MnSO +2NH ↑+CO↑+HO (2)①(NH )SO
3 4 2 4 4 3 2 2 4 2 4
②NaCO 溶液碱性较强,会有部分Mn(OH) 沉淀生成 ③2MnCO +O+2HO=2MnO(OH)+2CO
2 3 2 3 2 2 2 2
【解析】根据碳酸锰矿中所含成分,以及焙烧、制备过程可知,碳酸锰与硫酸铵反应生成硫酸锰、
氨气和二氧化碳,铁的氧化物、氧化铝、二氧化硅不与硫酸铵反应,加水溶解后,得到含硫酸锰溶液;
向净化后的MnSO 溶液中缓慢滴加沉淀剂NH HCO 溶液,过滤、洗涤、干燥,得到MnCO 固体。
4 4 3 3
(1)据分析可知,碳酸锰与硫酸铵反应生成硫酸锰、氨气和二氧化碳,焙烧时所发生反应的化学方
程式为:MnCO+(NH )SO ============MnSO +2NH ↑+CO↑+HO;(2)①过滤得到的滤液中主
3 4 2 4 4 3 2 2
要含有硫酸铵,将其蒸发浓缩、冷却结晶可得到的晶体(NH )SO ;②NaCO 属于强碱弱酸盐,溶液显
4 2 4 2 3
碱性,且碱性较强,会有部分Mn元素转化成Mn(OH) 沉淀,所得MnCO 不纯,而碳酸氢铵溶液的碱性
2 3
相对较弱,能更好地控制反应条件,减少锰的损失;③MnCO 在空气中一段时间后,与空气中的氧气和
3
水反应,生成MnO(OH),故方程式为:2MnCO +O+2HO=2MnO(OH)+2CO。
2 3 2 2 2 2
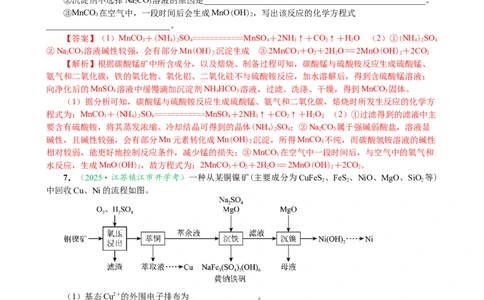
7.(2025·江苏镇江市开学考)一种从某铜镍矿(主要成分为CuFeS 、FeS 、NiO、MgO、SiO 等)
2 2 2
中回收Cu、Ni的流程如图。
(1)基态Cu2+的外围电子排布为________________。
(2)“氧压浸出”过程中,加压的目的是___________________________________________。
(3)“萃铜"时发生的反应为Cu2+(水相)+2HR(有机相) CuR (有机相)+2H+(水相),适当增
2
大溶液pH有利于铜的萃取,其原因是______________________________________________。
(4)“沉铁"过程生成黄钠铁矾沉淀的离子方程式为
___________________________________________________________。
(5)单质镍与碳、镁形成某晶体的晶胞结构如图所示,该晶体中Mg和Ni的原子个数之比为
_______。微专题突破6 无机化工流程题透一
(6)“沉镍"时为确保Ni2+沉淀完全,理论上应调节溶液pH≥_______。(已知:25℃时,
K [Ni(OH)]=4.0×10-15;lg2=0.3;当溶液中c(Ni2+)≤1.0×10-5 mol·L-1时,可认为该Ni2+沉淀完全)。
sp 2
(7)测定NiSO •7HO粗品的纯度。取3.000 gNiSO •7HO粗品溶于水(滴加几滴稀硫酸)配成100.0
4 2 4 2
mL溶液,取25.00 mL溶液于锥形瓶中,滴入几滴指示剂,用0.05000 mol·L-1的NaHY标准溶液滴定,
2 2
平均消耗标准溶液50.00 mL。计算确定粗品中NiSO •7HO的纯度_____________。(已知:Ni2++HY2-
4 2 2
=NiY2-+2H+,写出计算过程)。
【答案】(1)3d9 (2)增大氧气浓度,加快氧气氧化Fe2+的速率 (3)增大溶液pH则c(H+)减
小,平衡正向移动 (4)3Fe3++Na++2SO 2-+6HO=NaFe (SO )(OH)↓+6H+ (5)1∶3 (6)
4 2 3 4 2 6
9.3 (7)93.67%
【解析】向铜镍矿(主要成分为CuFeS 、FeS 、NiO、MgO、SiO 等)中加入O 、HSO 进行氧压浸
2 2 2 2 2 4
出,将铁元素转化为Fe (SO ) ,镍元素转化为NiSO 、铜元素转化为CuSO 、镁元素转化为MgSO ,硫
2 4 3 4 4 4
元素转化为S单质,过滤得到滤渣主要成分为 SiO 和S,用铜离子萃取剂萃取出Cu2+,分液得到萃取液,
2
萃余液中主要含有 Fe3+、Mg2+、Ni2+,向萃余液中加入 NaSO 和 MgO 进行沉铁将 Fe3+转化为
2 4
NaFe (SO )(OH) 、过滤出沉淀,向滤液中加入MgO将Ni2+以Ni(OH) 的形成沉淀,最后对Ni(OH) 进
3 4 2 6 2 2
行处理制得Ni,母液中主要溶质为MgSO 。
4
(1)Cu核外电子排布为1s22s22p63s23p63d104s1,失去4s能级1个电子、3d能级1个电子形成Cu2+,
Cu2+的外围电子排布式为3d9;(2)“氧压浸出"通入氧气时加压的目的是增大氧气浓度,加快氧气氧化
Fe2+的速率;(3)适当增大溶液pH则c(H+)减小,平衡正向移动,有利于铜的萃取;(4)萃余液呈酸
性,加入氧化镁调节pH,向萃余液中加入NaSO 进行沉铁将Fe3+转化为NaFe (SO )(OH),“沉铁"过
2 4 3 4 2 6
程生成黄钠铁矾沉淀的离子方程式为3Fe3++Na++2SO 2-+6HO=NaFe (SO )(OH)↓+6H+;(5)
4 2 3 4 2 6
由均摊法,晶胞中Mg个数为8×=1,Ni个数为3×=3,该晶体中Mg和Ni的原子个数之比为1∶3;
(6)“沉镍"时为确保Ni2+沉淀完全,此时c(Ni2+)≤1.0×10-5 mol·L-1,由K [Ni(OH)]=c(Ni2
sp 2
+)•c2(OH-);则溶液c(OH-)===2.0×10-5 mol·L-1, 常温下c(H+)===5.0×10-10 mol·L-1,溶液的
pH=-lgc(H+)=-1+lg2+10=9.3;(7)已知:Ni2++HY2-=NiY2-+2H+,则n(Ni2+)=n(HY2-)
2 2
=0.05000 mol·L-1×50.00×10-3 L=2.5000×10-3 mol,粗品中n(Ni2+)=2.5000×10-3 mol×=
1.000×10-2 mol,粗品中NiSO •7HO的纯度=≈93.67%
4 2
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找