文档内容
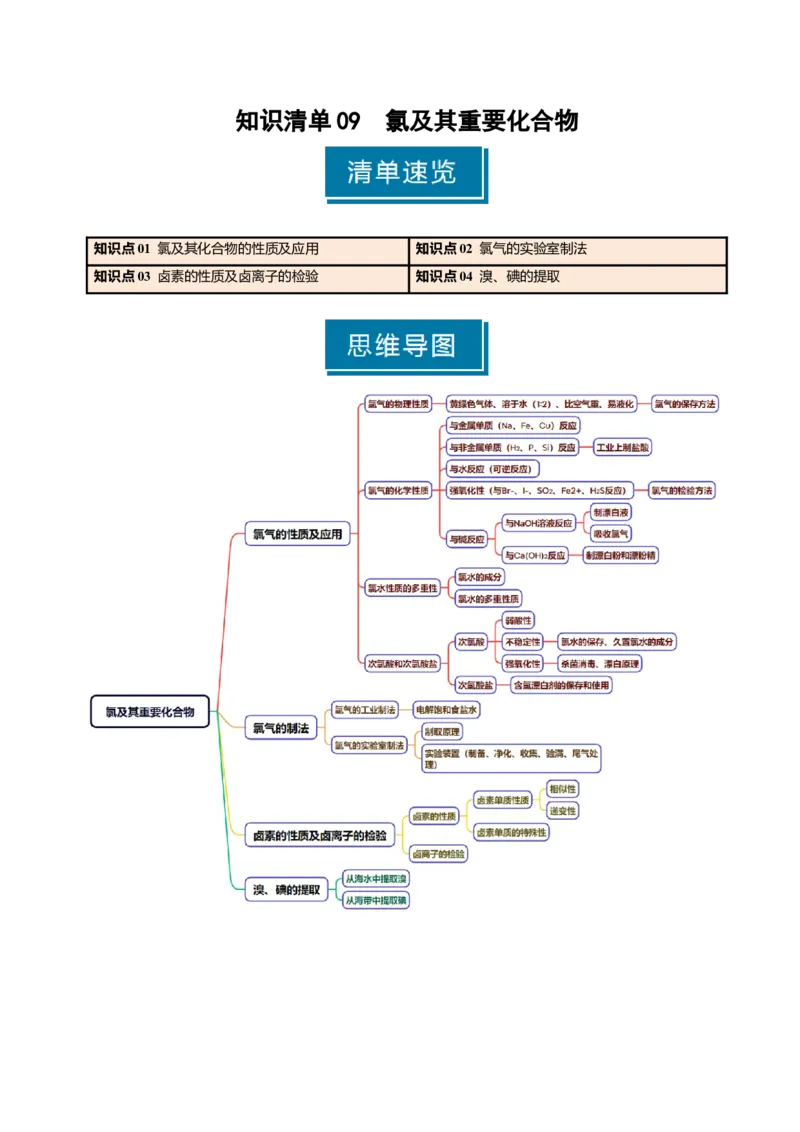
知识清单 09 氯及其重要化合物
知识点01 氯及其化合物的性质及应用 知识点02 氯气的实验室制法
知识点03 卤素的性质及卤离子的检验 知识点04 溴、碘的提取知识点 01 氯及其化合物的性质及应用
一、氯气的性质
1.氯气的物理性质
氯气是一种黄绿色、有刺激性气味的气体,密度比空气大,可溶于水(1:2),易液化,有毒。
工业上通常将氯气液化后保存在钢瓶里。
实验室里闻有毒气体及未知气体气味的方法是:用手在瓶口轻轻扇动,仅使极少量气体飘进鼻孔。
2.氯气的化学性质
(1)氧化性
①与金属单质反应:
与铁反应:2Fe+3Cl =====2FeCl ,实验现象:生成棕色烟。
2 3
与铜反应:Cu+Cl =====CuCl ,实验现象:生成棕黄色烟。
2 2
②与非金属单质反应:
a.与H 反应:H+Cl=====CuCl ,实验现象:有苍白色火焰,出现白雾。
2 2 2 2
应用:工业上制盐酸。
H 与Cl 的混合物点燃或光照发生爆炸。
2 2
b.能将P氧化为PCl 、PCl ,与Si反应生成SiCl 。
3 5 4
③与还原性物质反应:
与KI溶液反应:Cl+2KI===2KCl+I,实验室用湿润的淀粉碘化钾试纸检验Cl。
2 2 2
与SO 水溶液反应:Cl+SO +2HO===H SO +2HCl。
2 2 2 2 2 4
与FeCl 溶液反应:Cl+ 2FeCl===2FeCl。
2 2 2 3
(2)Cl 与水和碱反应——歧化反应
2
a.与水反应:Cl+H OHCl+HClO(可逆反应)
2 2
b.与NaOH溶液反应:Cl+2NaOH===NaCl+NaClO+HO。
2 2
应用:实验室用NaOH溶液吸收多余的氯气,工业上制取消毒液。
c.与石灰乳反应制取漂白粉:2Cl+2Ca(OH)===CaCl +Ca(ClO) +2HO
2 2 2 2 2
漂白粉的主要成分是CaCl 、Ca(ClO) ,有效成分是Ca(ClO) ,漂粉精的主要成分是Ca(ClO) 。
2 2 2 2
3.氯水的成分和性质
氯气的水溶液称为氯水,溶于水的氯气只有少量与水反应。
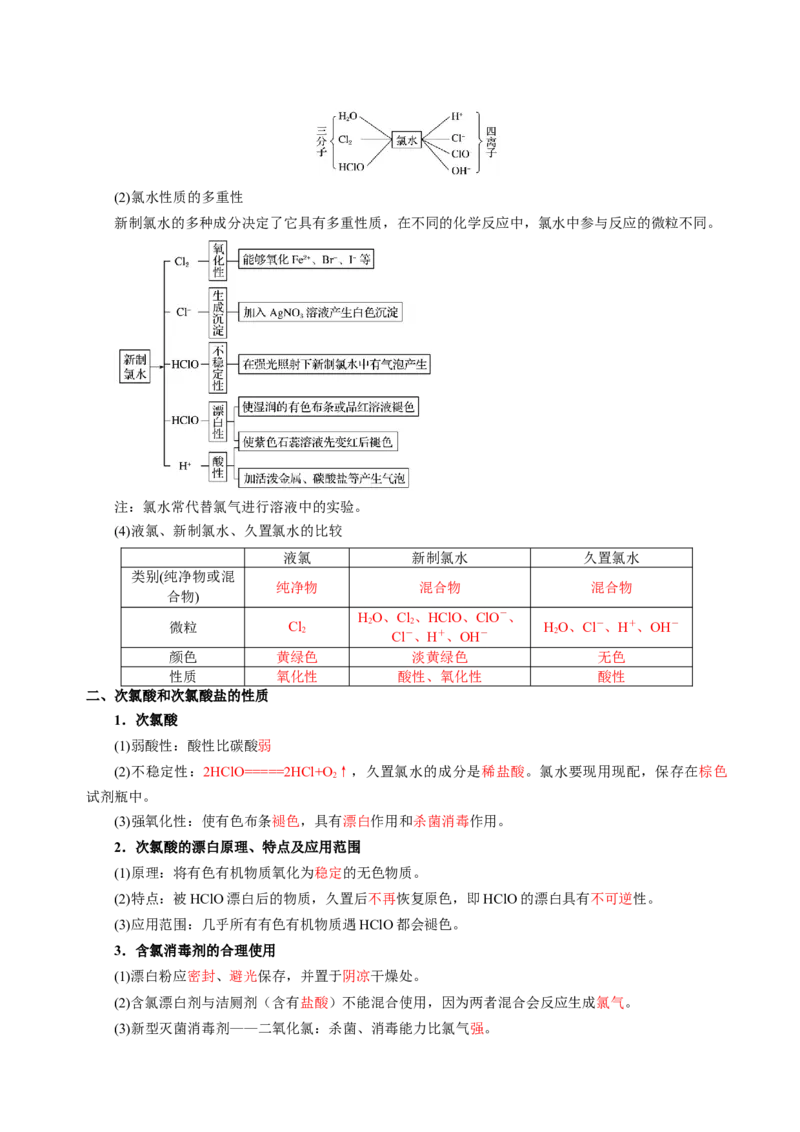
(1)氯水中存在三种平衡关系:
①Cl+HOHCl+HClO ②HClOH++ClO- ③HOH++OH-
2 2 2
氯水中存在的微粒:(2)氯水性质的多重性
新制氯水的多种成分决定了它具有多重性质,在不同的化学反应中,氯水中参与反应的微粒不同。
注:氯水常代替氯气进行溶液中的实验。
(4)液氯、新制氯水、久置氯水的比较
液氯 新制氯水 久置氯水
类别(纯净物或混
纯净物 混合物 混合物
合物)
HO、Cl、HClO、ClO-、
微粒 Cl 2 2 HO、Cl-、H+、OH-
2 Cl-、H+、OH- 2
颜色 黄绿色 淡黄绿色 无色
性质 氧化性 酸性、氧化性 酸性
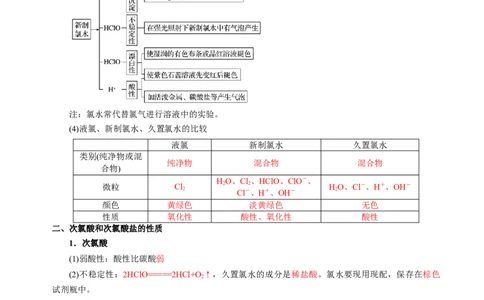
二、次氯酸和次氯酸盐的性质
1.次氯酸
(1)弱酸性:酸性比碳酸弱
(2)不稳定性:2HClO=====2HCl+O↑,久置氯水的成分是稀盐酸。氯水要现用现配,保存在棕色
2
试剂瓶中。
(3)强氧化性:使有色布条褪色,具有漂白作用和杀菌消毒作用。
2.次氯酸的漂白原理、特点及应用范围
(1)原理:将有色有机物质氧化为稳定的无色物质。
(2)特点:被HClO漂白后的物质,久置后不再恢复原色,即HClO的漂白具有不可逆性。
(3)应用范围:几乎所有有色有机物质遇HClO都会褪色。
3.含氯消毒剂的合理使用
(1)漂白粉应密封、避光保存,并置于阴凉干燥处。
(2)含氯漂白剂与洁厕剂(含有盐酸)不能混合使用,因为两者混合会反应生成氯气。
(3)新型灭菌消毒剂——二氧化氯:杀菌、消毒能力比氯气强。(1)发生氯气泄漏时,污染区的居民应向低洼处转移(×)
错因:氯气密度比空气大,应向高处转移。
(2)Cu在Cl 中燃烧产生棕黄色的烟,若反应后,向集气瓶中加少量水振荡,可得到棕黄色溶液(×)
2
错因:CuCl 溶液呈蓝绿色。
2
(3)Cl 与HO反应生成HCl和HClO,故氯水中无Cl 分子(×)
2 2 2
错因:Cl 与HO的反应是可逆反应,故氯水中有Cl 分子。
2 2 2
(4)氯气溶于水得氯水,溶液呈酸性且可以导电,所以氯气是电解质(×)
错因:电解质必须是化合物,Cl 是单质。
2
(5)过量的铁粉在少量氯气中加热,充分反应后产物为FeCl (×)
2
错因:氯气有强氧化性,直接把铁氧化到+3 价。
(6)Cl 具有很强的氧化性,在化学反应中只能作氧化剂(×)
2
错因:Cl 中氯元素的化合价是0价,能升高也能降低,既能作氧化剂,又能作还原剂。
2
(7)氯气与水反应,其中氯气是氧化剂,水是还原剂(×)
错因:Cl+HOHCl+HClO,其中氯气既是氧化剂又是还原剂。
2 2
(8)标准状况下,11.2 L Cl 与水充分反应转移电子数为0.5N (×)
2 A
错因:该反应为可逆反应,Cl 不能完全反应,转移电子数小于0.5N 。
2 A
(9)1 mol Cl 与足量强碱完全反应转移电子数为N (√)
2 A
提示:Cl 与强碱是完全反应。
2
(10)可以用pH试纸测定氯水的pH(×)
错因:氯水有漂白性,能使pH试纸褪色,用pH试纸无法测其pH。
(11)常温下液态氯与铁不反应,故可用钢瓶贮运液氯(√)
提示:常温下,氯气不与Fe反应。
(12)工业制漂白粉应选择石灰乳,而不是石灰水、石灰粉(√)
提示:工业上制漂白粉不能选择石灰水,因为浓度太低,石灰粉是固体,很难与氯气反应。
(13)ClO-与Fe2+、I-、S2-、HS-、SO等在水中因发生氧化还原反应而不能大量共存(√)
(14)84消毒液和洁厕灵混合施用效果更好(×)
错因:84消毒液(主要成分NaClO)和洁厕灵(主要成分HCl)不能混合使用,否则会产生有毒气体——氯气。
(15)“84”消毒液的消毒原理与HO 的相同,都是利用强氧化性(√)
2 2
提示:两者都具有强氧化性,都是利用其强氧化性消毒杀菌。
一、氯气及氯水的性质
1.根据下列装置图回答问题(1)A、B通入Cl 后,观察到的现象是______________________________________,根据现象可得出的结
2
论是__________________________________________________。
(2)集气瓶B中发生反应的离子方程式是_____________________________。
(3)F装置的作用是______________________________。
(4)实验开始后,观察装置C中的现象是__________________________________。
(5)装置E中发生反应的离子方程式是______________________________。
(6)通入Cl 时装置D中发生反应的离子方程式是___________________________。
2
答案:(1)干燥的红色(或A中)布条不褪色,湿润的红色(或B中)布条褪色 Cl 无漂白性,Cl 与水反应生
2 2
成的HClO有漂白性
(2)Cl +HOH++Cl-+HClO
2 2
(3)吸收氯气,防止污染环境
(4)溶液先变为红色,然后褪色
(5)2Fe2++Cl===2Fe3++2Cl-
2
(6)H O+SO+Cl===2H++SO+2Cl-
2 2
2.某学习小组设计以下六个实验探究氯水的成分,请填表。
实验序号 操作及现象 结论
① 观察氯水的颜色呈黄绿色 氯水中含________
② 将氯水滴加到AgNO 溶液中产生白色沉淀 氯水中含________
3
③ 将氯水滴到淀粉-KI试纸上,试纸变蓝 氯水中含________
④ 将足量的氯水滴加到NaCO 溶液中,产生气泡 氯水中含________
2 3
⑤ 将氯水滴加到石蕊溶液中,溶液先变红后褪色 氯水中含______和_____
⑥ 将氯水滴加到有色布条上,布条褪色 氯水含______
答案:①Cl ②Cl- ③Cl ④H+ ⑤H+ HClO ⑥HClO
2 2
3.氯水中含有多种成分,因而具有多种性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、
d重合部分代表物质间反应,且氯水足量)。
(1)能证明氯水具有漂白性的是________(填“a”“b”“c”或“d”)。
(2)c过程中的现象是____________________________。(3)b过程中反应的离子方程式为_______________________________________。
(3)a过程中反应的化学方程式为__________________________________。
答案:(1)d
(2)产生白色沉淀 2H++CO===H O+CO↑
2 2
(3)Cl +2FeCl ===2FeCl
2 2 3
二、含氯消毒剂的应用
1.NaClO是“84”消毒液的有效成分。请回答下列问题:
(1)NaClO中Cl元素的化合价是______。
(2)浸泡衣物时加入“84”消毒液,在空气中放置一段时间后漂白效果更好,结合离子方程式解释原因:
_____________________________________________________________。
(3)若将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,会产生黄绿色的有毒气体,其反应的离子方程
式是_____________________________________________。
答案:(1)+1 (2)与空气中的二氧化碳和水反应生成次氯酸,ClO-+CO +HO===HClO+HCO,HClO
2 2
浓度增大,漂白效果增强 (3)Cl-+ClO-+2H+===Cl↑+HO
2 2
2.漂白粉在空气中长时间放置,最终得到的固体产物为___________,结合化学方程式解释原因:
_____________________________________________________________。
答案:CaCO 和CaCl Ca(ClO) +HO+CO===CaCO ↓+2HClO,2HClO=====2HCl+O↑,CaCO +
3 2 2 2 2 3 2 3
2HCl===CaCl +CO↑+HO
2 2 2
3.二氧化氯(ClO )是一种黄绿色易溶于水的气体,常用于饮用水的消毒。
2
(1)NaClO 在酸性条件下反应生成ClO 和NaCl,写出反应的离子方程式:
2 2
______________________________________________。
(2)ClO 在强碱性环境中失效,可能的原因是会发生歧化反应生成ClO和ClO, 写出反应的离子方程式:
2
___________________________________________________。
答案:(1)5ClO+4H+===Cl-+4ClO ↑+2HO (2)2ClO+2OH-===ClO+ClO+HO
2 2 2 2
知识点 02 氯气的实验室制法
1.制取原理
实验室通常用强氧化剂(如KMnO 、KCr O、KClO、MnO 等)氧化浓盐酸制取氯气。
4 2 2 7 3 2
用MnO 制取Cl 的方程式:MnO +4HCl(浓)=====MnCl +Cl↑+2HO。
2 2 2 2 2 2
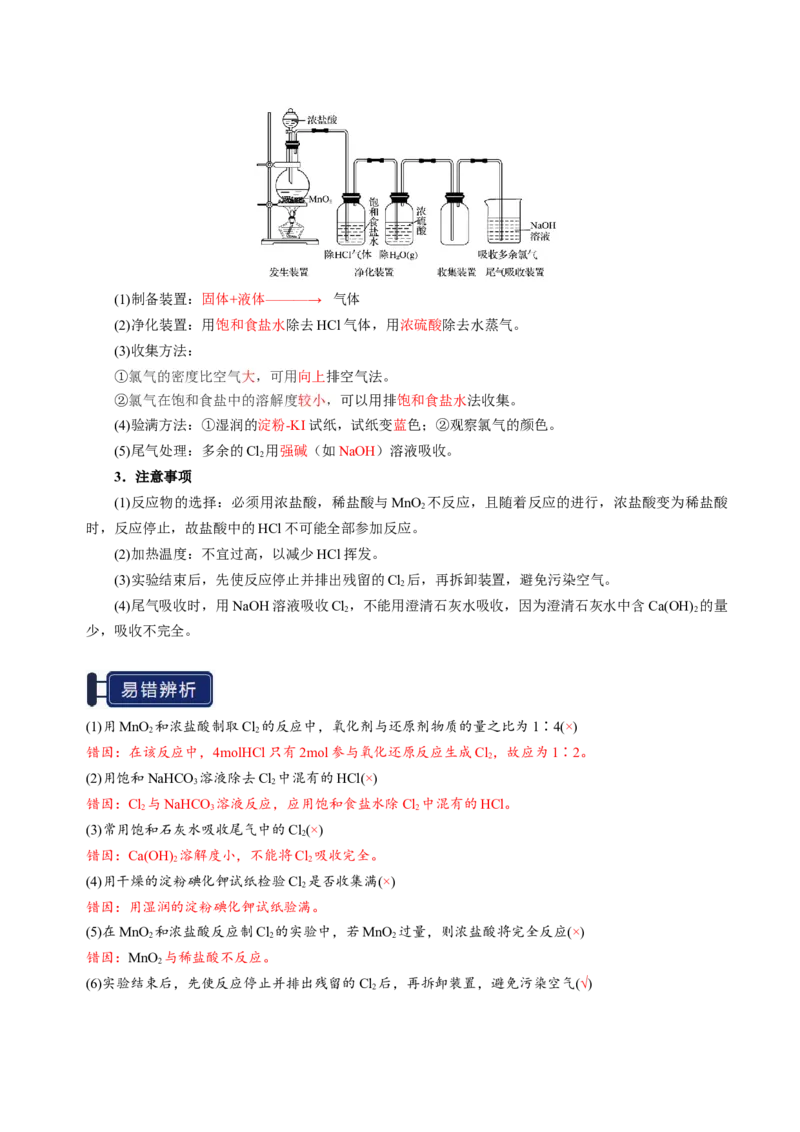
2.实验装置(1)制备装置:固体+液体———→ 气体
(2)净化装置:用饱和食盐水除去HCl气体,用浓硫酸除去水蒸气。
(3)收集方法:
①氯气的密度比空气大,可用向上排空气法。
②氯气在饱和食盐中的溶解度较小,可以用排饱和食盐水法收集。
(4)验满方法:①湿润的淀粉-KI试纸,试纸变蓝色;②观察氯气的颜色。
(5)尾气处理:多余的Cl 用强碱(如NaOH)溶液吸收。
2
3.注意事项
(1)反应物的选择:必须用浓盐酸,稀盐酸与MnO 不反应,且随着反应的进行,浓盐酸变为稀盐酸
2
时,反应停止,故盐酸中的HCl不可能全部参加反应。
(2)加热温度:不宜过高,以减少HCl挥发。
(3)实验结束后,先使反应停止并排出残留的Cl 后,再拆卸装置,避免污染空气。
2
(4)尾气吸收时,用NaOH溶液吸收Cl,不能用澄清石灰水吸收,因为澄清石灰水中含Ca(OH) 的量
2 2
少,吸收不完全。
(1)用MnO 和浓盐酸制取Cl 的反应中,氧化剂与还原剂物质的量之比为1∶4(×)
2 2
错因:在该反应中,4molHCl只有2mol参与氧化还原反应生成Cl,故应为1∶2。
2
(2)用饱和NaHCO 溶液除去Cl 中混有的HCl(×)
3 2
错因:Cl 与NaHCO 溶液反应,应用饱和食盐水除Cl 中混有的HCl。
2 3 2
(3)常用饱和石灰水吸收尾气中的Cl(×)
2
错因:Ca(OH) 溶解度小,不能将Cl 吸收完全。
2 2
(4)用干燥的淀粉碘化钾试纸检验Cl 是否收集满(×)
2
错因:用湿润的淀粉碘化钾试纸验满。
(5)在MnO 和浓盐酸反应制Cl 的实验中,若MnO 过量,则浓盐酸将完全反应(×)
2 2 2
错因:MnO 与稀盐酸不反应。
2
(6)实验结束后,先使反应停止并排出残留的Cl 后,再拆卸装置,避免污染空气(√)
2氯气的实验室制法
1.Ca(ClO) 、KClO、KMnO 均能将盐酸中的Cl-氧化成Cl,试分别写出反应的离子方程式。
2 3 4 2
①________________________________________________。
②________________________________________________。
③________________________________________________。
答案:①ClO-+Cl-+2H+===Cl↑+HO
2 2
②ClO+5Cl-+6H+===3Cl↑+3HO
2 2
③2MnO+10Cl-+16H+===2Mn2++5Cl↑+8HO
2 2
2.如图是用KMnO 与浓盐酸反应制取适量氯气的简易装置。
4
装置B、C、D的作用分别是:
B_______________________________________________________;
C________________________________________________________;
D_________________________________________________________。
答案:向上排空气法收集氯气 安全瓶作用,防止D中的液体倒吸入B中 吸收尾气,防止氯气扩散到
空气中污染环境
3.某同学欲利用浓盐酸、MnO 、Fe等试剂制取无水氯化铁、收集一定量的氯气并验证其某些性质,实
2
验装置如图所示(制气装置省略)。下列说法错误的是( )
A.④中a导管应向下延伸至接近瓶底
B.若撤去⑥,则⑤中可能有Fe O 生成
2 3
C.当⑤中充满黄绿色气体时再点燃⑤处酒精灯
D.③中试纸若是湿润的,则根据产生的现象可证明氯气有酸性、漂白性
答案:D
解析:A.氯气的密度比空气的大,应采用向上排空气法收集,故需要将a导管延长至接近瓶底,A正确;
B.若撤去⑥,则⑦中的水蒸气逆向进入⑤中,导致 FeCl 水解生成 Fe(OH) ,Fe(OH) 受热分解变为
3 3 3
Fe O ,B正确;C.加热时装置中的空气会与Fe反应,故应先通入一段时间Cl ,以排尽装置中的空气,
2 3 2
防止加热时被空气氧化,C正确;D.③中试纸若是湿润的,氯气与水反应生成HCl和HClO,使试纸先变
红后褪色,而干燥的氯气无漂白性、酸性,D错误。知识点 03 卤素的性质及卤离子的检验
1.卤素单质性质的相似性
(1)与大多数金属反应,如Br 与Fe反应:2Fe+3Br ===2FeBr ,但I 与Fe反应生成FeI。
2 2 3 2 2
(2)与H 反应生成HX:X+H===2HX(X代表F、Cl、Br、I,下同)。
2 2 2
(3)与水反应:X+HOHX+HXO(F 例外)。
2 2 2
(4)与碱溶液反应:X+2NaOH===NaX+NaXO+HO(F 、I 例外)。
2 2 2 2
2.卤素单质的递变性
性质 F Cl Br I 规律
2 2 2 2
颜色 淡黄绿色 黄绿色 深红棕色 紫黑色 逐渐加深
状态 气体 气体 液体 固体 熔、沸点逐渐升高
与氢气化合 由易到难 逐渐减弱
简单离子(X-)
单质的氧化性越弱,对应离子的还原性越强 逐渐增强
的还原性
3.卤素单质及化合物性质的特殊性
(1)夫及其化合物
①无正价,非金属性最强,F-的还原性最弱;
②与水反应:2F+2HO===4HF+O,与H 反应在暗处即爆炸;
2 2 2 2
③氢氟酸是弱酸,能腐蚀玻璃,故应保存在塑料瓶中。
(2)Br 的性质
2
①Br 是深红棕色液体,易挥发;
2
②Br 易溶于有机溶剂;
2
③盛溴的试剂瓶中加水,进行水封,保存液溴不能用橡胶塞。
(3)I 的性质
2
①淀粉遇I 变蓝色;
2
②I 加热时易升华;
2
③I 易溶于有机溶剂。
2
4.卤素离子的检验方法
(1)沉淀法
未知液―――――――――――→生成
(2)置换——萃取法
未知液―――――――――→――――――――――――→有机层呈
(3)氧化——淀粉法检验I-
未知液――――――――――――――→――――→溶液变蓝色,表明有I-(1)使用含氟牙膏能预防龋齿(√)
(2)向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液,现象为先变橙色,后变蓝色,则氧化性:Cl >
2
Br >I(×)
2 2
错因:氯水过量,过量的Cl 会与KI反应,不能证明Br >I 。
2 2 2
(3)向无色溶液中滴加CCl ,振荡,静置,通过溶液的颜色判断是否含有I-(×)
4
错因:I-不溶于CCl 。
4
(4)卤素气态氢化物的水溶液都是强酸(×)
错因:HF的水溶液是弱酸。
(5)类比Fe与Cl 的反应判断Fe与I 反应时生成FeI(×)
2 2 3
错因:Fe与I 反应生成FeI。
2 2
(6)浓HSO 能干燥HCl,所以浓HSO 也能干燥HBr、HI(×)
2 4 2 4
错因:浓HSO 能氧化HBr、HI。
2 4
(7)加碘盐能使淀粉变蓝(×)
错因:加碘盐中含KIO ,淀粉遇I 变蓝。
3 2
一、卤素性质的实验探究
1.某化学小组用如图所示装置验证卤素单质氧化性的相对强弱。下列说法不正确的是( )
A.E处棉花球变成黄色,说明Cl 的氧化性比Br 强
2 2
B.F处棉花球变成蓝色,说明Br 的氧化性比I 强
2 2
C.E处发生反应的离子方程式为Cl+2Br-===2Cl-+Br
2 2
D.G装置中NaOH溶液与Cl 反应的离子方程式为2OH-+Cl===ClO-+Cl-+HO
2 2 2
答案:B
解析:在F处,可能是未反应完的Cl 与KI发生反应置换出I,使淀粉变蓝色,不能说明Br 的氧化性比
2 2 2
I 强。
2
2.为验证卤素单质氧化性的相对强弱,某小组用如图所示装置进行实验(夹持仪器已略去,气密性已检
查)。实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,其电子式是_____________________。
(2)验证氯气的氧化性强于碘的实验现象是________________________________________。
(3)B中溶液发生反应的离子方程式是____________________________________。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是____________________________________。
(5)过程Ⅲ实验的目的是____________________________________________。
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下____________________,得电子能力
逐渐减弱。
答案:(1)
(2)湿润的淀粉KI试纸变蓝
(3)Cl +2Br-===Br +2Cl-
2 2
(4)打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡,静置后CCl 层变为紫红色
4
(5)确认C的黄色溶液中无Cl,排除Cl 对Br 置换I 实验的干扰
2 2 2 2
(6)原子半径逐渐增大
解析:A中滴加浓盐酸后,发生反应:2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO,生成黄绿
4 2 2 2
色气体Cl ,在A、B、C中分别发生反应:Cl +2KI===2KCl+I ,Cl +2NaBr===2NaCl+Br ,Cl +
2 2 2 2 2 2
2NaBr===2NaCl+Br ,由于B、C中生成了Br 而使溶液变为黄色,打开活塞b,C中生成的Br 在D中
2 2 2
发生反应:Br +2KI===2KBr+I 。过程Ⅲ,当B中黄色溶液继续通入过量Cl 时,溶液变为红棕色,以
2 2 2
此为对照,说明C中黄色溶液无Cl,从而排除Cl 对Br 置换I 实验的干扰。
2 2 2 2
二、卤离子的鉴别
1.下列叙述中正确的是( )
A.能使湿润的淀粉KI试纸变成蓝色的物质一定是Cl
2
B.用硝酸酸化的硝酸银溶液能一次鉴别NaCl、NaBr、KI三种失去标签的溶液
C.某溶液加入CCl ,CCl 层显紫色,证明原溶液中存在I-
4 4
D.某浅黄色的溴水,加入CCl 振荡静置后,上层显橙红色
4
答案:B
解析:还有很多氧化剂(如HNO 、O 等)能将I-氧化为I ,A项错误;碘单质的CCl 溶液显紫色, C项
3 3 2 4错误;CCl 的密度比水大,应下层显橙红色,D项错误。
4
2.鉴别NaCl、NaBr、NaI可以选用的试剂是( )
①碘水、淀粉溶液 ②氯水、CCl ③溴水、苯 ④稀硝酸、AgNO 溶液 ⑤氯水、苯 ⑥FeCl 溶
4 3 3
液、CCl
4
A.①②④ B.②③⑥ C.②④⑤ D.④⑤⑥
答案:C
解析:①NaCl、NaBr、NaI中加碘水和淀粉溶液均变蓝色;②氯水加入NaBr、NaI中后,再加CCl 萃取,
4
下层分别为橙红色和紫红色,加入NaCl中不发生反应,可以鉴别;③溴水与NaCl、NaBr不反应,与
NaI反应生成I ,用苯萃取后,前两种上层均为橙红色,无法鉴别;④NaCl、NaBr、NaI与AgNO 溶液
2 3
反应分别生成AgCl、AgBr、AgI沉淀,且均不溶于稀HNO ,沉淀颜色依次为白色、淡黄色、黄色;⑤
3
与②的原理相似,只是有色层在上层;⑥FeCl 溶液只能氧化I-生成I,不能鉴别。
3 2
3.有一包白色固体,它可能含有KCl、KCO、KNO 中的一种或几种,现进行如下实验:
2 3 3
①溶于水,得无色溶液;
②向上述溶液中滴加AgNO 溶液,生成白色沉淀;
3
③再滴加稀硝酸,沉淀减少但不完全消失,同时有气泡生成。
根据上述现象判断:
(1)白色固体一定含有的成分是________________,可能含有的成分是________。
(2)写出上述实验中有关反应的离子方程式:__________________________________________________。
答案:(1)KCl和KCO KNO
2 3 3
(2)Ag++Cl-===AgCl↓、2Ag++CO===Ag CO↓、Ag CO+2H+===2Ag++HO+CO↑
2 3 2 3 2 2
解析:由②产生白色沉淀知,可能含有KCO 和KCl中的一种或两种;由③沉淀减少且有气泡生成知,
2 3
一定含有KCO;由沉淀不完全消失可知,一定含有KCl。
2 3
三、拟卤素和卤素互化物
1.氰[(CN) ]的结构简式为N≡C—C≡N,其化学性质与卤素(X )很相似,化学上称之为拟卤素,其氧化性
2 2
介于Br 和I 之间。
2 2
(1)写出(CN) 的电子式_________________________。
2
(2)写出(CN) 在常温下与烧碱溶液反应的化学方程式:____________________________________。
2
(3) 在 KBr 、 KI 、 KCN 的 混 合 溶 液 中 通 入 少 量 氯 气 , 发 生 反 应 的 离 子 方 程 式 为
__________________________。
答案:(1)
(2)(CN) +2NaOH===NaCN+NaCNO+HO
2 2
(3)2I-+Cl===I +2Cl-
2 2
2.一氯化碘(ICl)、三氯化碘(ICl )是卤素互化物,它们的性质与卤素单质相似。
3
(1)ICl 与水反应的产物可能为________(填化学式)。
3
(2)ICl在常温下与烧碱溶液反应的离子方程式为_____________________________________,该反应是否
是氧化还原反应?_________(填“是”或“否”)。
答案:(1)HCl、HIO
2(2)ICl+2OH-===Cl-+IO-+HO 否
2
知识点 04 溴、碘的提取
1.海水提取溴 (吹出法)
(1)流程
(2)主要过程及反应原理
浓缩:海水晒盐和海水淡化的过程中副产物Br-得到浓缩;
氧化:向浓缩的海水中通入Cl,将Br-氧化成Br ,离子方程式为:2Br-+Cl===Br +2Cl-;
2 2 2 2
吹出:利用溴的挥发性,通入热空气和水蒸气,吹出溴蒸气;
吸收:吹出的溴蒸气用SO 吸收,化学方程式为:Br +SO+2H O===H SO +2HBr;
2 2 2 2 2 4
蒸馏:再用Cl 将HBr氧化得到产品溴后蒸馏分离,化学方程式为:2HBr+Cl ===Br +2HCl。
2 2 2
2.从海带中提取碘
(1)流程
(2)主要过程及反应原理
浸泡:将海带灰中的I-溶解提取出来;
氧化:向滤液中通入Cl,将I-氧化成I,得到含I 的水溶液,离子方程式为:2I-+Cl===I +2Cl-;
2 2 2 2 2
萃取:用有机溶剂将I 从水溶液中提取出来,分液得到I 的有机溶液;
2 2
蒸馏:将I 与有机溶剂分离。
2
(1)海水提溴的过程中不发生氧化还原反应(×)
错因:海水提溴过程中涉及Br-与Br 之间的转化是氧化还原反应。
2
(2)用CCl 萃取碘水中的碘,先振荡,后静置,液体分层,下层呈无色(×)
4
错因:CCl 比水重,下层是碘的CCl 溶液。
4 4
(3)碘易升华,可用加热升华法除去NH Cl中混有的I(×)
4 2错因:NH Cl受热分解生成NH 和HCl,遇冷又生成NH Cl。
4 3 4
(4)实验室在蒸发皿中灼烧干海带,并且用玻璃棒搅拌(×)
错因:灼烧固体时应在坩埚中。
溴、碘的提取
1.海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图所示:
(1)步骤①反应的离子方程式是________________________________________。
(2)步骤③反应的化学方程式是_______________________________________。
(3)步骤②中,用热空气将Br 吹出,利用溴的性质为________________,从步骤②到步骤④的目的是
2
____________________________________。
(4)从理论上考虑,下列物质也能充分吸收Br 的是________(填字母)。
2
A.NaOH B.FeCl C.NaSO D.HO
2 2 3 2
(5)步骤⑤蒸馏过程中,温度应控制在80~90 ℃。温度过高或过低都不利于生产,若温度过高,大量水蒸
气随溴排出,溴蒸气中水分增加;若温度过低,则_________________________。
答案:(1)2Br-+Cl===Br +2Cl-
2 2
(2)SO +Br +2HO===H SO +2HBr
2 2 2 2 4
(3)易挥发 将溴浓缩,提高Br 的提取率
2
(4)ABC
(5)溴不能完全蒸出,产率太低
解析:(4)NaOH和Br 反应生成NaBr、NaBrO和HO,可以吸收,A正确;Fe2+有还原性,可以被溴氧
2 2
化为Fe3+,Br 被还原为Br-,可以吸收Br ,B正确;NaSO 可以和Br 反应,将Br 还原为Br-,能吸
2 2 2 3 2 2
收Br ,C正确;HO和Br 反应微弱,不能充分吸收Br ,D错误。
2 2 2 2
2.海洋是生命的摇篮,海水不仅是宝贵的水资源,而且蕴藏着丰富的化学资源。从海水中提取一些重
要的化工产品的工艺流程如图所示。根据上述流程图回答下列问题:
(1)海水淡化处理的方法有蒸馏法、冷冻法、_______________________________(写出1种即可)。
(2)图中制漂白粉的反应中,消耗标准状况下11.2 L Cl ,转移的电子数是__________N 。
2 A
(3)步骤Ⅰ需事先向浓缩海水中加入硫酸酸化,再通入氯气,可提高 Cl 的利用率,理由是
2
_______________
________________________________________________。
(4)步骤Ⅰ到步骤Ⅲ的变化为“Br-→Br →Br-→Br ”,其目的是________________________________。
2 2
(5)写出下列步骤中化学反应的离子方程式:步骤Ⅱ_______________________________________;
步骤Ⅲ____________________________________。
答案:(1)离子交换法(或电渗析法或反渗析法) (2)0.5 (3)中和海水的弱碱性,避免氯气、溴与海水反应
(或者酸化可抑制氯气、溴与海水反应) (4)富集(或浓缩)溴元素 (5)Br +SO +2HO===4H++2Br-+SO
2 2 2
Cl+2Br-===Br +2Cl-
2 2
解析:(1)海水淡化处理的方法有:蒸馏法、冷冻法、离子交换膜法、电渗析法、反渗析法等;(2)图中制
漂白粉的反应是:2Cl +2Ca(OH) ===CaCl +Ca(ClO) +2HO,氯元素化合价由0价变化为-1价和+1
2 2 2 2 2
价,则2 mol 氯气反应转移电子2 mol,标准状况下11.2 L Cl 的物质的量为11.2 L÷22.4 L/mol =0.5 mol,
2
故转移电子0.5 mol,即转移电子数目为0.5N ;(3)步骤Ⅰ需事先向浓缩海水中加入硫酸酸化,再通入氯
A
气,可提高Cl 的利用率,原因是:海水呈弱碱性,氯气、溴单质与海水之间能发生反应,酸化可抑制
2
它们与海水的反应;(4)步骤Ⅰ得到的溴溶液的浓度太低,所以步骤Ⅰ到步骤Ⅲ的变化目的是:增大溴的
浓度,实现溴的富集;(5)步骤Ⅱ的离子方程式为:Br +SO +2HO===4H++2Br-+ SO,步骤Ⅲ的离子
2 2 2
方程式为:Cl+2Br-===Br +2Cl-。
2 2