文档内容
云南省师范大学附属中学 2023 届高考适应性月考卷(一)
化学试题
注意事项:
1.答题前,考生务必用黑色碳素笔将自己的姓名、准考证号、考场号、座位号在答题卡上填
写清楚。
2.每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。在试题卷上作答无效。
3.考试结束后,请将本试卷和答题卡一并交回。满分100分,考试用时120分钟。
以下数据可供解题时参考。
可能用到的相对原子质量: H-1 C-12 O16 Al-27 S -32 Cl- 35.5
一、选择题:本题共14小题,每小题3分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1. 化学与生产、生活等密切相关。下列说法错误的是
A. CHCHCl可用作快速镇痛剂
3 2
B. BaCO 可用作肠胃检查的内服剂
3
C. 聚乙炔可用于制备导电高分子材料
D. 工业废气中的CO 能用于生产可降解塑料
2
2. 下列各项中不属于化学变化的是
A. 焰色试验 B. 油脂硬化 C. 煤的液化 D. 橡胶硫化
3. 下列物质不能通过相应单质一步化合而成的是
A. HCl B. NO C. CuS D. Al O
2 3
4. 下列化学用语表达正确的是
A. 乙烯的结构简式: CHCH
2 2
B. Cl-的结构示意图:
C. 乙醇中官能团的电子式:
D. 基态碘原子的简化电子排布式: [ Kr ]5s25p5
5. N 为阿伏加德罗常数的值。下列有关说法正确的是
AA. 室温下,22. 4L乙烷中含有的碳原子数小于2N
A
B. 1L 0.1mol/L NH Cl溶液中 的数目为0.1N
4 A
C. 标准状况下,11. 2L CHCl 中所含的氯原子数为1. 5N
3 A
D. 室温下,27g Al与足量浓硫酸反应,转移的电子数为3N
A
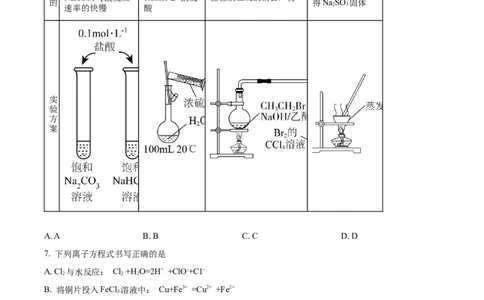
6. 下列实验方案能达到实验目的的是
选
A B C D
项
比较NaCO、 配制100mL
目 2 3 由 NaSO 溶液制
NaHCO 与酸反应 0.1mol·L-1的硫 检验溴乙烷的消去产物 2 3
的 3 得NaSO 固体
速率的快慢 酸 2 3
实
验
方
案
A. A B. B C. C D. D
7. 下列离子方程式书写正确的是
A. Cl 与水反应: Cl +H O=2H+ +ClO-+C1-
2 2 2
B. 将铜片投入FeCl 溶液中: Cu+Fe3+ =Cu2+ +Fe2+
3
C. 将SO 通入BaCl 溶液中: SO +Ba2+ =BaSO ↓+2H+
2 2 2 3
D. 铝片与NaOH溶液反应: 2Al+2OH- +2H O= 2 +3H ↑
2 2
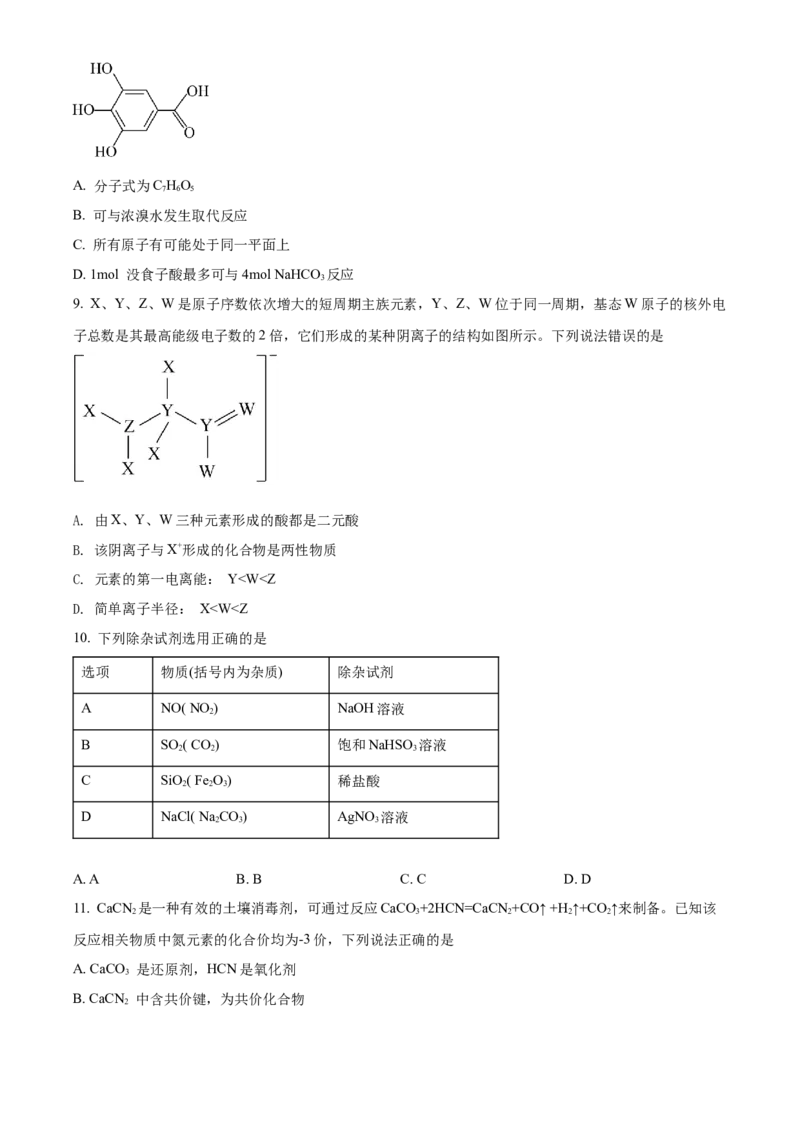
8. 三百多年前,著名化学家波义耳使用铁盐和没食子酸(结构简式如图)制造了墨水。下列有关没食子酸的
说法错误的是A. 分子式为C HO
7 6 5
B. 可与浓溴水发生取代反应
C. 所有原子有可能处于同一平面上
D. 1mol 没食子酸最多可与4mol NaHCO 反应
3
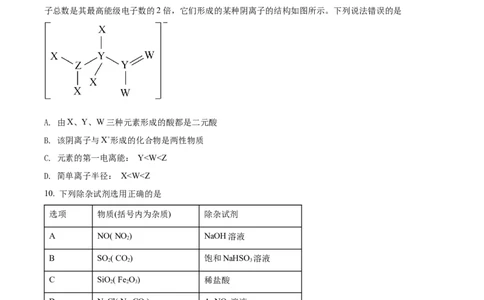
9. X、Y、Z、W是原子序数依次增大的短周期主族元素,Y、Z、W位于同一周期,基态W原子的核外电
子总数是其最高能级电子数的2倍,它们形成的某种阴离子的结构如图所示。下列说法错误的是
A. 由X、Y、W三种元素形成的酸都是二元酸
B. 该阴离子与X+形成的化合物是两性物质
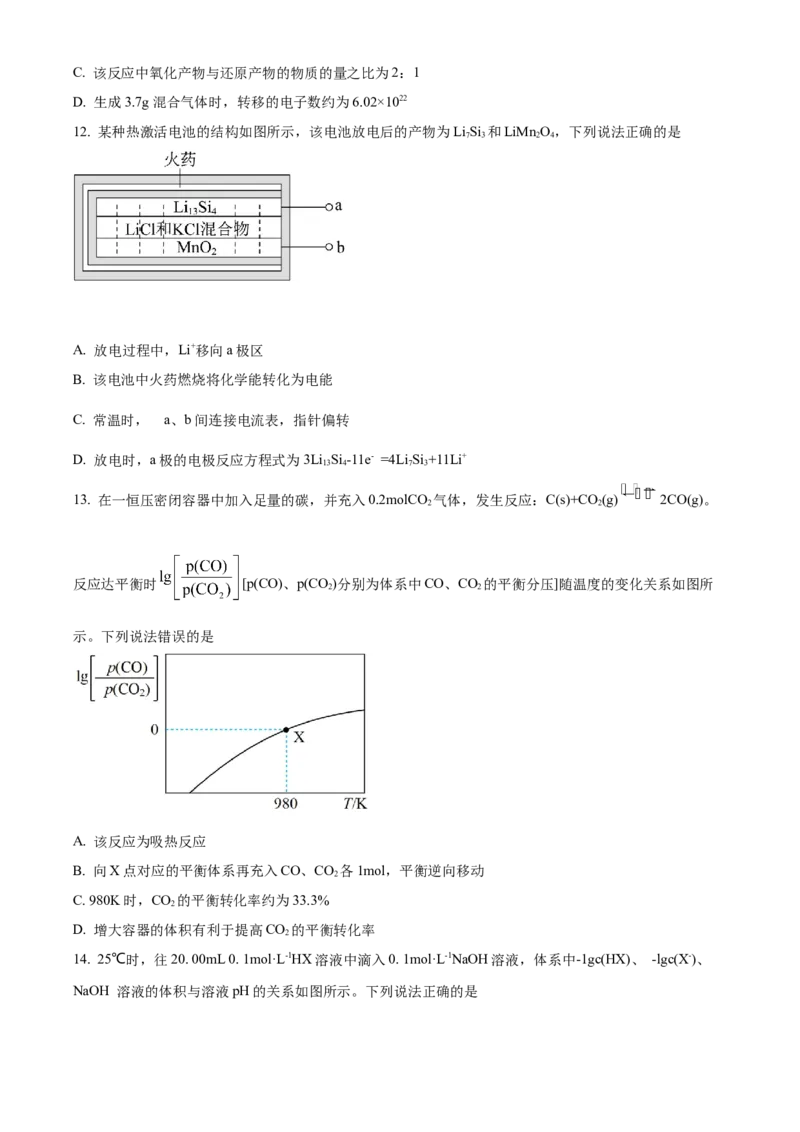
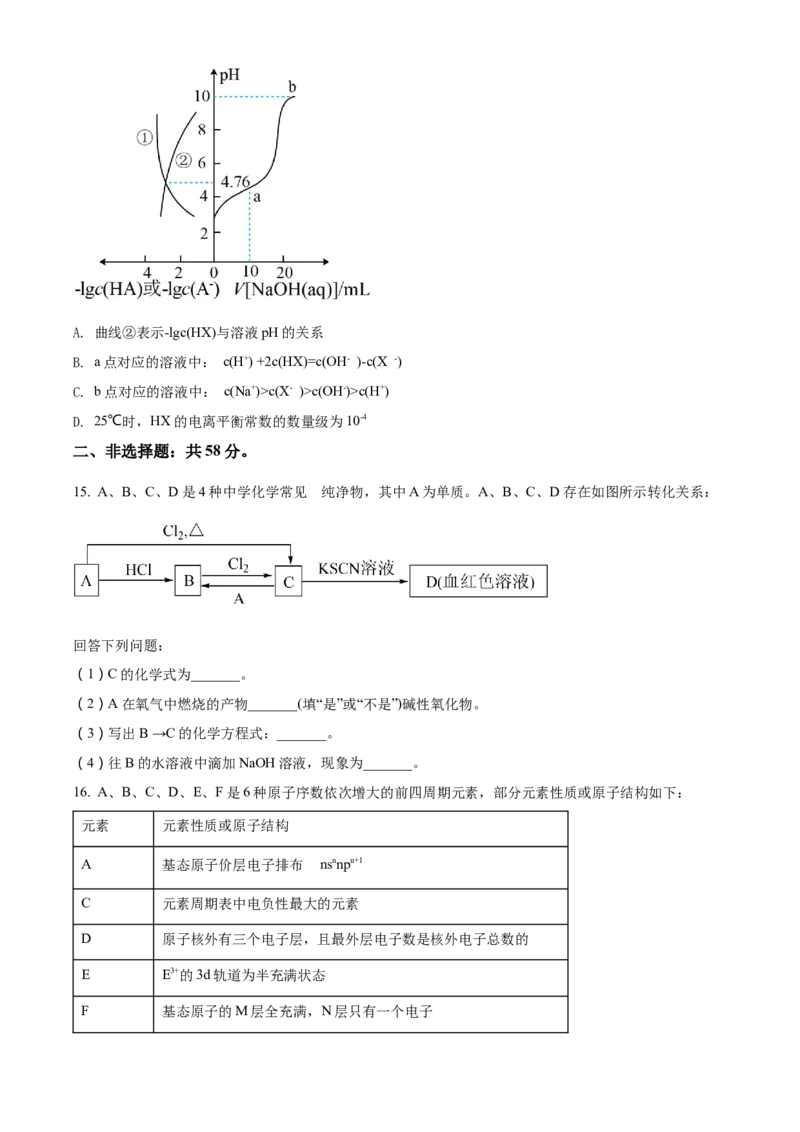
C. 元素的第一电离能: Yc(X- )>c(OH-)>c(H+)
D. 25℃时,HX的电离平衡常数的数量级为10-4
二、非选择题:共58分。
的
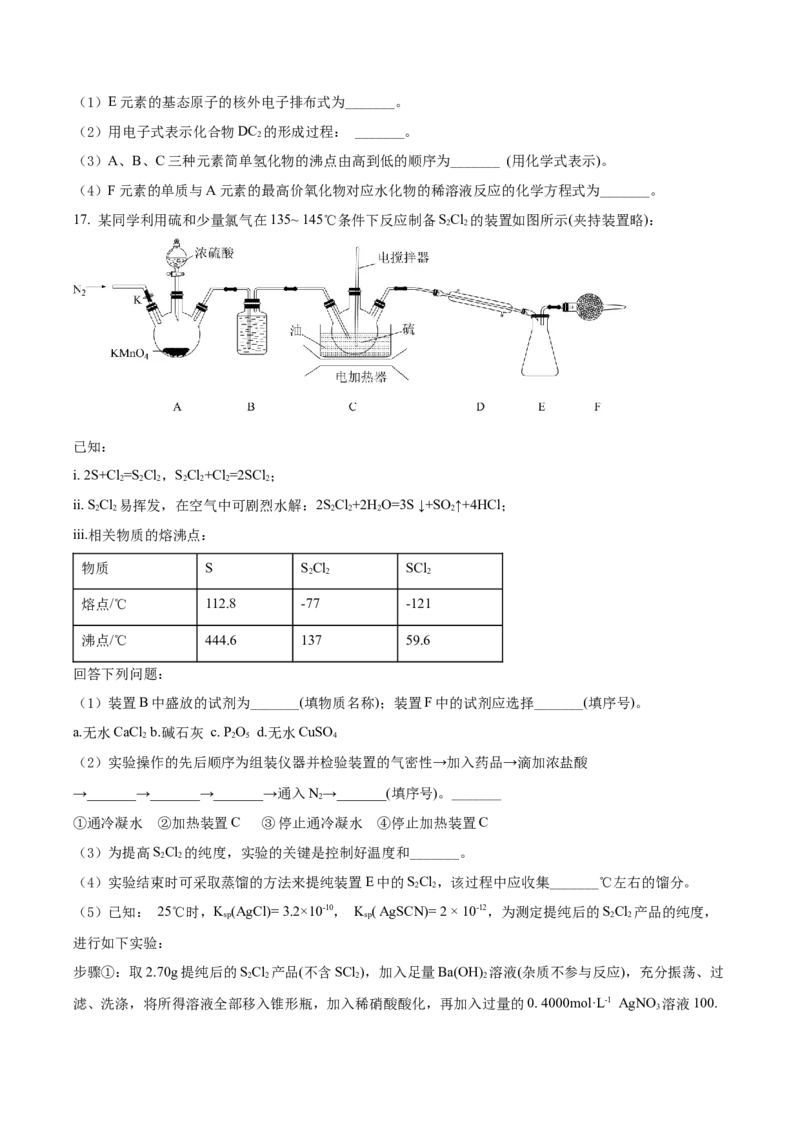
15. A、B、C、D是4种中学化学常见 纯净物,其中A为单质。A、B、C、D存在如图所示转化关系:
回答下列问题:
(1)C的化学式为_______。
(2)A在氧气中燃烧的产物_______(填“是”或“不是”)碱性氧化物。
(3)写出B →C的化学方程式:_______。
(4)往B的水溶液中滴加NaOH溶液,现象为_______。
16. A、B、C、D、E、F是6种原子序数依次增大的前四周期元素,部分元素性质或原子结构如下:
元素 元素性质或原子结构
A 基态原子价层电子排布 为nsnnpn+1
C 元素周期表中电负性最大的元素
D 原子核外有三个电子层,且最外层电子数是核外电子总数的
E E3+的3d轨道为半充满状态
F 基态原子的M层全充满,N层只有一个电子(1)E元素的基态原子的核外电子排布式为_______。
(2)用电子式表示化合物DC 的形成过程: _______。
2
(3)A、B、C三种元素简单氢化物的沸点由高到低的顺序为_______ (用化学式表示)。
(4)F元素的单质与A元素的最高价氧化物对应水化物的稀溶液反应的化学方程式为_______。
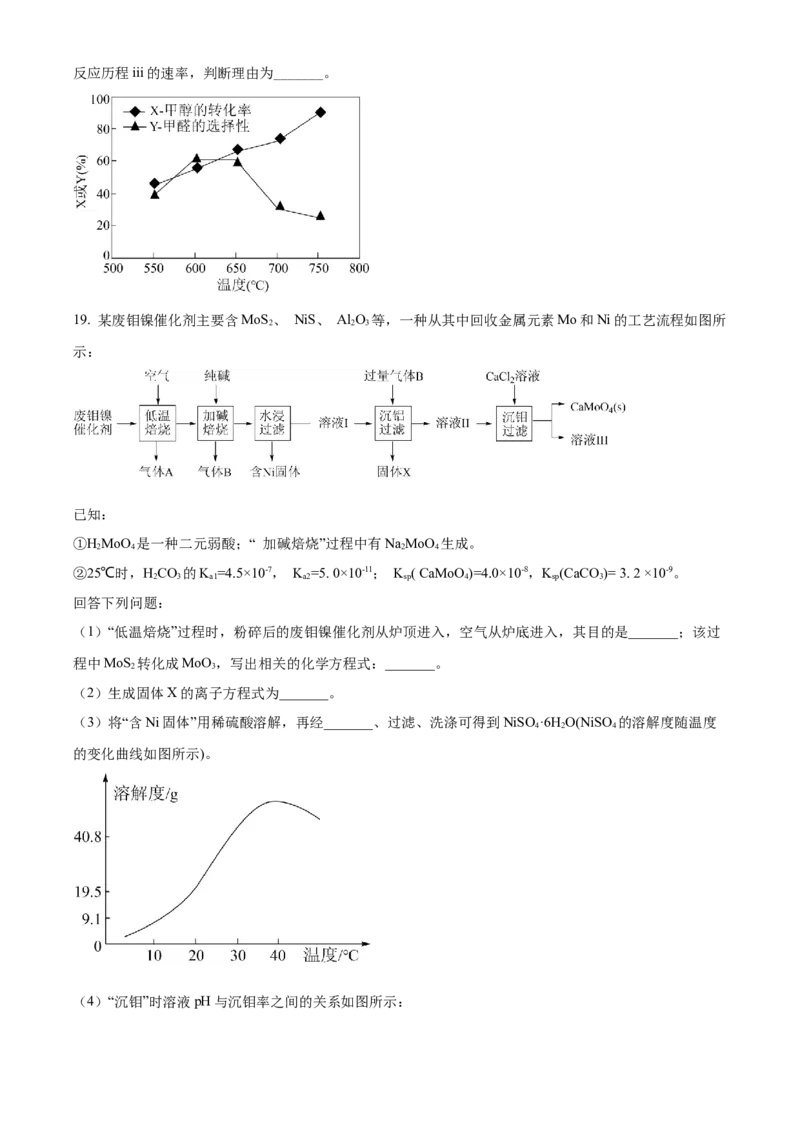
17. 某同学利用硫和少量氯气在135~ 145℃条件下反应制备SCl 的装置如图所示(夹持装置略):
2 2
已知:
i. 2S+Cl =S Cl,SCl+Cl=2SCl ;
2 2 2 2 2 2 2
ii. S Cl 易挥发,在空气中可剧烈水解:2SCl+2H O=3S ↓+SO ↑+4HCl;
2 2 2 2 2 2
iii.相关物质的熔沸点:
物质 S SCl SCl
2 2 2
熔点/℃ 112.8 -77 -121
沸点/℃ 444.6 137 59.6
回答下列问题:
(1)装置B中盛放的试剂为_______(填物质名称);装置F中的试剂应选择_______(填序号)。
a.无水CaCl b.碱石灰 c. P O d.无水CuSO
2 2 5 4
(2)实验操作的先后顺序为组装仪器并检验装置的气密性→加入药品→滴加浓盐酸
→_______→_______→_______→通入N→_______(填序号)。_______
2
①通冷凝水 ②加热装置C ③停止通冷凝水 ④停止加热装置C
(3)为提高SCl 的纯度,实验的关键是控制好温度和_______。
2 2
(4)实验结束时可采取蒸馏的方法来提纯装置E中的SCl,该过程中应收集_______℃左右的馏分。
2 2
(5)已知: 25℃时,K (AgCl)= 3.2×10-10, K ( AgSCN)= 2 × 10-12,为测定提纯后的SCl 产品的纯度,
sp sp 2 2
进行如下实验:
步骤①:取2.70g提纯后的SCl 产品(不含SCl ),加入足量Ba(OH) 溶液(杂质不参与反应),充分振荡、过
2 2 2 2
滤、洗涤,将所得溶液全部移入锥形瓶,加入稀硝酸酸化,再加入过量的0. 4000mol·L-1 AgNO 溶液100.
300mL。
步骤②:向锥形瓶中加入2mL硝基苯,用力摇动使有机物充分覆盖沉淀;再滴入2滴Fe( NO) 溶液作指
3 3
示剂,用0.2000mol ·L-1KSCN标准液滴定至终点,消耗KSCN标准液10.00mL。
滴定终点的实验现象为_______;所得产品中SCl 的质量分数为_______。
2 2
18. 甲醛在医药方面有重要用途。工业上可利用反应Ⅰ: CHOH(g) HCHO(g)+H(g)来合成甲醛。
3 2
(1)已知:
.
反应Ⅱ : 2CHOH(g)+O (g) 2HCHO(g) +2H O(g) △H=-3132kJ·mol-1
3 2 2 2
反应Ⅲ: 2H(g)+O g) 2HO(g) △H=-483. 6kJ ·mol-1
2 2( 2 3
则反应Ⅰ : CHOH(g) HCHO(g)+H(g) 的△H=_______kJ·mol-1。
3 2 1
(2)利用反应Ⅰ合成甲醛时,为加快化学反应速率,同时提高CHOH的平衡转化率,可采取的措施为
3
_______。
(3)T ℃时,向体积恒为2L的密闭容器中充入8mol CHOH(g)发生反应Ⅰ,5min后反应达到平衡,测得
3
混合体系中的HCHO( g)的体积分数为20%。
①下列事实不能说明该反应已达到化学平衡状态的是_______(填序号)。
A. v ( HCHO)=v (H )
正 逆 2
B. c(CHOH) : c(HCHO) : c(H)=1 :1: 1
3 2
C.混合气体的平均相对分子质量不变
D.混合气体的密度保持不变
②5min内,v( CH OH)=_______mol· L-1· min-1。
3
③其他条件不变时,向已达平衡的反应体系中充入1mol CHOH(g)和1mol H(g),则此时v _______v (填
3 2 正 逆
“大于”“小于”或“等于”)。
(4)在催化剂作用下,甲醇脱氢制甲醛的部分机理如下:
历程i : CHOH→·H+·CHOH
3 2
历程ii: ·CHOH-→·H+HCHO
2
历程iii:·CHOH+3·H+CO
2
历程iv:·H+·H→H
2
一定条件下测得温度对甲醇的转化率(X)、甲醛的选择性(Y)的影响如图所示[甲醛的选择性(Y)=
]。 则650℃ ~750℃,反应历程ii的速率。_______(填“大于”“小于”或“等于”)反应历程iii的速率,判断理由为_______。
19. 某废钼镍催化剂主要含MoS 、 NiS、 Al O 等,一种从其中回收金属元素Mo和Ni的工艺流程如图所
2 2 3
示:
已知:
①HMoO 是一种二元弱酸;“ 加碱焙烧”过程中有NaMoO 生成。
2 4 2 4
②25℃时,HCO 的K =4.5×10-7, K =5. 0×10-11; K ( CaMoO )=4.0×10-8,K (CaCO)= 3. 2 ×10-9。
2 3 a1 a2 sp 4 sp 3
回答下列问题:
(1)“低温焙烧”过程时,粉碎后的废钼镍催化剂从炉顶进入,空气从炉底进入,其目的是_______;该过
程中MoS 转化成MoO ,写出相关的化学方程式:_______。
2 3
(2)生成固体X的离子方程式为_______。
(3)将“含Ni固体”用稀硫酸溶解,再经_______、过滤、洗涤可得到NiSO ·6H O(NiSO 的溶解度随温度
4 2 4
的变化曲线如图所示)。
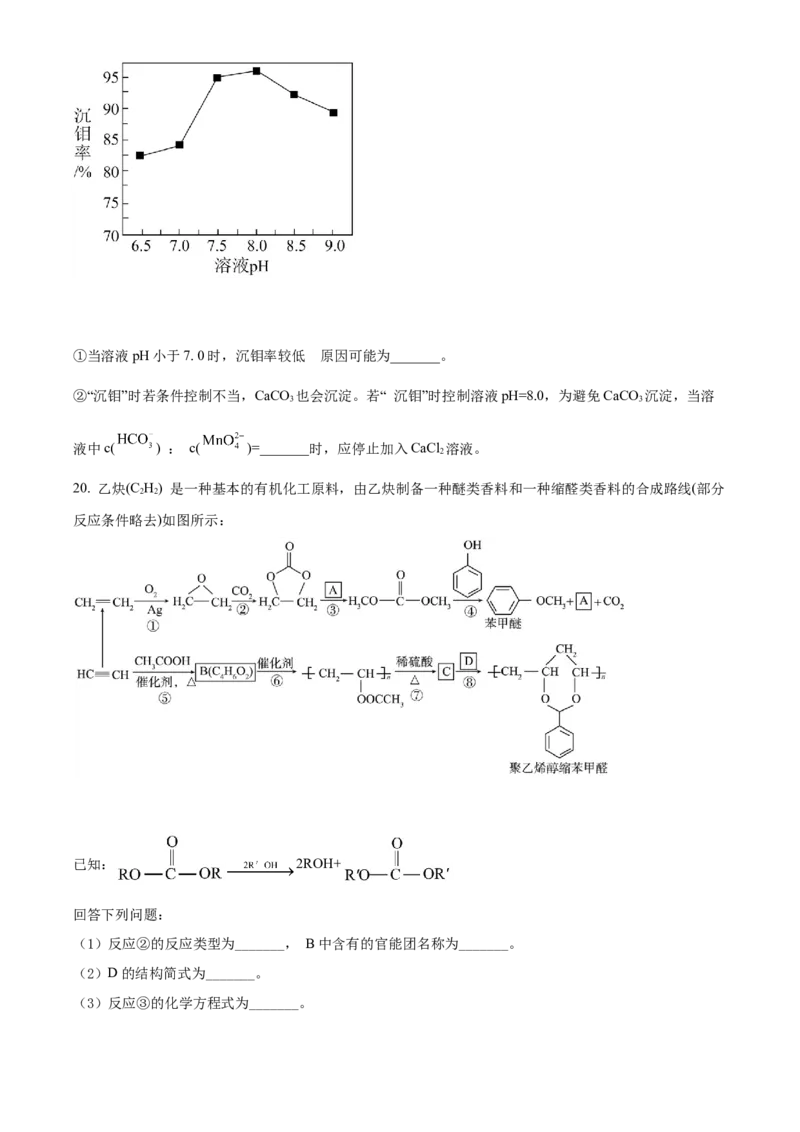
(4)“沉钼”时溶液pH与沉钼率之间的关系如图所示:的
①当溶液pH小于7. 0时,沉钼率较低 原因可能为_______。
②“沉钼”时若条件控制不当,CaCO 也会沉淀。若“ 沉钼”时控制溶液pH=8.0,为避免CaCO 沉淀,当溶
3 3
液中c( ) : c( )=_______时,应停止加入CaCl 溶液。
2
20. 乙炔(C H) 是一种基本的有机化工原料,由乙炔制备一种醚类香料和一种缩醛类香料的合成路线(部分
2 2
反应条件略去)如图所示:
已知: 2ROH+
回答下列问题:
(1)反应②的反应类型为_______, B中含有的官能团名称为_______。
(2)D的结构简式为_______。
(3)反应③的化学方程式为_______。(4)若化合物M为苯甲醚的同系物,且相对分子质量比苯甲醚大14,则能使FeCl 溶液显色的M的同分
3
异构体共有_______种。
(5)参照上述合成路线,以1-溴丁烷为原料(无机试剂任选),设计一条制备 的合成
路线。_______