文档内容
考点 01 物质的分类及转化
1.3年真题考点分布
年
省份 高考考点
份
202
2
202
辽宁卷 物质的组成
1
202
0
202
2
202 物质的成分
广东卷
1
202
0
202 物质变化类型
2
202 物质变化类型
湖南卷
1
202
0
202 物质变化类型
2
202
湖北卷
1
202
0
202
2
202 物质的组成和性质
福建卷
1
202
0
202
2
202 物质分类
天津卷
1
202
0
202
2
202 物质的转化、物质的变化
江苏卷
1
202 物质的转化
0
202 微粒间的关系、物质分类、物质的组成
2
202 物质分类、物质的组成
浙江卷
1
202 物质分类、物质的组成
0
2.命题规律及备考策略
【命题规律】近3年新高考卷对于物质分类和转化主要考查:
(1)物质的组成与分类
资料收集整理【淘宝店铺:向阳百分百】(2)物质组成与分类的判断
(3)物质变化的判断
(4)物质间的转化
(5)微粒间的关系
(6)胶体的结构和性质
【备考策略】高考对本专题的考查多集中在物质的组成、性质与分类上以选择题的形式出现,本部分内容的考
查力度将有加大的趋势,考生在备考时要加强对基础知识的掌握。对于物质性质与变化的考查,近几年高考题
倾向于从传统文化中寻找切入点来考查化学知识,备考时考生要积累工业生产中的常见物质的名称及日常生活
中常见现象涉及的化学知识。近几年,高考对分散系及其性质的考查一般以某一选项的形式出现在选择题中,
考查溶液和胶体的本质区别、胶体的丁达尔效应、透过性及其应用等,考生在备考时要学会用思维导图、对比
记忆(如胶体和溶液)的方法来加强复习效果。
【命题预测】物质的组成、分类、性质与转化在高考选择题中主要以考查物质的组成和分类为出发点,以重大
科技成果和人们普遍关注的社会问题和传统文化等的描述为切入点,将有关物质的组成、分类、胶体知识融合
于试题之中。预计今后的高考中基本概念与其他部分化学知识和能力的相互渗透和结合将会有所加强。
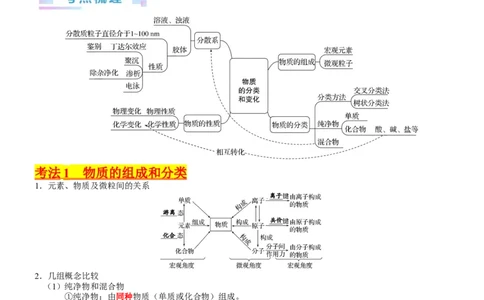
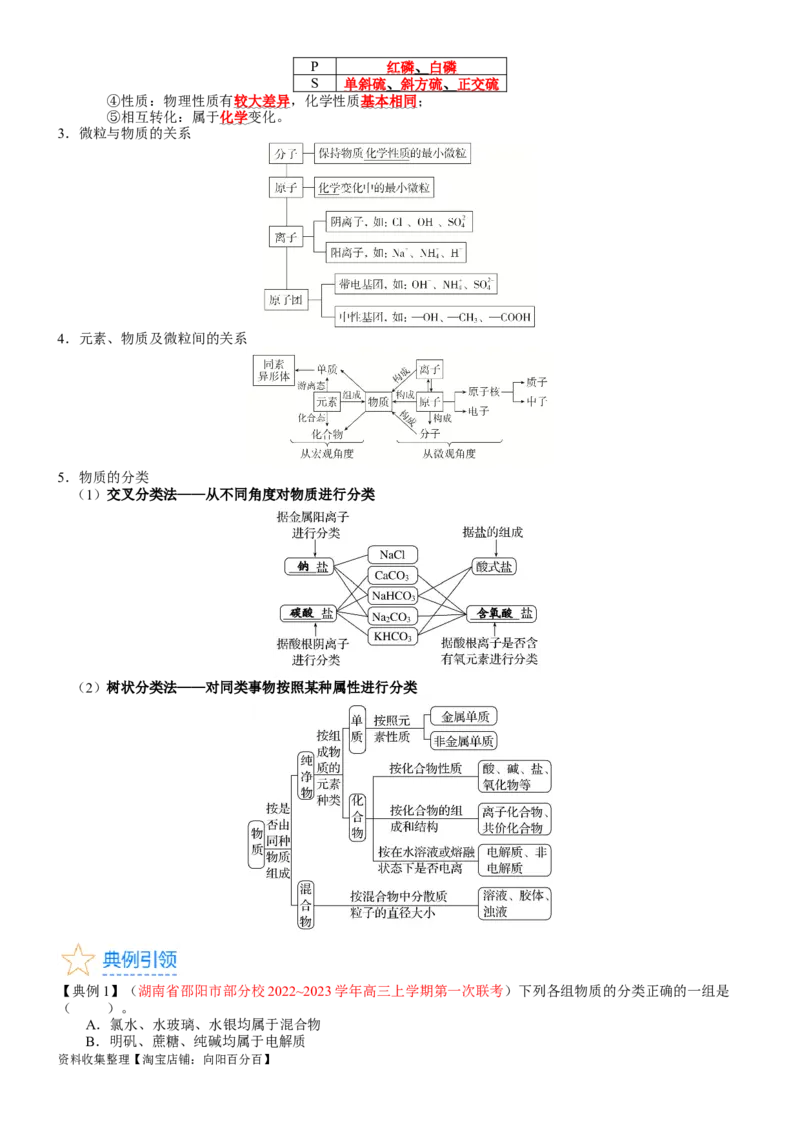
考法 1 物质的组成和分类
1.元素、物质及微粒间的关系
2.几组概念比较
(1)纯净物和混合物
①纯净物:由同种物质(单质或化合物)组成。
②混合物:由两种或多种不同的物质(单质或化合物)组成。
(2)单质和化合物
①单质:由同种元素组成的纯净物。
②化合物:由不同种元素组成的纯净物。
(3)游离态和化合态
①游离态:元素以单质形式存在的状态。
②化合态:元素以化合物形式存在的状态。
(4)同素异形体
①概念:同一种元素形成的几种性质不同的单质;
②成因:原子间排列方式或成键方式不同;
③实例
元素 同素异形体
C 金刚石、石墨、C
60
O O、O
2 3
资料收集整理【淘宝店铺:向阳百分百】P 红磷、白磷
S 单斜硫、斜方硫、正交硫
④性质:物理性质有较大差异,化学性质基本相同;
⑤相互转化:属于化学变化。
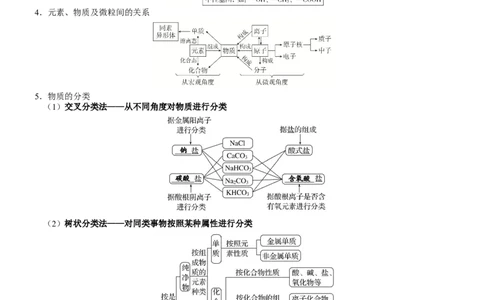
3.微粒与物质的关系
4.元素、物质及微粒间的关系
5.物质的分类
(1)交叉分类法——从不同角度对物质进行分类
(2)树状分类法——对同类事物按照某种属性进行分类
【典例1】(湖南省邵阳市部分校2022~2023学年高三上学期第一次联考)下列各组物质的分类正确的一组是
( )。
A.氯水、水玻璃、水银均属于混合物
B.明矾、蔗糖、纯碱均属于电解质
资料收集整理【淘宝店铺:向阳百分百】C.NaO、NaO 均为碱性氧化物
2 2 2
D.CuSO ·5HO、C HOH均为纯净物
4 2 2 5
【解析】选D。由两种或两种以上物质构成的是混合物,而水银化学式是Hg属于纯净物,故A错误;蔗糖在
水溶液中和熔融状态下都不能导电,为非电解质,故B错误;能和酸反应生成盐和水的氧化物为碱性氧化物,
NaO 不是碱性氧化物,故C错误;CuSO ·5HO、C HOH都表示一种物质,均为纯净物,故D正确。
2 2 4 2 2 5
【拓展延伸】
1.常见的混合物
(1)气体混合物:空气、水煤气(CO和H)、爆鸣气(H 和O)、天然气(主要成分是CH)、焦炉气
2 2 2 4
(主要成分是H 和CH)、高炉煤气、石油气、裂解气。
2 4
(2)液体混合物:氨水、氯水、王水、天然水、水玻璃、福尔马林、浓硫酸、盐酸、汽油、植物油、部分胶
体。
(3)固体混合物:大理石、碱石灰、漂白粉、固体高分子、玻璃、水泥、固体合金、铝热剂。
2.纯净物和混合物判断中的特殊情况
(1)只含一种元素的物质不一定是纯净物,也可能是混合物,如O 和O,金刚石和石墨,红磷和白磷。
2 3
(2)结晶水合物属于纯净物,如CuSO ·5HO、KAl(SO )·12HO等物质。
4 2 4 2 2
(3)由同位素的不同原子形成的单质或化合物是纯净物,如H 与D、HO和DO。
2 2 2 2
(4)分子式为C H 的物质可能是纯净物,也可能是混合物。
5 10
(5)有机高分子属于混合物,如聚乙烯、淀粉等。
【典例2】(湖北省第七届2022届高三4月调研模拟)下列关于CO、SiO、ClO 、CaO 的说法正确的是(
2 2 2 2
)。
A.CO 的水溶液可导电,所以CO 是电解质
2 2
B.由2C+SiO Si+2CO↑可知C的非金属性强于Si
2
C.由2ClO +2NaOH NaClO+NaClO +H O可知ClO 为酸性氧化物
2 2 3 2 2
D.CaO 中阴离子、阳离子个数比为1∶1
2
【解析】选D。CO 的水溶液可导电,是因为生成的HCO 电离出自由移动的离子导电,所以CO 不是电解质,
2 2 3 2
A选项错误;在2C+SiO Si+2CO↑中C元素的化合价升高,C单质表现还原性,而非金属性是氧化性,B
2
选项错误;ClO 与NaOH溶液发生2ClO +2NaOH NaClO+NaClO +H O,化合价发生变化,因此ClO 不是酸
2 2 2 3 2 2
性氧化物,故、C选项错误;CaO 由Ca2+和O2-构成的离子化合物,阴离子、阳离子个数比为1∶1,D选项正
2 2
确。
【拓展延伸】
1.氧化物的类型
(1)酸性氧化物:与碱反应生成相应的盐和水的氧化物,如SO 、CO、SO 、NO、PO 等。
2 2 3 2 5 2 5
(2)碱性氧化物:与酸反应生成相应的盐和水的氧化物,如NaO、CaO、CuO、Fe O、FeO等。
2 2 3
(3)两性氧化物:既能与酸反应生成盐和水,又能与碱反应生成盐和水的氧化物,如Al O。
2 3
(4)不成盐氧化物:如CO、NO等。
(5)特殊氧化物:如NaO 等。
2 2
2.有关氧化物中的“一定”和“不一定”
(1)酸性氧化物、碱性氧化物不一定都能与水反应生成相应的酸或碱,如SiO、Fe O。
2 2 3
(2)能与碱反应生成盐和水的氧化物不一定是酸性氧化物,如NO 。
2
(3)碱性氧化物都是金属氧化物,但金属氧化物不一定是碱性氧化物,如MnO 为酸性氧化物,Al O 为两
2 7 2 3
性氧化物,NaO 为过氧化物。
2 2
(4)酸性氧化物不一定是非金属氧化物,如MnO;非金属氧化物不一定是酸性氧化物,如CO、NO。
2 7
【典例3】(广东梅州2022~2023学年度高三3月模拟)下图是磷酸、亚磷酸、次磷酸的结构式,其中磷酸为三
元中强酸,亚磷酸为二元弱酸,则下列说法正确的是( )。
A.磷酸(HPO )的电离方程式为:HPO 3H++PO 3-
3 4 3 4 4
B.亚磷酸(HPO )与足量NaOH溶液反应生成NaPO
3 3 3 3
C.NaH PO 溶液呈酸性,是因为HPO 2-的水解程度比电离程度大
2 4 4
D.NaH PO 溶液呈碱性
2 2
【解析】选D。磷酸为三元中强酸,应分步电离,且可逆,电离方程式为HPO H++HPO -,HPO -
3 4 2 4 2 4
H++HPO 2-,HPO 2- H++PO 3-,故A错误;亚磷酸为二元弱酸,只能电离出两个氢离子,所以与足
4 4 4
量NaOH溶液反应生成NaHPO ,故B错误;如果NaH PO 溶液呈酸性,说明HPO 2-电离程度大于水解程度,
2 3 2 4 4
故C错误;磷酸含有三个羟基氢为三元酸,亚磷酸含有两个羟基氢为二元酸,而次磷酸只含一个羟基氢,所以
资料收集整理【淘宝店铺:向阳百分百】应为一元酸,所以NaH PO 为正盐,且为强碱弱酸盐,溶液中存在次磷酸根的水解,使溶液显碱性,故D正确。
2 2
【拓展延伸】
1.无机含氧酸的分类:
(1)按照电离出氢离子个数
①一元酸:电离出1个氢离子,如CHCOOH、HMnO 、HNO 等
3 4 3
②二元酸:电离出2个氢离子,如HSO 、HCO、HSO 等
2 4 2 3 2 3
③多元酸:电离出多个氢离子,如HSiO、HPO 等
4 4 3 4
(2)按照中心元素是否具有强氧化性
①氧化性酸:中心元素具有强氧化性,如浓HSO 、浓HNO、稀HNO、HClO等
2 4 3 3
②非氧化性酸:中心元素没有强氧化性,如稀HSO 、盐酸、醋酸等
2 4
2.无机含氧酸和含氧酸盐
(1)含氧酸的结构
含氧酸 HSO HPO HCO HNO
2 4 3 4 2 3 3
结构简式
酸的元数 二元酸 三元酸 二元酸 一元酸
(2)含氧酸和其相应含氧酸盐种类的关系
n元酸 n 种正盐, n - 1 种酸式盐
【典例4】(2022·浙江6月选考)下列说法不正确的是( )。
A.乙醇和丙三醇互为同系物
B.35Cl和37Cl互为同位素
C.O 和O 互为同素异形体
2 3
D.丙酮(CH- -CH)和环氧丙烷( )互为同分异构体
3 3
【解析】选A。结构相似,组成上相差若干个CH 原子团的有机化合物为同系物,乙醇(CHCHOH)是饱和
2 3 2
一元醇,丙三醇是饱和三元醇,两者所含官能团数目不同,不互为同系物,A错误;质子数相同、中子数不同
的同种元素互为同位素,35Cl的质子数为17,中子数为18,37Cl的质子数为17,中子数为20,两者质子数相同、
中子数不同,互为同位素,B正确;由同种元素组成的不同的单质互为同素异形体,O 和O 是由氧元素组成的
2 3
不同的单质,两者互为同素异形体,C正确;分子式相同、结构不同的化合物互为同分异构体,丙酮和环氧丙
烷的分子式相同、结构不同,两者互为同分异构体,D正确。
【拓展延伸】物质间的关系
1.“四同”概念的比较
同位素 同素异形体 同系物 同分异构体
质子数相同, 结构相似,分子组 分子式相同,
由同一种元素组
定义 中子数不同的 成相差一个或若干 结构不同的化
成的不同单质
原子(核素) 个CH 基团的物质 合物
2
对象 原子 单质 化合物 化合物
元素符号表示 元素符号表示相
化学 1 同,分子式可以
不同,如1H、 不同 相同
式 不同,如O 和
2 3 2
1 H、1H O 3
电子层结构相
单质的组成或结
结构 同,原子核结 相似 不同
构不同
构不同
物理性质不 物理性质不
物理性质不同, 物理性质不同,化
性质 同,化学性质 同,化学性质
化学性质相同 学性质相似
相同 不一定相同
相互
核变化 化学变化 化学变化 化学变化
转化
2.同种物质:完全相同的物质
(1)同一物质有不同名称:三氯甲烷和氯仿
(2)同一物质有不同写法:HSiO 和Si(OH)、Al(OH) 与HAlO
4 4 4 3 3 3
资料收集整理【淘宝店铺:向阳百分百】(3)分子式相同的一碳有机物: 和
(4)分子式相同书写顺序不同的有机物
①(CH)CHCH 和CH- CH
3 2 3 3 3
② - CH-CH 与CHCH- CH-CH
2 2 3 3 2 2 3
③ 和
④HOOC-CH- -COOH与HOOC- -CH-COOH
2 2
⑤ 、 、
(5)邻二取代苯: 和
3.同类不同种分子:相同元素不同核素组成的分子
(1)氢气分子:H、D、T、HD、HT、DT
2 2 2
(2)水分子:HO、DO、TO、HDO、HTO、DTO
2 2 2
(3)氯化氢分子:HCl、DCl、TCl
1.(石家庄精英中学2022~2023学年高三第一学期第一次考试)下表中各组物质分类全部正确的是( )。
选项 纯净物 碱 碱性氧化物 强电解质
A 碱石灰 纯碱 CaO 醋酸
B 烧碱 氢氧化钾 Al O 硫酸钡
2 3
84消毒 澄清石灰
C NaO 氯化钠
液 水 2 2
D 胆矾 NH ·HO Fe O 碳酸钙
3 2 2 3
【解析】选D。碱石灰是氢氧化钠和氧化钙的混合物;纯碱是碳酸钠属于盐;CaO能与酸反应生成盐和水是碱
性氧化物;醋酸是弱酸是弱电解质,故A错误;烧碱是氢氧化钠的俗名,氢氧化钠是纯净物;氢氧化钾是强碱;
Al O 属于两性氧化物;硫酸钡虽然是难溶物,但溶于水的部分是完全电离的,是强电解质,故B错误;84消
2 3
毒液属于混合物;澄清石灰水属于混合物;NaO 与酸反应生成盐和水外还生成氧气,不属于碱性氧化物,属于
2 2
过氧化物;氯化钠在熔融态和水溶液状态均能完全电离,是强电解质,故C错误;胆矾是五水硫酸铜晶体,属
于纯净物;NH ·HO是弱碱,属于碱;Fe O 与酸反应生成盐和水是碱性氧化物;碳酸钙虽然是难溶物,但溶于
3 2 2 3
水的部分是完全电离的,是强电解质,故D正确。
2.(石家庄2022~2023学年高三第一学期第一次考试)下列说法正确的是( )。
A.氯气的水溶液可以导电,说明氯气是电解质
B.PM2.5(微粒直径约为2.5×10-6m)分散在空气中形成气溶胶,能产生丁达尔效应
C.电离时生成的阴离子全部是OH-的化合物叫做碱
D.含钙、钡、铁等金属元素的物质有绚丽的颜色,可用于制造焰火
【解析】选C。氯气为单质,既不是电解质也不是非电解质,故A错误;胶体的粒子直径在1~100nm,PM2.5
(微粒直径约为2.5×10-6m)分散在空气中不能形成气溶胶,故B错误;电离时生成的阴离子全部是OH-的化
合物叫做碱,故C正确;含钙、钡等金属元素的物质有绚丽的颜色,可用于制造焰火,铁元素不具有焰色试验,
故D错误。
3.(内蒙古彦淖尔市临河区2022届高三上学期第一次模拟)下列各组物质,按化合物、单质、混合物顺序排
列的是( )。
A.烧碱、液态氧、碘酒
B.生石灰、白磷、熟石灰
C.干冰、铁、氯化氢
D.空气、氮气、胆矾
【解析】选A。烧碱是NaOH的俗称,是化合物,液态氧是单质,碘酒是溶液,属于混合物。选A;生石灰是
CaO的俗称,是化合物,白磷是单质,熟石灰是Ca(OH) 的俗称,是化合物,故不选B;干冰是指固态的二
2
氧化碳,是化合物,铁是单质,氯化氢是化合物,故不选C;空气中含有氮气、氧气等多种成分是混合物,氮
气是单质,胆矾是五水合硫酸铜,是化合物,故不选D。
4.(2023年1月浙江省选考仿真模拟卷B)下列关于物质的分类不正确的是( )。
A.尿素-有机物 B.云-气溶胶
C.纤维素-纯净物 D.硝酸-共价化合物
【解析】选C。A项,尿素的化学式为:CO(NH ),含有碳和氢两种元素,属于有机物,A正确;B项,云
2 2
资料收集整理【淘宝店铺:向阳百分百】和雾分散制粒径均在1~100纳米之间,属于气溶胶,B正确;C项,纤维素的化学式为:(C H O),属于混
6 10 6 n
合物,C错误;D项,硝酸的化学式为HNO 分子中只含有非金属元素,且不含铵根离子,属于共价化合物,D
3
正确。
5.(温州市普通高中2023届高三第一次适应性考试)下列说法正确的是( )。
A.1H-、2H、3H+具有相同质子数,互为同位素
B.乙酸、硬脂酸互为同系物
C.乙醇和乙醚互为同分异构体
D.碘和碘蒸气互为同素异形体
【解析】选B。1H-、3H+均不是原子,故不是同位素,A错误;乙酸、硬脂酸均为饱和脂肪酸,互为同系物,B
正确;乙醇分子式为C HO,乙醚分子式为C H O,不是同分异构体,C错误;碘和碘蒸气的分子式均为I,
2 6 4 10 2
是同一物质的不同状态,D错误。
6.(贵州省2023届高三上学期联合考试)下列说法错误的是( )。
A.漂白粉、福尔马林、王水、水玻璃均为混合物
B.工厂中常用的静电除尘与胶体的性质有关
C.金属氧化物一定是碱性氧化物
D.非金属氧化物不一定是酸性氧化物
【解析】选C。本题主要考查物质的分类等知识,侧重考查学生对基础知识的应用能力。金属氧化物不一定是
碱性氧化物,如氧化铝和过氧化钠等,C项错误。
考法 2 物质的转化
1.化学反应类型
2.酸、碱、盐、氧化物和单质之间的转化
【典例5】(2022·湖南省等级考)化学促进了科技进步和社会发展,下列叙述中没有涉及化学变化的是
( )。
A.《神农本草经》中记载的“石胆能化铁为铜”
B.利用“侯氏联合制碱法”制备纯碱
C.科学家成功将CO 转化为淀粉或葡萄糖
2
D.北京冬奥会场馆使用CO 跨临界直冷制冰
2
【解析】选D。“石胆能化铁为铜”指的是铁可以与硫酸铜发生置换反应生成铜,发生了化学变化,A不符合
题意;工业上利用“侯氏联合制碱法”制备纯碱,二氧化碳、氨气、氯化钠和水发生反应生成的碳酸氢钠晶体
经加热后分解生成碳酸钠即纯碱,发生了化学变化,B不符合题意;CO 转化为淀粉或葡萄糖,有新物质生成,
2
发生了化学变化,C不符合题意;使用CO 跨临界直冷制冰,将水直接转化为冰,没有新物质生成,只发生了
2
物理变化,没有涉及化学变化,D符合题意。
【拓展延伸】
1.常见的物理变化和化学变化
项目 物理变化 化学变化
三馏 分馏、蒸馏 干馏
资料收集整理【淘宝店铺:向阳百分百】三色 焰色试验 显色反应、指示剂变色反应
五解 潮解 分解、电解、水解、裂解
氢化、氧化、水化、风化、炭化、钝化、煤的气
熔化、汽化、液化、升
十八化(华) 化、煤的液化、皂化、歧化、卤化、硝化、酯化、
华
裂化
2.有关物质变化的几点误区
(1)电解质的电离是物理变化,电解质溶液导电是化学变化。
(2)同素异形体的转化(如:O 与O 的相互转化),结晶水合物形成(如:CuSO +5H O=
2 3 4 2
CuSO ·5HO),结晶水合物失水(如:CuSO ·5HO CuSO +5H O)是化学变化;原子核的裂变、聚变不是
4 2 4 2 4 2
化学变化。
(3)蛋白质的变性属于化学变化;蛋白质的盐析属于物理变化。
【典例6】(2023·四川德阳模拟)下列物质在给定条件下的转化均能一步实现的是( )。
A.Fe Fe O FeCl
2 3 3
B.Na NaO NaOH
2
C.CaCl 溶液 CaCO CO
2 3 2
D.CuSO 溶液 Cu CuO
4
【解析】选D。铁和水蒸气高温生成四氧化三铁,A错误;钠和氧气加热生成过氧化钠,B错误;二氧化碳和
氯化钙不反应,C错误;CuSO 溶液与Fe反应生成硫酸亚铁和Cu,Cu与氧气加热反应生成CuO,D正确。
4
【拓展延伸】
1.物质间转化的几个常见误区
(1)S燃烧不能直接生成SO 而是生成SO 。
3 2
(2)Al O、SiO、Fe O 与水不反应,不能直接转化为Al(OH)、HSiO、Fe(OH)。
2 3 2 2 3 3 2 3 3
(3)NH 催化氧化不能直接生成NO 而是生成NO。
3 2
(4)Fe分别与Cl、Br 反应生成FeCl 、FeBr ,Fe分别与S、I 反应生成FeS、FeI,Cu与S反应生成
2 2 3 3 2 2
Cu S。
2
(5)Fe与H+、Cu2+反应不能生成Fe3+。
2.不同类别的无机物之间转化的2条主线
(1)金属单质及其化合物的转化
①转化关系:金属单质 碱性氧化物 碱 盐
②典型实例:Na NaO NaOH NaSO
2 2 4
③符合元素:Na、K、Ca、Ba等,但Mg、Fe、Al、Cu等不符合上述转化关系。
(2)非金属单质及其化合物的转化
①转化关系:非金属单质 酸性氧化物 酸 盐
②典型实例:S SO HSO NaSO
2 2 3 2 3
③符合元素:C、S、P等,但N、Si等不符合上述转化关系。
3.常见物质的转化规律
(1)“易溶制难溶”规律
①Na SO 溶液与BaCl 溶液反应:Ba2++SO2- BaSO↓
2 4 2 4 4
②加碳酸钠使水垢中的CaSO 转化成CaCO :CaSO(s)+CO 2-(aq)=CaCO (s)+SO2-(aq)
4 3 4 3 3 4
(2)“难挥发制易挥发”规律
①实验室制取HBr气体:HPO (浓)+NaBr(固) NaH PO +HBr↑
3 4 2 4
②实验室制取HCl气体:NaCl(固)+H SO (浓) NaHSO+HCl↑
2 4 4
(3)“强制弱”规律
分类 实例 离子方程式
酸 CHCOONa+HCl CHCOO-+H+ CHCOOH
3 3 3
碱 FeCl +NaOH Fe3++3OH- Fe(OH)↓
3 3
氧化
Cl+KI Cl+2I- I+2Cl-
剂 2 2 2
还原
Fe+CuSO Cu2++Fe Cu+Fe2+
剂 4
【典例7】(2023·威海模拟)一种提纯白磷样品(含惰性杂质)的工艺流程如图所示。下列说法不正确的是
资料收集整理【淘宝店铺:向阳百分百】