高频考点 29 化学反应速率和化学平衡图像
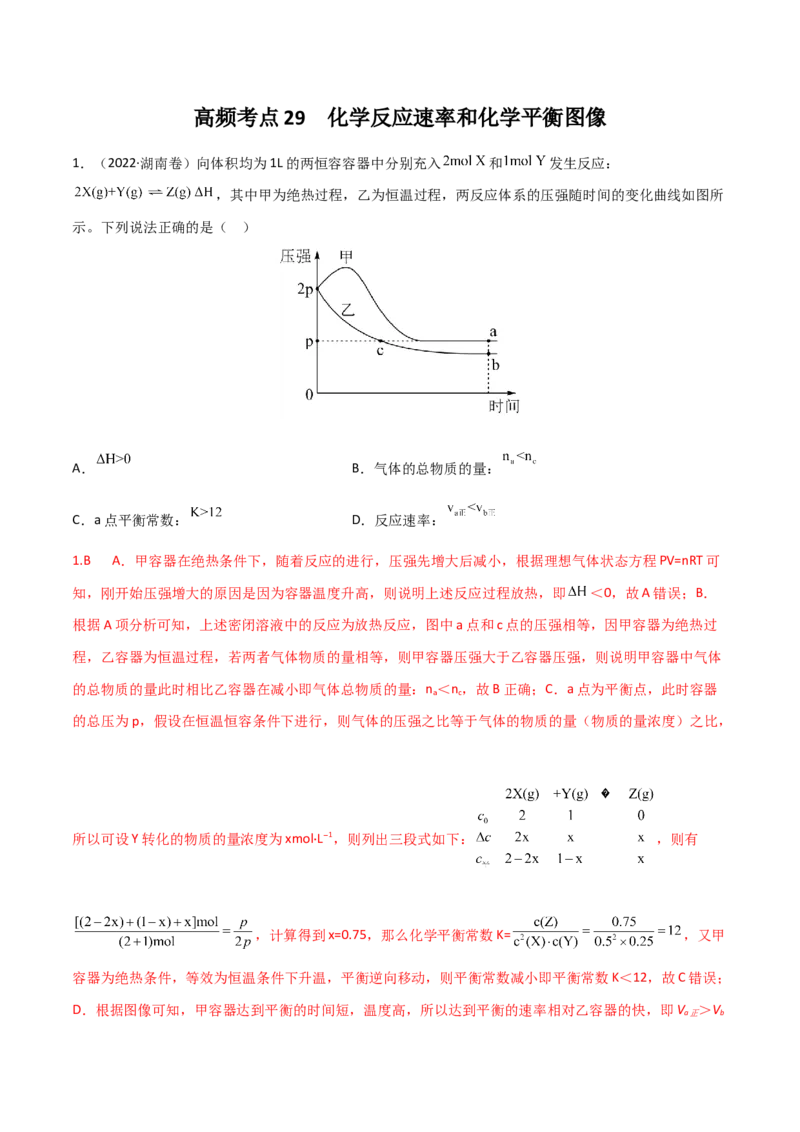
1.(2022·湖南卷)向体积均为1L的两恒容容器中分别充入 和 发生反应:
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所
示。下列说法正确的是( )
A. B.气体的总物质的量:
C.a点平衡常数: D.反应速率:
1.B A.甲容器在绝热条件下,随着反应的进行,压强先增大后减小,根据理想气体状态方程PV=nRT可
知,刚开始压强增大的原因是因为容器温度升高,则说明上述反应过程放热,即 <0,故A错误;B.
根据A项分析可知,上述密闭溶液中的反应为放热反应,图中a点和c点的压强相等,因甲容器为绝热过
程,乙容器为恒温过程,若两者气体物质的量相等,则甲容器压强大于乙容器压强,则说明甲容器中气体
的总物质的量此时相比乙容器在减小即气体总物质的量:n<n,故B正确;C.a点为平衡点,此时容器
a c
的总压为p,假设在恒温恒容条件下进行,则气体的压强之比等于气体的物质的量(物质的量浓度)之比,
所以可设Y转化的物质的量浓度为xmol∙L−1,则列出三段式如下: ,则有
,计算得到x=0.75,那么化学平衡常数K= ,又甲
容器为绝热条件,等效为恒温条件下升温,平衡逆向移动,则平衡常数减小即平衡常数K<12,故C错误;
D.根据图像可知,甲容器达到平衡的时间短,温度高,所以达到平衡的速率相对乙容器的快,即V >V
a正 b,故D错误。综上所述,答案为B。
正
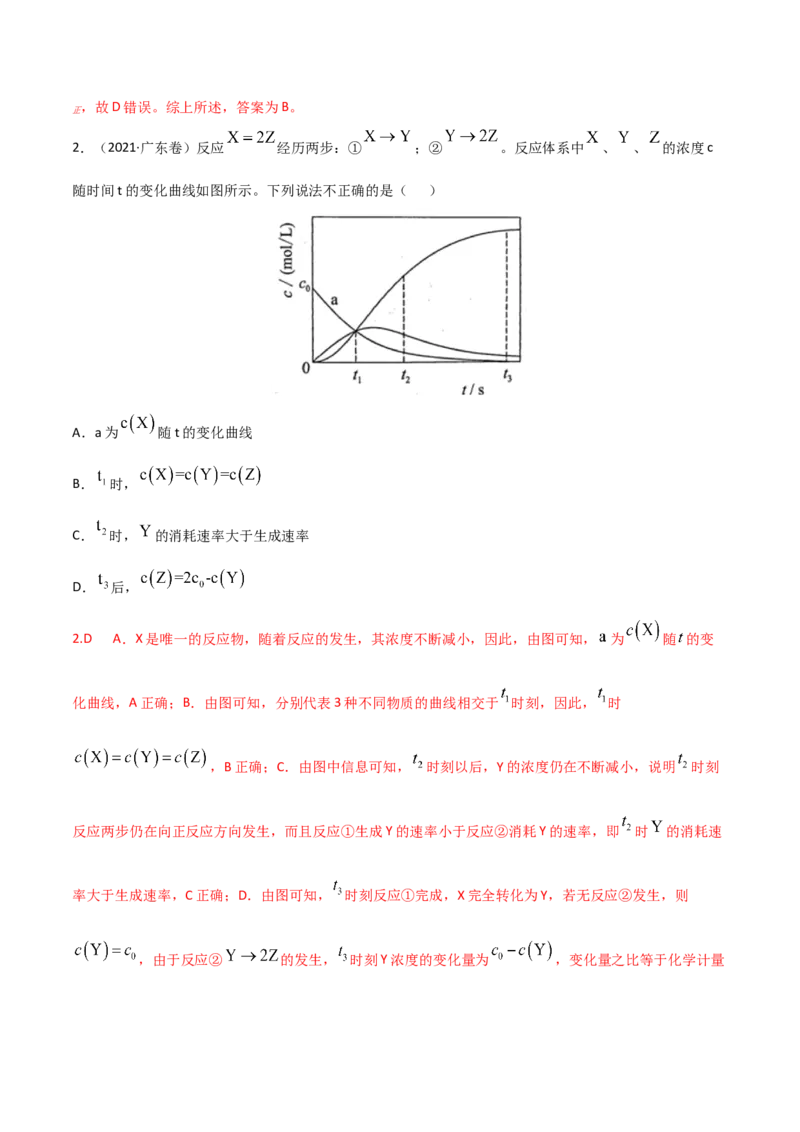
2.(2021·广东卷)反应 经历两步:① ;② 。反应体系中 、 、 的浓度c
随时间t的变化曲线如图所示。下列说法不正确的是( )
A.a为 随t的变化曲线
B. 时,
C. 时, 的消耗速率大于生成速率
D. 后,
2.D A.X是唯一的反应物,随着反应的发生,其浓度不断减小,因此,由图可知, 为 随 的变
化曲线,A正确;B.由图可知,分别代表3种不同物质的曲线相交于 时刻,因此, 时
,B正确;C.由图中信息可知, 时刻以后,Y的浓度仍在不断减小,说明 时刻
反应两步仍在向正反应方向发生,而且反应①生成Y的速率小于反应②消耗Y的速率,即 时 的消耗速
率大于生成速率,C正确;D.由图可知, 时刻反应①完成,X完全转化为Y,若无反应②发生,则
,由于反应② 的发生, 时刻Y浓度的变化量为 ,变化量之比等于化学计量数之比,所以Z的浓度的变化量为 ,这种关系在 后仍成立, 因此,D不正确。综上所述,
本题选D。
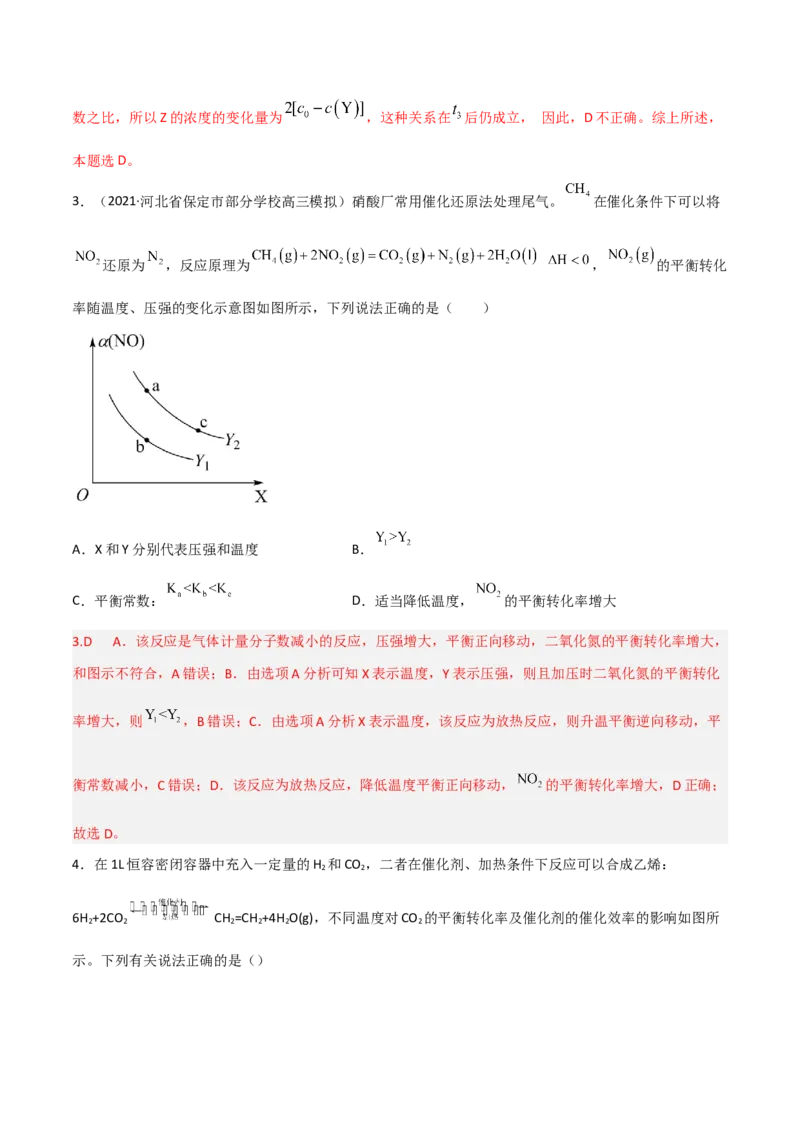
3.(2021·河北省保定市部分学校高三模拟)硝酸厂常用催化还原法处理尾气。 在催化条件下可以将
还原为 ,反应原理为 , 的平衡转化
率随温度、压强的变化示意图如图所示,下列说法正确的是( )
A.X和Y分别代表压强和温度 B.
C.平衡常数: D.适当降低温度, 的平衡转化率增大
3.D A.该反应是气体计量分子数减小的反应,压强增大,平衡正向移动,二氧化氮的平衡转化率增大,
和图示不符合,A错误;B.由选项A分析可知X表示温度,Y表示压强,则且加压时二氧化氮的平衡转化
率增大,则 ,B错误;C.由选项A分析X表示温度,该反应为放热反应,则升温平衡逆向移动,平
衡常数减小,C错误;D.该反应为放热反应,降低温度平衡正向移动, 的平衡转化率增大,D正确;
故选D。
4.在1L恒容密闭容器中充入一定量的H 和CO ,二者在催化剂、加热条件下反应可以合成乙烯:
2 2
6H +2CO CH =CH +4H O(g),不同温度对CO 的平衡转化率及催化剂的催化效率的影响如图所
2 2 2 2 2 2
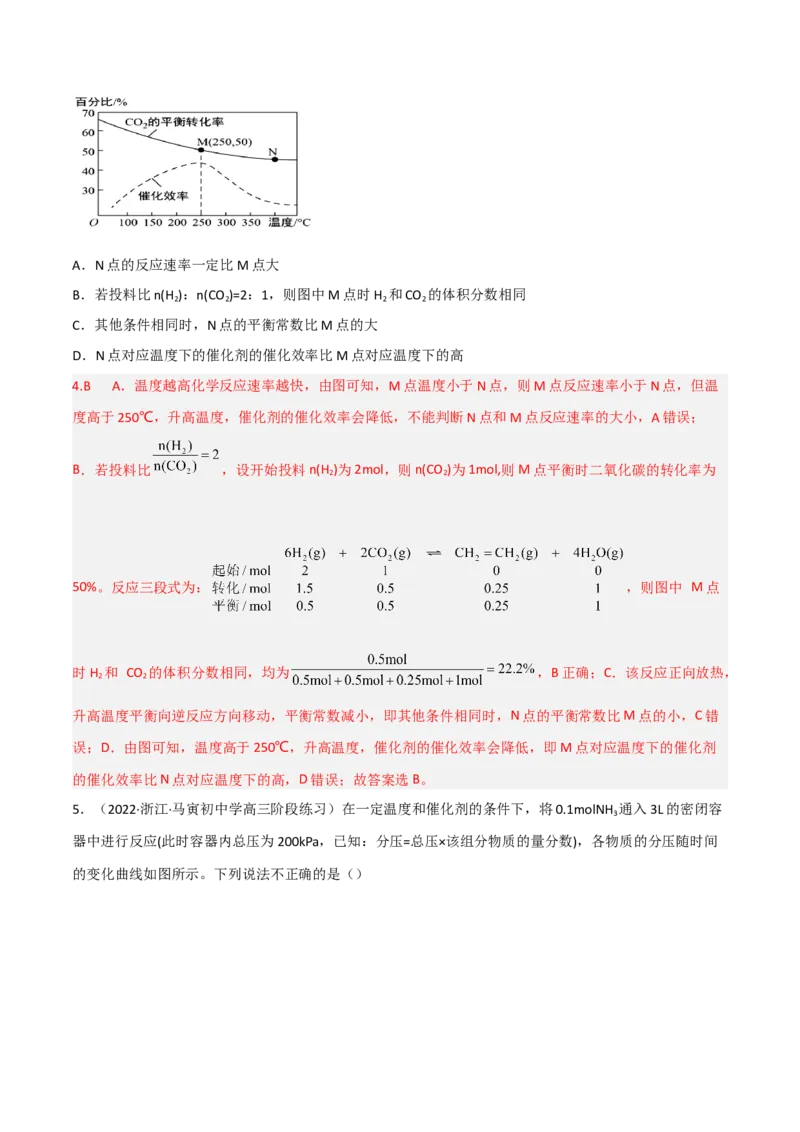
示。下列有关说法正确的是()A.N点的反应速率一定比M点大
B.若投料比n(H ):n(CO )=2:1,则图中M点时H 和CO 的体积分数相同
2 2 2 2
C.其他条件相同时,N点的平衡常数比M点的大
D.N点对应温度下的催化剂的催化效率比M点对应温度下的高
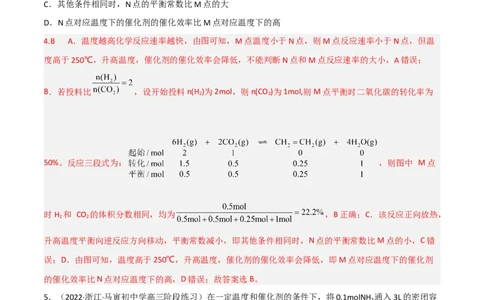
4.B A.温度越高化学反应速率越快,由图可知,M点温度小于N点,则M点反应速率小于N点,但温
度高于250℃,升高温度,催化剂的催化效率会降低,不能判断N点和M点反应速率的大小,A错误;
B.若投料比 ,设开始投料n(H )为2mol,则n(CO )为1mol,则M点平衡时二氧化碳的转化率为
2 2
50%。反应三段式为: ,则图中 M点
时H 和 CO 的体积分数相同,均为 ,B正确;C.该反应正向放热,
2 2
升高温度平衡向逆反应方向移动,平衡常数减小,即其他条件相同时,N点的平衡常数比M点的小,C错
误;D.由图可知,温度高于250℃,升高温度,催化剂的催化效率会降低,即M点对应温度下的催化剂
的催化效率比N点对应温度下的高,D错误;故答案选B。
5.(2022·浙江·马寅初中学高三阶段练习)在一定温度和催化剂的条件下,将0.1molNH 通入3L的密闭容
3
器中进行反应(此时容器内总压为200kPa,已知:分压=总压×该组分物质的量分数),各物质的分压随时间
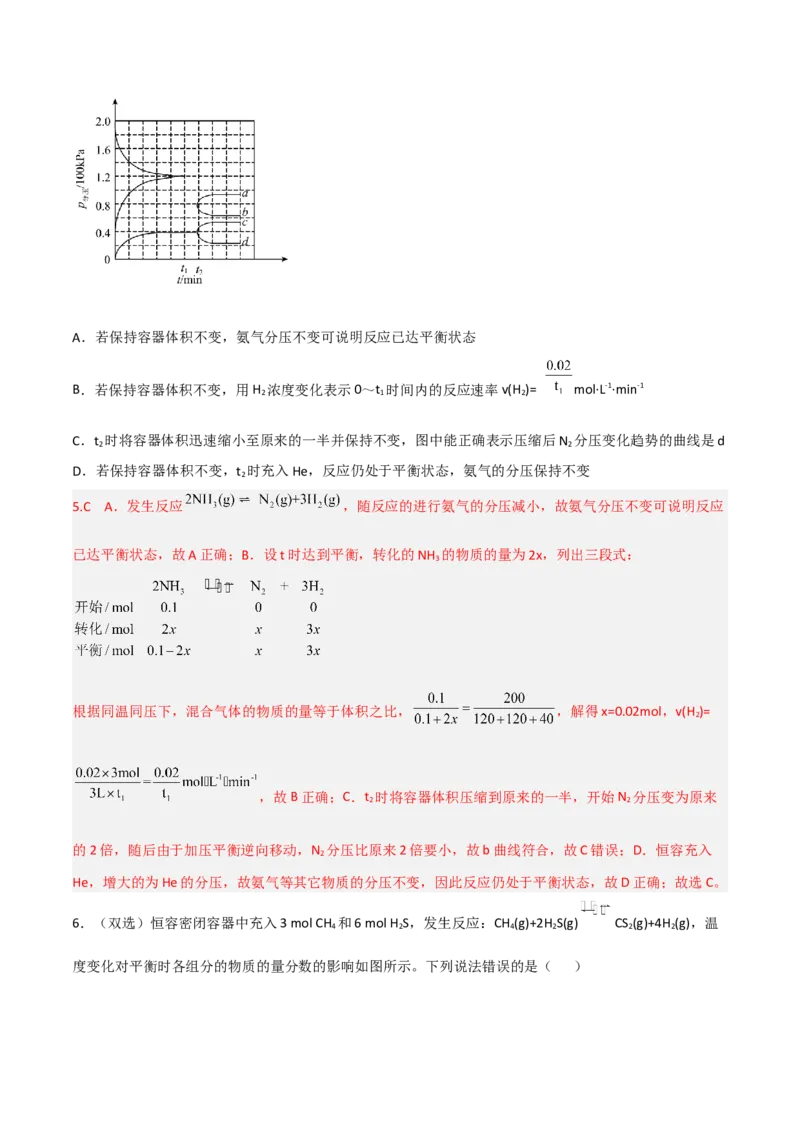
的变化曲线如图所示。下列说法不正确的是()A.若保持容器体积不变,氨气分压不变可说明反应已达平衡状态
B.若保持容器体积不变,用H 浓度变化表示0~t 时间内的反应速率v(H )= mol·L-1·min-1
2 1 2
C.t 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N 分压变化趋势的曲线是d
2 2
D.若保持容器体积不变,t 时充入He,反应仍处于平衡状态,氨气的分压保持不变
2
5.C A.发生反应 ,随反应的进行氨气的分压减小,故氨气分压不变可说明反应
已达平衡状态,故A正确;B.设t时达到平衡,转化的NH 的物质的量为2x,列出三段式:
3
根据同温同压下,混合气体的物质的量等于体积之比, ,解得x=0.02mol,v(H )=
2
,故B正确;C.t 时将容器体积压缩到原来的一半,开始N 分压变为原来
2 2
的2倍,随后由于加压平衡逆向移动,N 分压比原来2倍要小,故b曲线符合,故C错误;D.恒容充入
2
He,增大的为He的分压,故氨气等其它物质的分压不变,因此反应仍处于平衡状态,故D正确;故选C。
6.(双选)恒容密闭容器中充入3 mol CH 和6 mol H S,发生反应:CH (g)+2H S(g) CS (g)+4H (g),温
4 2 4 2 2 2
度变化对平衡时各组分的物质的量分数的影响如图所示。下列说法错误的是( )A.当满足v (H S)=2v (H )时,反应达到平衡状态
逆 2 正 2
B.高温、低压条件有利于提高CH 的平衡转化率
4
C.M点时,保持温度不变,继续充入3 mol CH 和6 mol H S,达到新平衡时,CH 的物质的量分数小于H
4 2 4 2
D.图中N点对应温度下,以物质的量分数表示的化学平衡常数K=
x
6.AC A.反应速率之比等于化学计量数之比,则2v (H S)=v (H ),即v (H ) =v (H ),说明反应达到平
逆 2 逆 2 逆 2 正 2
衡状态,A错误;B.由图可知:升高温度,反应物物质的量分数下降,生成物物质的量分数上升,说明升
高温度化学平衡正向移动,则该反应是气体体积增大的吸热反应;采用高温、低压条件,有利于平衡正向
移动,因此有利于提高CH 的平衡转化率,B正确;C.图中M点时,CH 的物质的量分数等于H 的物质的
4 4 2
量分数,保持温度不变,再向容器中充入3 mol CH 和6 mo H S,等效于起始加入充入6 mol CH 和12 mol
4 2 4
H S,相当于增大压强,化学平衡向气体体积减小的逆反应方向移动,则CH 的物质的量分数增大,H 物质
2 4 2
的量分数减小,达到新平衡时,CH 的物质的量分数大于H 的物质的量分数,C错误;D.根据N点数据,
4 2
H S的物质的量分数等于H 的物质的量分数,设CH 转化物质的量为x mol,故反应方程式CH (g)+2H S(g)
2 2 4 4 2
CS (g)+4H (g)中物质反应转化关系可知:反应消耗H S物质的量为 n(H S)=2x mol,反应产生CS 物质
2 2 2 2 2
△
的量 n(CS )=x mol,反应产生H 的物质的量为 n(H )=4x mol,故平衡时n(CH )=(3-x)mol,n(CS )=(6-2x)
2 2 2 4 2
mol,△n(CS )=x mol,n(H )=4x mol,根据N点时△H S的物质的量与H 的物质的量相等可得:6-2x=4x,解得
2 2 2 2
x=1 mol,所以平衡时n(CH )=2 mol,n(H S)=n(H )=4 mol,n(CS )=1 mol,气体的总物质的量为11 mol,化学
4 2 2 2
平衡常数K= ,D正确;故合理选项是AC。
x
7.(2022·江苏省如东高级中学高三开学考试)合成气是一种重要的化工原料气,主要组分为CO和H 。
2
用甲烷、二氧化碳自热重整可制备合成气,反应原理如下:反应I:CH (g)+2O (g) CO (g)+2H O(g) H =-820.6kJ·mol-1
4 2 2 2 1
△
反应II:CH (g)+CO (g) 2CO(g)+2H (g) H =+247.1kJ·mol-1
4 2 2 2
△
反应III:CH (g)+H O(g) CO(g)+3H (g) H =+205.9kJ·mol-1
4 2 2 3
△
反应IV:CO (g)+H (g) CO(g)+H O(g) H
2 2 2 4
△
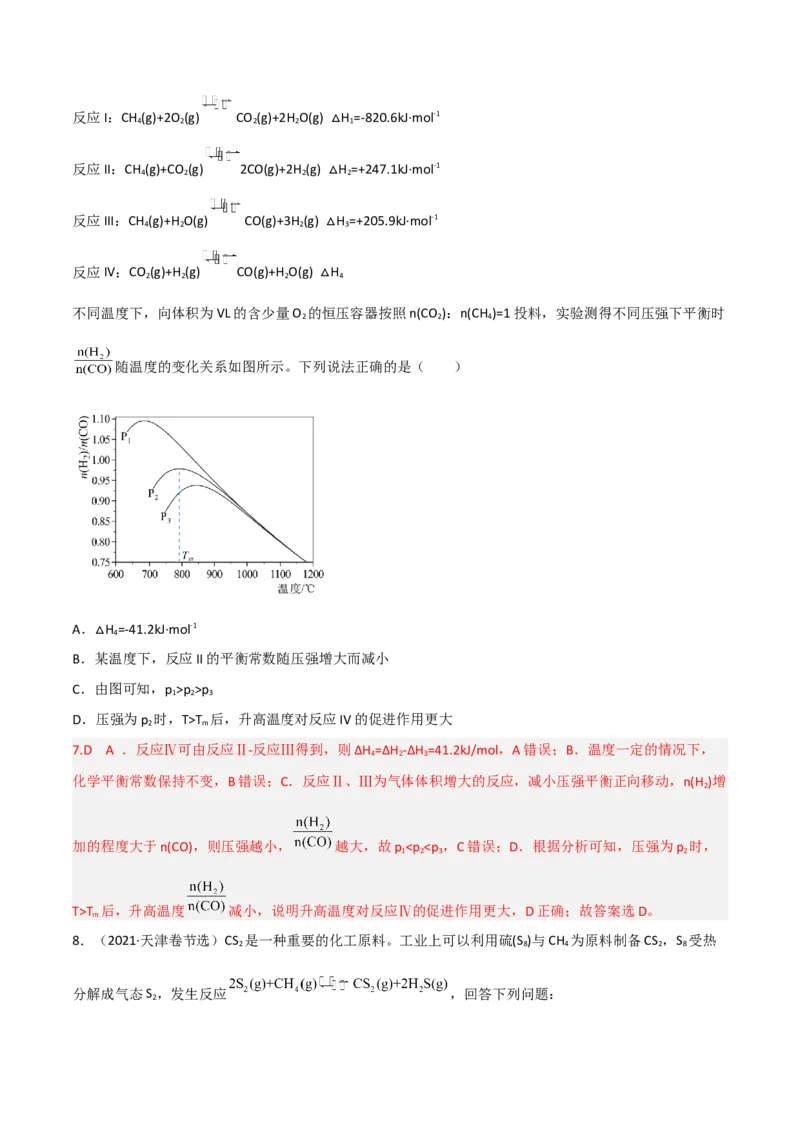
不同温度下,向体积为VL的含少量O 的恒压容器按照n(CO ):n(CH )=1投料,实验测得不同压强下平衡时
2 2 4
随温度的变化关系如图所示。下列说法正确的是( )
A. H =-41.2kJ·mol-1
4
B.某△温度下,反应II的平衡常数随压强增大而减小
C.由图可知,p >p >p
1 2 3
D.压强为p 时,T>T 后,升高温度对反应IV的促进作用更大
2 m
7.D A .反应Ⅳ可由反应Ⅱ-反应Ⅲ得到,则ΔH =ΔH -ΔH =41.2kJ/mol,A错误;B.温度一定的情况下,
4 2 3
化学平衡常数保持不变,B错误;C.反应Ⅱ、Ⅲ为气体体积增大的反应,减小压强平衡正向移动,n(H )增
2
加的程度大于n(CO),则压强越小, 越大,故p
T 后,升高温度 减小,说明升高温度对反应Ⅳ的促进作用更大,D正确;故答案选D。
m
8.(2021·天津卷节选)CS 是一种重要的化工原料。工业上可以利用硫(S )与CH 为原料制备CS ,S 受热
2 8 4 2 8
分解成气态S ,发生反应 ,回答下列问题:
2(1)某温度下,若S 完全分解成气态S 。在恒温密闭容器中,S 与CH 物质的量比为2∶1时开始反应。
8 2 2 4
①当CS 的体积分数为10%时,CH 的转化率为___________。
2 4
②当以下数值不变时,能说明该反应达到平衡的是___________(填序号)。
a.气体密度b.气体总压c.CH 与S 体积比d.CS 的体积分数
4 2 2
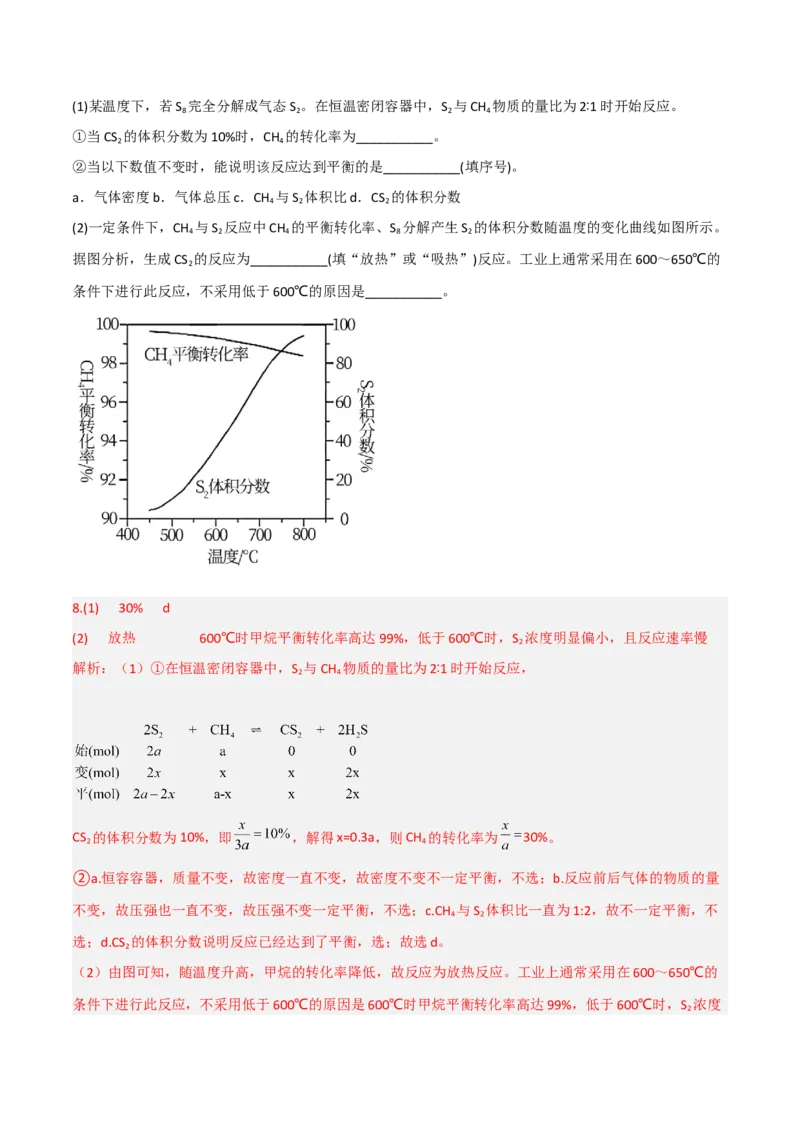
(2)一定条件下,CH 与S 反应中CH 的平衡转化率、S 分解产生S 的体积分数随温度的变化曲线如图所示。
4 2 4 8 2
据图分析,生成CS 的反应为___________(填“放热”或“吸热”)反应。工业上通常采用在600~650℃的
2
条件下进行此反应,不采用低于600℃的原因是___________。
8.(1) 30% d
(2) 放热 600℃时甲烷平衡转化率高达99%,低于600℃时,S 浓度明显偏小,且反应速率慢
2
解析:(1)①在恒温密闭容器中,S 与CH 物质的量比为2∶1时开始反应,
2 4
CS 的体积分数为10%,即 ,解得x=0.3a,则CH 的转化率为 30%。
2 4
②a.恒容容器,质量不变,故密度一直不变,故密度不变不一定平衡,不选;b.反应前后气体的物质的量
不变,故压强也一直不变,故压强不变一定平衡,不选;c.CH 与S 体积比一直为1:2,故不一定平衡,不
4 2
选;d.CS 的体积分数说明反应已经达到了平衡,选;故选d。
2
(2)由图可知,随温度升高,甲烷的转化率降低,故反应为放热反应。工业上通常采用在600~650℃的
条件下进行此反应,不采用低于600℃的原因是600℃时甲烷平衡转化率高达99%,低于600℃时,S 浓度
2明显偏小,且反应速率慢。
9.CO 资源化利用对缓解碳减排压力具有重要意义。在二氧化碳催化加氢制甲烷的反应体系中,发生的主
2
要反应的热化学方程式如下:
反应I:CO (g)+4H (g) CH (g)+2H O(g) H =-164.7kJ·mol-1
2 2 4 2 1
△
反应II:CO (g)+H (g) CO(g)+H O(g) H =+41.2kJ·mol-1
2 2 2 2
△
反应III:2CO(g)+2H (g) CO (g)+CH (g) H =-247.1kJ·mol-1
2 2 4 3
△
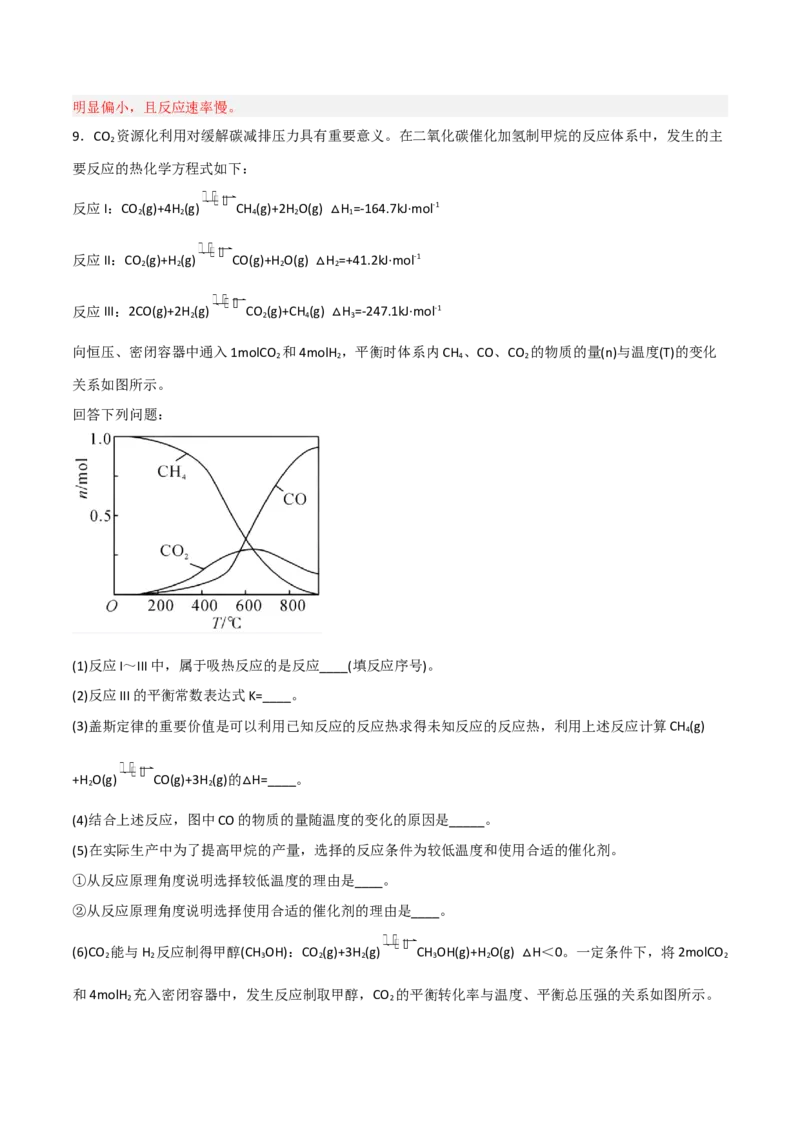
向恒压、密闭容器中通入1molCO 和4molH ,平衡时体系内CH 、CO、CO 的物质的量(n)与温度(T)的变化
2 2 4 2
关系如图所示。
回答下列问题:
(1)反应I~III中,属于吸热反应的是反应____(填反应序号)。
(2)反应III的平衡常数表达式K=____。
(3)盖斯定律的重要价值是可以利用已知反应的反应热求得未知反应的反应热,利用上述反应计算CH (g)
4
+H O(g) CO(g)+3H (g)的 H=____。
2 2
△
(4)结合上述反应,图中CO的物质的量随温度的变化的原因是_____。
(5)在实际生产中为了提高甲烷的产量,选择的反应条件为较低温度和使用合适的催化剂。
①从反应原理角度说明选择较低温度的理由是____。
②从反应原理角度说明选择使用合适的催化剂的理由是____。
(6)CO 能与H 反应制得甲醇(CH OH):CO (g)+3H (g) CH OH(g)+H O(g) H<0。一定条件下,将2molCO
2 2 3 2 2 3 2 2
△
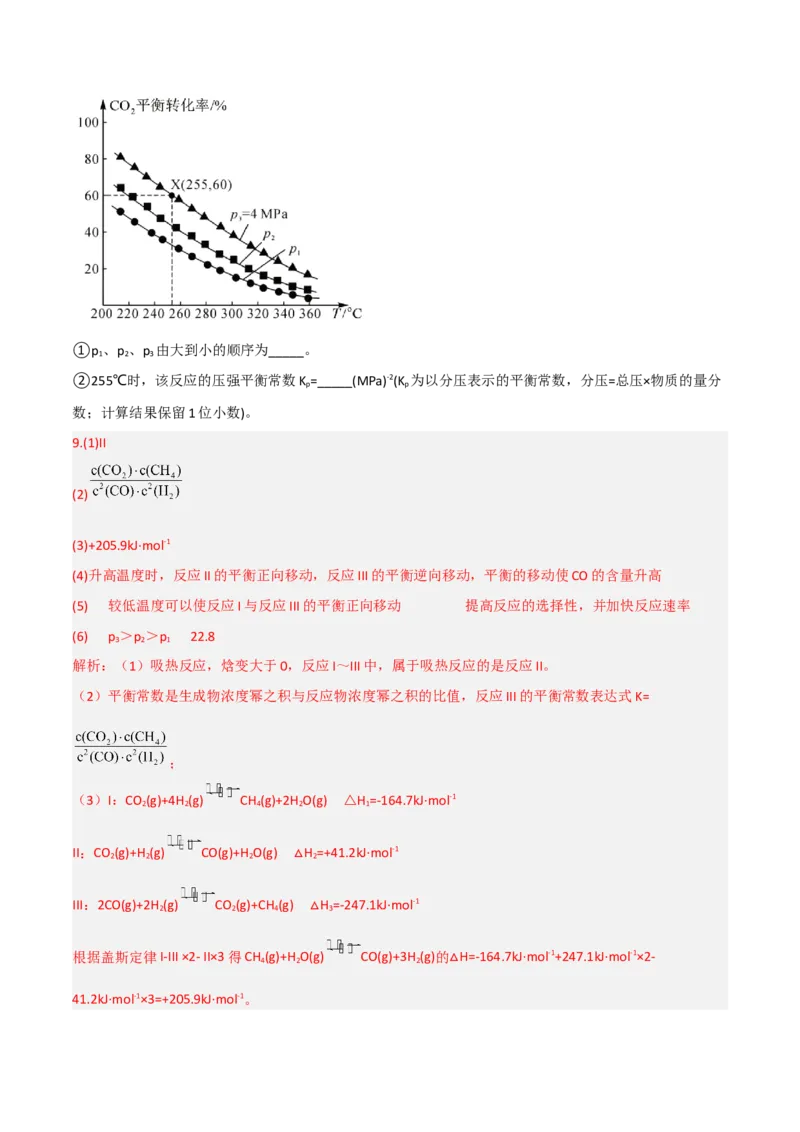
和4molH 充入密闭容器中,发生反应制取甲醇,CO 的平衡转化率与温度、平衡总压强的关系如图所示。
2 2①p 、p 、p 由大到小的顺序为_____。
1 2 3
②255℃时,该反应的压强平衡常数K=_____(MPa)-2(K 为以分压表示的平衡常数,分压=总压×物质的量分
p p
数;计算结果保留1位小数)。
9.(1)II
(2)
(3)+205.9kJ·mol-1
(4)升高温度时,反应II的平衡正向移动,反应III的平衡逆向移动,平衡的移动使CO的含量升高
(5) 较低温度可以使反应I与反应III的平衡正向移动 提高反应的选择性,并加快反应速率
(6) p >p >p 22.8
3 2 1
解析:(1)吸热反应,焓变大于0,反应I~III中,属于吸热反应的是反应II。
(2)平衡常数是生成物浓度幂之积与反应物浓度幂之积的比值,反应III的平衡常数表达式K=
;
(3)I:CO (g)+4H (g) CH (g)+2H O(g) △H =-164.7kJ·mol-1
2 2 4 2 1
II:CO (g)+H (g) CO(g)+H O(g) H =+41.2kJ·mol-1
2 2 2 2
△
III:2CO(g)+2H (g) CO (g)+CH (g) H =-247.1kJ·mol-1
2 2 4 3
△
根据盖斯定律I-III ×2- II×3得CH (g)+H O(g) CO(g)+3H (g)的 H=-164.7kJ·mol-1+247.1kJ·mol-1×2-
4 2 2
△
41.2kJ·mol-1×3=+205.9kJ·mol-1。(4)升高温度时,反应II的平衡正向移动,反应III的平衡逆向移动,平衡的移动使CO的含量升高,所以
CO的物质的量随温度的升高而增大;
(5)①降低温度可以使反应I与反应III的平衡正向移动,所以选择较低温度。
②催化剂能提高反应的选择性,并加快反应速率,所以选择使用合适的催化剂。
(6)①CO (g)+3H (g) CH OH(g)+H O(g)正反应气体系数和减小,增大压强,平衡正向移动,CO 的平衡
2 2 3 2 2
转化率增大,所以p 、p 、p 由大到小的顺序为p >p >p 。
1 2 3 3 2 1
②根据X点数值,
255℃时,该反应的压强平衡常数K= (MPa)-2。
p