文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(广东专用)
黄金卷02
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5
第Ⅰ卷
一、选择题:本题共16个小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在
每小题给出的四个选项中,只有一项是符合题目要求的。
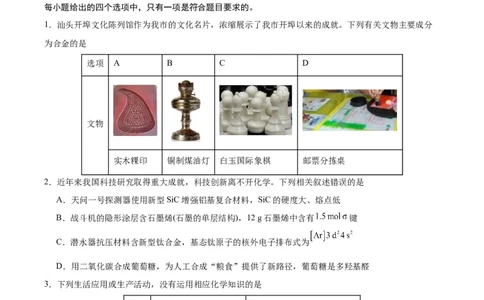
1.汕头开埠文化陈列馆作为我市的文化名片,浓缩展示了我市开埠以来的成就。下列有关文物主要成分
为合金的是
选项 A B C D
文物
实木粿印 铜制煤油灯 白玉国际象棋 邮票分拣桌
2.近年来我国科技研究取得重大成就,科技创新离不开化学。下列相关叙述错误的是
A.天问一号探测器使用新型SiC增强铝基复合材料,SiC的硬度大、熔点低
B.战斗机的隐形涂层含石墨烯(石墨的单层结构),12 g石墨烯中含有 键
C.潜水器抗压材料含新型钛合金,基态钛原子的核外电子排布式为
D.用二氧化碳合成葡萄糖,为人工合成“粮食”提供了新路径,葡萄糖是多羟基醛
3.下列生活应用或生产活动,没有运用相应化学知识的是
选
生活应用或生产活动 化学知识
项
A 用SO 漂白纸张 SO 具有氧化性
2 2
B 用铝槽车运输浓硝酸 Al在冷的浓硝酸中发生钝化
C 用生石灰作食品干燥剂 CaO易与水反应
D 用Si制作芯片 Si是良好的半导体材料
4.锂碘电池可用于心脏起搏器,电池反应可简化为:2Li+I=2LiI。电池工作时,下列说法正确的是
2A.碘电极是电池的负极
B.锂电极发生还原反应
C.电池正极反应:Li-e-=Li+
D.电流从碘电极经外电路流向锂电极
5.中草药蛔蒿常用于治疗蛔虫病。从蛔蒿中提取的抗癌活性成分的结构简式如图所示。下列有关该有机
物说法不正确的是
A.受热时易失去抗癌活性 B.能发生取代、加成、氧化反应
C.一溴代物共有7种 D.同分异构体中可能存在苯环结构
6.在酸性溶液中能大量共存且为无色透明溶液的是
A.
B.
C.
D.
7.从海带中提取碘的部分实验操作为:①灼烧干海带;②海带灰浸泡、过滤;③海带浸取液中通入适量
得到含 的水溶液;④萃取、分液得到含 的 溶液。上述操作中,不需要用到的仪器为
A. B. C. D.
8.“结构决定性质”是化学学科的核心观念。下列有关性质的比较正确的是
A.在水中的溶解度:戊醇<乙醇 B.熔点:MgO<CaO
C.硬度:金刚石<碳化硅<硅 D.第一电离能:Cl<P<S
9.家庭的厨卫管道内常因留有油脂、毛发、菜渣等而造成堵塞,此时可用一种固体疏通剂疏通。疏通剂
主要成分有生物酶、铝粉和 固体。下列有关说法错误的是A.大多数生物酶的主要成分为蛋白质
B.疏通剂使用时会产生大量可燃性气体,应避免接触明火
C.疏通剂可用于疏通陶瓷、铁制、铝制、塑料管道
D.使用过程中产生的热量和碱性环境可以加速油脂的水解
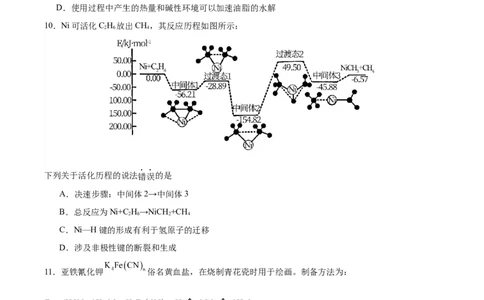
10.Ni可活化C H 放出CH,其反应历程如图所示:
2 6 4
下列关于活化历程的说法错误的是
A.决速步骤:中间体2→中间体3
B.总反应为Ni+C H→NiCH+CH
2 6 2 4
C.Ni—H键的形成有利于氢原子的迁移
D.涉及非极性键的断裂和生成
11.亚铁氰化钾 俗名黄血盐,在烧制青花瓷时用于绘画。制备方法为:
。设 为阿伏加德罗常数,下列说法正确的是
A. 分子中含有 键数目为
B.配合物 的中心离子价电子排布式为 ,该中心离子的配位数为6
C.每生成 时,反应过程中转移电子数目为D. 中阴离子的空间构型为平面三角形,其中碳原子的价层电子对数目为4
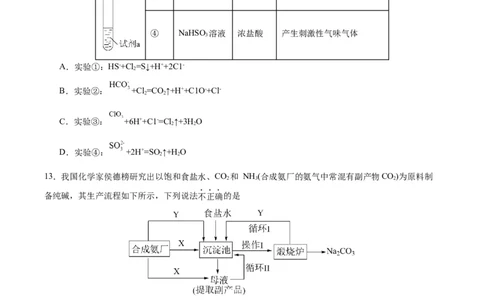
12.下列实验对应反应离子方程式书写正确的是
实验 编号 试剂a 含氯物质 现象
① NaHS溶液 新制氯水 出现乳黄色沉淀
② NaHCO 溶液 新制氯水 产生无色气体
3
③ KClO 溶液 浓盐酸 产生黄绿色刺激性气味气体
3
④ NaHSO 溶液 浓盐酸 产生刺激性气味气体
3
A.实验①:HS-+Cl=S↓+H++2C1-
2
B.实验②: +Cl=CO ↑+H++C1O-+Cl-
2 2
C.实验③: +6H++C1-=Cl↑+3H O
2 2
D.实验④: +2H+=SO↑+H O
2 2
13.我国化学家侯德榜研究出以饱和食盐水、CO 和 NH (合成氨厂的氨气中常混有副产物CO)为原料制
2 3 2
备纯碱,其生产流程如下所示,下列说法不正确的是
A.沉淀池中应先通入 NH ,再通入 CO
3 2
B.流程中的 X 为 CO,Y 为 NH
2 3
C.沉淀池中发生反应:
D.操作 I 为过滤,母液中的一种副产品为 NH Cl,可在农业上用作化肥
4
14.2022年我国科学家首次在月球上发现一种硅酸盐矿物,该物质含有X、Y、Z、W、E五种主族元素,
原子序数依次增大且均不大于20,X、W为非金属元素,Y、Z、E为金属元素,Y的最高正化合价为 ,Z和E同族。下列说法不正确的是
A.原子半径:
B.X和Y可形成含有非极性键的离子化合物
C.Y、Z、E的最高价氧化物对应的水化物均为强碱
D.简单气态氢化物稳定性:
15.2021年3月5日,李克强总理在国务院政府报告中指出,扎实做好碳达峰、碳中和各项工作。科研工
作者通过开发新型催化剂,利用太阳能电池将工业排放的CO 转化为CO,实现节能减排的目标。如图所
2
示,下列有关说法正确的是
A.N极为阴极
B.离子交换膜为阴离子交换膜
C.阳极的电极反应式为CO+2e-+2H+=CO+H O
2 2
D.理论上该装置在工作时,HPO 与KH PO 缓冲溶液的pH保持不变
3 4 2 4
16.甲酸铵常用于电解、电容器行业。25℃时,用HCl或NaOH固体改变0.1 mol/L的HCOONH 溶液的
4
pH,1gc(HCOOH)、1gc(NH ·H O)、1gc(H+)和1gc(OH-)随pH变化的关系如图所示。下列说法错误的是
3 2
[已知:K(HCOOH)=1.8×10-4,K(NH ·H O)=1.8×10-5]
a b 3 2
A.Q点对应溶液pH=7
B.曲线①代表lgc(H+),曲线③代表1gc(NH ·H O)
3 2C.0.1 mol/LHCOONH 溶液中,c(H+)+c(HCOOH)=c(OH-)+c(NH·H O)
4 3 2
D.P点存在c(NH ·H O)>c(OH-)=c(HCOOH)>c(H+)
3 2
第Ⅱ卷
二、非选择题:本题共4个小题,共56分。
17.(14分)过氧化氢是一种常用的绿色试剂,某学习小组针对HO 性质进行如图实验。
2 2
Ⅰ.验证HO 的还原性
2 2
查阅资料:HO 溶液与氯水发生反应时表现还原性。
2 2
(1)制取氯水
①仪器X的名称是 ,生成Cl 的化学方程式为
2
。
②饱和食盐水的作用是 。
(2)取5mL上述新制饱和氯水于试管中,向其中加入HO 溶液至过量,产生大量气泡(该气体可使余烬
2 2
复燃),还观察到溶液颜色发生的变化是 。
Ⅱ.探究Cl-、NO 对HO 分解的影响
2 2
选用CuCl 溶液和Cu(NO ) 溶液,探究Cl-、NO 对HO 分解的影响。记录数据如下:
2 3 2 2 2
实验
添加试剂及用量 HO 完全分解所需时间/min
2 2
序号
1 amLbmol·L-1CuCl 溶液 t
2 1
2 amLbmol·L-1Cu(NO ) 溶液 t
3 2 2(3)实验结果显示tt)
液和② (填标号) 4 4 2
(6)根据实验1~4中测得的HO 完全分解所需时间,小组同学认为Cl- (填“增强”或“减
2 2
弱”,下同)Cu2+的催化效果,NO Cu2+的催化效果。
18.(14分)氮化镓(GaN)具有优异的光电性能。一种利用炼锌矿渣[主要含铁酸镓 、铁酸锌
、 ]制备GaN的工艺流程如下:
已知:
①Ga与Al同主族,化学性质相似。②常温下, , , 。
③ 、 在该工艺条件下的反萃取率(进入水相中金属离子的百分数)与盐酸浓度的关系见下表。
反萃取率/%
盐酸浓度/
2 86.9 9.4
4 69.1 52.1
6 17.5 71.3
回答下列问题:
(1)“酸浸”时 发生反应的离子方程式为 。“酸溶”
所得滤渣的主要成分是 (填化学式)。
(2)“酸浸”所得浸出液中 、 浓度分别为0.21 、65 。常温下,为尽可能多地提取
并确保不混入 ,“调pH”时需用CaO调pH至 (假设调pH时溶液体积
不变)。
(3)“脱铁”和“反萃取”时,所用盐酸的浓度a= ,b= (选填上表中
盐酸的浓度)。
(4)“沉镓”时,若加入NaOH的量过多,会导致 的沉淀率降低,原因是
(用离子方程式表示)。
(5)利用CVD(化学气相沉积)技术,将热分解得到的 与 在高温下反应可制得GaN,同时生成
另一种产物,该反应化学方程式为 。
(6)①GaN的熔点为1700℃, 的熔点为77.9℃,它们的晶体类型依次为 、
。
②GaN晶体的一种立方晶胞如图所示。该晶体中与Ga原子距离最近且相等的N原子个数为
。该晶体密度为 ,GaN的式量为 ,则晶胞边长为 nm。(列出计算式,为阿伏加德罗常数的值)
19.(14分)降低大气中CO 的含量和有效地开发利用CO 正成为研究的主要课题。
2 2
(1)已知在常温常压下:
① 2CHOH(l) + 3O(g) = 2CO(g) + 4HO(g) ΔH =-1275.6 kJ/mol
3 2 2 2
② 2CO (g)+ O (g) = 2CO(g) ΔH =-566.0 kJ/mol
2 2
③ HO(g) = HO(l) ΔH =-44.0 kJ/mol
2 2
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
。
(2)在容积为2L的密闭容器中,充入2mol CO 和6mol H,在温度500℃时发生反应:
2 2
CO(g)+ 3H (g) CHOH(g)+ H O(g) △H<0。
2 2 3 2
CHOH的浓度随时间变化如图。回答有关问题:
3
①从反应开始到20分钟时,H 的平均反应速率v(H )=
2 2
②从30分钟到35分钟达到新的平衡,改变的条件可能是 (填序号)。
A.增大压强 B.加入催化剂 C.升高温度 D.增大反应物的浓度
③列式计算该反应在35分钟达到新平衡时的平衡常数(保留2位小数)
④如果在30分钟时,再向容器中充入2mol CO 和6mol H,保持温度不变,达到新平衡时,CHOH的浓度
2 2 3
1mol·L-1(填“>”、“<”或“=”)。
(3)一种原电池的工作原理为:2NaS + NaBr NaS + 3NaBr。用该电池为电源,以氢氧化钾水溶液
2 2 3 2 4
作电解质进行电解,使CO 在铜电极上可转化为甲烷。
2
①该电池负极的电极反应式为:
②电解池中产生CH 一极的电极反应式为: 。
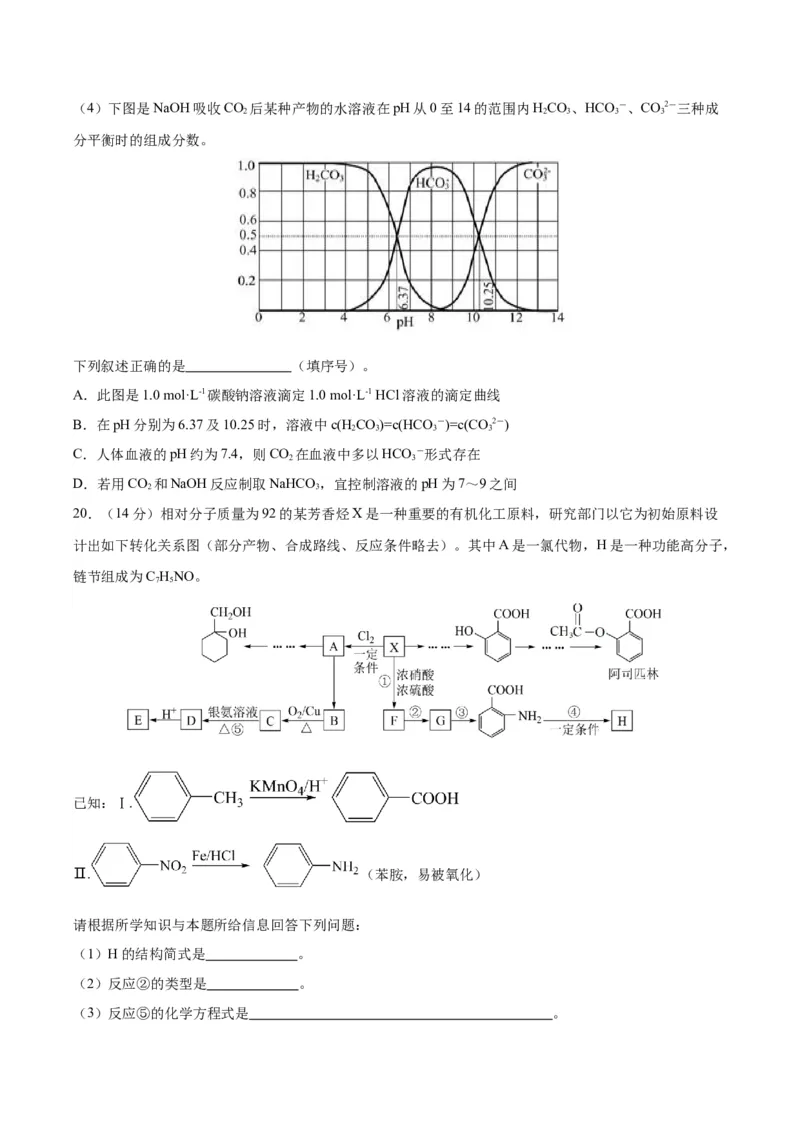
4(4)下图是NaOH吸收CO 后某种产物的水溶液在pH从0至14的范围内HCO、HCO -、CO2-三种成
2 2 3 3 3
分平衡时的组成分数。
下列叙述正确的是 (填序号)。
A.此图是1.0 mol·L-1碳酸钠溶液滴定1.0 mol·L-1 HCl溶液的滴定曲线
B.在pH分别为6.37及10.25时,溶液中c(HCO)=c(HCO-)=c(CO 2-)
2 3 3 3
C.人体血液的pH约为7.4,则CO 在血液中多以HCO -形式存在
2 3
D.若用CO 和NaOH反应制取NaHCO ,宜控制溶液的pH为7~9之间
2 3
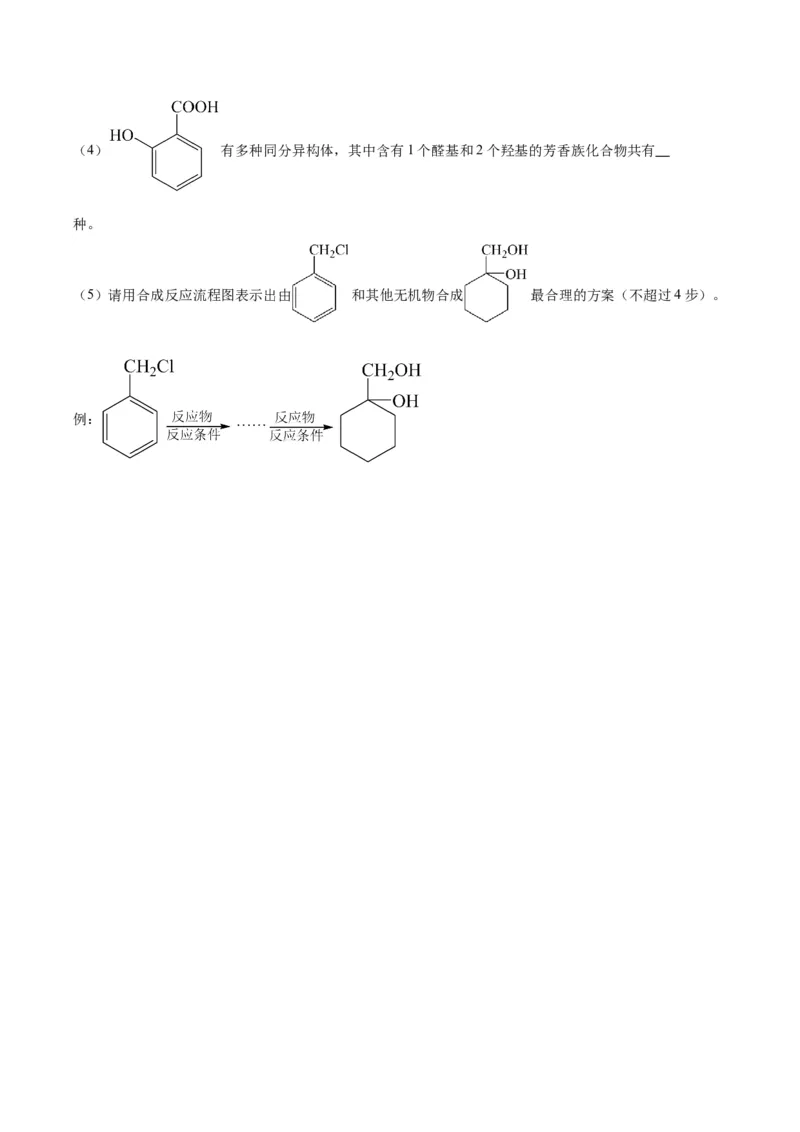
20.(14分)相对分子质量为92的某芳香烃X是一种重要的有机化工原料,研究部门以它为初始原料设
计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,
链节组成为C HNO。
7 5
已知:Ⅰ.
Ⅱ. (苯胺,易被氧化)
请根据所学知识与本题所给信息回答下列问题:
(1)H的结构简式是 。
(2)反应②的类型是 。
(3)反应⑤的化学方程式是 。(4) 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有
种。
(5)请用合成反应流程图表示出由 和其他无机物合成 最合理的方案(不超过4步)。
例: