文档内容
2022 年广东省普通高中学业水平选择性考试
化学
本试卷共8页,21小题,满分100分,考试用时75分钟。
注意事项:
1.答卷前,考生务必用黑色字迹钢笔或签字笔将自己的姓名、考生号、考场号和座位号填写
在答题卡上。用2B铅笔将试卷类型(A)填涂在答题卡相应位置上。将条形码横贴在答题卡右
上角“条形码粘贴处”。
2.作答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目选项的答案信息点涂黑;
如需改动,用橡皮擦干净后,再选涂其他答案,答案不能答在试卷上。
3.非选择题必须用黑色字迹钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内相应
位置上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液。不
按以上要求作答的答案无效。
4.作答选考题时,请先用2B铅笔填涂选做题的题号对应的信息点,再作答。漏涂、错涂、多
涂的,答案无效。
5.考生必须保持答题卡的整洁。考试结束后,将试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 S 32 Cl 35.5
Fe 56
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题
4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 中华文明源远流长,在世界文明中独树一帜,汉字居功至伟。随着时代发展,汉字被不断赋予新的文化
内涵,其载体也发生相应变化。下列汉字载体主要由合金材料制成的是
汉
字
载
体
选
A.兽骨 B.青铜器 C.纸张 D.液晶显示屏
项
第1页 | 共30页A. A B. B C. C D. D
【答案】B
【解析】
【详解】A.兽骨,甲骨文的契刻载体之一,主要是牛的肩胛骨,一小部分是羊、猪、鹿的肩胛骨,还有
极少部分的牛肋骨,其主要成分是碳酸钙和其它钙盐,故A不符合题意;
B.青铜器是红铜与其他化学元素锡、铅等的合金,属于合金材料,故B项符合题意;
C.纸张的主要成分是纤维素,故C不符合题意;
D.液晶显示器是一种采用液晶为材料的显示器,液晶是一类介于固态和液态间的有机化合物,故D不符
合题意;
综上所述,答案为B项。
2. 北京冬奥会成功举办、神舟十三号顺利往返、“天宫课堂”如期开讲及“华龙一号”核电海外投产等,均展
示了我国科技发展的巨大成就。下列相关叙述正确的是
A. 冬奥会“飞扬”火炬所用的燃料 为氧化性气体
B. 飞船返回舱表层材料中的玻璃纤维属于天然有机高分子
C. 乙酸钠过饱和溶液析出晶体并放热的过程仅涉及化学变化
D. 核电站反应堆所用轴棒中含有的 与 互为同位素
【答案】D
【解析】
【详解】A.H 作为燃料在反应中被氧化,体现出还原性,故A项说法错误;
2
B.玻璃纤维是一种性能优异的无机非金属材料,故B项说法错误;
C.乙酸钠饱和溶液中析出晶体的过程中无新物质生成,因此属于物理变化,故C项说法错误;
D. 与 是质子数均为92,中子数不同的核素,因此二者互为同位素,故D项说法正确;
综上所述,叙述正确的是D项。
3. 广东一直是我国对外交流的重要窗口,馆藏文物是其历史见证。下列文物主要由硅酸盐制成的是
第2页 | 共30页文
物
选
A.南宋鎏金饰品 B.蒜头纹银盒 C.广彩瓷咖啡杯 D.铜镀金钟座
项
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.鎏金饰品是用金汞合金制成的金泥涂饰器物的表面,经过烘烤,汞蒸发而金固结于器物上的
一种传统工艺,其中不含硅酸盐,故A项不符合题意;
B.蒜头纹银盒中主要成分为金属银,其中不含硅酸盐,故B项不符合题意;
C.广彩瓷咖啡杯是由黏土等硅酸盐产品烧制而成,其主要成分为硅酸盐,故C项符合题意;
D.铜镀金钟座是铜和金等制得而成,其中不含硅酸盐,故D项不符合题意;
综上所述,答案为C。
4. 实验室进行粗盐提纯时,需除去 和 ,所用试剂包括 以及
A. B.
C. D.
【答案】A
【解析】
【分析】除杂过程中不能引入新杂质,同时为保证除杂完全,所加除杂试剂一般过量,然后选择合适的试
剂将所加过量的物质除去。
【详解】粗盐中主要成分为NaCl。除去Ca2+选用 将其转化为沉淀,为了不引入新杂质,所加物质的
阳离子为Na+,即选用NaCO 除去Ca2+,同理可知,除去Mg2+需选用NaOH,除去 需选用BaCl ,因
2 3 2
第3页 | 共30页所加除杂试剂均过量,因此向粗盐样品中加入除杂试剂的顺序中,BaCl 先于NaCO 加入,利用NaCO 除
2 2 3 2 3
去Ca2+和多余的BaCl ,因NaCO、NaOH均过量,成为新杂质,需要过滤后向滤液中加入HCl,至溶液
2 2 3
中不再有气泡产生,以此除去NaCO、NaOH,然后将溶液蒸干得到较为纯净的食盐产品,综上所述,答
2 3
案为A。
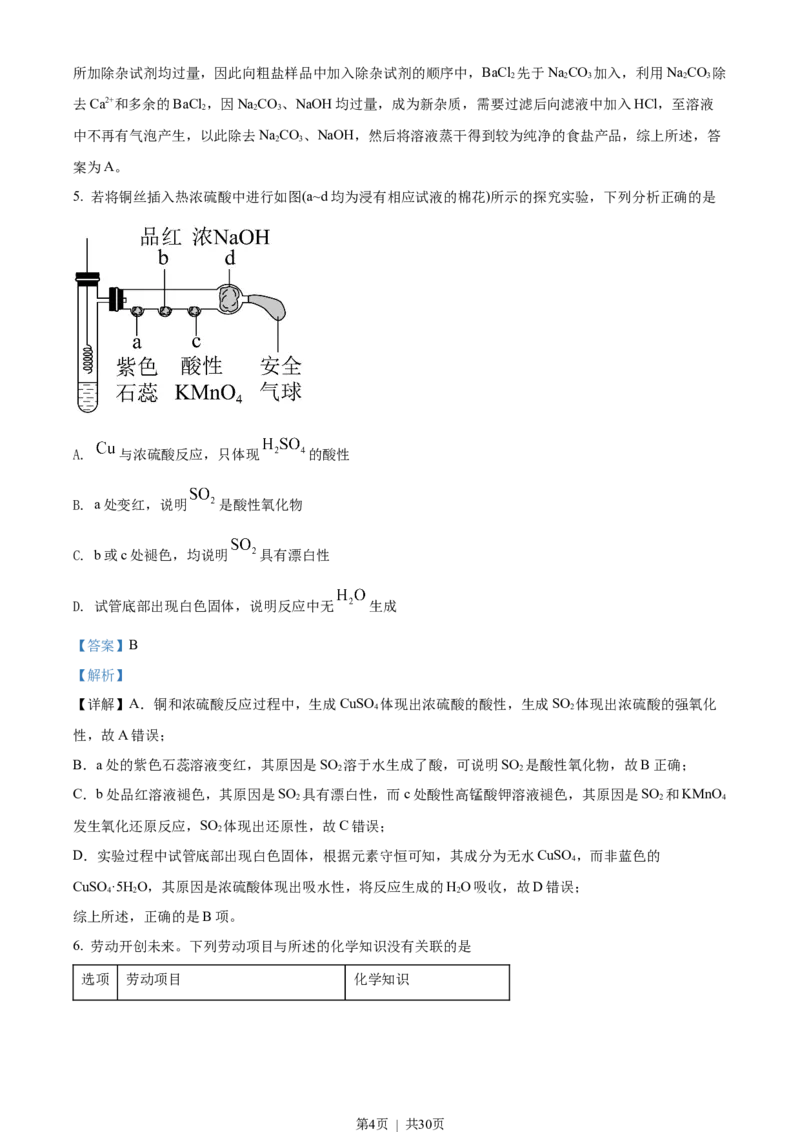
5. 若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实验,下列分析正确的是
A. 与浓硫酸反应,只体现 的酸性
B. a处变红,说明 是酸性氧化物
C. b或c处褪色,均说明 具有漂白性
D. 试管底部出现白色固体,说明反应中无 生成
【答案】B
【解析】
【详解】A.铜和浓硫酸反应过程中,生成CuSO 体现出浓硫酸的酸性,生成SO 体现出浓硫酸的强氧化
4 2
性,故A错误;
B.a处的紫色石蕊溶液变红,其原因是SO 溶于水生成了酸,可说明SO 是酸性氧化物,故B正确;
2 2
C.b处品红溶液褪色,其原因是SO 具有漂白性,而c处酸性高锰酸钾溶液褪色,其原因是SO 和KMnO
2 2 4
发生氧化还原反应,SO 体现出还原性,故C错误;
2
D.实验过程中试管底部出现白色固体,根据元素守恒可知,其成分为无水CuSO ,而非蓝色的
4
CuSO ·5H O,其原因是浓硫酸体现出吸水性,将反应生成的HO吸收,故D错误;
4 2 2
综上所述,正确的是B项。
6. 劳动开创未来。下列劳动项目与所述的化学知识没有关联的是
选项 劳动项目 化学知识
第4页 | 共30页面包师用小苏打作发泡剂烘焙面
A 可与酸反应
包
环保工程师用熟石灰处理酸性废
B 熟石灰具有碱性
水
工人将模具干燥后再注入熔融钢
C 铁与 高温下会反应
水
技术人员开发高端耐腐蚀镀铝钢
D 铝能形成致密氧化膜
板
A. A B. B C. C D. D
【答案】A
【解析】
【详解】A.小苏打是碳酸氢钠,不是碳酸钠,主要用来做膨松剂,故A符合题意;
B.熟石灰是氢氧化钙,具有碱性,可以用于处理酸性废水,故B不符合题意;
C.熔融的铁与水蒸气在高温下反应会生成四氧化三铁和氢气,因此必须将模具干燥,故C不符合题意;
D.钢板上镀铝,保护钢板,金属铝表面形成致密氧化膜而保护金属铝不被腐蚀,,故D不符合题意。
综上所述,答案为A。
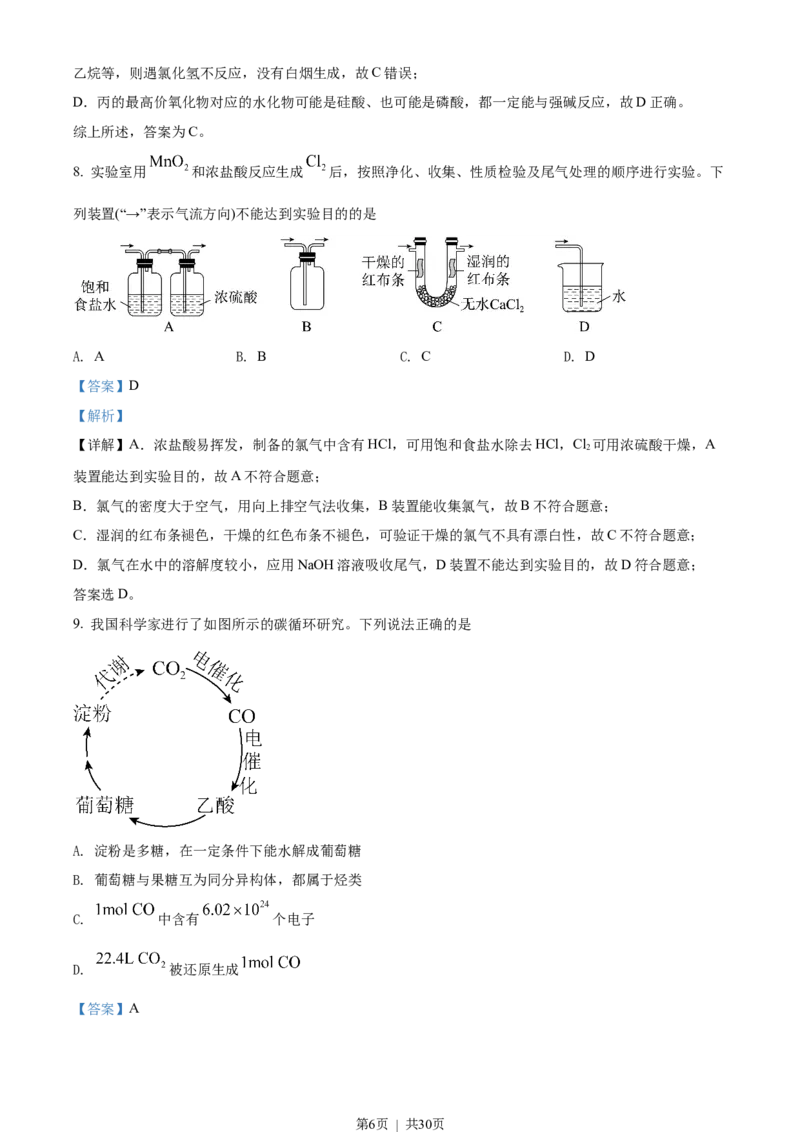
7. 甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对应的水化物为强酸。
下列说法不正确的是
A. 原子半径:丁>戊>乙
B. 非金属性:戊>丁>丙
C. 甲的氢化物遇氯化氢一定有白烟产生
D. 丙 的最高价氧化物对应的水化物一定能与强碱反应
【答案】C
【解析】
【分析】甲~戊是短周期元素,戊中的最高价氧化物对应水化物为强酸,则可能是硫酸或高氯酸,若是高
氯酸,则戊为Cl,甲为N、乙为F、丙为P、丁为S,若是硫酸,则戊为S,甲为C、乙为O、丙为Si、丁
为P。
【详解】A.根据层多径大,同电子层结构核多径小原则,则原子半径:丁>戊>乙,故A正确;
B.根据同周期从左到右非金属性逐渐增强,则非金属性:戊>丁>丙,故B正确;
C.甲的氢化物可能为氨气,可能为甲烷、乙烷等,若是氨气,则遇氯化氢一定有白烟产生;若是甲烷、
第5页 | 共30页乙烷等,则遇氯化氢不反应,没有白烟生成,故C错误;
D.丙的最高价氧化物对应的水化物可能是硅酸、也可能是磷酸,都一定能与强碱反应,故D正确。
综上所述,答案为C。
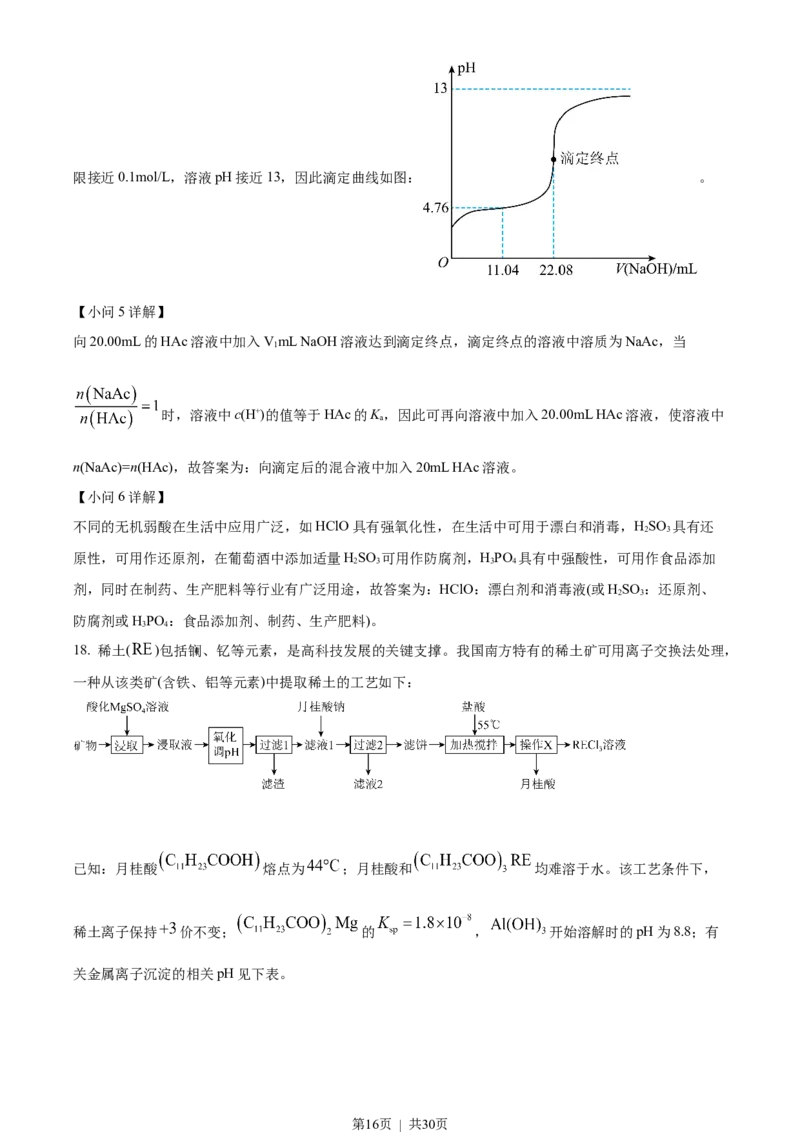
8. 实验室用 和浓盐酸反应生成 后,按照净化、收集、性质检验及尾气处理的顺序进行实验。下
列装置(“→”表示气流方向)不能达到实验目的的是
A. A B. B C. C D. D
【答案】D
【解析】
【详解】A.浓盐酸易挥发,制备的氯气中含有HCl,可用饱和食盐水除去HCl,Cl 可用浓硫酸干燥,A
2
装置能达到实验目的,故A不符合题意;
B.氯气的密度大于空气,用向上排空气法收集,B装置能收集氯气,故B不符合题意;
C.湿润的红布条褪色,干燥的红色布条不褪色,可验证干燥的氯气不具有漂白性,故C不符合题意;
D.氯气在水中的溶解度较小,应用NaOH溶液吸收尾气,D装置不能达到实验目的,故D符合题意;
答案选D。
9. 我国科学家进行了如图所示的碳循环研究。下列说法正确的是
A. 淀粉是多糖,在一定条件下能水解成葡萄糖
B. 葡萄糖与果糖互为同分异构体,都属于烃类
C. 中含有 个电子
D. 被还原生成
【答案】A
第6页 | 共30页【解析】
【详解】A.淀粉是由葡萄糖分子聚合而成的多糖,在一定条件下水解可得到葡萄糖,故A正确;
的
B.葡萄糖与果糖 分子式均为C H O,结构不同,二者互为同分异构体,但含有O元素,不是烃类,属
6 12 6
于烃的衍生物,故B错误;
C.一个CO分子含有14个电子,则1molCO中含有14×6.02×1023=8.428×1024个电子,故C错误;
D.未指明气体处于标况下,不能用标况下的气体摩尔体积计算其物质的量,故D错误;
答案选A。
10. 以熔融盐为电解液,以含 和 等的铝合金废料为阳极进行电解,实现 的再生。该过程中
A. 阴极发生的反应为 B. 阴极上 被氧化
C. 在电解槽底部产生含 的阳极泥 D. 阳极和阴极的质量变化相等
【答案】C
【解析】
【分析】根据电解原理可知,电解池中阳极发生失电子的氧化反应,阴极发生得电子的还原反应,该题中
以熔融盐为电解液,含 和 等的铝合金废料为阳极进行电解,通过控制一定的条件,从而可使
阳极区Mg和Al发生失电子的氧化反应,分别生成Mg2+和Al3+,Cu和Si不参与反应,阴极区Al3+得电子
生成Al单质,从而实现Al的再生,据此分析解答。
【详解】A.阴极应该发生得电子的还原反应,实际上Mg在阳极失电子生成Mg2+,A错误;
B.Al在阳极上被氧化生成Al3+,B错误;
C.阳极材料中Cu和Si不参与氧化反应,在电解槽底部可形成阳极泥,C正确;
D.因为阳极除了铝参与电子转移,镁也参与了电子转移,且还会形成阳极泥,而阴极只有铝离子得电子
生成铝单质,根据电子转移数守恒及元素守恒可知,阳极与阴极的质量变化不相等,D错误;
故选C。
11. 为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌铁片放入酸化的 溶液
中。一段时间后,取溶液分别实验,能说明铁片没有被腐蚀的是
A. 加入 溶液产生沉淀 B. 加入淀粉碘化钾溶液无蓝色出现
C. 加入 溶液无红色出现 D. 加入 溶液无蓝色沉淀生成
第7页 | 共30页【答案】D
【解析】
【分析】镀层有破损的镀锌铁片被腐蚀,则将其放入到酸化的3%NaCl溶液中,会构成原电池,由于锌比
铁活泼,作原电池的负极,而铁片作正极,溶液中破损的位置会变大,铁也会继续和酸化的氯化钠溶液反
应产生氢气,溶液中会有亚铁离子生成,据此分析解答。
【详解】A.氯化钠溶液中始终存在氯离子,所以加入硝酸银溶液后,不管铁片是否被腐蚀,均会出现白
色沉淀,故A不符合题意;
B.淀粉碘化钾溶液可检测氧化性物质,但不论铁片是否被腐蚀,均无氧化性物质可碘化钾发生反应,故
B不符合题意;
C.KSCN溶液可检测铁离子的存在,上述现象中不会出现铁离子,所以无论铁片是否被腐蚀,加入KSCN
溶液后,均无红色出现,故C不符合题意;
D.K[Fe(CN) ]是用于检测Fe2+的试剂,若铁片没有被腐蚀,则溶液中不会生成亚铁离子,则加入
3 6
K[Fe(CN) ]溶液就不会出现蓝色沉淀,故D符合题意。
3 6
综上所述,答案为D。
12. 陈述Ⅰ和Ⅱ均正确但不具有因果关系的是
选
陈述Ⅰ 陈述Ⅱ
项
A 用焦炭和石英砂制取粗硅 可制作光导纤维
B 利用海水制取溴和镁单质 可被氧化, 可被还原
C 石油裂解气能使溴的 溶液褪色 石油裂解可得到乙烯等不饱和烃
D 水解可生成 胶体 可用作净水剂
A. A B. B C. C D. D
【答案】A
【解析】
【详解】A.焦炭具有还原性,工业上常利用焦炭与石英砂(SiO)在高温条件下制备粗硅,这与SiO 是
2 2
否做光导纤维无因果关系,故A符合题意;
B.海水中存在溴离子,可向其中通入氯气等氧化剂将其氧化为溴单质,再经过萃取蒸馏物理操作分离提
纯溴单质,另外,通过富集海水中的镁离子,经过沉淀、溶解等操作得到无水氯化镁,随后电解熔融氯化
镁可制备得到镁单质,陈述I和陈述II均正确,且具有因果关系,B不符合题意;
第8页 | 共30页C.石油在催化剂加热条件下进行裂解可得到乙烯等不饱和烃,从而使溴的CCl 溶液褪色,陈述I和陈述
4
II均正确,且具有因果关系,C不符合题意;
D.FeCl 溶液中铁离子可发生水解,生成具有吸附性的氢氧化铁胶体,从而可用作净水机,陈述I和陈述
3
II均正确,且具有因果关系,D不符合题意;
综上所述,答案为A。
13. 恒容密闭容器中, 在不同温度下达平衡时,各组分的
物质的量(n)如图所示。下列说法正确的是
A. 该反应的
B. a为 随温度的变化曲线
C. 向平衡体系中充入惰性气体,平衡不移动
D. 向平衡体系中加入 ,H 的平衡转化率增大
2
【答案】C
【解析】
【详解】A.从图示可以看出,平衡时升高温度,氢气的物质的量减少,则平衡正向移动,说明该反应的
正反应是吸热反应,即ΔH>0,故A错误;
B.从图示可以看出,在恒容密闭容器中,随着温度升高氢气的平衡时的物质的量减少,则平衡随着温度
升高正向移动,水蒸气的物质的量增加,而a曲线表示的是物质的量不随温度变化而变化,故B错误;
C.容器体积固定,向容器中充入惰性气体,没有改变各物质的浓度,平衡不移动,故C正确;
D.BaSO 是固体,向平衡体系中加入BaSO,不能改变其浓度,因此平衡不移动,氢气的转化率不变,故
4 4
D错误;
故选C。
第9页 | 共30页14. 下列关于 的化合物之间转化反应的离子方程式书写正确的是
A. 碱转化为酸式盐:
B. 碱转化为两种盐:
C. 过氧化物转化为碱:
D. 盐转化为另一种盐:
【答案】B
【解析】
【详解】A.向氢氧化钠溶液中通入足量的二氧化碳,碱可以转化成酸式盐,离子方程式为:CO+OH-=
2
,故A错误;
B.氯气通入NaOH溶液中可以生成氯化钠和次氯酸钠两种盐,其离子方程式为:Cl+2OH-=Cl-+ClO-
2
+H O,故B正确;
2
C.钠的过氧化物为NaO,可以和水反应生成氢氧化钠,但在离子方程式里NaO 不能拆成离子,故C错
2 2 2 2
误;
D.硅酸钠溶于水,在离子方程式里要写成离子,故D错误;
故选B。
15. 在相同条件下研究催化剂I、Ⅱ对反应 的影响,各物质浓度c随反应时间t的部分变化曲线如
图,则
A. 无催化剂时,反应不能进行
B. 与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C. a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
第10页 | 共30页D. 使用催化剂Ⅰ时, 内,
【答案】D
【解析】
【详解】A.由图可知,无催化剂时,随反应进行,生成物浓度也在增加,说明反应也在进行,故A错误;
B.由图可知,催化剂I比催化剂II催化效果好,说明催化剂I使反应活化能更低,反应更快,故B错误;
C.由图可知,使用催化剂II时,在0~2min 内Y的浓度变化了2.0mol/L,而a曲线表示的X的浓度变化
了2.0mol/L,二者变化量之比不等于化学计量数之比,所以a曲线不表示使用催化剂II时X浓度随时间t
的变化,故C错误;
D.使用催化剂I时,在0~2min 内,Y的浓度变化了4.0mol/L,则 (Y) = = =2.0
, (X) = (Y) = 2.0 =1.0 ,故D正确;
答案选D。
16. 科学家基于 易溶于 的性质,发展了一种无需离子交换膜的新型氯流电池,可作储能设备(如
图)。充电时电极a的反应为: 。下列说法正确的是
A. 充电时电极b是阴极
B. 放电时 溶液的 减小
C. 放电时 溶液的浓度增大
第11页 | 共30页D. 每生成 ,电极a质量理论上增加
【答案】C
【解析】
【详解】A.由充电时电极a的反应可知,充电时电极a发生还原反应,所以电极a是阴极,则电极b是阳
极,故A错误;
B.放电时电极反应和充电时相反,则由放电时电极a的反应为
可知,NaCl溶液的pH不变,故B错误;
C.放电时负极反应为 ,正极反应为 ,反
应后Na+和Cl-浓度都增大,则放电时NaCl溶液的浓度增大,故C正确;
D.充电时阳极反应为 ,阴极反应为 ,
由得失电子守恒可知,每生成1molCl ,电极a质量理论上增加23g/mol 2mol=46g,故D错误;
2
答案选C。
二、非选择题:共56分。第17~19题为必考题,考生都必须作答。第20~21题为选考题,考
生根据要求作答。
(一)必考题:共42分。
17. 食醋是烹饪美食的调味品,有效成分主要为醋酸(用 表示)。 的应用与其电离平衡密切相关。
25℃时, 的 。
(1)配制 的 溶液,需 溶液的体积为_______mL。
(2)下列关于 容量瓶的操作,正确的是_______。
第12页 | 共30页(3)某小组研究25℃下 电离平衡的影响因素。
提出假设。稀释 溶液或改变 浓度, 电离平衡会发生移动。设计方案并完成实验用浓度均为
的 和 溶液,按下表配制总体积相同的系列溶液;测定 ,记录数据。
序号
Ⅰ 40.00 / / 0 2.86
Ⅱ 4.00 / 36.00 0 3.36
…
Ⅶ 4.00 a b 3:4 4.53
Ⅷ 4.00 4.00 32.00 1:1 4.65
①根据表中信息,补充数据: _______, _______。
②由实验Ⅰ和Ⅱ可知,稀释 溶液,电离平衡_______(填”正”或”逆”)
向移动;结合表中数据,给出判断理由:_______。
③由实验Ⅱ~VIII可知,增大 浓度, 电离平衡逆向移动。
实验结论假设成立。
(4)小组分析上表数据发现:随着 的增加, 的值逐渐接近 的 。
查阅资料获悉:一定条件下,按 配制的溶液中, 的值等于 的 。
对比数据发现,实验VIII中 与资料数据 存在一定差异;推测可能由物质浓度准确程
度不够引起,故先准确测定 溶液的浓度再验证。
①移取 溶液,加入2滴酚酞溶液,用 溶液滴定至终点,消耗体积为
,则该 溶液的浓度为_______ 。在答题卡虚线框中,画出上述过程的滴定曲线示
意图并标注滴定终点_______。
第13页 | 共30页②用上述 溶液和 溶液,配制等物质的量的 与 混合溶液,测定
pH,结果与资料数据相符。
(5)小组进一步提出:如果只有浓度均约为 的 和 溶液,如何准确测定 的
?小组同学设计方案并进行实验。请完成下表中Ⅱ的内容。
Ⅰ 移取 溶液,用 溶液滴定至终点,消耗 溶液
Ⅱ _______,测得溶液的pH为4.76
实验总结 得到的结果与资料数据相符,方案可行。
(6)根据 可以判断弱酸的酸性强弱。写出一种无机弱酸及其用途_______。
【答案】(1)5.0 (2)C
(3) ①. 3.00 ②. 33.00 ③. 正 ④. 实验II相较于实验I,醋酸溶液稀释了10倍,而实验II
的pH增大值小于1
(4) ①. 0.1104 ②.
(5)向滴定后的混合液中加入20mL HAc溶液
(6)HClO:漂白剂和消毒液(或HSO :还原剂、防腐剂或HPO :食品添加剂、制药、生产肥料)
2 3 3 4
【解析】
【小问1详解】
溶液稀释过程中,溶质的物质的量不变,因此250mL×0.1mol/L=V×5mol/L,解得V=5.0mL,故答案为:
5.0。
【小问2详解】
A.容量瓶使用过程中,不能用手等触碰瓶口,以免污染试剂,故A错误;
B.定容时,视线应与溶液凹液面和刻度线“三线相切”,不能仰视或俯视,故B错误;
第14页 | 共30页C.向容量瓶中转移液体,需用玻璃棒引流,玻璃棒下端位于刻度线以下,同时玻璃棒不能接触容量瓶口,
故C正确;
D.定容完成后,盖上瓶塞,将容量瓶来回颠倒,将溶液摇匀,颠倒过程中,左手食指抵住瓶塞,防止瓶
塞脱落,右手扶住容量瓶底部,防止容量瓶从左手掉落,故D错误;
综上所述,正确的是C项。
【小问3详解】
的
①实验VII 溶液中n(NaAc):n(HAc)=3:4,V(HAc)=4.00mL,因此V(NaAc)=3.00mL,即a=3.00,,由实
验I可知,溶液最终的体积为40.00mL,因此V(H O)=40.00mL-4.00mL-3.00mL=33.00mL,即b=33.00,故
2
答案为:3.00;33.00。
②实验I所得溶液的pH=2.86,实验II的溶液中c(HAc)为实验I的 ,稀释过程中,若不考虑电离平衡移
动,则实验II所得溶液的pH=2.86+1=3.86,但实际溶液的pH=3.36<3.86,说明稀释过程中,溶液中n(H+)
增大,即电离平衡正向移动,故答案为:正;实验II相较于实验I,醋酸溶液稀释了10倍,而实验II的
pH增大值小于1。
【小问4详解】
(i)滴定过程中发生反应:HAc+NaOH=NaAc+H O,由反应方程式可知,滴定至终点时,
2
n(HAc)=n(NaOH),因此22.08mL×0.1mol/L=20.00mL×c(HAc),解得c(HAc)=0.1104mol/L,故答案为:
0.1104。
(ii)滴定过程中,当V(NaOH)=0时,c(H+)= ≈ mol/L=10-2.88mol/L,溶液的
pH=2.88,当V(NaOH)=11.04mL时,n(NaAc)=n(HAc),溶液的pH=4.76,当V(NaOH)=22.08mL时,达到滴
定终点,溶液中溶质为NaAc溶液,Ac-发生水解,溶液呈弱碱性,当NaOH溶液过量较多时,c(NaOH)无
第15页 | 共30页限接近0.1mol/L,溶液pH接近13,因此滴定曲线如图: 。
【小问5详解】
向20.00mL的HAc溶液中加入VmL NaOH溶液达到滴定终点,滴定终点的溶液中溶质为NaAc,当
1
时,溶液中c(H+)的值等于HAc的K,因此可再向溶液中加入20.00mL HAc溶液,使溶液中
a
n(NaAc)=n(HAc),故答案为:向滴定后的混合液中加入20mL HAc溶液。
【小问6详解】
不同的无机弱酸在生活中应用广泛,如HClO具有强氧化性,在生活中可用于漂白和消毒,HSO 具有还
2 3
原性,可用作还原剂,在葡萄酒中添加适量HSO 可用作防腐剂,HPO 具有中强酸性,可用作食品添加
2 3 3 4
剂,同时在制药、生产肥料等行业有广泛用途,故答案为:HClO:漂白剂和消毒液(或HSO :还原剂、
2 3
防腐剂或HPO :食品添加剂、制药、生产肥料)。
3 4
18. 稀土( )包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可用离子交换法处理,
一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下:
已知:月桂酸 熔点为 ;月桂酸和 均难溶于水。该工艺条件下,
稀土离子保持 价不变; 的 , 开始溶解时的pH为8.8;有
关金属离子沉淀的相关pH见下表。
第16页 | 共30页离子
开始沉淀时的pH 8.8 1.5 3.6 6.2~7.4
沉淀完全时的pH / 3.2 4.7 /
(1)“氧化调pH”中,化合价有变化的金属离子是_______。
(2)“过滤1”前,用 溶液调pH至_______的范围内,该过程中 发生反应的离子方程式为
_______。
(3)“过滤2”后,滤饼中检测不到 元素,滤液2中 浓度为 。为尽可能多地提取 ,
可提高月桂酸钠的加入量,但应确保“过滤2”前的溶液中 低于_______ (保留两位
有效数字)。
(4)①“加热搅拌”有利于加快 溶出、提高产率,其原因是_______。
②“操作X”的过程为:先_______,再固液分离。
(5)该工艺中,可再生循环利用的物质有_______(写化学式)。
(6)稀土元素钇(Y)可用于制备高活性的合金类催化剂 。
①还原 和 熔融盐制备 时,生成1mol 转移_______ 电子。
② 用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化 的还原,发生的电极反应为
_______。
【答案】(1)Fe2+
(2) ①. 4.7 pH<6.2 ②.
(3)4.0 10-4
(4) ①. 加热搅拌可加快反应速率 ②. 冷却结晶
(5)MgSO (6) ①. 15 ②. O+4e-+2H O=4OH-
4 2 2
【解析】
【分析】由流程可知,该类矿(含铁、铝等元素)加入酸化MgSO 溶液浸取,得到浸取液中含有 、
4
第17页 | 共30页、 、 、 、 等离子,经氧化调pH使 、 形成沉淀,经过滤除去,滤液1
中含有 、 、 等离子,加入月桂酸钠,使 形成 沉淀,滤液2主要
含有MgSO 溶液,可循环利用,滤饼加盐酸,经加热搅拌溶解后,再冷却结晶,析出月桂酸,再固液分离
4
得到RECl 溶液。
3
【小问1详解】
由分析可知,“氧化调pH”目的是除去含铁、铝等元素的离子,需要将Fe2+氧化为Fe3+,以便后续除杂,所
以化合价有变化的金属离子是Fe2+,故答案为:Fe2+;
【小问2详解】
由表中数据可知, 沉淀完全的pH为4.7,而 开始沉淀的pH为6.2~7.4,所以为保证 、
沉淀完全,且 不沉淀,要用 溶液调pH至4.7 pH<6.2的范围内,该过程中 发生反应的
离子方程式为 ,故答案为:4.7 pH<6.2; ;
【小问3详解】
滤液2中 浓度为 ,即0.1125mol/L,根据
,若要加入月桂酸钠后只生成 ,
而不产生 ,则 = =4 10-4
,故答案为:4 10-4;
【小问4详解】
①“加热搅拌”有利于加快 溶出、提高产率,其原因是加热搅拌可加快反应速率,故答案为:加热搅
拌可加快反应速率;
② “操作X”的结果是分离出月桂酸,由信息可知,月桂酸 熔点为 ,故“操作X”的过
程为:先冷却结晶,再固液分离,故答案为:冷却结晶;
第18页 | 共30页【小问5详解】
由分析可知,该工艺中,可再生循环利用的物质有MgSO ,故答案为:MgSO ;
4 4
【小问6详解】
① 中Y为+3价, 中Pt为+4价,而 中金属均为0价,所以还原 和 熔融盐制备
时,生成1mol 转移15 电子,故答案为:15;
②碱性溶液中,氢氧燃料电池正极发生还原反应,发生的电极反应为O+4e-+2H O=4OH,故答案为:
2 2
O+4e-+2H O=4OH-。
2 2
19. 铬及其化合物在催化、金属防腐等方面具有重要应用。
(1)催化剂 可由 加热分解制备,反应同时生成无污染气体。
①完成化学方程式: _______ _______。
② 催化丙烷脱氢过程中,部分反应历程如图, 过程的焓变为_______(列式表示)。
③ 可用于 的催化氧化。设计从 出发经过3步反应制备 的路线_______(用“→”表示含
氮物质间的转化);其中一个有颜色变化的反应的化学方程式为_______。
(2) 溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
(ⅰ)
(ⅱ)
①下列有关 溶液的说法正确的有_______。
第19页 | 共30页A.加入少量硫酸,溶液的pH不变
B.加入少量水稀释,溶液中离子总数增加
C.加入少量 溶液,反应(ⅰ)的平衡逆向移动
D.加入少量 固体,平衡时 与 的比值保持不变
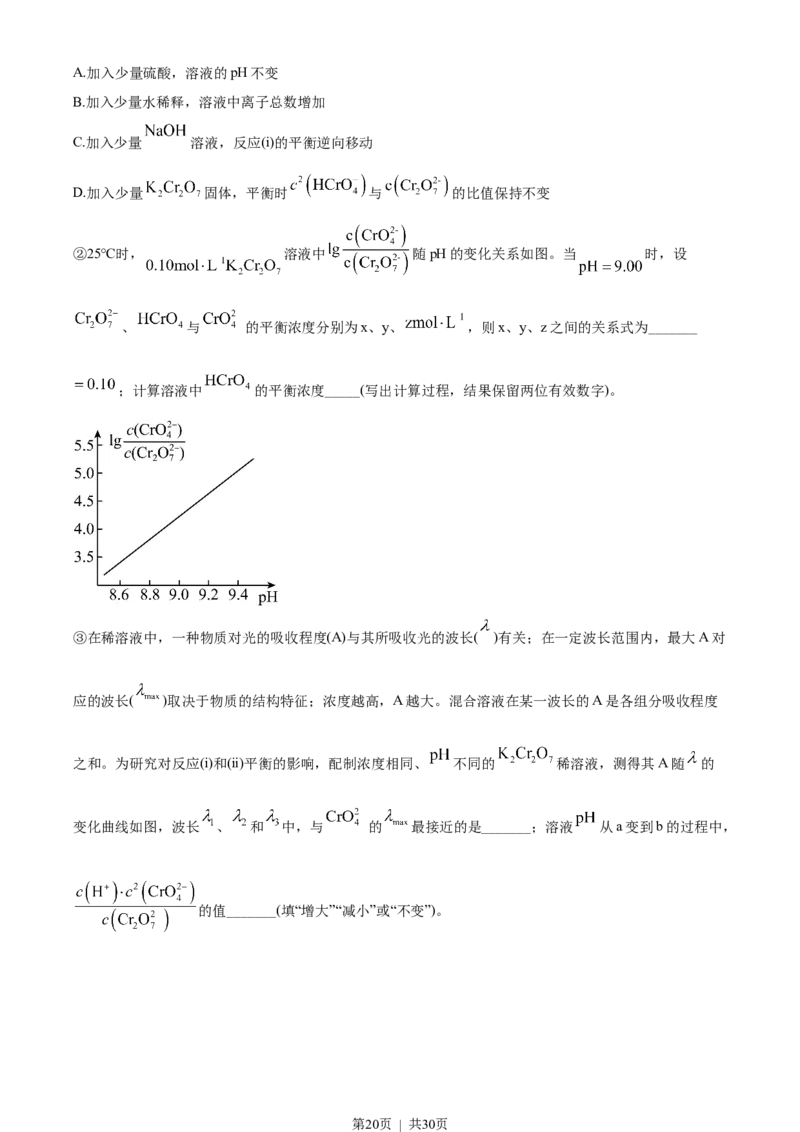
②25℃时, 溶液中 随pH的变化关系如图。当 时,设
、 与 的平衡浓度分别为x、y、 ,则x、y、z之间的关系式为_______
;计算溶液中 的平衡浓度_____(写出计算过程,结果保留两位有效数字)。
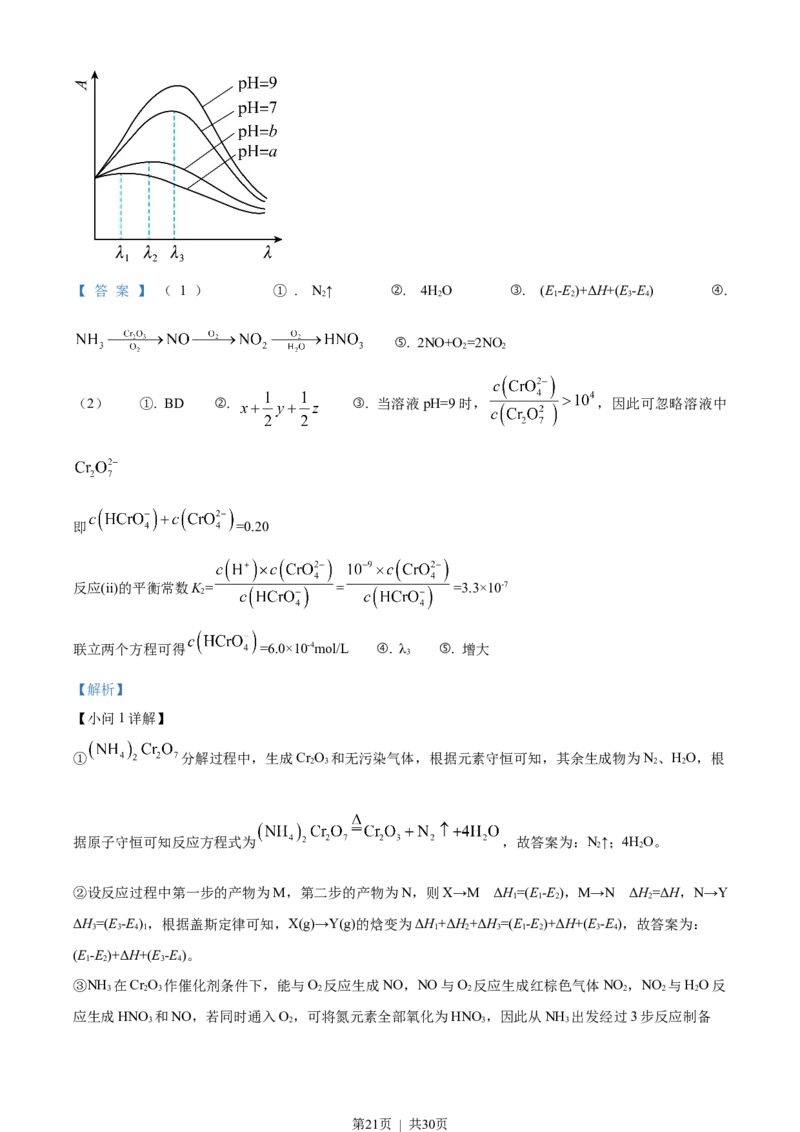
③在稀溶液中,一种物质对光的吸收程度(A)与其所吸收光的波长( )有关;在一定波长范围内,最大A对
应的波长( )取决于物质的结构特征;浓度越高,A越大。混合溶液在某一波长的A是各组分吸收程度
之和。为研究对反应(ⅰ)和(ⅱ)平衡的影响,配制浓度相同、 不同的 稀溶液,测得其A随 的
变化曲线如图,波长 、 和 中,与 的 最接近的是_______;溶液 从a变到b的过程中,
的值_______(填“增大”“减小”或“不变”)。
第20页 | 共30页【 答 案 】 ( 1 ) ① . N↑ ②. 4HO ③. (E-E)+ΔH+(E-E) ④.
2 2 1 2 3 4
⑤. 2NO+O =2NO
2 2
(2) ①. BD ②. ③. 当溶液pH=9时, ,因此可忽略溶液中
即 =0.20
反应(ii)的平衡常数K = = =3.3×10-7
2
联立两个方程可得 =6.0×10-4mol/L ④. λ ⑤. 增大
3
【解析】
【小问1详解】
① 分解过程中,生成Cr O 和无污染气体,根据元素守恒可知,其余生成物为N、HO,根
2 3 2 2
据原子守恒可知反应方程式为 ,故答案为:N↑;4HO。
2 2
②设反应过程中第一步的产物为M,第二步的产物为N,则X→M ΔH=(E-E),M→N ΔH=ΔH,N→Y
1 1 2 2
ΔH=(E-E),根据盖斯定律可知,X(g)→Y(g)的焓变为ΔH+ΔH+ΔH=(E-E)+ΔH+(E-E),故答案为:
3 3 4 1 1 2 3 1 2 3 4
(E-E)+ΔH+(E-E)。
1 2 3 4
③NH 在Cr O 作催化剂条件下,能与O 反应生成NO,NO与O 反应生成红棕色气体NO ,NO 与HO反
3 2 3 2 2 2 2 2
应生成HNO 和NO,若同时通入O,可将氮元素全部氧化为HNO,因此从NH 出发经过3步反应制备
3 2 3 3
第21页 | 共30页HNO 的路线为 ;其中NO反应生成NO 过程中,气体颜色
3 2
发生变化,其反应方程式为2NO+O =2NO,故答案为: ;
2 2
2NO+O =2NO。
2 2
【
小问2详解】
①KCr O 溶液中存在平衡:(i) 、(ii)
2 2 7
。
A.向溶液中加入少量硫酸,溶液中c(H+)增大,(ii)平衡逆向移动,根据勒夏特列原理可知,平衡移动只是
减弱改变量,平衡后,溶液中c(H+)依然增大,因此溶液的pH将减小,故A错误;
B.加水稀释过程中,根据“越稀越水解”、“越稀越电离”可知,(i)和(ii)的平衡都正向移动,两个平衡正向
都是离子数增大的反应,因此稀释后,溶液中离子总数将增大,故B正确;
C.加入少量NaOH溶液,(ii)正向移动,溶液中 将减小,(i)将正向移动,故C错误;
D.平衡(i)的平衡常数K = ,平衡常数只与温度和反应本身有关,因此加入少量KCr O 溶液,
1 2 2 7
不变,故D正确;
综上所述,答案为:BD。
②0.10mol/L K Cr O 溶液中,Cr原子的总浓度为0.20mol/L,当溶液pH=9.00时,溶液中Cr原子总浓度为
2 2 7
=0.20mol/L, 、 与 的平衡浓度分别为x、y、z
mol/L,因此 =0.10;由图8可知,当溶液pH=9时, ,因此可忽略溶液中
,即 =0.20,反应(ii)的平衡常数K = =
2
第22页 | 共30页=3.3×10-7,联立两个方程可得 =6.0×10-4mol/L。
③根据反应(i)、(ii)是离子浓度增大的平衡可知,溶液pH越大,溶液中
越大,混合溶液在某一波长的A越大,溶液的pH越大,溶液中
越大,因此与 的λ 最接近的是λ;反应(i)的平衡常数K = ,反应(ii)的平
max 3 1
衡常数K = , = =
2
,因此 = ,由上述分析逆推可知,b>a,即溶液pH
从a变到b的过程中,溶液中c(H+)减小,所以 的值将增大,故答案为:λ;增大。
3
(二)选考题:共14分。请考生从2道题中任选一题作答。如果多做,则按所做的第一题计分。
[选修3:物质结构与性质]
20. 硒( )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚
集诱导发光( )效应以来, 在发光材料、生物医学等领域引起广泛关注。一种含 的新型 分
子 的合成路线如下:
第23页 | 共30页(1) 与S同族,基态硒原子价电子排布式为_______。
(2) 的沸点低于 ,其原因是_______。
(3)关于I~III三种反应物,下列说法正确的有_______。
A.I中仅有 键
B.I中的 键为非极性共价键
C.II易溶于水
D.II中原子的杂化轨道类型只有 与
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有_______。
(5)硒的两种含氧酸的酸性强弱为 _______ (填“>”或“<”)。研究发现,给小鼠喂食适量
硒酸钠( )可减轻重金属铊引起的中毒。 的立体构型为_______。
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于
加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,
沿x、y、z轴方向的投影均为图2。
①X的化学式为_______。
②设X的最简式的式量为 ,晶体密度为 ,则X中相邻K之间的最短距离为_______ (列出
计算式, 为阿伏加德罗常数的值)。
【答案】(1)4s24p4
第24页 | 共30页(2)两者都 是分子晶体,由于水存在分子间氢键,沸点高
(3)BDE (4)O、Se
(5) ①. > ②. 正四面体形
(6) ①. KSeBr ②.
2 6
【解析】
【小问1详解】
基态硫原子价电子排布式为3s23p4, 与S同族,Se为第四周期元素,因此基态硒原子价电子排布式为
4s24p4;故答案为:4s24p4。
【小问2详解】
的沸点低于 ,其原因是两者都是分子晶体,由于水存在分子间氢键,沸点高;故答案为:两者
都是分子晶体,由于水存在分子间氢键,沸点高。
【小问3详解】
A.I中有 键,还有大π键,故A错误;B.Se−Se是同种元素,因此I中的 键为非极性共价键,
故B正确;C.烃都是难溶于水,因此II难溶于水,故B错误;D.II中苯环上的碳原子和碳碳双键上的
碳原子杂化类型为sp2,碳碳三键上的碳原子杂化类型为sp,故D正确;E.根据同周期从左到右电负性逐
渐增大,同主族从上到下电负性逐渐减小,因此I~III含有的元素中,O电负性最大,故E正确;综上所述,
答案为:BDE。
【小问4详解】
根据题中信息IV中O、Se都有孤对电子,碳、氢、硫都没有孤对电子;故答案为:O、Se。
【小问5详解】
根据非羟基氧越多,酸性越强,因此硒的两种含氧酸的酸性强弱为 > 。 中Se价层
电子对数为 ,其立体构型为正四面体形;故答案为:>;正四面体形。
【小问6详解】
①根据晶胞结构得到K有8个, 有 ,则X的化学式为KSeBr ;故答案为:
2 6
第25页 | 共30页KSeBr 。
2 6
②设X的最简式的式量为 ,晶体密度为 ,设晶胞参数为anm,得到
,解得 ,X中相邻K之间的最短距离为晶胞参数
的一半即 ;故答案为: 。
【选修5:有机化学基础】
21. 基于生物质资源开发常见的化工原料,是绿色化学的重要研究方向。以化合物I为原料,可合成丙烯
酸V、丙醇VII等化工产品,进而可制备聚丙烯酸丙酯类高分子材料。
(1)化合物I的分子式为_______,其环上的取代基是_______(写名称)。
(2)已知化合物II也能以II′的形式存在。根据II′的结构特征,分析预测其可能的化学性质,参考①的示
例,完成下表。
序 可反应的试
结构特征 反应形成的新结构 反应类型
号 剂
① 加成反应
② _______ _______ _______ 氧化反应
③ _______ _______ _______ _______
(3)化合物IV能溶于水,其原因是_______。
(4)化合物IV到化合物V的反应是原子利用率 的反应,且 与 化合物a反应得到
第26页 | 共30页,则化合物a为_______。
(5)化合物VI有多种同分异构体,其中含 结构的有_______种,核磁共振氢谱图上只有一组峰
的结构简式为_______。
(6)选用含二个羧基的化合物作为唯一的含氧有机原料,参考上述信息,制备高分子化合物VIII的单体。
写出VIII的单体的合成路线_______(不用注明反应条件)。
【答案】(1) ①. C HO ②. 醛基
5 4 2
(2) ①. -CHO ②. O ③. -COOH ④. -COOH ⑤. CHOH ⑥. - COOCH ⑦. 酯
2 3 3
化反应(取代反应)
(3)Ⅳ中羟基能与水分子形成分子间氢键
(4)乙烯 (5) ①. 2 ②.
(6)
【解析】
【小问1详解】
根据化合物Ⅰ的结构简式可知,其分子式为C HO;其环上的取代基为醛基,故答案为:C HO;醛基;
5 4 2 5 4 2
【小问2详解】
②化合物Ⅱ'中含有的-CHO可以被氧化为-COOH,故答案为:-CHO;O;-COOH;
2
③化合物Ⅱ'中含有-COOH,可与含有羟基的物质(如甲醇)发生酯化反应生成酯,故答案为:-COOH;
第27页 | 共30页CHOH;- COOCH ;酯化反应(取代反应);
3 3
【小问3详解】
化合物Ⅳ中含有羟基,能与水分子形成分子间氢键,使其能溶于水,故答案为:Ⅳ中羟基能与水分子形成
分子间氢键;
【小问4详解】
化合物Ⅳ到化合物Ⅴ的反应是原子利用率100%的反应,且1 molⅣ与1 mola反应得到2molV,则a的分子
式为C H,为乙烯,故答案为:乙烯;
2 4
【小问5详解】
化合物Ⅵ的分子式为C HO,其同分异构体中含有 ,则符合条件的同分异构体有
3 6
和 ,共2种,其中核磁共振氢谱中只有一组峰的结构简式为
,故答案为: ;
【小问6详解】
根据化合物Ⅷ的结构简式可知,其单体为 ,其原料中的含氧有机物只有一种含
二个羧基的化合物,原料可以是 , 发生题干Ⅳ→V的
反应得到 , 还原为 ,再加成得到 ,
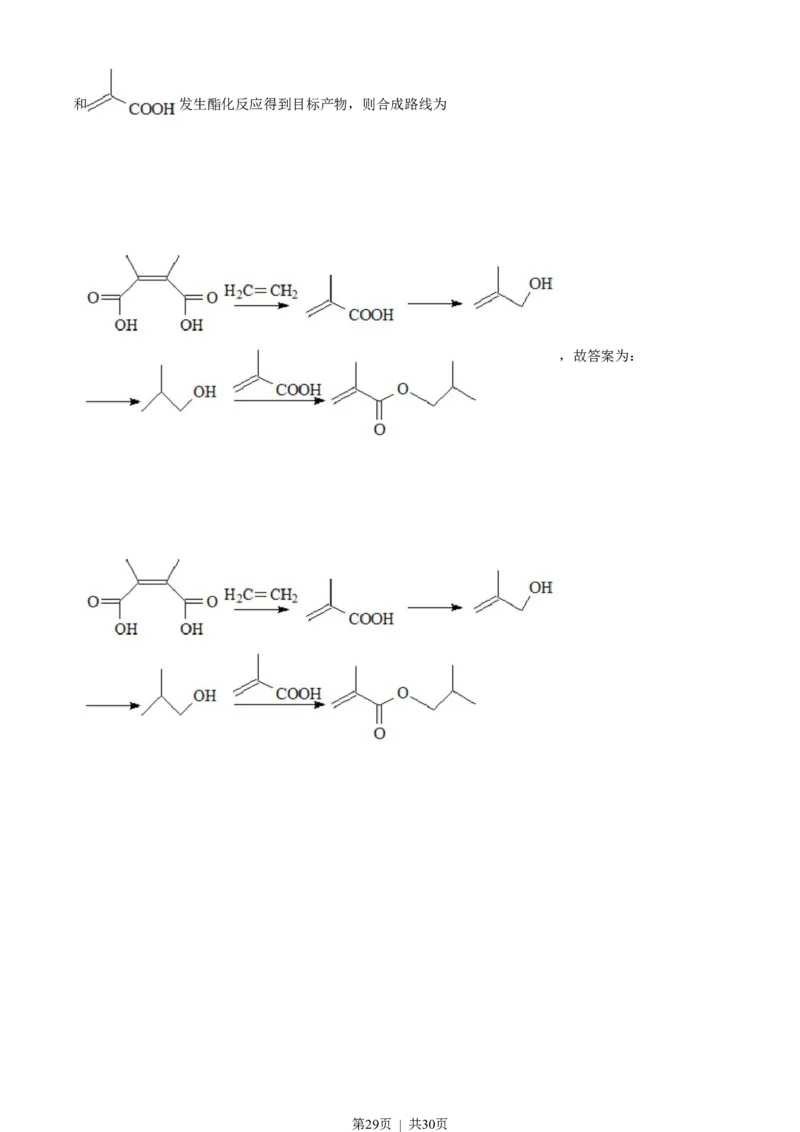
第28页 | 共30页和 发生酯化反应得到目标产物,则合成路线为
,故答案为:
第29页 | 共30页第30页 | 共30页