文献讲解(十二)AI驱动身体成分图谱与NSCLC免疫治疗疗效及分子机制研究
非小细胞肺癌(NSCLC)作为全球高发恶性肿瘤,免疫检查点抑制剂(ICIs)已重塑治疗格局,但患者响应率差异大、疗效预测缺乏精准指标。传统 BMI 等单一指标无法全面反映身体状态与肿瘤免疫的关联,身体成分的性别差异、部位差异更是被长期忽视,成为免疫治疗精准化的关键瓶颈。
近期发表于npj Precision Oncology的一项多中心研究,基于 AI 深度学习全自动提取 CT 影像 92 项身体成分参数,整合 2132 例患者数据、转录组与单细胞测序,首次系统揭示身体成分与 NSCLC 免疫治疗疗效的关联,明确性别与部位特异性规律,为免疫治疗获益分层提供全新无创预测思路。

一、文献基本信息
文章题目:AI-driven body composition atlas reveals its association with NSCLC immunotherapy outcome and molecular background: a multicenter study
发表期刊:npj Precision Oncology
发表时间:2026 年 3 月
核心团队:华中科技大学 Yang Lian、Zheng Chuansheng、Peng Shu 团队
研究核心:AI 量化多维身体成分,揭示其与 NSCLC 免疫治疗预后、免疫微环境的性别 / 部位特异性关联
核心结论:身体成分具显著性别差异与部位差异;男性高肌间脂肪体积(IMFV)是免疫治疗独立保护因素,女性 T12 皮下脂肪密度与预后相关;身体成分通过调控免疫细胞状态影响免疫疗效。
二、研究背景:肺癌免疫治疗的 “被忽视” 预测维度
临床困境:免疫治疗疗效个体差异大,缺乏无创、精准的预后预测指标,BMI 等传统指标存在 “肥胖悖论”,临床指导有限。
科学空白:既往研究仅聚焦单一身体成分指标,缺乏多维、跨部位分析,未揭示性别差异的分子机制,未结合单细胞解析免疫微环境调控通路。
技术契机:AI 深度学习实现 CT 身体成分全自动精准分割;多队列大数据验证可靠性;单细胞转录组打通 “影像表型 — 细胞状态 — 疗效” 的完整链路。
三、研究思路:从 AI 量化到疗效机制的完整闭环
1.研究队列:纳入 8 个独立队列共 2132 例 NSCLC 患者,含 5 个免疫治疗预后队列、2 个转录组队列、1 个单细胞队列;
2.AI 量化:基于 nnUNet 模型从 CT 自动提取 92 项 2D+3D 身体成分参数(T8–L3),覆盖脂肪、肌肉、椎体等维度;
3.预后关联:分析身体成分与总生存期(OS)的关联,筛选独立预测因子;
4.分子解析:结合转录组与单细胞测序,解析身体成分调控肿瘤免疫微环境的机制;
5.差异挖掘:明确性别特异性、部位特异性的身体成分预后规律。
四、结果解析:身体成分重塑肺癌免疫治疗预测体系
1.研究设计与研究对象
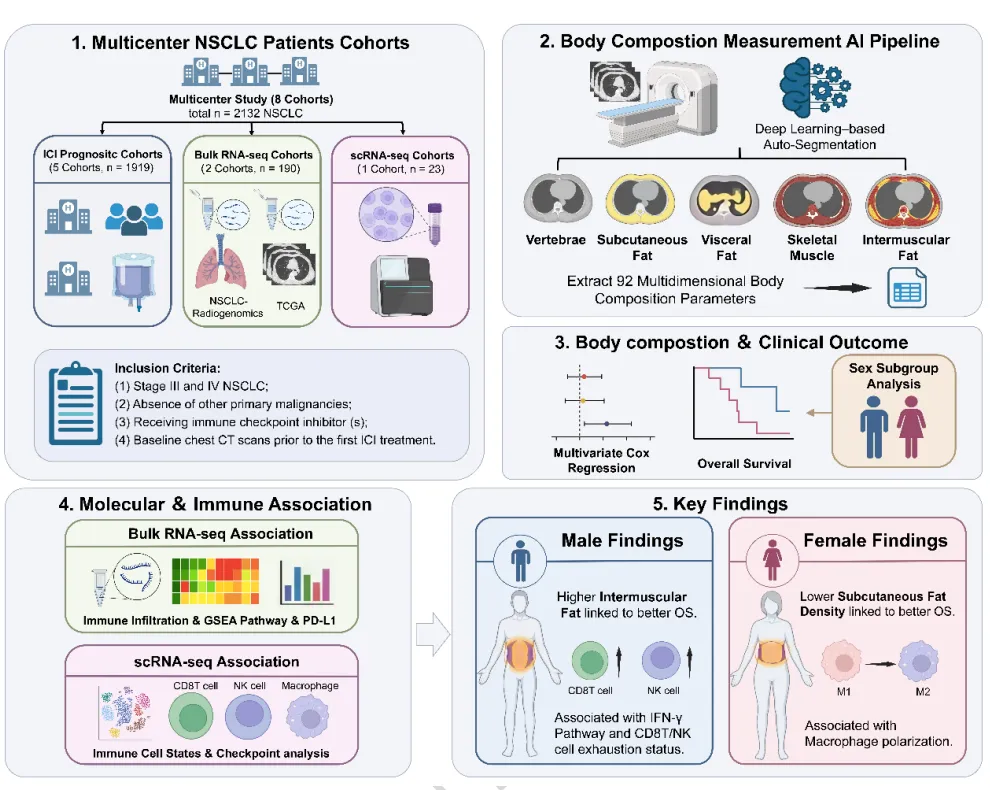
本研究纳入 8 个独立队列、共 2132 例非小细胞肺癌患者。其中 5 个队列共 1919 例患者具备 CT 影像、临床数据及预后信息,用于评估多维度身体成分与免疫治疗后临床结局的关联。两个队列共 190 例患者具备配对 CT 影像与批量 RNA 测序数据,用于探索身体成分与肿瘤微环境特征的关系。另有 23 例患者具备匹配的 CT 影像与单细胞 RNA 测序数据,用于深入解析身体成分与肿瘤分子背景的关联。
接受免疫检查点抑制剂治疗的临床队列中,男性占 84.8%(1629 例),女性占 15.2%(290 例)。全组中位年龄 64 岁(四分位距 58–69 岁);男性中位年龄 65 岁(59–70 岁),女性中位年龄 59 岁(51–66 岁)。
图一:A:研究设计,覆盖正常肝、原发肿瘤、PVTT、MLN 四阶段。B:7 类主要细胞的标记基因表达。C:细胞分群的 UMAP 可视化。D/E:进展期细胞比例变化,肿瘤与髓系细胞富集。F:细胞相关性,基质–髓系与淋巴细胞呈负相关。
2.非小细胞肺癌患者身体成分参数的相关性
既往研究提示身体成分存在性别差异。本研究三维分析结果一致显示:男性骨骼肌体积、椎体体积显著更高,女性皮下脂肪体积显著更高,肌间脂肪体积无性别差异。
进一步分析发现:骨骼肌体积与年龄呈负相关,肌间脂肪体积与年龄呈正相关,皮下脂肪体积与年龄无显著关联。皮下脂肪体积、骨骼肌体积、肌间脂肪体积均随体重指数升高而增加。
基于各椎体层面的二维身体成分测量,开展全面相关性分析。同一层面内,同类参数(如骨骼肌面积、密度、指数)呈强相关,脂肪相关参数同理。同一类参数即便跨不同椎体层面,仍呈极强相关,该模式在所有测量参数中均稳定存在。
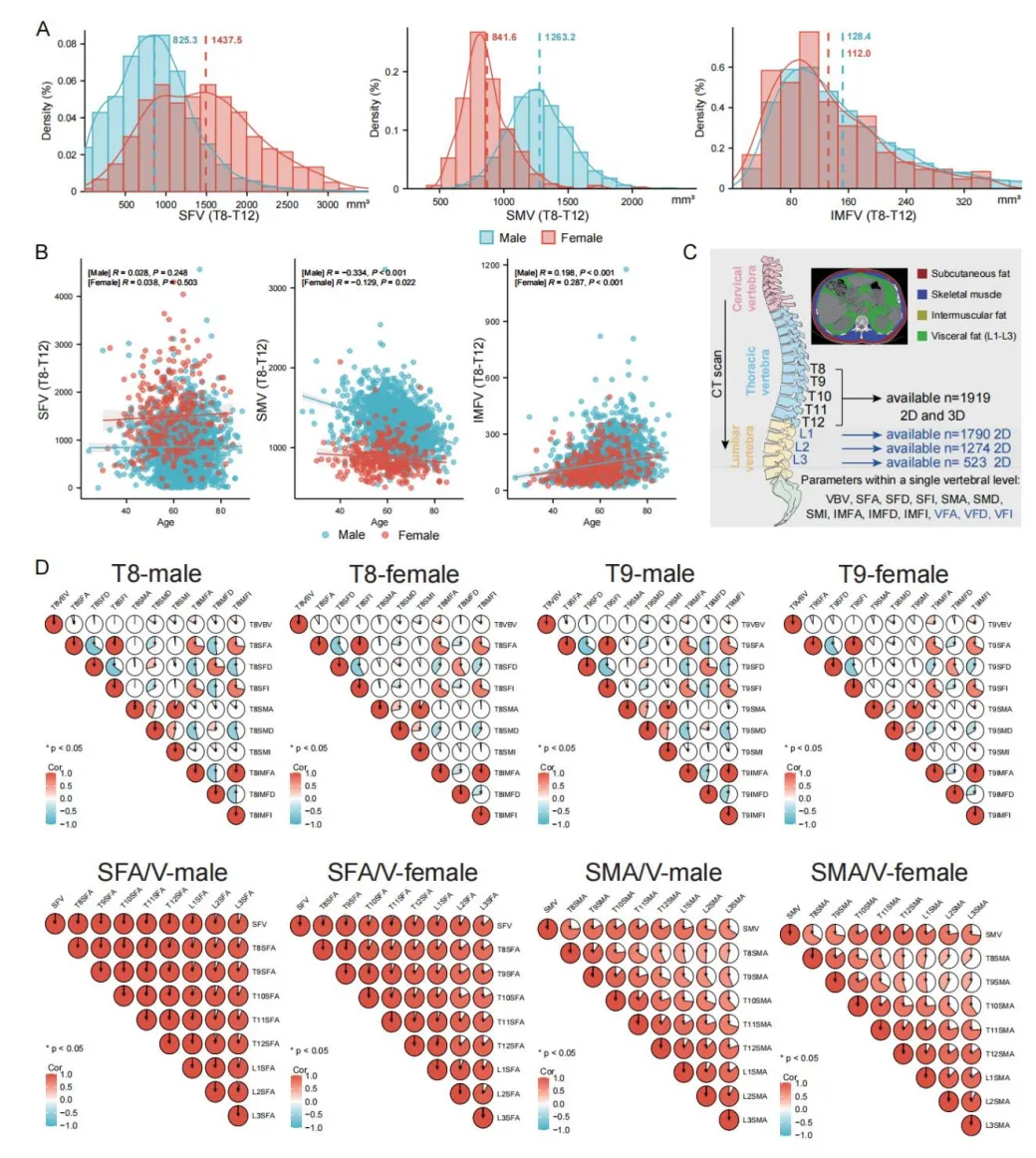
图2:A:15 个表达程序聚成 4 类 meta-program。B/C:四类程序在肿瘤细胞中的分布。D:不同进展阶段程序构成差异。E:各类程序的特征标记基因。F:功能通路富集结果。G/H:恶性细胞演化轨迹。I–K:与泛癌及肝癌分型对应验证
3. 四种 meta-program 重构恶性细胞异质性,并揭示其动态演化关系
与既往体重指数与免疫治疗结局相关的报道一致,本研究观察到体重指数>20.9 的患者免疫治疗后总生存期更长,但以中位值分组时该关联不显著。
为系统评估各类身体成分参数与总生存期的关系,以连续变量形式构建单因素 Cox 回归热图。随访期间,男性亚组 712 例死亡(43.7%),女性亚组 135 例死亡(46.5%)。
男性患者:肌间脂肪体积、肌间脂肪面积、肌间脂肪指数、椎体体积、T11 皮下脂肪面积升高与总生存期改善相关;皮下脂肪密度、T11 骨骼肌密度、T12 骨骼肌密度、T9 骨骼肌指数降低也与更长生存期相关。将肌间脂肪体积临界值设为 0.196 时,生存曲线差异最大;校正年龄与体重指数后,死亡风险随肌间脂肪体积升高而降低。T8 椎体体积以 32.3 为临界值时生存差异最大,死亡风险随 T8 椎体体积升高而降低。以中位值二分法分组,生存曲线差异仍显著。限制性立方样条图进一步展示 T12 皮下脂肪密度、T11 肌间脂肪面积的关联趋势。
女性患者:T12 皮下脂肪密度、T9 肌间脂肪密度、T10 肌间脂肪密度、T12 肌间脂肪密度更低与总生存期改善相关。T12 皮下脂肪密度以−90.8 为临界值时生存差异最显著,但校正年龄与体重指数后,其与死亡风险的正向关联无统计学意义。T9 肌间脂肪密度以−70.3 为临界值时生存差异最大,死亡风险随 T9 肌间脂肪密度升高而增加。以中位值分组结果相似。
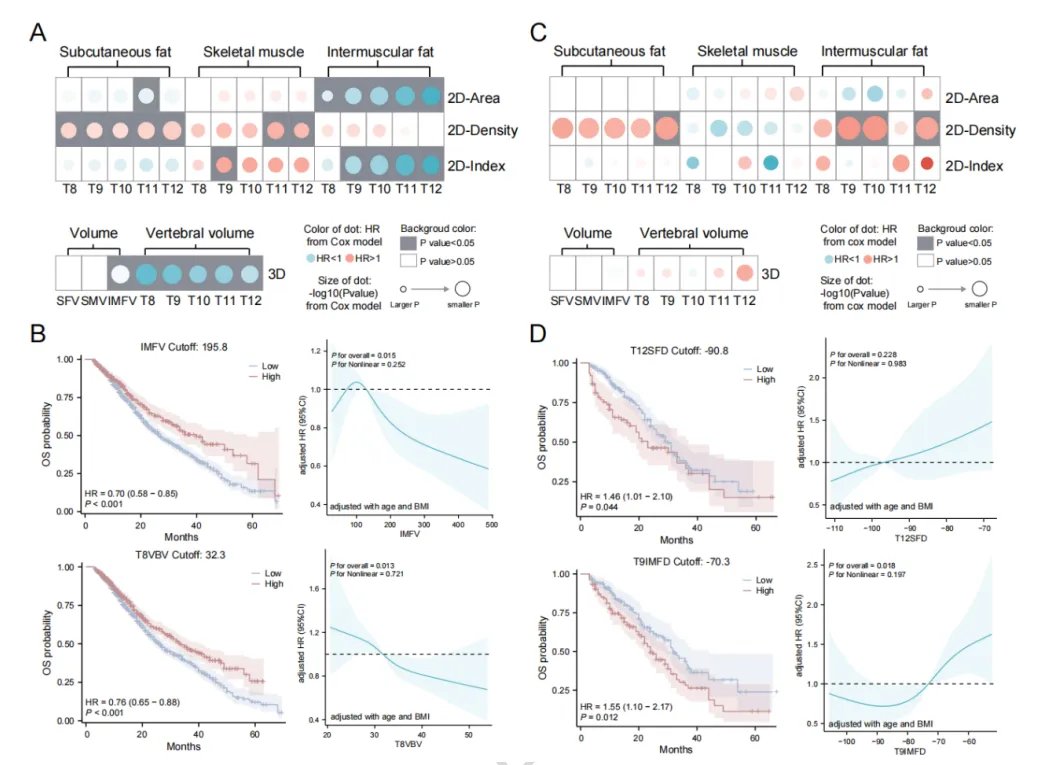
图3:A:状态特异转录因子活性。B/C:细胞状态演化与关键基因切换。D–G:四类程序与患者生存关系。H:索拉非尼耐药组程序富集。I/J:不同状态对应药物敏感性预测。
4. 多维度腹部身体成分与生存结局的关联
鉴于 L3 层面被广泛视为身体成分的代表性截面,本研究将分析扩展至 L1–L3 椎体层面,纳入内脏脂肪组织测量。
男性患者:L1 皮下脂肪面积升高与死亡风险降低相关;L1、L2、L3 皮下脂肪密度,L1、L2 内脏脂肪密度,L3 肌间脂肪密度升高与死亡风险升高相关。
女性患者:L3 皮下脂肪面积、L3 内脏脂肪面积、L1 皮下脂肪密度、L1 内脏脂肪密度、L3 皮下脂肪指数、L3 内脏脂肪指数与死亡风险存在潜在关联。
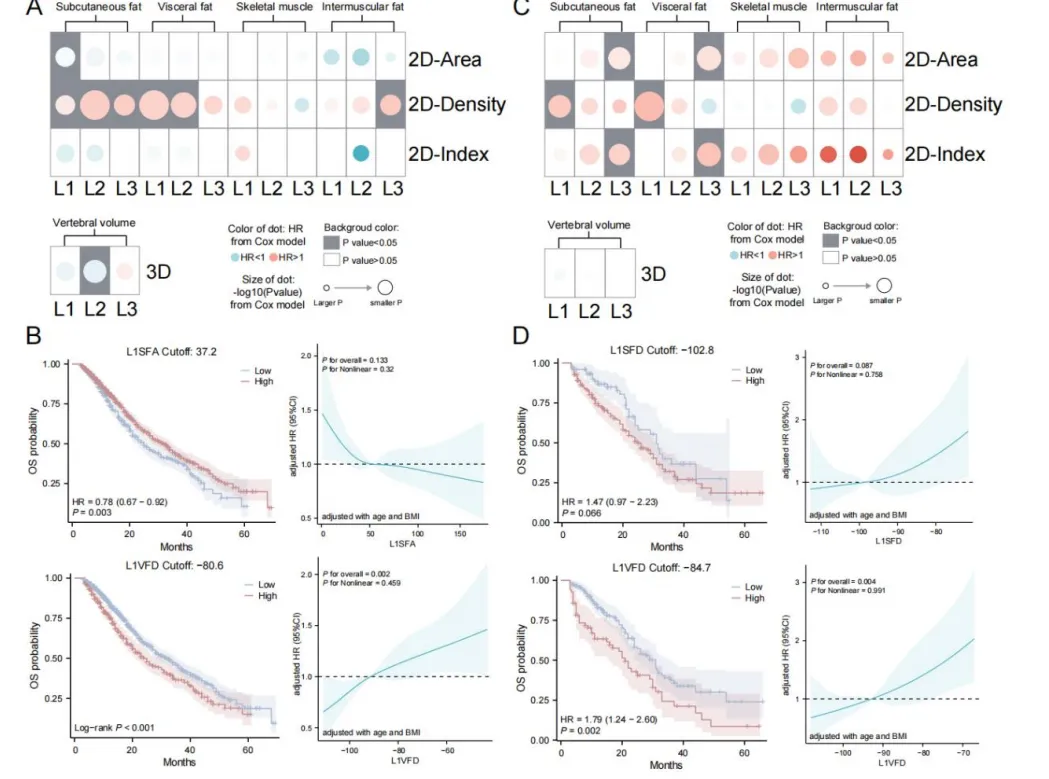
图4:A/B:髓系细胞分群与组织分布。C/D:巨噬细胞 10 个亚群分布。E–M:关键亚群功能特征。N:Macro-SPP1 与 TREM2 通路比较。
5.特定身体成分参数为总生存期的独立预测因子
多因素 Cox 回归校正全部可用临床变量(临床分期、年龄、病理亚型、体重指数、总胆红素、白蛋白、血钙、中性粒细胞 / 淋巴细胞比值、血小板 / 淋巴细胞比值)并经多重检验校正后,男性患者中 15 项身体成分参数与死亡风险仍显著相关。排除体重指数与年龄后再次校正风险比,24 项男性特异性身体成分参数与死亡风险相关。
女性患者经相同多因素 Cox 回归与多重检验校正后,仅 L1 内脏脂肪密度与死亡风险显著相关;校正前有 7 项参数显示预后价值。
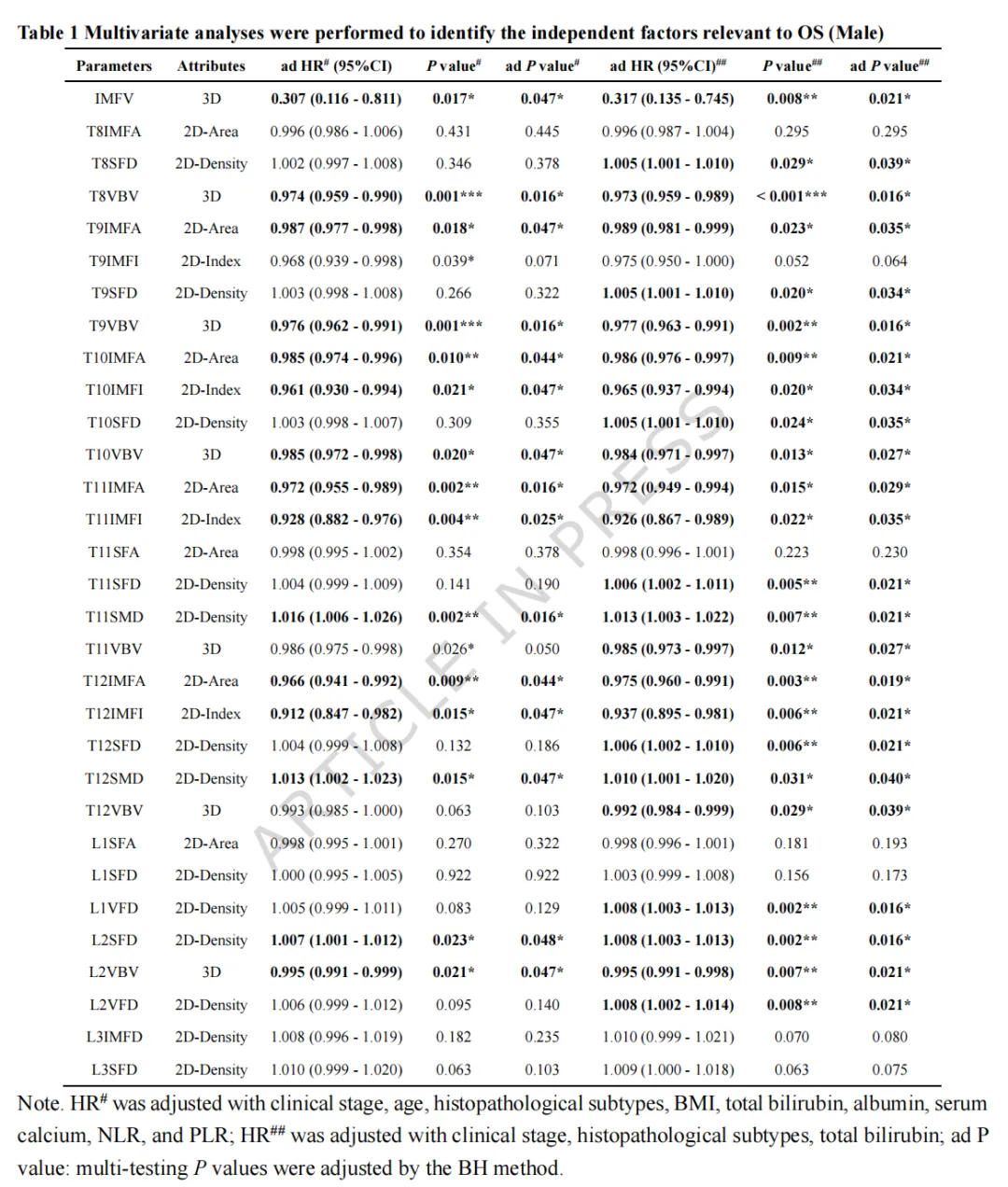
表1:男性患者总生存期独立影响因素的多因素分析
6.多维度身体成分与肿瘤分子特征相关
免疫治疗疗效与肿瘤内免疫浸润程度、免疫检查点分子表达密切相关。本研究对免疫检查点分子表达与多维度身体成分参数进行相关性分析并聚类。结果显示,在非小细胞肺癌放射基因组学队列的男、女性患者中,均出现特定相关模块聚集;免疫浸润也呈现类似聚类模式,并在 TCGA 队列中得到验证。
以身体成分参数、CD274(PDL1)表达、免疫评分(代表免疫浸润)的相关系数构建象限图。男性患者中,肌间脂肪面积、肌间脂肪体积等参数与 CD274 及免疫评分均呈正相关,骨骼肌体积、骨骼肌面积、皮下脂肪密度呈负相关,与免疫治疗临床结局趋势高度一致。女性患者中,肌间脂肪密度等指标主要位于第二象限,与 CD274 表达呈负相关,与临床队列结果一致。
基因集富集分析显示:男性患者中,T9 肌间脂肪面积升高与 T 细胞受体信号通路等激活相关,T8 皮下脂肪密度升高与干扰素 α/β 信号通路抑制相关;女性患者中,T8 皮下脂肪密度、T10 肌间脂肪密度升高与干扰素 γ 应答等通路抑制相关。
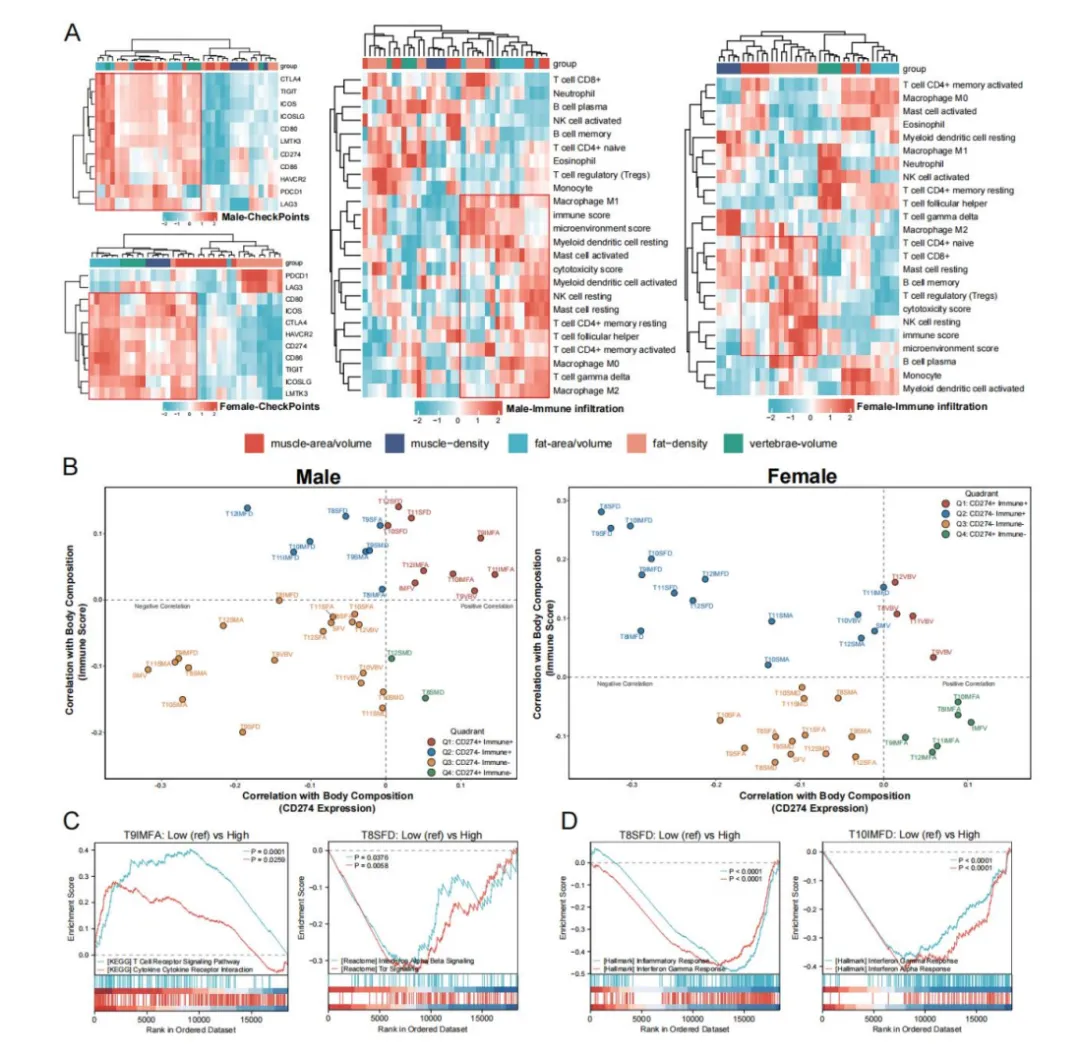
图5:A–G:内皮细胞分群,Endo-ESM1 与不良预后相关。H–N:成纤维细胞分群,Fib-CD36/POSTN 为恶性基质亚群。
7.单细胞 RNA 测序揭示身体成分与免疫微环境的关联
为进一步探索身体成分与肿瘤内免疫微环境的关联,分析 23 例非小细胞肺癌样本的单细胞 RNA 测序数据(男性 12 例,女性 11 例)。基于经典标志基因将细胞群注释为 T/NK 细胞、上皮细胞、髓系细胞、B 细胞、成纤维细胞、浆细胞、增殖细胞、内皮细胞、肥大细胞,男女样本分布相似。
重点分析男性代表性身体成分参数 —— 肌间脂肪体积。对 T/NK 细胞进一步细分:NK 细胞、CD4+T 细胞、CD8+T 细胞、调节性 T 细胞。高、低肌间脂肪体积组男性的各亚群比例无显著差异。通路分析显示,高肌间脂肪体积组 CD8+T 细胞中干扰素 α/β 信号通路显著富集,NK 细胞中干扰素相关通路也上调。高肌间脂肪体积组 CD8+T 细胞与 NK 细胞的耗竭评分更低,氧化磷酸化通路上调。
对髓系细胞细分:树突状细胞、单核细胞、巨噬细胞。高、低肌间脂肪体积组各亚群比例无显著差异,但高肌间脂肪体积组男性树突状细胞抗原呈递上调、氧化磷酸化通路增强。高肌间脂肪体积组男性巨噬细胞 M1 评分更高、M2 评分更低,干扰素相关通路与氧化磷酸化通路上调。
典型病例对比展示高、低肌间脂肪体积男性患者的细胞分布模式。高肌间脂肪体积组免疫检查点分子(LAG3、PD1、TIM3)表达整体更低,提示细胞耗竭水平可能更低。
随后分析女性代表性参数 T12 皮下脂肪密度。高 T12 皮下脂肪密度女性的 CD8+T 细胞、NK 细胞耗竭评分无显著差异,但巨噬细胞 M1 评分更高、M2 评分更低。女性高肌间脂肪体积则与 T 细胞、NK 细胞耗竭评分更高相关,与男性相反;但巨噬细胞同样呈现 M1 高、M2 低的趋势,与男性一致。
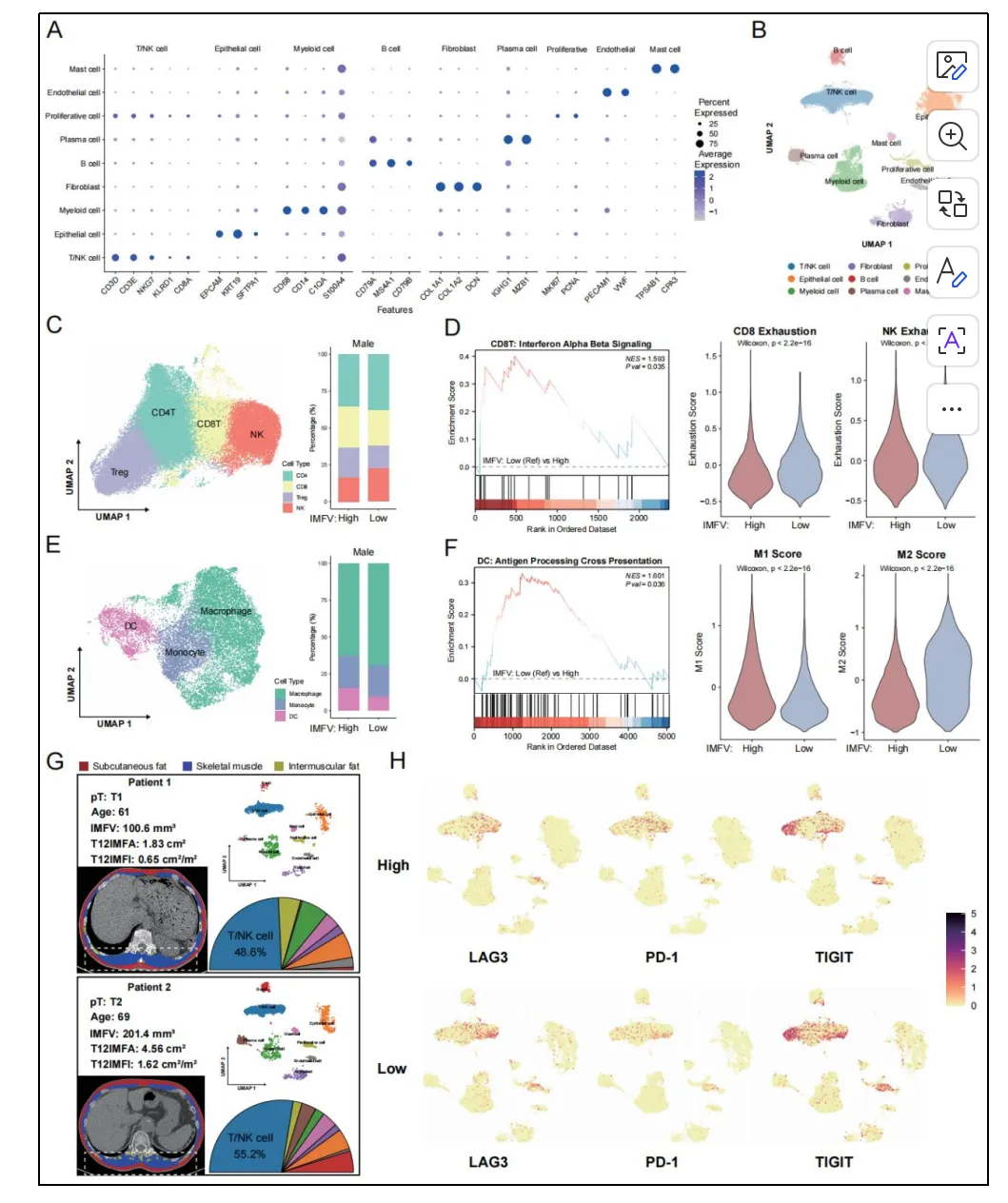
图6:A/B:进展期细胞互作强度增强。C:关键亚群通讯差异。D/E:内皮–成纤维–巨噬–肿瘤细胞核心互作轴。
五、关键方法
本研究为多中心、大样本、多组学联合研究,整合 8 个独立队列共 2132 例非小细胞肺癌(NSCLC)患者,构建了AI 驱动的 CT 身体成分全自动量化体系。基于nnUNet深度学习模型,从 T8–L3 椎体范围 CT 影像中自动分割椎体、皮下脂肪、骨骼肌、肌间脂肪、内脏脂肪,提取92 个二维 + 三维身体成分参数,效率较人工提升 100 倍以上,一致性 ICC>0.87。研究采用单 / 多因素 Cox 回归、Kaplan–Meier、限制性立方样条分析身体成分与免疫治疗总生存期(OS)的关联;通过bulk RNA-seq解析肿瘤免疫浸润、PD-L1 表达及通路富集;利用scRNA-seq在细胞水平揭示身体成分与肿瘤免疫微环境的调控机制,明确性别与解剖部位差异。
六、总结
总体而言,这篇发表于 npj Precision Oncology 的 NSCLC 研究,以 AI 驱动的 CT 影像身体成分量化为核心工具,系统解析了非小细胞肺癌患者身体成分与免疫治疗预后的关联及分子机制。它通过 nnUNet 深度学习模型实现了身体成分的全自动、高精度量化,揭示了身体成分预后价值的显著性别与解剖部位差异,阐明了男性高肌间脂肪体积通过重塑肿瘤免疫微环境发挥保护作用的内在机制,并最终验证了多维身体成分作为 NSCLC 免疫治疗无创预后标志物的临床应用潜力。
对肿瘤研究者而言,这篇文章的价值不仅在于身体成分与免疫治疗预后的关联结果,更在于它示范了一种值得学习的研究路径:从大样本多队列临床数据出发,以 AI 技术实现无创指标的精准量化,用多组学解析分子机制,再将结果推进到临床可应用的预后分层。这或许正是未来肿瘤精准医学研究最有代表性的方向之一。


 夜雨聆风
夜雨聆风




