文档内容
2 0 2 5 年 上 教 师 资 格 · 化 学 学 科 笔 试
主讲老师 岳筱涵
粉笔教师教育 粉笔教师氯、溴、碘及其化合物二、氯气的制法 P64
(一)氯气的实验室制法
1.反应的原理:
用强氧化性物质(如MnO 、KMnO 、KClO 等)和浓盐酸反应。
2 4 3
MnO +4HCl(浓) MnCl +Cl ↑+2H O
2 2 2 2
2KMnO +16HCl(浓) 2KCl+2MnCl +5Cl ↑+8H O(不需加热)
4 2 2 2
KClO +6HCl(浓) KCl+3Cl ↑+3H O(不需加热)
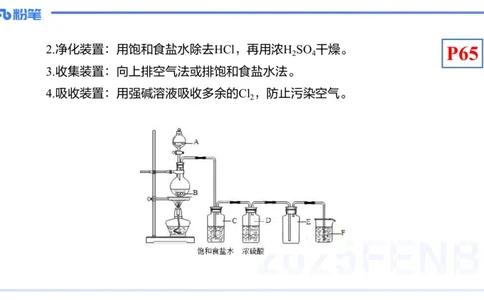
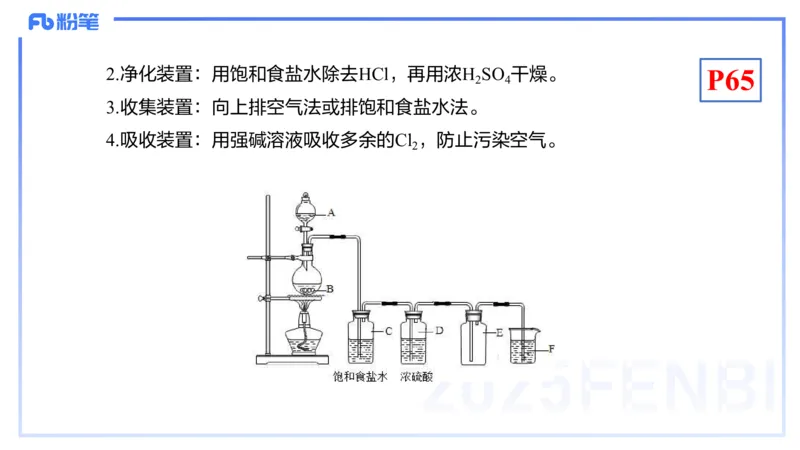
3 2 22.净化装置:用饱和食盐水除去HCl,再用浓H SO 干燥。
P65
2 4
3.收集装置:向上排空气法或排饱和食盐水法。
4.吸收装置:用强碱溶液吸收多余的Cl ,防止污染空气。
2(二)氯气的工业制法 P65
1.电解饱和食盐水(氯碱工业)
2NaCl+2H O 2NaOH+H ↑+Cl ↑
2 2 2
2.电解熔融的氯化钠和氯化镁制取金属钠和镁时,副产品是氯气。三、卤素及其化合物的递变规律及特性 P65
(一)卤素及化合物的递变规律
1.单质氧化性:F >Cl >Br >I
2 2 2 2
2.离子还原性:I->Br->Cl->F-
3.HX的稳定性:HF>HCl>HBr>HI
4.HX的熔点:HI>HF(含氢键)>HBr>HCl
5.HX的沸点:HF(含氢键)>HI>HBr>HCl
6.最高价含氧酸的酸性:HClO >HBrO >HIO
4 4 4P65
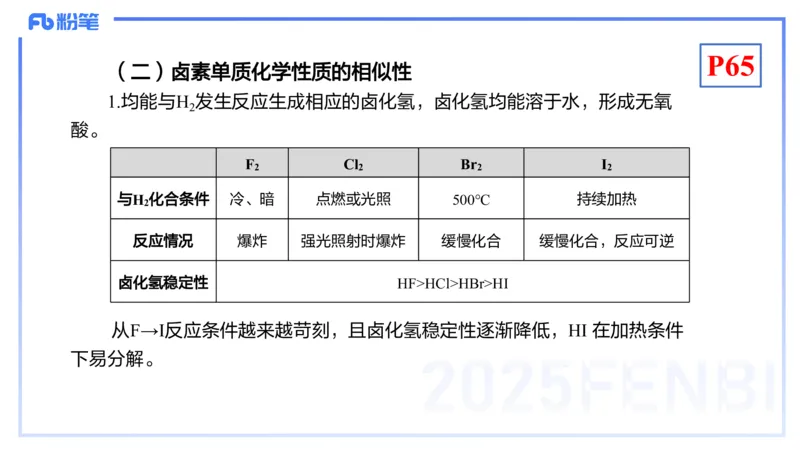
(二)卤素单质化学性质的相似性
1.均能与H 发生反应生成相应的卤化氢,卤化氢均能溶于水,形成无氧
2
酸。
F Cl Br I
2 2 2 2
与H 化合条件 冷、暗 点燃或光照 500℃ 持续加热
2
反应情况 爆炸 强光照射时爆炸 缓慢化合 缓慢化合,反应可逆
卤化氢稳定性 HF>HCl>HBr>HI
从F→I反应条件越来越苛刻,且卤化氢稳定性逐渐降低,HI 在加热条件
下易分解。2.与水反应
P66
均能与水反应生成相应的氢卤酸和次卤酸(氟除外)
X +H O HX+HXO(X= Cl、Br、I)
2 2
2F +2H O 4HF+O (注:将 F 通入某物质的水溶液中,F 先
2 2 2 2 2
跟H O反应)
2
3.与金属反应
(1)F 、Cl 可与绝大多数金属化合(除Au、Pt外),Br 、I 可与大
2 2 2 2
多数金属化合。
(2)对于变价金属,如Fe、Cu,Cl 、Br 将金属氧化到最高价,I
2 2 2
将金属氧化到较低价。P66
4.与碱反应
以NaOH为例:X +2NaOH NaX+NaXO+H O(X= Cl、Br)
2 2
3I +6NaOH 5NaI+NaIO +3H O
2 3 2
5.氧化还原反应(氧化性Cl >Br >I )
2 2 2
(1)Cl +2NaBr 2NaCl+Br
2 2
Cl +2NaI 2NaCl+I
2 2
Br +2NaI 2NaBr+I
2 2
(2)X +H SO +H O H SO +2HX (X= Cl、Br、I)
2 2 3 2 2 4P66
(三)卤素中的某些特性及相关应用
1.氟
(1)无正价和含氧酸,非金属性最强。
(2)2F +2H O 4HF+O ,与H 反应在冷暗处即爆炸。
2 2 2 2
(3)HF是弱酸,能腐蚀玻璃,保存在铅皿或塑料瓶中;有毒,
在HX中沸点最高。
(4)AgF易溶于水,没有感光性。2.溴
P66
(1)Br 是深红棕色液体,易挥发,盛溴的试剂瓶中加水,进行
2
水封,保存液溴不能用橡胶塞。
(2)Br 易溶于有机溶剂。
2
(3)AgBr可作感光材料,用于照相(AgX中,除AgF外,其余均
有感光性)。(4)从海水中提取溴的工业流程:
P67P67
从海水中提取溴的过程中涉及的主要化学反应方程式:
①向酸化的海水中通入适量的氯气,使Br-转化为Br :
2
2NaBr+Cl Br +2NaCl。
2 2
②含Br 的空气在盛有SO 溶液的吸收塔中被吸收:
2 2
Br +SO +2H O 2HBr + H SO
2 2 2 2 4
③向吸收塔内的溶液中通入适量的氯气:
2HBr + Cl 2HCl + Br
2 2【粉笔提示】 P67
溴水褪色的六种常见情况
1.因萃取而褪色:苯、CCl 与溴水混合后,水层几乎为无色。
4
2.因歧化而褪色:溴水中加入强碱,发生歧化反应
(Br → Br-+BrO-或BrO -,橙色褪去)。
2 3
3.因被还原而褪色:镁粉、锌粉、H S、SO 、SO 2-、Fe2+、I-等
2 2 3
能将Br 还原为Br-而使溴水褪色。
2P67
4.因沉淀而褪色:溴水中加入AgNO 溶液,生成浅黄色AgBr沉淀,
3
溴水褪色。
5.因加成而褪色:含碳碳双键、碳碳三键的有机物与Br 发生加成反
2
应而使溴水褪色。
6.因取代而褪色:酚类物质与浓溴水反应,酚羟基邻、对位上的氢
原子被溴原子取代而使浓溴水褪色。P67
3.碘
(1)淀粉遇I 变蓝色。
2
(2)I 加热时易升华,常利用此性质与其他物质分离。
2
(3)I 易溶于有机溶剂。
2
(4)食用盐中加入KIO 可防治甲状腺肿大。
3
(5)AgI用于人工降雨。P68
(6)从海带中提取碘的工业生产流程:
从海带中提取碘的过程中涉及的化学方程式:
Cl + 2I- I + 2Cl-
2 2P68
2. 化学与生产、生活密切相关,下列说法正确的是( )。
A. 蛋白质、纤维素都是天然有机高分子化合物
B. FeCl 可用作止血剂是因为 Fe3+ 具有氧化性
3
C. 用米汤可以检验加碘盐中是否含有碘
D. 造成光化学烟雾的物质是 SO
2P68
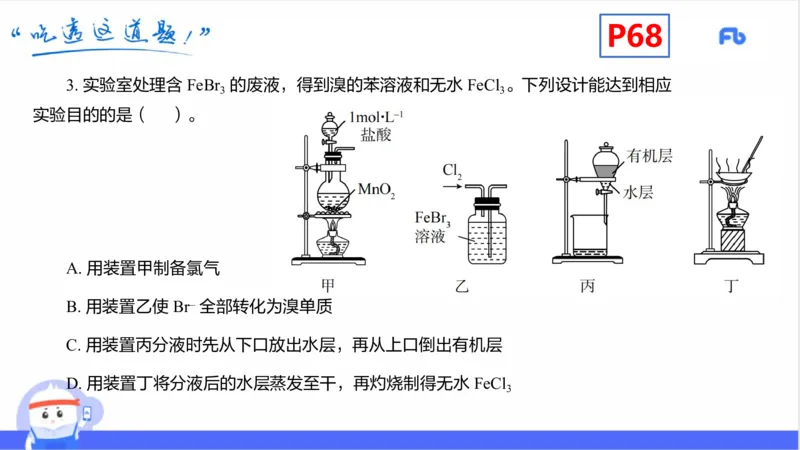
3. 实验室处理含 FeBr 的废液,得到溴的苯溶液和无水 FeCl 。下列设计能达到相应
3 3
实验目的的是( )。
A. 用装置甲制备氯气
B. 用装置乙使 Br– 全部转化为溴单质
C. 用装置丙分液时先从下口放出水层,再从上口倒出有机层
D. 用装置丁将分液后的水层蒸发至干,再灼烧制得无水 FeCl
3硫及其化合物P69
一、硫的性质和用途
(一)物理性质
硫(俗称硫黄)是一种淡黄色晶体,质脆,易研成粉末。
硫不溶于水,微溶于酒精,易溶于CS 。
2
硫是一种生命元素,组成某些蛋白质时离不开它,这也正是石油
、天然气、煤等化石燃料中经常含硫的原因。(二)化学性质 P69
1.与非金属单质反应
S+O SO
2 2
现象:硫在空气中燃烧发出淡蓝色火焰,在纯氧中燃烧发出蓝紫
色火焰。
2.与金属单质反应
Fe+S FeS(黑色固体)
2Cu+S Cu S(黑色固体)
23.与强氧化性酸反应
P70
S+2H SO (浓) 3SO ↑+2H O
2 4 2 2
4.与强碱反应
3S+6NaOH 2Na S+Na SO +3H O
2 2 3 2
(三)用途
制硫酸、橡胶、黑火药、医药、农药、火柴。P70
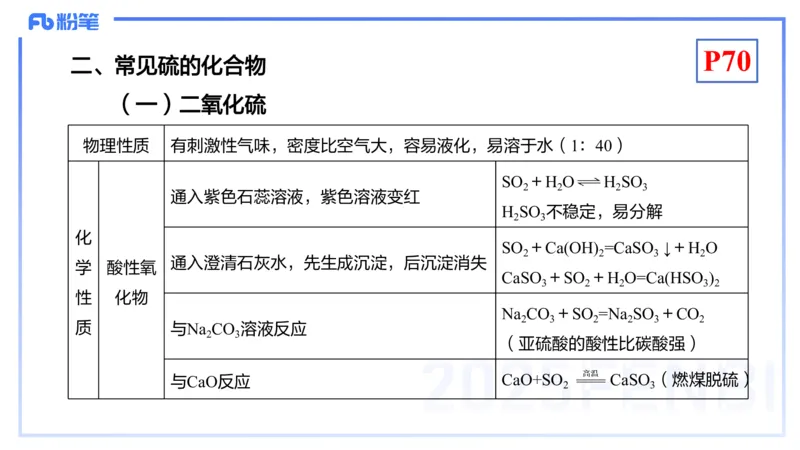
二、常见硫的化合物
(一)二氧化硫
物理性质 有刺激性气味,密度比空气大,容易液化,易溶于水(1:40)
SO +H O H SO
2 2 2 3
通入紫色石蕊溶液,紫色溶液变红
H SO 不稳定,易分解
2 3
化
SO +Ca(OH) =CaSO ↓+H O
2 2 3 2
通入澄清石灰水,先生成沉淀,后沉淀消失
学 酸性氧
CaSO +SO +H O=Ca(HSO )
3 2 2 3 2
性 化物
Na CO +SO =Na SO +CO
2 3 2 2 3 2
质 与Na CO 溶液反应
2 3
(亚硫酸的酸性比碳酸强)
与CaO反应 CaO+SO CaSO (燃煤脱硫)
2 3P70
漂白性 使品红溶液褪色(加热可恢复)
化
学 氧化性 与H S反应,生成淡黄色固体 SO +2H S=3S↓+2H O
2 2 2 2
性
使溴水褪色 SO +Br +2H O=H SO +2HBr
2 2 2 2 4
还原性
质
与O 反应 2SO +O 2SO
2 2 2 31.SO 不能漂白酸碱指示剂,如SO 通入紫色的石蕊溶液中,溶液
P70
2 2
变红。而氧化类漂白剂(如氯水、Na O 等)能漂白酸碱指示剂。
2 2
2.SO 使溴水、KMnO 溶液褪色,是利用SO 的还原性,而不是漂
2 4 2
白性:
2KMnO +5SO +2H O 2MnSO +K SO +2H SO
4 2 2 4 2 4 2 43.若向品红溶液中通入等物质的量的Cl 和SO ,则二者不是“强 P71
2 2
强联手”,而是“两败俱伤”,发生的反应为:
SO +Cl +2H O H SO +2HCl,品红溶液不褪色。
2 2 2 2 4
向品红溶液和紫色石蕊试液中通入SO 和Cl ,相关的变化和现象
2 2
分别为:P71
4.二氧化硫对环境的污染及治理
(1)二氧化硫的污染:SO 是污染大气的主要有害物质之一,对人体的
2
直接危害是引起呼吸道疾病,严重时致人死亡。
(2)酸雨的形成
煤、石油和某些金属矿物中含硫或硫的化合物,因此燃烧或冶炼时,往
往会生成SO 。
2
在机动车内燃机中燃料燃烧产生的高温条件下,空气中的N 往往也会参
2
与反应,这也是汽车尾气中含有NO的原因,NO极易与空气中的O 结合形成
2
NO 。大气中SO 和NO 溶于空气中的水蒸气形成酸性小液滴,随雨水下降,
2 2 2
就可能形成酸雨,酸雨的pH小于5.6。P71
(3)酸雨的危害
酸雨能直接破坏农作物、森林、草原,使土壤、湖泊酸化,还会
加速建筑物、工业设备和名胜古迹的腐蚀。(4)治理方法
P71
①调整能源结构,发展清洁能源,优化能源质量,提高能源利用
率,减少燃煤产生的SO 和氮氧化物等。
2
②加强环境管理,强化环保执法,严格控制SO 的排放量。
2
③研究、开发适合我国国情的SO 治理技术和设备。
2
a.原煤脱硫技术,可以除去燃煤中40%~60%的无机硫。
b.改进燃烧技术,减少燃煤过程中SO 和氮氧化物的排放量。
2
c.对煤燃烧后形成的烟气进行脱硫。目前主要用石灰法,脱硫效
果较好,可以除去烟气中85%~90%的SO ,但是成本较高。
2P74
1. 下列说法正确的是( )。
A. 可以用聚氯乙烯制作食品包装袋
B. 人类需要的能量都是由化学反应产生的
C. 为增加农作物产量,大量使用化肥和农药
D. 用可燃冰代替煤作燃料可减少二氧化硫的排放P74
2. 下列说法正确的是( )。
A. Cl 具有漂白性,故可用于自来水的消毒
2
B. SO 具有还原性,故能使酸性 KMnO 溶液褪色
2 4
C. 单质硅化学性质稳定,故可用于制造光纤和太阳能电池
D. NH 是一种碱性气体,故可用 P O 或碱石灰干燥
3 2 5P72
【粉笔提示】
实验:二氧化硫气体的制备
1.反应原理:Na SO (s)+H SO (浓) Na SO +H O+SO ↑
2 3 2 4 2 4 2 2
2.实验装置:制Cl 装置(但不需加热)
2
3.注意事项
(1)由于SO 易溶于水,所以应选用浓H SO 和固体Na SO 反应,反应是
2 2 4 2 3
在固体和液体不加热反应装置中进行的。通常Na SO (s)为粉末状,为控制反
2 3
应速率,浓H SO 应从分液漏斗中逐滴滴下。
2 4P72
(2)不能采用浓盐酸,因为其中含有大量的水(市售浓盐酸的质量分数
约为 37%),会有大量的 SO 溶解在其中。
2
(3)也不能采用18.4 mol/L的浓H SO (即质量分数为98%的浓H SO ),
2 4 2 4
因为其中缺少水分,硫酸几乎没有电离,仍以分子形式存在,而Na SO (s)与
2 3
H SO 的反应是在H SO 电离成离子的状态下才能顺利进行的。故通常采用质
2 4 2 4
量分数为70%的浓H SO 。
2 4
(4)不宜采用Na SO 溶液,因为其中含有大量水。
2 3(二)硫酸的性质和用途
P72
1.物理性质
无色油状液体,难挥发,密度比水大。
2.化学性质
属于二元强酸,稀硫酸具有酸的通性。
3.浓硫酸的稀释方法
将浓硫酸沿器壁慢慢注入水中,并不断搅拌。(酸入水、沿器壁、慢慢倒、勤搅拌)P73
4.浓硫酸的特性
(1)吸水性:浓硫酸常作干燥剂,但不能干燥NH 、H S、HI等。
3 2
(2)脱水性:将有机物质中氢、氧元素的原子按2:1的个数比脱去
生成水。如使蔗糖炭化变黑。(3)强氧化性
P73
Cu+2H SO (浓) CuSO +SO ↑+2H O
2 4 4 2 2
C+2H SO (浓) 2SO ↑+CO ↑+2H O
2 4 2 2 2
(4)浓硫酸与金属的反应
①钝化:常温下,冷的浓硫酸对Al、Fe有“钝化”作用,可用铝
槽车装运浓硫酸。
②活泼金属(如Zn):开始产生SO ,浓度变小后产生H 。
2 2
③不活泼金属(如Cu):开始产生SO (加热),浓度变小后,
2
稀硫酸不再与Cu反应。P74
3. 下列实验现象所涉及的化学原理相同的是( )。
A. 浓盐酸和浓硫酸暴露在空气中浓度均降低
B. 硫酸亚铁和亚硫酸钠在空气中久置均会变质
C. 氯水和二氧化硫均能使品红溶液褪色
D. 氯化铵和碘都可以用加热的方法提纯粉笔教师教育 粉笔教师