文档内容
福州三中 2024-2025 学年高三第十四次质量检查
化学试题
(满分 100分,考试时间 75分钟)
可能用到的原子量:Li-7
一、选择题(本题共10小题,每小题4分,共40分。在每小题给出的四个选项
中,只有一项是符合题目要求的。)
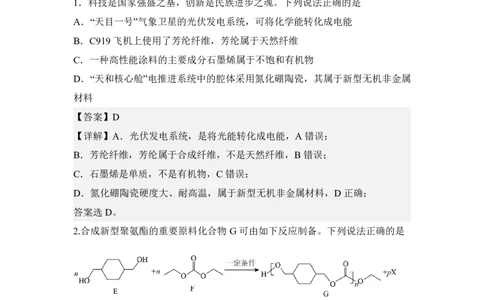
1.科技是国家强盛之基,创新是民族进步之魂。下列说法正确的是
A.“天目一号”气象卫星的光伏发电系统,可将化学能转化成电能
B.C919飞机上使用了芳纶纤维,芳纶属于天然纤维
C.一种高性能涂料的主要成分石墨烯属于不饱和有机物
D.“天和核心舱”电推进系统中的腔体采用氮化硼陶瓷,其属于新型无机非金属
材料
【答案】D
【详解】A.光伏发电系统,是将光能转化成电能,A错误;
B.芳纶纤维,芳纶属于合成纤维,不是天然纤维,B错误;
C.石墨烯是单质,不是有机物,C错误;
D.氮化硼陶瓷硬度大、耐高温,属于新型无机非金属材料,D正确;
答案选D。
2.合成新型聚氨酯的重要原料化合物G可由如下反应制备。下列说法正确的是
A.p=n-1,化合物X为乙醇
B.化合物F分子中最多有8个原子共平面
C.1molG与足量NaOH溶液反应,理论上最多可消耗2nmolNaOH
D.该合成反应为缩聚反应,且化合物E易形成分子内氢键
【答案】C
【详解】A.结合原子守恒可知,X为乙醇,n个E 分子和n个F 分子脱去2n
试卷第1页,共17页
{#{QQABTYiUggCIABJAAQgCQwFSCkGQkACCCYoGwBAUsAAAgQFABAA=}#}个乙醇分子,链端的两端都留了一个发生缩聚的官能团,故p2n1,A错误;
B.单键可以旋转,甲基上的三个氢原子最多可以有一个与分子共面,化合物F
分子中最多有10个原子共平面,B 错误;
C.1molG水解会生成nmolH CO ,与足量NaOH溶液反应,理论上最多可消耗
2 3
2nmolNaOH,C正确;
D.该反应有小分子的乙醇生成,是缩聚反应,化合物E两个羟基较远,不能形
成分子内氢键,易形成分子间氢键,D错误;
故选C。
3.解耦电解水可实现用电低谷期的过剩电力向氢能的高效转化,一种以多硫化物
离子为介质的转化关系如图。设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.1mol的S2 中含有σ键数目为xN
x1 A
B.1L0.1molL1Na S溶液中含阴离子的数目小于0.1N
2 A
C.用电低谷期生成1molS2得到电子数目为4N
x A
D.用电高峰期生成11.2LH 时,发生还原反应的H O分子数为N
2 2 A
【答案】A
【知识点】22.4L/mol 适用条件、氧化还原反应与NA 相关推算、物质结构基础
与NA相关推算
【分析】用电低谷期的反应方程式为:2H O+2S2- =2S2-+2S2-+O +4H+ ,用电高峰
2 x+1 x 2
期的反应方程式为:S2-+S2-+2H O=H +S2- +2OH-。
x 2 2 x+1
【详解】A.S2 中硫元素之间以单键相连,S-S键个数为x个,则1mol的S2 中
x1 x1
含有σ键数目为xN ,A正确;
A
B.Na S 溶液中存在S2-+H OHS-+OH-,所以1L0.1mol•L-1Na S 溶液中含阴离
2 2 2
试卷第2页,共17页
{#{QQABTYiUggCIABJAAQgCQwFSCkGQkACCCYoGwBAUsAAAgQFABAA=}#}子的数目大于0.lNA,B 错误;
C.用电低谷期的反应方程式为:2H O+2S2- =2S2-+2S2-+O +4H+ ,O元素从-2 升
2 x+1 x 2
到0价,有2个O变价,则生成1molS2得到电子数目为2N ,C 错误;
x A
D.选项中没有指明在标准状况下,无法进行计算,D错误;
故选A。
4.能正确表示下列反应的电极或离子方程式的为
A.将BrCl滴入NaOH溶液中:BrCl+2OH- Br-+ClO-+H O
2
B.将等体积等物质的量浓度的Ba(OH) 和NH HSO 溶液混合:
2 4 4
Ba2++2OH-+2H++SO2 BaSO +2H O
4 4 2
C.将硫酸铬溶液滴入含有NaClO的碱性溶液中:
2Cr3++3ClO+8OH Cr O2+3Cl+4H O
2 7 2
D.铅酸蓄电池放电时的正极反应:PbO +4H++2e+SO2 PbSO +2H O
2 4 4 2
【答案】D
【详解】A. BrCl 与NaOH溶液反应实际上是BrCl 的水解反应,Cl-与H O 电
2
离的H+结合成HCl,Br+与OH-结合成HBrO,最后在与NaOH 反应生成NaBrO
和NaCl,离子方程式为:BrCl+2OH- Cl-+BrO-+H O,故A错误;
2
B.等物质的量的Ba(OH) 和NH HSO 反应生成硫酸钡沉淀、一水合氨和水,
2 4 4
正确的离子方程式为:Ba2++2OH-+NH+H++SO2 BaSO +NH H O+H O,故B
4 4 4 3 2 2
错误;
C.硫酸铬溶液滴入含NaClO的碱性溶液生成Na CrO ,离子方程式为
2 4
2Cr3++3ClO+10OH 2CrO2+3Cl+5H O,故C 错误;
4 2
D.铅酸蓄电池放电时PbO 发生还原反应生成PbSO ,正极反应式为
2 4
PbO +4H++2e+SO2 PbSO +2H O,故D正确;
2 4 4 2
故选:D。
试卷第3页,共17页
{#{QQABTYiUggCIABJAAQgCQwFSCkGQkACCCYoGwBAUsAAAgQFABAA=}#}5.LiTFSI是一种亲水有机盐,其结构如图所示,其中A、B、C、D为同一短
周期元素,C 与E位于同一主族。下列叙述正确的是
A.C 是空气中含量最高的元素
B.简单气态氢化物的稳定性:DCE
C. Al3与E 的简单阴离子在溶液中能大量共存
D.该化合物中只有A、C、D元素原子的最外层满足8电子稳定结构
【答案】B
【知识点】盐类双水解反应、元素金属性与非金属性递变规律的理解及应用
【分析】结合图示可知,有4个C 形成2个共价键,E形成6个共价键,C 与E
位于同一主族,二者应该位于VIA 族,故C 为O,E 为S;A形成4个共价键,
D形成1个共价键,且A、B、C、D为同一短周期,元素则A为C,D 为F;B
形成2个单键同时得到1个电子使整个原子团带有1个单位负电荷,故B为N,
以此分析解答;
【详解】A.空气中含量最高的是N,不是O,故A 错误;
B.非金属性越强,简单气态氢化物稳定性越强,非金属性:F>O>S,简单氢
化物的稳定性:HF>H O>H S,故B正确;
2 2
C. E的简单阴离子为S2-, Al3与S2-在水溶液中相互促进水解不能大量共存,
故C 错误;
D.该化合物中C、N、O、F 元素原子最外层均满足 8电子稳定结构,S 不满足,
故D错误;
答案选B。
6.有关下图及实验的描述正确的是
A.用图1装置蒸发FeCl 溶液制备无水FeCl
3 3
B.用图2装置精炼铝
试卷第4页,共17页
{#{QQABTYiUggCIABJAAQgCQwFSCkGQkACCCYoGwBAUsAAAgQFABAA=}#}C.用图3装置证明浓硫酸具有脱水性和强氧化性
D.用图4装置可比较氯、碳、硅三种元素的非金属性强弱
【答案】C
【详解】A.FeCl 溶液发生水解生成挥发性的氯化氢,蒸发得不到无水FeCl ,
3 3
故A错误;
B.用图2装置阴极发生氯离子的放电反应,故 B错误;
C.浓硫酸滴入蔗糖中,蔗糖体积迅速膨胀,说明浓硫酸检验脱水性,若酸性高
锰酸钾褪色,说明浓硫酸与碳发生了氧化还原反应,生成了二氧化硫,故C 正
确;
D.盐酸检验挥发性,不能证明碳酸的酸性比硅酸强,故D错误;
答案选C。
7.实验室提取桂花精油的流程如下。下列说法错误的是
A.“操作①”所需的玻璃仪器有烧杯、漏斗、玻璃棒
B.“操作②”为过滤,所得的石油醚可循环利用
C.“乙醇洗涤”可提高桂花精油的收率
D.“减压蒸馏”可防止桂花精油在较高温度下变质
【答案】B
【分析】向桂花中加入石油醚,充分振荡,过滤,分离除去不溶物,得到溶液,
然后根据物质沸点的不同,将溶液进行蒸馏,分离出沸点低的石油醚和桂花浸膏,
再向桂花浸膏中加入无水乙醇回流1小时,进行抽滤,并用乙醇洗涤固体残渣,
充分回收桂花精油,将分离得到溶液进行减压蒸馏,分离得到桂花精油。
【详解】A.“操作①”是分离难溶性固体与可溶性液体混合物的操作,该操作名
称为过滤,所需的玻璃仪器有烧杯、漏斗、玻璃棒,A正确;
B.“操作②”为分离互溶的、沸点不同的混合物,名称为蒸馏,所得的沸点较低
的石油醚可循环利用,B 错误;
C.残留在固体上的桂花精油能够溶于乙醇,“乙醇洗涤”抽滤时的固体残渣,可
试卷第5页,共17页
{#{QQABTYiUggCIABJAAQgCQwFSCkGQkACCCYoGwBAUsAAAgQFABAA=}#}提高桂花精油的收率,C 正确;
D.桂花精油不稳定,高温易变质。利用物质沸点随压强的减小而降低的性质进
行“减压蒸馏”就可防止桂花精油在较高温度下变质,D正确;
故合理选项是B。
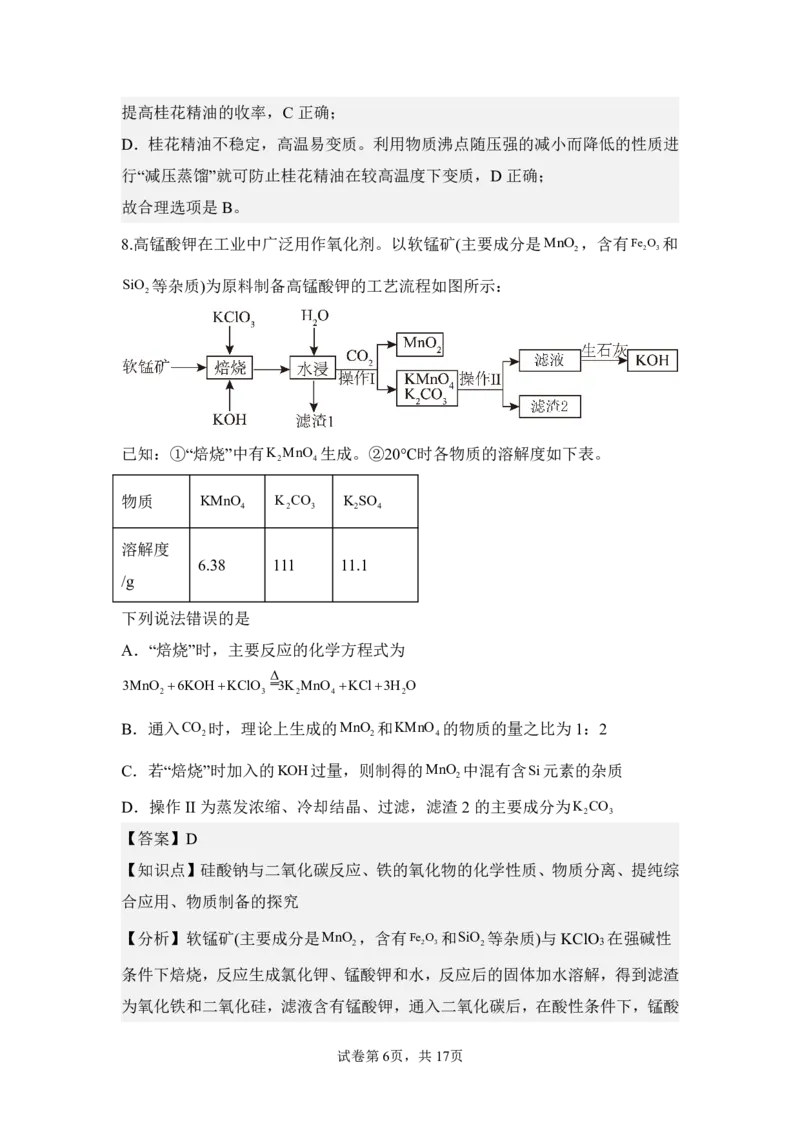
8.高锰酸钾在工业中广泛用作氧化剂。以软锰矿(主要成分是MnO ,含有Fe O 和
2 2 3
SiO 等杂质)为原料制备高锰酸钾的工艺流程如图所示:
2
已知:①“焙烧”中有K MnO 生成。②20℃时各物质的溶解度如下表。
2 4
物质 KMnO K CO K SO
4 2 3 2 4
溶解度
6.38 111 11.1
/g
下列说法错误的是
A.“焙烧”时,主要反应的化学方程式为
3MnO 6KOHKClO 3K MnO KCl3H O
2 3 2 4 2
B.通入CO 时,理论上生成的MnO 和KMnO 的物质的量之比为1:2
2 2 4
C.若“焙烧”时加入的KOH过量,则制得的MnO 中混有含Si元素的杂质
2
D.操作II 为蒸发浓缩、冷却结晶、过滤,滤渣2的主要成分为K CO
2 3
【答案】D
【知识点】硅酸钠与二氧化碳反应、铁的氧化物的化学性质、物质分离、提纯综
合应用、物质制备的探究
【分析】软锰矿(主要成分是MnO ,含有Fe O 和SiO 等杂质)与KClO 在强碱性
2 2 3 2 3
条件下焙烧,反应生成氯化钾、锰酸钾和水,反应后的固体加水溶解,得到滤渣
为氧化铁和二氧化硅,滤液含有锰酸钾,通入二氧化碳后,在酸性条件下,锰酸
试卷第6页,共17页
{#{QQABTYiUggCIABJAAQgCQwFSCkGQkACCCYoGwBAUsAAAgQFABAA=}#}钾发生歧化反应得到二氧化锰固体和高锰酸钾、碳酸钾,根据高锰酸钾、碳酸钾
的溶解度差别较大,可以采取蒸发浓缩、冷却结晶,过滤得到高锰酸钾固体和碳
酸钾,碳酸钾加入生石灰后,得到氢氧化钾,据以上分析解答。
【详解】A. “焙烧”时,根据已知有K MnO 生成,主要反应的化学方程式为
2 4
3MnO 6KOHKClO 3K MnO KCl3H O ,A项正确;
2 3 2 4 2
B. 根据工艺流程图可知,通入CO 时,“焙烧”生成的K MnO 反应得到MnO 、
2 2 4 2
KMnO 、K CO ,化学方程式为:3K MnO 2CO =2KMnO MnO 2K CO 理论上
4 2 3 2 4 2 4 2 2 3
生成的MnO 和KMnO 的物质的量之比为1:2,B 项正确;
2 4
C. 若“焙烧”时加入的KOH过量,SiO 也能与KOH反应生成K SiO ,通入CO 后,
2 2 3 2
K SiO 与CO 反应生成H SiO 沉淀,使制得的MnO 中混有含Si元素的杂质,C 项
2 3 2 2 3 2
正确;
D. 据表格中的溶解度,KMnO 的溶解度远小于K CO ,所以KMnO 、K CO 分离
4 2 3 4 2 3
操作为蒸发浓缩、冷却结晶、过滤,滤渣2的主要成分为KMnO ,D 项错误;
4
答案选D。
9.华中科技大学孙永明教授课题组利用一种“蓝”石墨电极(Li P基固态电解质界
3
面膜)实现了锂离子电池的极速充电和长循环寿命,工作原理如下图所示。下列
说法正确的是
A.充电时,N极发生还原反应
B.放电时, Li通过固态电解质向M 极移动
C.放电时,M极发生的电极反应为xLi++C+xe-=Li C
x
D.当电路中通过1mol电子时,理论上两电极的质量变化差为14g
试卷第7页,共17页
{#{QQABTYiUggCIABJAAQgCQwFSCkGQkACCCYoGwBAUsAAAgQFABAA=}#}【答案】D
【知识点】原电池、电解池综合考查
【分析】由图可知,N充电由LiNi Co Mn O -xe-→Li Ni Co Mn O +xLi+,
0.6 0.2 0.2 2 1-x 0.6 0.2 0.2 2
失电子,发生氧化反应为阳极,放电为正极,M 为负极或阴极,据此解答。
【详解】A.根据分析可知,充电时,N极失电子,发生氧化反应,故A错误;
B.结合图示可知,放电时,Li+向正极,即N极移动,故B 错误;
C.放电时,M 极发生氧化反应生成Li+,发生的电极反应为Li C-xe-=xLi++C,故
x
C 错误;
D.当电路中通过1mol 电子时,发生反应的Li+为1mol,质量为1mol×7g/mol=7g,
所以理论上两电极的质量变化差为14g(正负两极质量一增一减),故D 正确;
答案选D。
10.25℃时,将 4-氨基苯甲酸[ : pK -COOH2.40 ,
a
pK b NH 2 9.10 的稀溶液加入插有惰性电极的电解槽中,保持其他条件不变,
调节溶液pH,其离子向某一电极的迁移速率与溶液pH的关系如下图所示。下列
说法正确的是
A. 25C 时,pK :苯甲酸<4-氨基苯甲酸
a
B.N点溶液中:c( )4-氨基苯甲酸,A
a
错误;
试卷第8页,共17页
{#{QQABTYiUggCIABJAAQgCQwFSCkGQkACCCYoGwBAUsAAAgQFABAA=}#}B.4—氨基苯甲酸具有两性,pH较小时氨基与氢离子作用,生成铵盐
,带正电,迁移速率大,即在M 点之前;在呈中性时,形成
分子内盐或净电荷为0,不带电,迁移速率为0;pH较大时形成羧酸盐
带负电,迁移速率大,即在M点之后,B错误;
C.设 为A、 为 A、
c
A
c
H
c
A
c
OH
为 A,则有K , K ,由于M点微粒不带电(或净电
a cA b c A
c
A
c
H
荷为零),故c A c A,故 K a cA c
H
c2 H
,所以
K c
A
c
OH
c
OH
K
b w
cA
1
pH pK pK pK 3.65,C 正确;
2 a w b
D.4—氨基苯甲酸在M点两侧分别形成铵盐和羧酸盐,溶解度较大;M点处于
分子形态(或净电荷为零),极性最小,在水中溶解度最小,D 错误;
故选C。
二、非选择题(本大题共4小题,共60分)
11(. 16分)铟(In)被广泛应用于电子、太阳能等领域。以某炼锌废渣(主要含ZnO、
In O ,还含少量SnO 、PbO、SiO 等物质)为原料,制备粗铟的工艺流程如下:
2 3 2 2
已知:①Sn(锡)是第IVA族元素;
②H A 和 煤 油 为 萃 取 剂 , 萃 取 In3+ 原 理 为 : In3+( 水 相 )+3H A ( 有 机
2 2 2 2
相) InA ·3HA(有机相)+3H+(水相)
3
(1)为提高“酸浸”效率,可采取的措施有 (任意写一条),滤渣的主
要成分是 、 。
(2)“反萃取”中,从有机相InA ·3HA中分离铟时,需加入浓度较大的盐酸,从
3
试卷第9页,共17页
{#{QQABTYiUggCIABJAAQgCQwFSCkGQkACCCYoGwBAUsAAAgQFABAA=}#}平衡移动的角度说明其原因 。
(3)“沉铟”中,SnCl 2-转化为SnO2-,SnO2-的VSEPR模型名称是 ,
6 3 3
写出SnCl 2-合转化为SnO2-的离子方程式 。
6 3
(4)“酸溶”后,铟以HInCl 形式存在溶液中,加入足量锌粉可制得粗铟,写出
4
该制得粗铟反应的化学方程式是 。
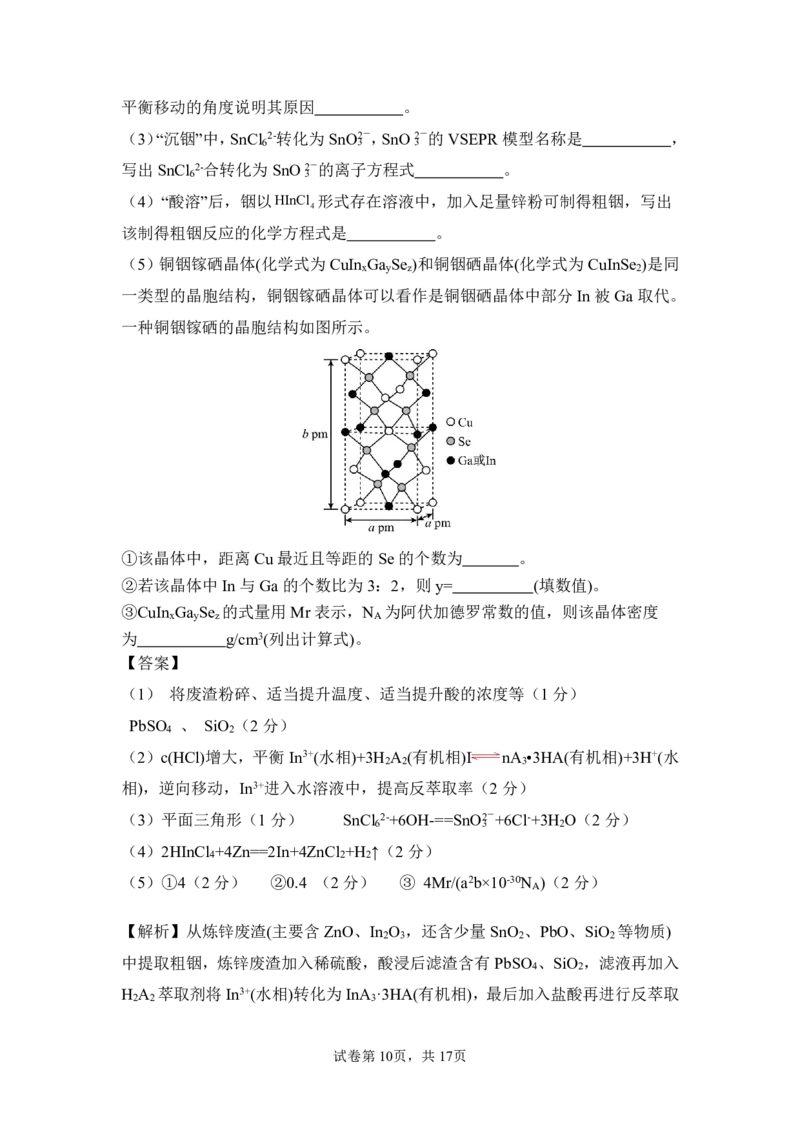
(5)铜铟镓硒晶体(化学式为CuIn Ga Se )和铜铟硒晶体(化学式为CuInSe )是同
x y z 2
一类型的晶胞结构,铜铟镓硒晶体可以看作是铜铟硒晶体中部分In 被Ga 取代。
一种铜铟镓硒的晶胞结构如图所示。
①该晶体中,距离Cu 最近且等距的 Se的个数为 。
②若该晶体中In 与Ga 的个数比为3:2,则y= (填数值)。
③CuIn Ga Se 的式量用Mr表示,N 为阿伏加德罗常数的值,则该晶体密度
x y z A
为 g/cm3(列出计算式)。
【答案】
(1) 将废渣粉碎、适当提升温度、适当提升酸的浓度等(1分)
PbSO 、 SiO (2分)
4 2
(2)c(HCl)增大,平衡In3+(水相)+3H A (有机相)I nA •3HA(有机相)+3H+(水
2 2 3
相),逆向移动,In3+进入水溶液中,提高反萃取率(2分)
(3)平面三角形(1分) SnCl 2-+6OH-==SnO2-+6Cl-+3H O(2分)
6 3 2
(4)2HInCl +4Zn==2In+4ZnCl +H ↑(2分)
4 2 2
(5)①4(2分) ②0.4 (2分) ③ 4Mr/(a2b×10-30N )(2分)
A
【解析】从炼锌废渣(主要含ZnO、In O ,还含少量SnO 、PbO、SiO 等物质)
2 3 2 2
中提取粗铟,炼锌废渣加入稀硫酸,酸浸后滤渣含有PbSO 、SiO ,滤液再加入
4 2
H A 萃取剂将In3+(水相)转化为InA ·3HA(有机相),最后加入盐酸再进行反萃取
2 2 3
试卷第10页,共17页
{#{QQABTYiUggCIABJAAQgCQwFSCkGQkACCCYoGwBAUsAAAgQFABAA=}#}得到含InCl -、SnCl 2-溶液。加烧碱沉铟后,SnCl 2-转化为SnO2-除去,加盐酸“酸
4 6 6 3
溶”后,铟主要以InCl -形式存在溶液中,加入锌粉还原制得粗铟。
4
(1)为提高“酸浸”效率,可采取的措施有将废渣粉碎、适当提升温度、适当提
升酸的浓度等;由分析可知,酸浸后滤渣含有PbSO 、SiO ;
4 2
(2)加入浓度较大的盐酸后,c(HCl)增大,平衡In3+(水相)+3H A (有机
2 2
相)I nA •3HA(有机相)+3H+(水相),逆向移动,In3+进入水溶液中,提高反萃
3
取率。
(3)SnO2-价层电子对个数=3+1/2(4+2-2×3)=3,所以原子杂化方式是sp2,
3
VSEPR为平面三角形结构;SnCl 2-在碱性条件转化为SnO2-的离子方程式为
6 3
SnCl 2-+6OH-==SnO2-+6Cl-+3H O;
6 3 2
(4)铟主要以HInCl 形式存在溶液中,加入锌粉制得粗铟,同时还生成一种具
4
有还原性的气体,发生反应的化学方程式2HInCl +4Zn==2In+4ZnCl +H ↑
4 2 2
(5)①以面心的Cu 为研究对象,与其距离最近的4个Se构成了正四面体,则
Cu 最近且等距的Se的个数为4;②铜铟镓硒晶体可以看作是铜铟硒晶体中部分
In 被Ga 取代,则In 和Ga总个数为1,In 与Ga的个数比为3:2,则y=0.4;晶
胞中Cu 原子个数为8×1/8+4×1/2+1=4,CuIn Ga Se 的式量用Mr表示,则晶胞
x y z
的质量为4Mr/N g,晶胞体积为a2b×10-30cm3,则晶胞密度为 4Mr/(a2b×10-30N )
A A
g/cm3
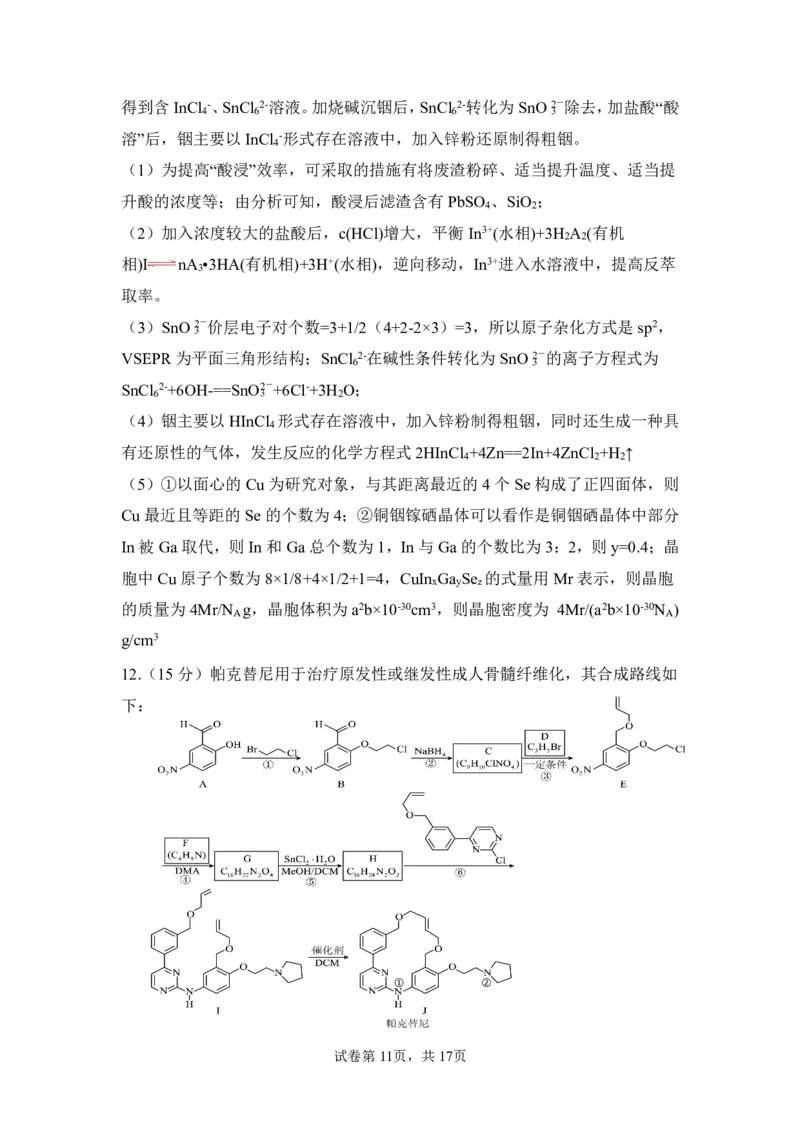
12.(15分)帕克替尼用于治疗原发性或继发性成人骨髓纤维化,其合成路线如
下:
试卷第11页,共17页
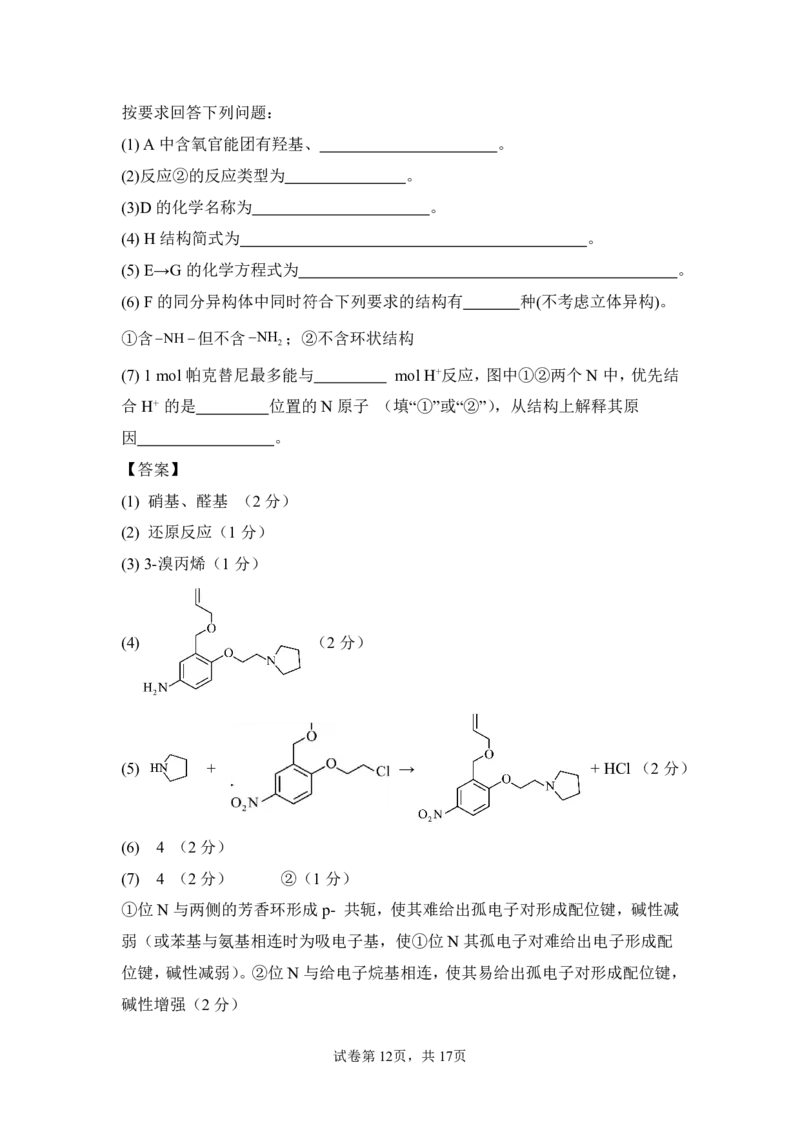
{#{QQABTYiUggCIABJAAQgCQwFSCkGQkACCCYoGwBAUsAAAgQFABAA=}#}按要求回答下列问题:
(1)A中含氧官能团有羟基、 。
(2)反应②的反应类型为 。
(3)D 的化学名称为 。
(4)H 结构简式为 。
(5)E→G 的化学方程式为 。
(6)F 的同分异构体中同时符合下列要求的结构有 种(不考虑立体异构)。
①含NH但不含NH ;②不含环状结构
2
(7)1mol 帕克替尼最多能与 molH+反应,图中①②两个N 中,优先结
合H+ 的是 位置的N原子 (填“①”或“②”),从结构上解释其原
因 。
【答案】
(1) 硝基、醛基 (2分)
(2) 还原反应(1分)
(3)3-溴丙烯(1分)
(4) (2分)
(5) + → + HCl (2分)
(6) 4 (2分)
(7) 4 (2分) ②(1分)
①位N与两侧的芳香环形成p- 共轭,使其难给出孤电子对形成配位键,碱性减
弱(或苯基与氨基相连时为吸电子基,使①位N其孤电子对难给出电子形成配
位键,碱性减弱)。②位N与给电子烷基相连,使其易给出孤电子对形成配位键,
碱性增强(2分)
试卷第12页,共17页
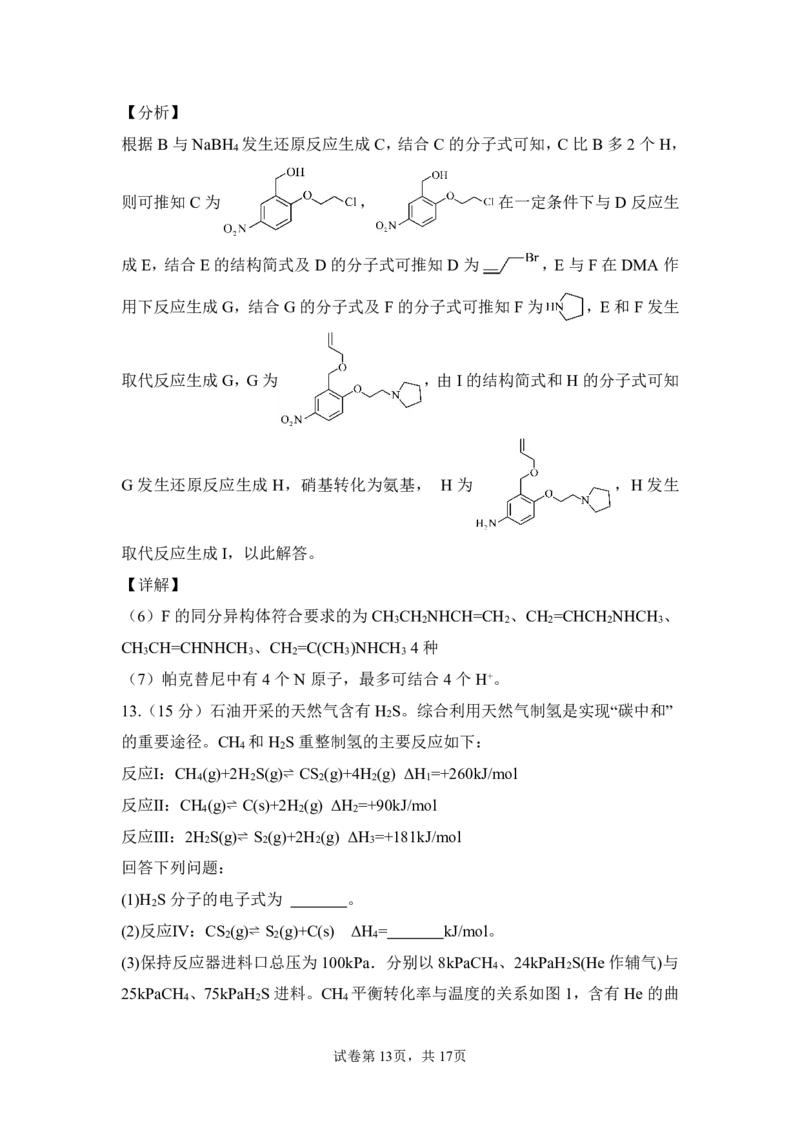
{#{QQABTYiUggCIABJAAQgCQwFSCkGQkACCCYoGwBAUsAAAgQFABAA=}#}【分析】
根据B 与NaBH 发生还原反应生成C,结合C 的分子式可知,C 比B多2个H,
4
则可推知C 为 , 在一定条件下与D 反应生
成E,结合E的结构简式及D的分子式可推知D 为 ,E 与F在DMA 作
用下反应生成G,结合G的分子式及F 的分子式可推知F为 ,E 和F 发生
取代反应生成G,G 为 ,由I的结构简式和H 的分子式可知
G 发生还原反应生成 H,硝基转化为氨基, H 为 ,H 发生
取代反应生成I,以此解答。
【详解】
(6)F的同分异构体符合要求的为CH CH NHCH=CH 、CH =CHCH NHCH 、
3 2 2 2 2 3
CH CH=CHNHCH 、CH =C(CH )NHCH 4种
3 3 2 3 3
(7)帕克替尼中有4个N原子,最多可结合4个H+。
13.(15分)石油开采的天然气含有H S。综合利用天然气制氢是实现“碳中和”
2
的重要途径。CH 和H S重整制氢的主要反应如下:
4 2
反应Ⅰ:CH (g)+2H S(g)⇌ CS (g)+4H (g) ΔH =+260kJ/mol
4 2 2 2 1
反应Ⅱ:CH (g)⇌ C(s)+2H (g) ΔH =+90kJ/mol
4 2 2
反应Ⅲ:2H S(g)⇌ S (g)+2H (g) ΔH =+181kJ/mol
2 2 2 3
回答下列问题:
(1)H S 分子的电子式为 。
2
(2)反应Ⅳ:CS (g)⇌ S (g)+C(s)ㅤΔH = kJ/mol。
2 2 4
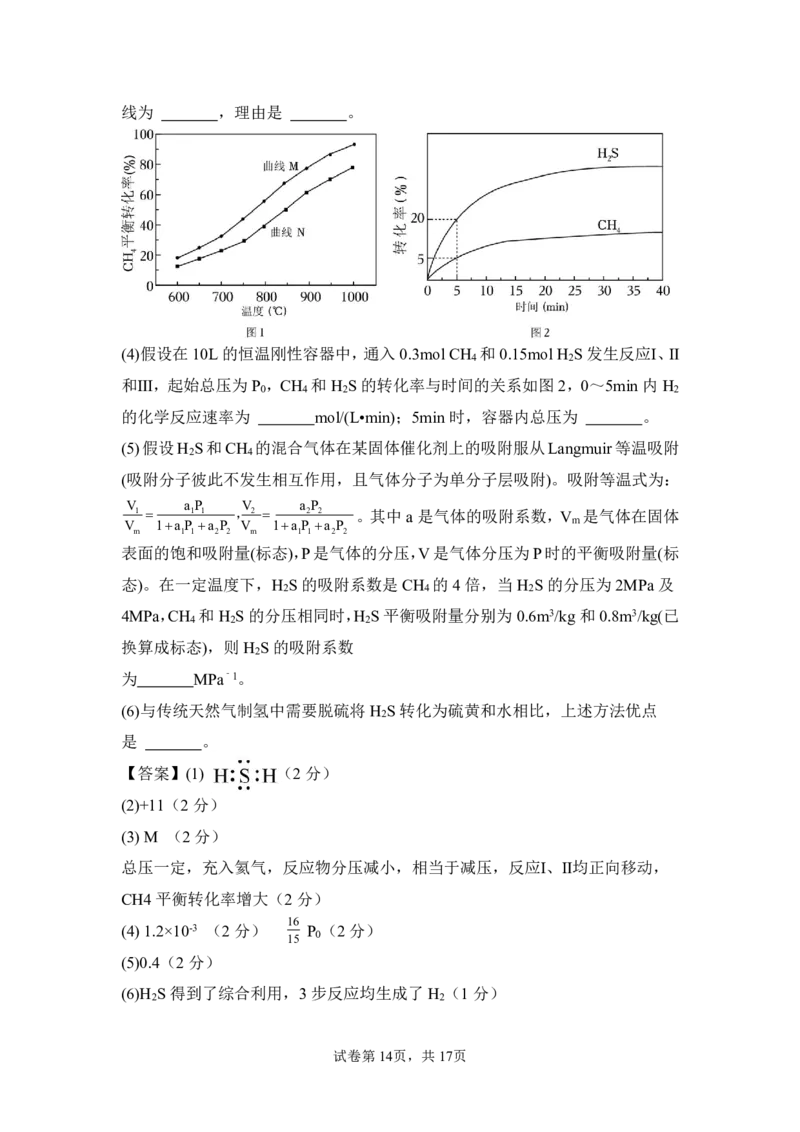
(3)保持反应器进料口总压为100kPa.分别以8kPaCH 、24kPaH S(He作辅气)与
4 2
25kPaCH 、75kPaH S 进料。CH 平衡转化率与温度的关系如图1,含有He 的曲
4 2 4
试卷第13页,共17页
{#{QQABTYiUggCIABJAAQgCQwFSCkGQkACCCYoGwBAUsAAAgQFABAA=}#}线为 ,理由是 。
(4)假设在10L 的恒温刚性容器中,通入0.3mol CH 和0.15mol H S 发生反应Ⅰ、Ⅱ
4 2
和Ⅲ,起始总压为P ,CH 和H S 的转化率与时间的关系如图2,0~5min 内H
0 4 2 2
的化学反应速率为 mol/(L•min);5min 时,容器内总压为 。
(5)假设H S和CH 的混合气体在某固体催化剂上的吸附服从Langmuir等温吸附
2 4
(吸附分子彼此不发生相互作用,且气体分子为单分子层吸附)。吸附等温式为:
V a P V a P
1 1 1 ,2 2 2 。其中a是气体的吸附系数,V 是气体在固体
V 1a P a P V 1a P a P m
m 1 1 2 2 m 1 1 2 2
表面的饱和吸附量(标态),P是气体的分压,V是气体分压为P时的平衡吸附量(标
态)。在一定温度下,H S 的吸附系数是CH 的4倍,当H S 的分压为2MPa及
2 4 2
4MPa,CH 和H S 的分压相同时,H S 平衡吸附量分别为0.6m3/kg 和0.8m3/kg(已
4 2 2
换算成标态),则H S 的吸附系数
2
为 MPa﹣1。
(6)与传统天然气制氢中需要脱硫将H S 转化为硫黄和水相比,上述方法优点
2
是 。
【答案】(1) (2分)
(2)+11(2分)
(3)M (2分)
总压一定,充入氦气,反应物分压减小,相当于减压,反应Ⅰ、Ⅱ均正向移动,
CH4 平衡转化率增大(2分)
16
(4)1.2×10-3 (2分) P (2分)
15 0
(5)0.4(2分)
(6)H S 得到了综合利用,3步反应均生成了H (1分)
2 2
试卷第14页,共17页
{#{QQABTYiUggCIABJAAQgCQwFSCkGQkACCCYoGwBAUsAAAgQFABAA=}#}【详解】(1)H S 为共价化合物,其电子式为 ;
2
(2)根据盖斯定律可知,反应Ⅱ+Ⅲ﹣Ⅰ=Ⅳ,则CS (g)⇌ S (g)+C(s)ㅤΔH =
2 2 4
ΔH +ΔH ﹣ΔH =(90+181-260)kJ/mol=+11kJ/mol;
2 3 1
(3)保持反应器进料口总压为100kPa。分别以8kPaCH 、24kPaH S(He 作辅
4 2
气)与25kPaCH 、75kPaH S 进料。CH 平衡转化率与温度的关系如图1,含有
4 2 4
He的曲线为M,理由是总压一定,充入氦气,反应物分压减小,相当于减压,
反应Ⅰ、Ⅱ均正向移动,CH 平衡转化率增大
4
(4)由图可知,0~5min内消耗的CH 为0.3mol×5%=0.015mol,消耗的H S
4 2
为0.15mol×20%=0.03mol,根据氢原子守恒,则生成H 的物质的量为n(H )=
2 2
2×0.015mol+0.03=0.06mol,0~5min内H 的化学反应速率为
2
0.06mol
v(H 2 ) 10L 1.2×10-3mol/(L•min);
5min
设反应Ⅰ转化了xmolCH ,则反应Ⅱ转化了(0.015-x)molCH ,反应Ⅰ转化了
4 4
2xmolH S,反应Ⅲ转化了(0.03-2x)molH S,列三段式有
2 2
CH g + 2H Sg CS g + 4H g
4 2 2 2
初始mol 0.3 0.15 0 0
变化mol x 2x x
平衡mol x
CH g Cs 2H g
4 2
初始mol 0.3
变化mol 0.015x 0.015x
平衡mol
2H Sg S g 2H g
2 2 2
初始mol 0.15 0
,5min 时,n(CH )=0.285mol,
变化mol 0.032x 0.015x 4
平衡mol 0.015 x
n(H S)=0.12mol,n(H )=0.06mol,n(CS )=xmol,n(S )=(0.015-x)mol,n(总)=0.48mol,
2 2 2 2
起始总压为P ,气体总量为0.45mol,根据压强之比等于物质的量之比,可得5min
0
0.48 16
时,容器内总压为 ×P = P ;
0 0
0.45 15
0.6m3/kg α 2MPa
1
(5)根据题意可知方程:① V 1 ,
m 1α 2MPa α 2MPa
1 4 1
0.8m3/kg α 4MPa
1
② V m 1α 4MPa 1 α 4MPa ,联立方程①与②,解得:α 1 =0.4MPa﹣1;
1 4 1
试卷第15页,共17页
{#{QQABTYiUggCIABJAAQgCQwFSCkGQkACCCYoGwBAUsAAAgQFABAA=}#}(6)与传统天然气制氢中需要脱硫将H S 转化为硫黄和水相比,上述方法优点
2
是H S 得到了综合利用,3步反应均生成了H 。
2 2
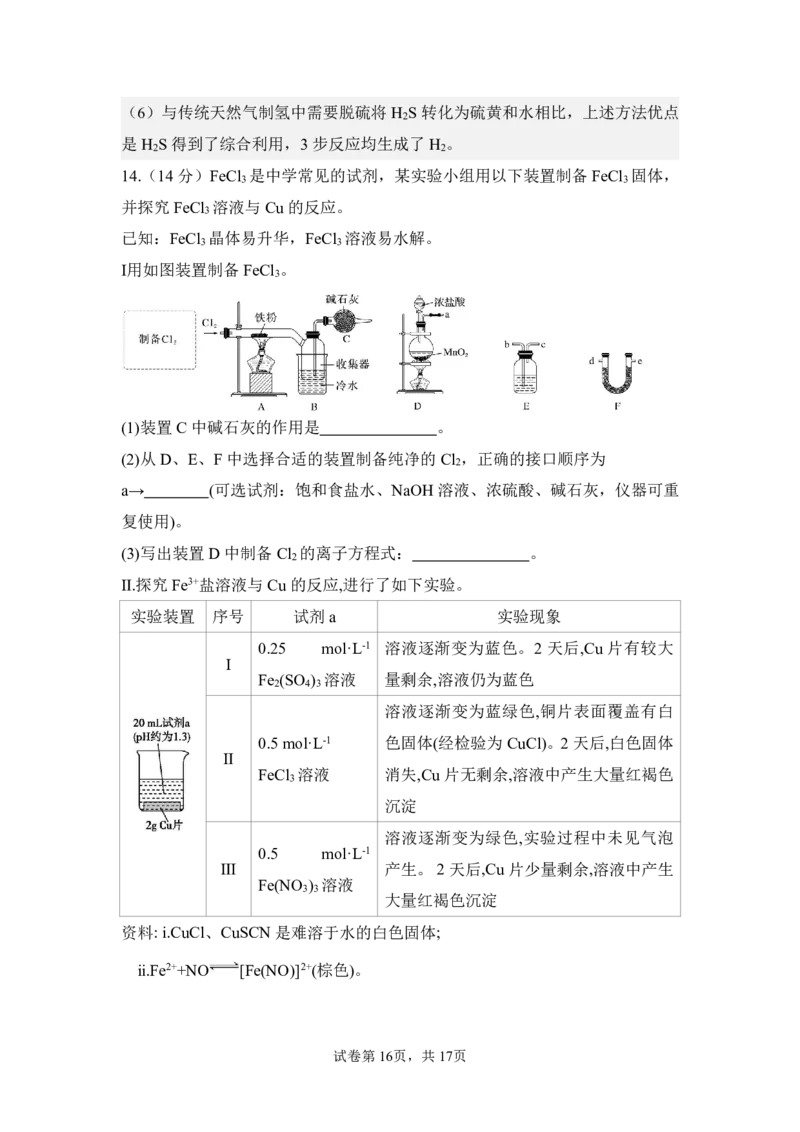
14.(14分)FeCl 是中学常见的试剂,某实验小组用以下装置制备FeCl 固体,
3 3
并探究FeCl 溶液与Cu 的反应。
3
已知:FeCl 晶体易升华,FeCl 溶液易水解。
3 3
Ⅰ用如图装置制备FeCl 。
3
(1)装置C 中碱石灰的作用是 。
(2)从D、E、F中选择合适的装置制备纯净的Cl ,正确的接口顺序为
2
a→ (可选试剂:饱和食盐水、NaOH 溶液、浓硫酸、碱石灰,仪器可重
复使用)。
(3)写出装置D 中制备Cl 的离子方程式: 。
2
Ⅱ.探究Fe3+盐溶液与Cu 的反应,进行了如下实验。
实验装置 序号 试剂a 实验现象
0.25 mol·L-1 溶液逐渐变为蓝色。2 天后,Cu 片有较大
Ⅰ
Fe (SO ) 溶液 量剩余,溶液仍为蓝色
2 4 3
溶液逐渐变为蓝绿色,铜片表面覆盖有白
0.5mol·L-1 色固体(经检验为CuCl)。2天后,白色固体
Ⅱ
FeCl 溶液 消失,Cu片无剩余,溶液中产生大量红褐色
3
沉淀
溶液逐渐变为绿色,实验过程中未见气泡
0.5 mol·L-1
Ⅲ 产生。2天后,Cu 片少量剩余,溶液中产生
Fe(NO ) 溶液
3 3
大量红褐色沉淀
资料:ⅰ.CuCl、CuSCN是难溶于水的白色固体;
ⅱ.Fe2++NO [Fe(NO)]2+(棕色)。
试卷第16页,共17页
{#{QQABTYiUggCIABJAAQgCQwFSCkGQkACCCYoGwBAUsAAAgQFABAA=}#}(4)小组同学取2mL实验Ⅰ中反应2天后的溶液于试管中,加入2滴1mol·L-1 KSCN
溶液,观察到溶液迅速变红,产生大量白色沉淀。
甲同学猜想Fe2+可能在该条件下被Cu2+氧化了。
①用离子方程式表示甲同学的猜想: 。
②若向100mLa mol·L¹CuSO₄溶液中滴加足量的KSCN和FeCl₂ 的混合溶液,
经过一系列操作得到白色沉淀 CuSCN的质量 bg, 则CuSCN 的产率为 。
(5)对比实验Ⅰ和实验Ⅱ,小组同学推测 Cl-可以催化 Fe3+与 Cu 反应。其理由
是 。
(6)实验Ⅲ所得溶液的颜色不是蓝色,小组同学猜测反应中生成了[Fe(NO)]2+,设计
并实施了以下实验,验证了其猜想。
步骤 实验操作 实验现象
向盛有 2 g 金属 Cu 片的烧杯中 2 天后溶液颜色无明显变化,铜片表面
①
加入试剂X 有细小气泡附着
② 继续加入少量FeSO 固体 溶液迅速变为浅棕色
4
试剂X是 。
综合以上实验,Fe3+盐溶液与Cu反应的多样性与阴离子种类、生成物存在形式等
有关。
【答案】
(1)吸收多余的Cl ,用于尾气处理,同时可以防止空气中的水蒸气进入收集器中,
2
防止FeCl 水解变质 (2 分)
3
(2) b→c→b→c (2分)
(3)MnO +4H++2Cl- Mn2++Cl ↑+2H O(2 分)
2 2 2
(4)①Fe2++Cu2++SCN- Fe3++CuSCN↓(2 分)
② (2 分)
(5) 产 生 白 色 固 体 :Cu+Fe3++Cl- CuCl+Fe2+; 白 色 固 体 消
失:CuCl+Fe3+ Fe2++Cu2++Cl-;总反应:2Fe3++Cu Cu2++2Fe2+。从现象上看,实验
Ⅱ反应更快,Cl-起催化作用(2 分)
(6)20 mLNaNO 与HNO 的混合溶液[pH约为1.3、c(N )=1.5 mol·L-1](2 分)
3 3
-
O3
试卷第17页,共17页
{#{QQABTYiUggCIABJAAQgCQwFSCkGQkACCCYoGwBAUsAAAgQFABAA=}#}