文档内容
2023 年高考考前押题密卷(山东卷)
化 学
本卷满分100分,考试时间90分钟。
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 P 31 S 32 K 39
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.山东历史悠久,文化底蕴深厚,是中华文明的发祥地之一。下列有关叙述正确的是
A.图甲文物玉璧的主要成分是CaCO
3
B.图乙文物表面的绿色物质可用饱和NH Cl溶液除去
4
C.图丙中演员挥舞的丝绸主要成分为纤维素
D.图丁中山东剪纸的材料遇水迅速水解
2.拟在实验室完成一系列实验:①粗盐提纯;②利用提纯后的NaCl模拟“侯氏制碱法”制备纯碱;③用
盐酸标准液滴定纯碱溶液以测定NaCO 含量。在实验过程中,下列仪器不可能用到的是
2 3
A. B. C. D.
3.下列说法正确的是
A.二氧化硫气体能用浓硫酸干燥,是因为二氧化硫无还原性
B.由于四水合铜离子
CuH 2 O 4
2
为蓝色,则铜盐溶液均为蓝色
C.可向食盐溶液中滴加淀粉溶液,观察是否变蓝,判断食盐中是否加碘
D.植物油中含有碳碳双键,具有还原性,能使酸性高锰酸钾溶液褪色
4.铁铝铅榴石主要成分为Fe Al Pb SiO ,其组成也可写成的氧化物形式:Fe O Al O 3PbO5SiO 。
3 2 3 4 5 3 x 2 3 2
学科网(北京)股份有限公司下列说法正确的是
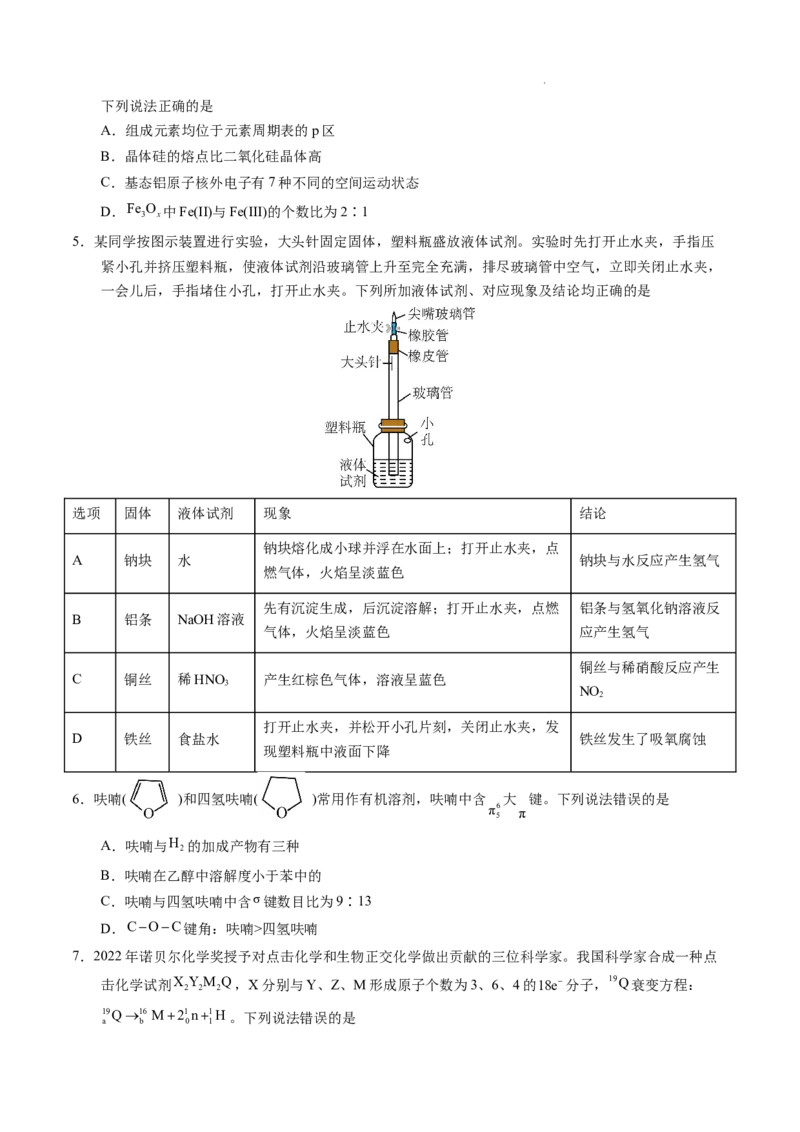
A.组成元素均位于元素周期表的p区
B.晶体硅的熔点比二氧化硅晶体高
C.基态铝原子核外电子有7种不同的空间运动状态
D.Fe O 中Fe(II)与Fe(III)的个数比为2∶1
3 x
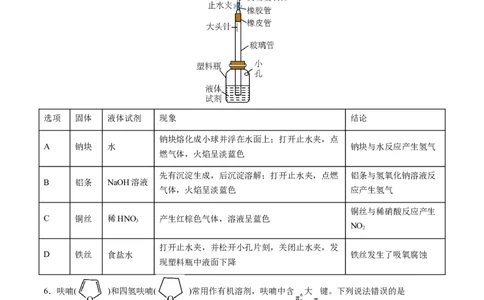
5.某同学按图示装置进行实验,大头针固定固体,塑料瓶盛放液体试剂。实验时先打开止水夹,手指压
紧小孔并挤压塑料瓶,使液体试剂沿玻璃管上升至完全充满,排尽玻璃管中空气,立即关闭止水夹,
一会儿后,手指堵住小孔,打开止水夹。下列所加液体试剂、对应现象及结论均正确的是
选项 固体 液体试剂 现象 结论
钠块熔化成小球并浮在水面上;打开止水夹,点
A 钠块 水 钠块与水反应产生氢气
燃气体,火焰呈淡蓝色
先有沉淀生成,后沉淀溶解;打开止水夹,点燃 铝条与氢氧化钠溶液反
B 铝条 NaOH溶液
气体,火焰呈淡蓝色 应产生氢气
铜丝与稀硝酸反应产生
C 铜丝 稀HNO 产生红棕色气体,溶液呈蓝色
3
NO
2
打开止水夹,并松开小孔片刻,关闭止水夹,发
D 铁丝 食盐水 铁丝发生了吸氧腐蚀
现塑料瓶中液面下降
6.呋喃( )和四氢呋喃( )常用作有机溶剂,呋喃中含 大 键。下列说法错误的是
π6 π
5
A.呋喃与H 的加成产物有三种
2
B.呋喃在乙醇中溶解度小于苯中的
C.呋喃与四氢呋喃中含σ键数目比为9∶13
D.COC键角:呋喃>四氢呋喃
7.2022年诺贝尔化学奖授予对点击化学和生物正交化学做出贡献的三位科学家。我国科学家合成一种点
击化学试剂X YM Q,X分别与Y、Z、M形成原子个数为3、6、4的18e分子,19Q衰变方程:
2 2 2
19Q16 M21n1H。下列说法错误的是
a b 0 1
学科网(北京)股份有限公司A.X的简单离子半径一定是周期表中最小的
B.
16M
和
18M
组成上属于同一种物质
2 2
C.同一周期中,第一电离能小于Z的有5种元素
D.Y、M形成简单氢化物的还原性:YM
8.某学校实验探究小组利用碎铜屑和浓硫酸制备CuSO ·5H O大晶体,实验步骤如下:
4 2
i.将过量铜屑加入一定量浓硫酸中,加热,生成的气体通入到浓碱液中;
ii.在反应混合体系中加入稍过量的CuO,过滤,除去虑渣:
iii.将虑液蒸发至饱和溶液状态,冷却,在饱和溶液中悬挂晶种,静置24小时。
下列说法错误的是
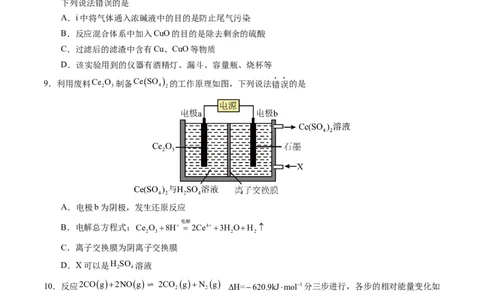
A.i中将气体通入浓碱液中的目的是防止尾气污染
B.反应混合体系中加入CuO的目的是除去剩余的硫酸
C.过滤后的滤渣中含有Cu、CuO等物质
D.该实验用到的仪器有酒精灯、漏斗、容量瓶、烧杯等
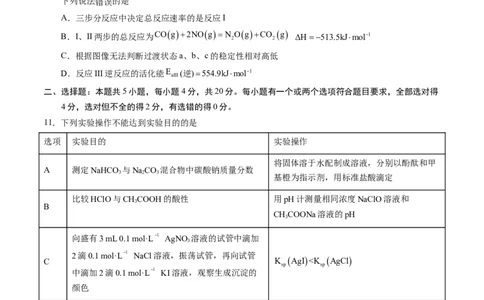
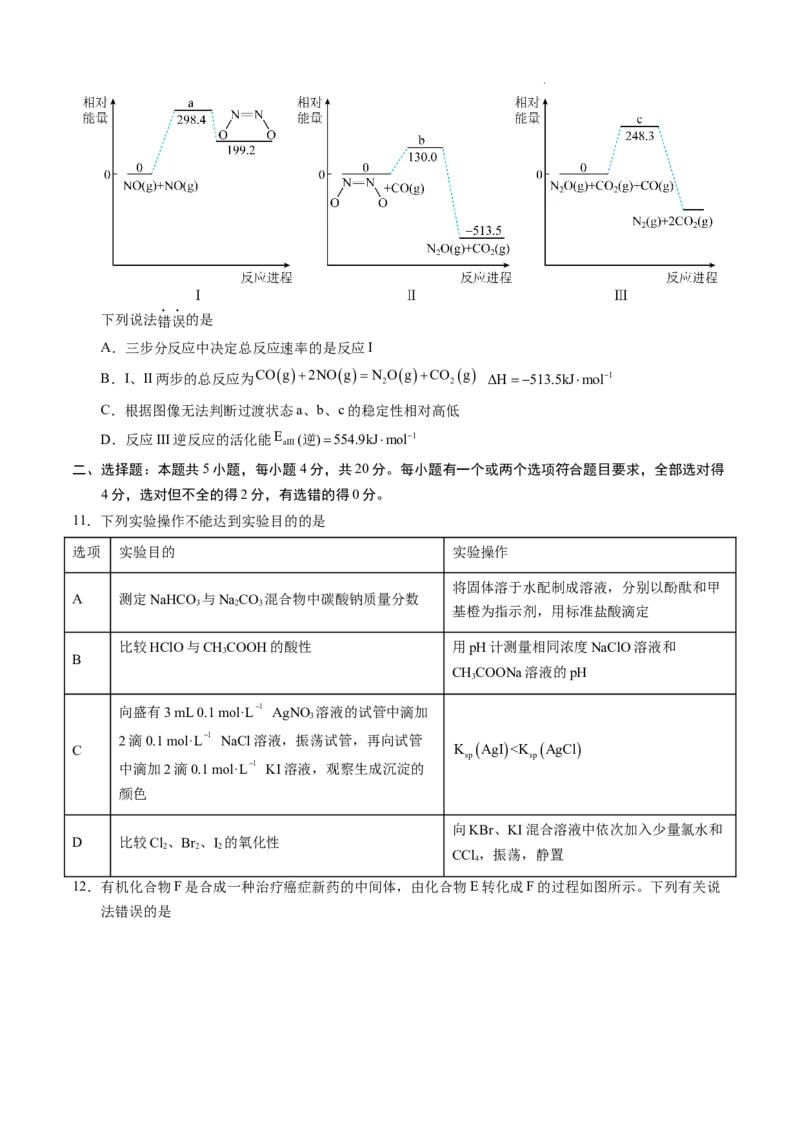
9.利用废料Ce
2
O
3
制备CeSO
4
2
的工作原理如图,下列说法错误的是
A.电极b为阴极,发生还原反应
电解
B.电解总方程式:Ce O 8H 2Ce43H OH
2 3 2 2
C.离子交换膜为阴离子交换膜
D.X可以是H SO 溶液
2 4
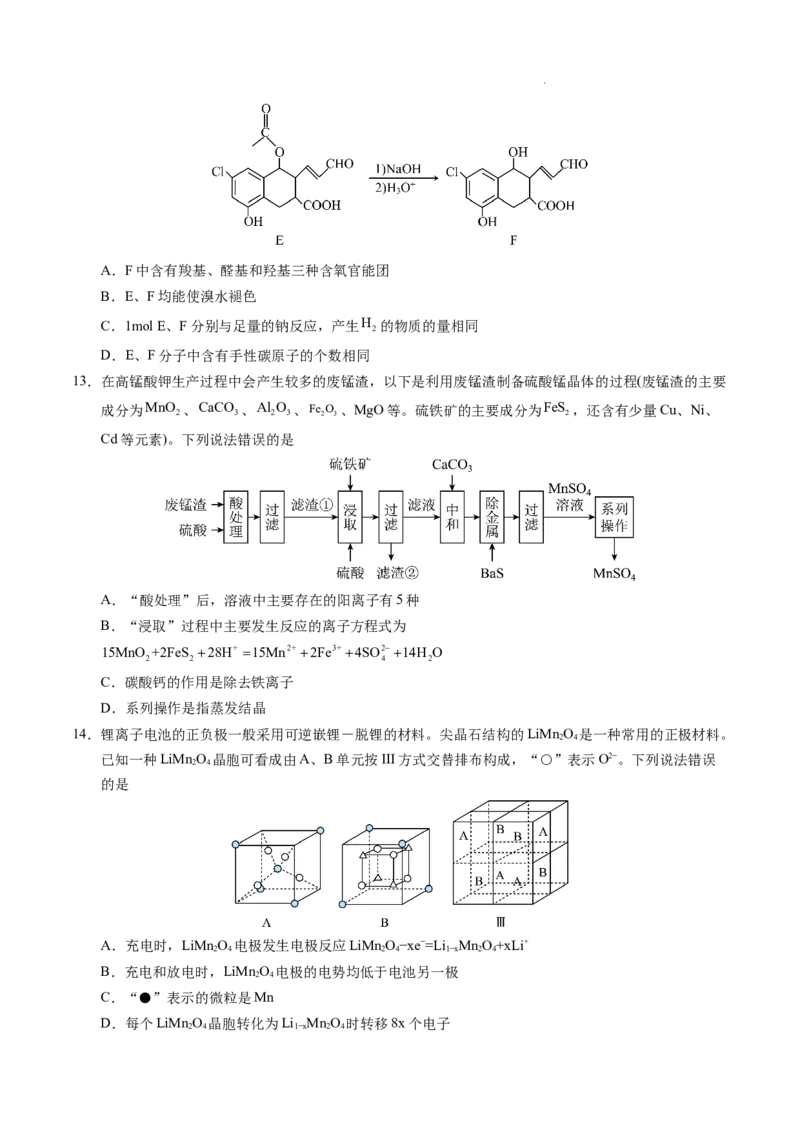
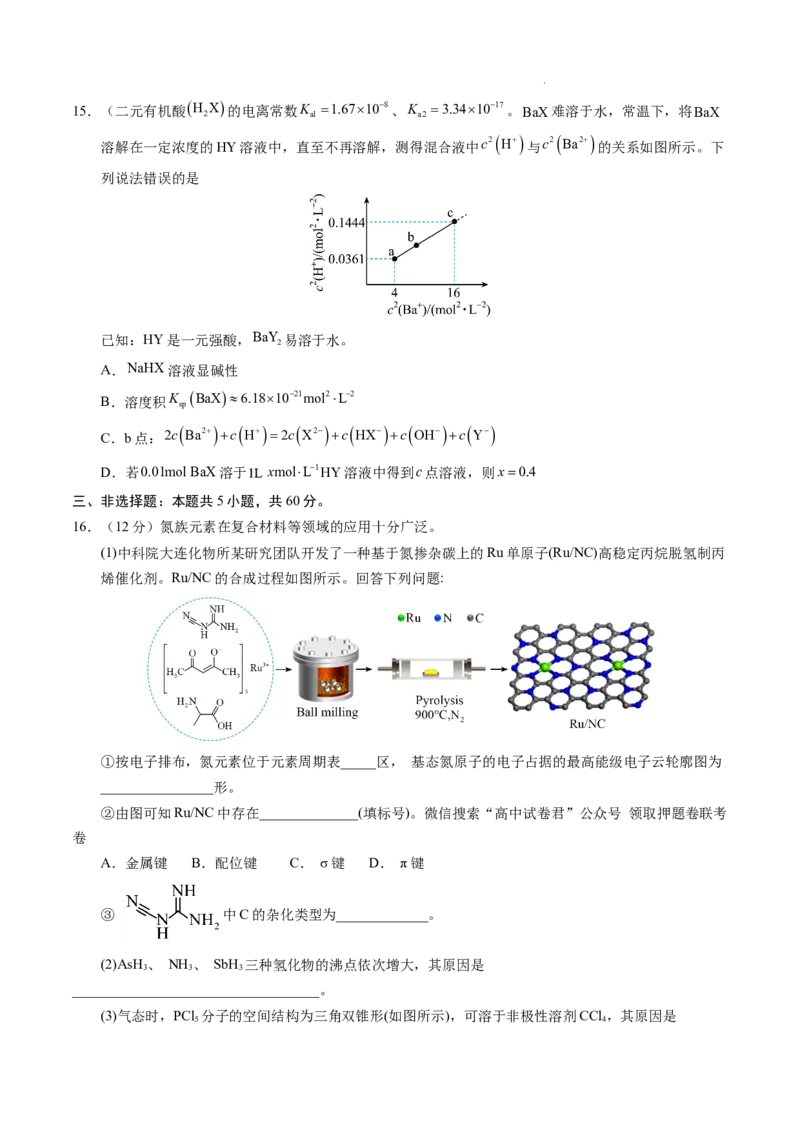
10.反应2COg2NOg 2CO
2
gN
2
g ΔH=620.9kJmol1分三步进行,各步的相对能量变化如
图I、II、III所示:
学科网(北京)股份有限公司下列说法错误的是
A.三步分反应中决定总反应速率的是反应I
B.I、II两步的总反应为COg2NOgN
2
OgCO
2
g
ΔH513.5kJmol1
C.根据图像无法判断过渡状态a、b、c的稳定性相对高低
D.反应III逆反应的活化能E (逆)554.9kJmol1
aIII
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得
4分,选对但不全的得2分,有选错的得0分。
11.下列实验操作不能达到实验目的的是
选项 实验目的 实验操作
将固体溶于水配制成溶液,分别以酚酞和甲
A 测定NaHCO 与NaCO 混合物中碳酸钠质量分数
3 2 3
基橙为指示剂,用标准盐酸滴定
比较HClO与CHCOOH的酸性 用pH计测量相同浓度NaClO溶液和
3
B
CHCOONa溶液的pH
3
向盛有3 mL 0.1 mol·L1 AgNO 溶液的试管中滴加
3
2滴0.1 mol·L1 NaCl溶液,振荡试管,再向试管
C K AgI ”或“=”)0。
a a
(2)总压恒定为100 kPa,向密闭容器中充入2 mol H S、3 mol O 、95 mol Ar,发生反应i和反应ii ,
2 2
反应过程中HS(g) ,SO (g)、S(g)等含硫物质的分布分数δ随时间变化如图所示。
2 2 2
学科网(北京)股份有限公司①表示SO 分布分数的曲线为___________(填“甲”“乙”或“丙”)。
2
②t 时测得HS转化率为α,此时体系中HO的物质的量为___________mol;用HS分压表示的平均
1 2 2 2
反应速率为___________(用含α、t 的式子表示)kPa· s−1。
1
(3)也可采用NaSO 氧化法对HS进行处理,过程中发生反应的方程式(均未配平)为:
2 3 2
i. SO2- +H S+H+ →S O2 +S↓+ H O
3 2 2 3 2
ii. HS(aq)+ SO2- (aq)+H+ (aq)→S(s) + H O(l)
2 3 2
iii.S(s) +SO2- (aq)→S O2 (aq)
3 2 3
实验测得,在T℃、pH=5时,NaSO 的投加量对平衡体系中部分微粒浓度的影响如图所示。
2 3
①T℃时,反应iii的平衡常数K=___________。
②结合三个反应分析,当NaSO 投加量高于5 g·L−1时,单位体积内S的质量减小的原因为
2 3
___________。
学科网(北京)股份有限公司学科网(北京)股份有限公司