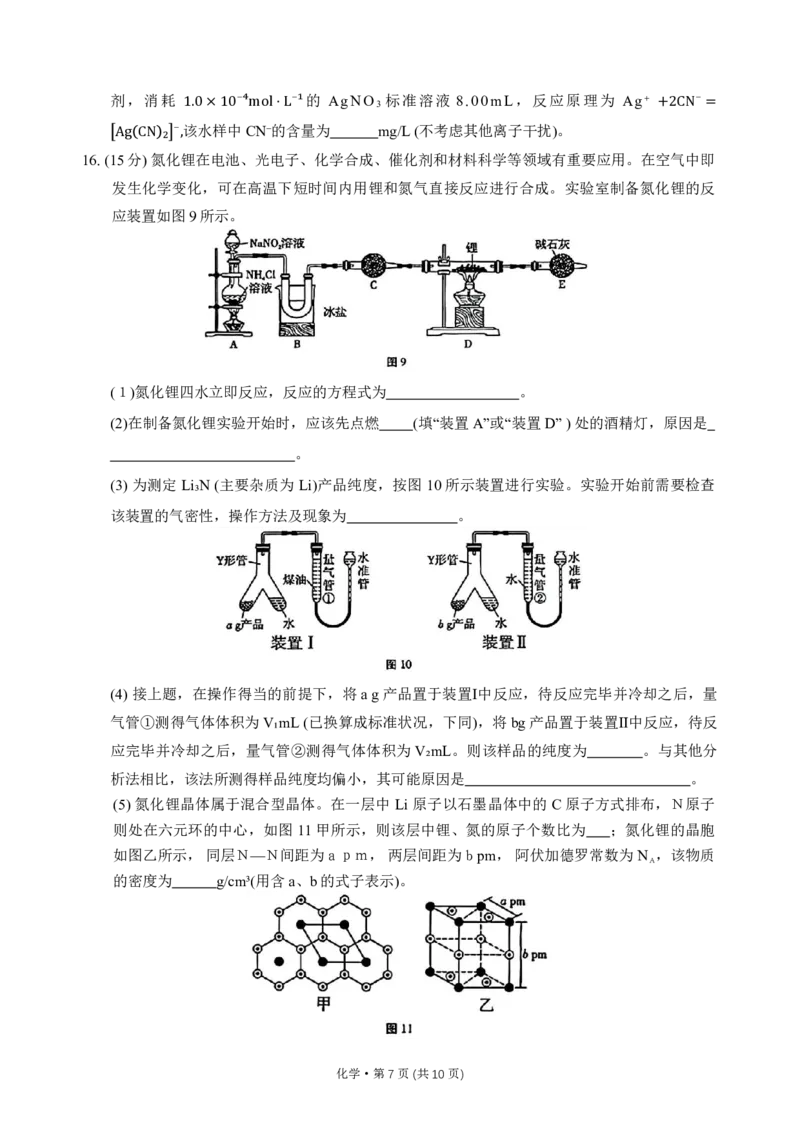
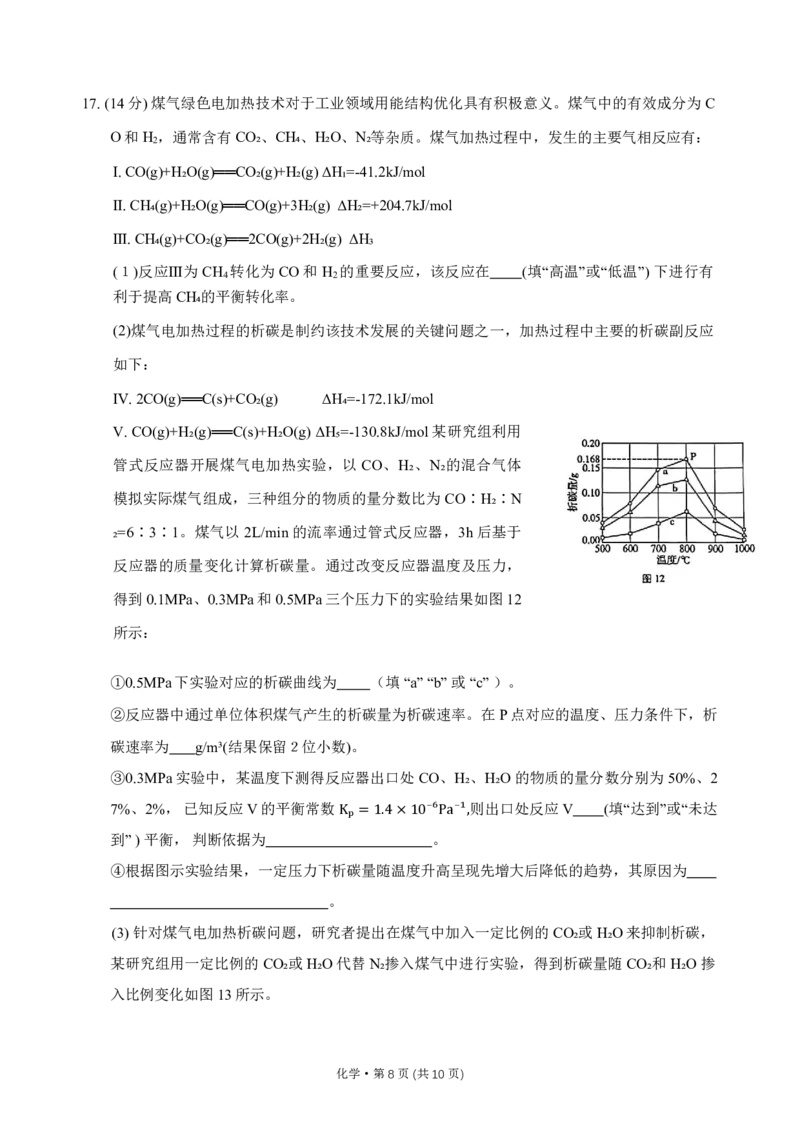
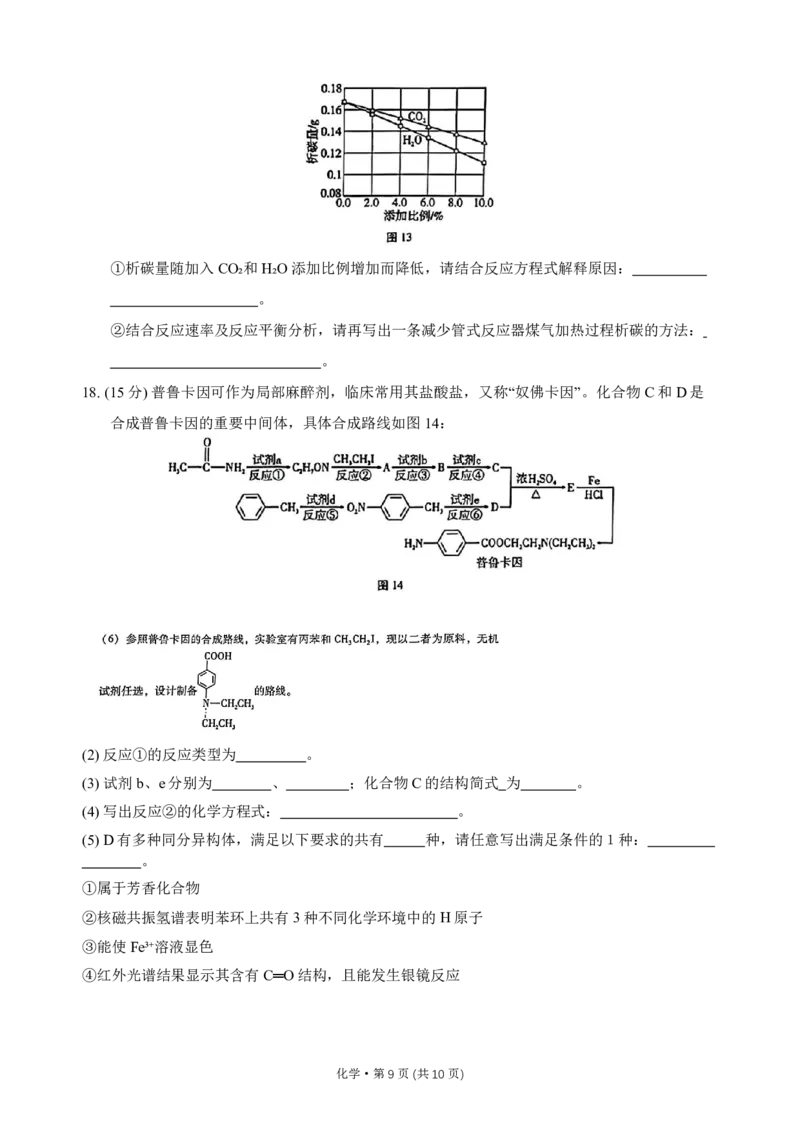
文档内容
巴蜀中学 届高考适应性月考卷 三
2024 ( )
化 学
注意事项:
1.答题前,考生务必用黑色碳素笔将自己的姓名、准考证号、考场号、座位号在答题卡上填写清
楚。
2.每小题选出答案后,用2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净
后,再选涂其他答案标号。在试题卷上作答无效。
3.考试结束后,请将本试卷和答题卡一并交回。满分100分,考试用时75分钟。
以下数据可供解题时参考。
可能用到的相对原子质量:H—1 Li—7 C—12 N—14 0—16 Cu—64
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.化学知识与科技、生产、生活有密切的关系。下列叙述错误的是
A.硬化油可作为制造肥皂和人造奶油的原料
B.可用含增塑剂的聚氯乙烯薄膜生产食品包装材料
C.利用秸秆为原料生产燃料乙醇,具有成本低,来源广等优点
D.使用酒精、紫外线杀菌消毒与蛋白质变性有关
2.下列化学用语或化学图谱不正确的是
A.CCl₄的电子式:
B.甲酸的结构式:
C.C₂H₂的空间填充模型:
D.乙醇的核磁共振氢谱:
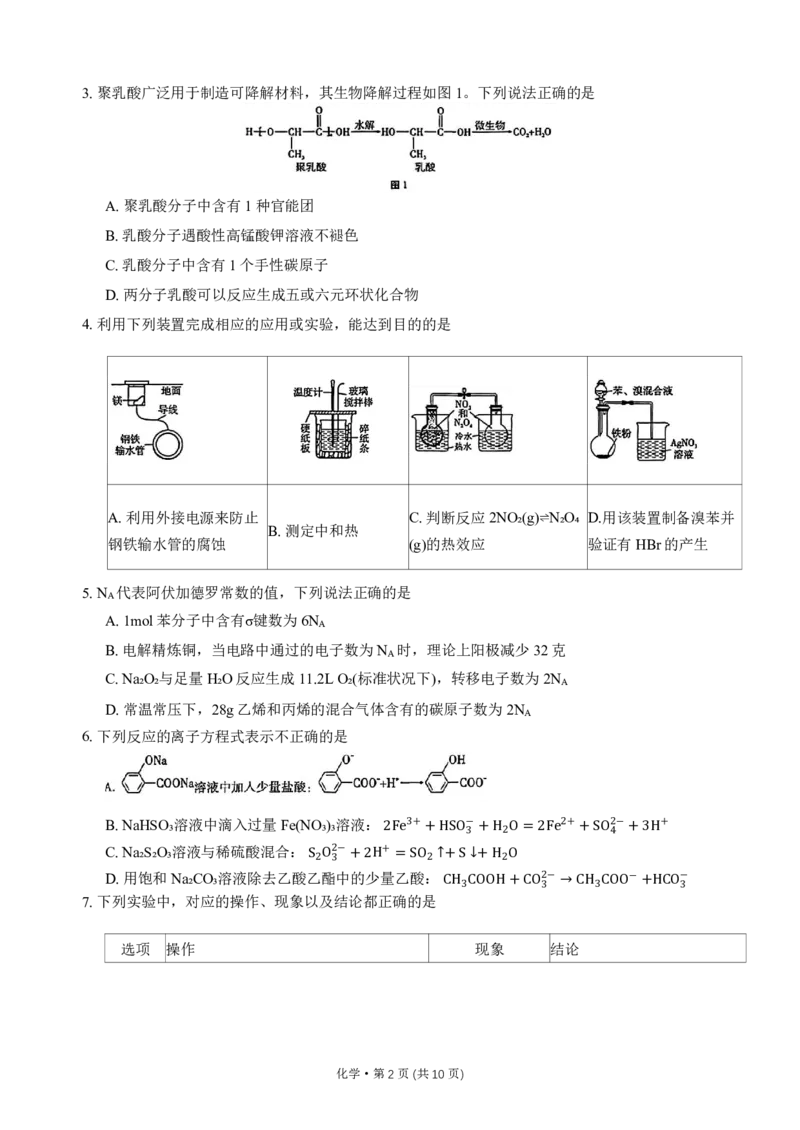
化学·第1页(共10页)3.聚乳酸广泛用于制造可降解材料,其生物降解过程如图1。下列说法正确的是
A.聚乳酸分子中含有1种官能团
B.乳酸分子遇酸性高锰酸钾溶液不褪色
C.乳酸分子中含有1个手性碳原子
D.两分子乳酸可以反应生成五或六元环状化合物
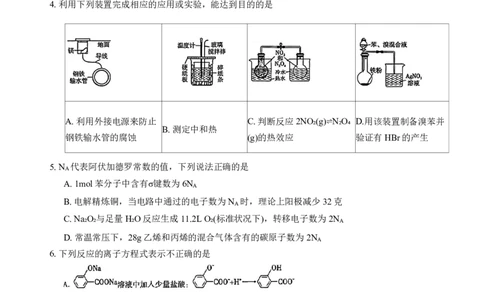
4.利用下列装置完成相应的应用或实验,能达到目的的是
A.利用外接电源来防止 C.判断反应2NO₂(g)⇌N₂O₄ D.用该装置制备溴苯并
B.测定中和热
钢铁输水管的腐蚀 (g)的热效应 验证有HBr的产生
5.N 代表阿伏加德罗常数的值,下列说法正确的是
A
A.1mol苯分子中含有σ键数为6N
A
B.电解精炼铜,当电路中通过的电子数为N 时,理论上阳极减少32克
A
C.Na₂O₂与足量H₂O反应生成11.2LO₂(标准状况下),转移电子数为2N
A
D.常温常压下,28g乙烯和丙烯的混合气体含有的碳原子数为2N
A
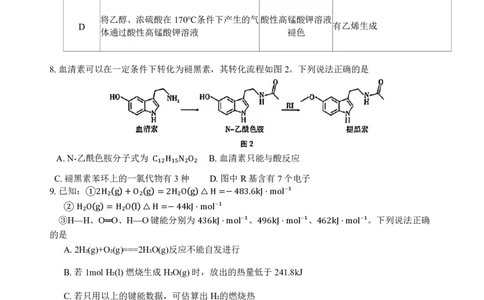
6.下列反应的离子方程式表示不正确的是
B.NaHSO₃溶液中滴入过量Fe(NO₃)₃溶液:
C.Na₂S₂O₃溶液与稀硫酸混合:
2Fe
3+
+HSO3
−
+H2O= 2Fe
2+
+SO4
2−
+3H
+
D.用饱和Na₂CO₃溶液除去乙酸乙
S2
酯
O3
2 中 −
+
的
2
少
H
量+
=
乙
S
酸
O
:
2 ↑+S ↓+H2O
7.下列实验中,对应的操作、现象以及结论都正确的是 2− − −
CH3COOH+CO3 →CH3COO +HCO3
选项 操作 现象 结论
化学·第2页(共10页)将镀层破坏的镀锌铁片放入酸化的3%Na
铁未被腐蚀,已破损的镀层锌
A Cl溶液中,一段时间后,取 溶液 于 试 无蓝色沉淀产生
仍能起到保护的作用
管中,滴加K₃[Fe(CN)₆]溶液
向含 0.1mol FeI₂ 的溶液中通入1mol Cl₂,
B 溶液变蓝色 还原性:I⁻>Fe²⁺
再滴加淀粉溶液
C 向CH₂═CHCHO溶液中滴加溴水 溴水褪色 CH₂═CHCHO中含有碳碳双键
将乙醇、浓硫酸在170℃条件下产生的气酸性高锰酸钾溶液
D 有乙烯生成
体通过酸性高锰酸钾溶液 褪色
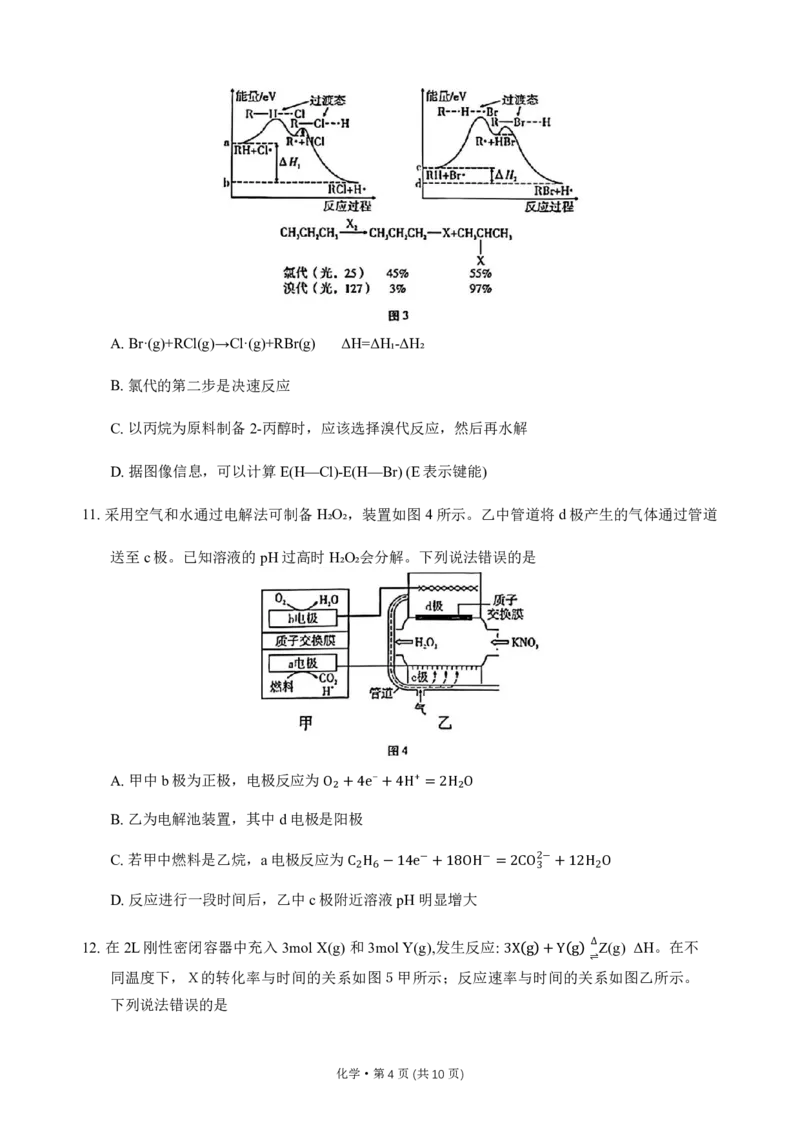
8.血清素可以在一定条件下转化为褪黑素,其转化流程如图2。下列说法正确的是
A.N-乙酰色胺分子式为 B.血清素只能与酸反应
C.褪黑素苯环上的一氯代C物₁₂有H₁3₅N种₂O₂ D.图中R基含有7个电子
9.已知:
①2H₂ g +O₂ g =2H₂O g △H=−483.6kJ⋅mol⁻¹
③H—H、O═O、H—O键能分别为 、 、 。下列说法正确
②H₂O g =H₂O l △H=−44kJ⋅mol⁻¹
的是
436kJ⋅mol⁻¹ 496kJ⋅mol⁻¹ 462kJ⋅mol⁻¹
A.2H₂(g)+O₂(g)===2H₂O(g)反应不能自发进行
B.若1molH₂(l)燃烧生成H₂O(g)时,放出的热量低于241.8kJ
C.若只用以上的键能数据,可估算出H₂的燃烧热
D.H₂(g)和O₂(g)的能量总和大于H₂O(g)的能量
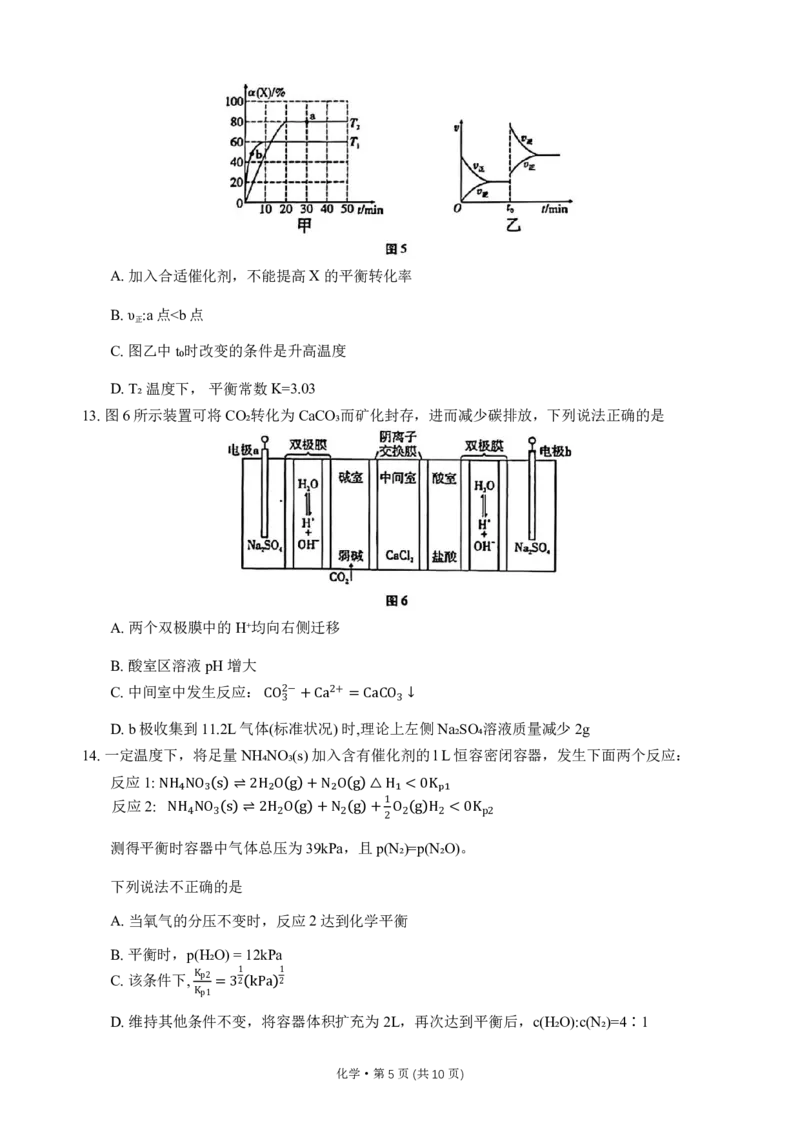
10.一定温度下,CH₃CH₂CH₃(g)(用RH表示)的氯代和溴代反应能量图及产率关系如图3(图中物质
均为气态)。下列说法正确的是
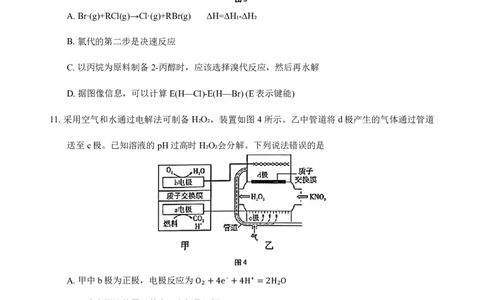
化学·第3页(共10页)A.Br·(g)+RCl(g)→Cl·(g)+RBr(g) ΔH=ΔH₁-ΔH₂
B.氯代的第二步是决速反应
C.以丙烷为原料制备2-丙醇时,应该选择溴代反应,然后再水解
D.据图像信息,可以计算E(H—Cl)-E(H—Br)(E表示键能)
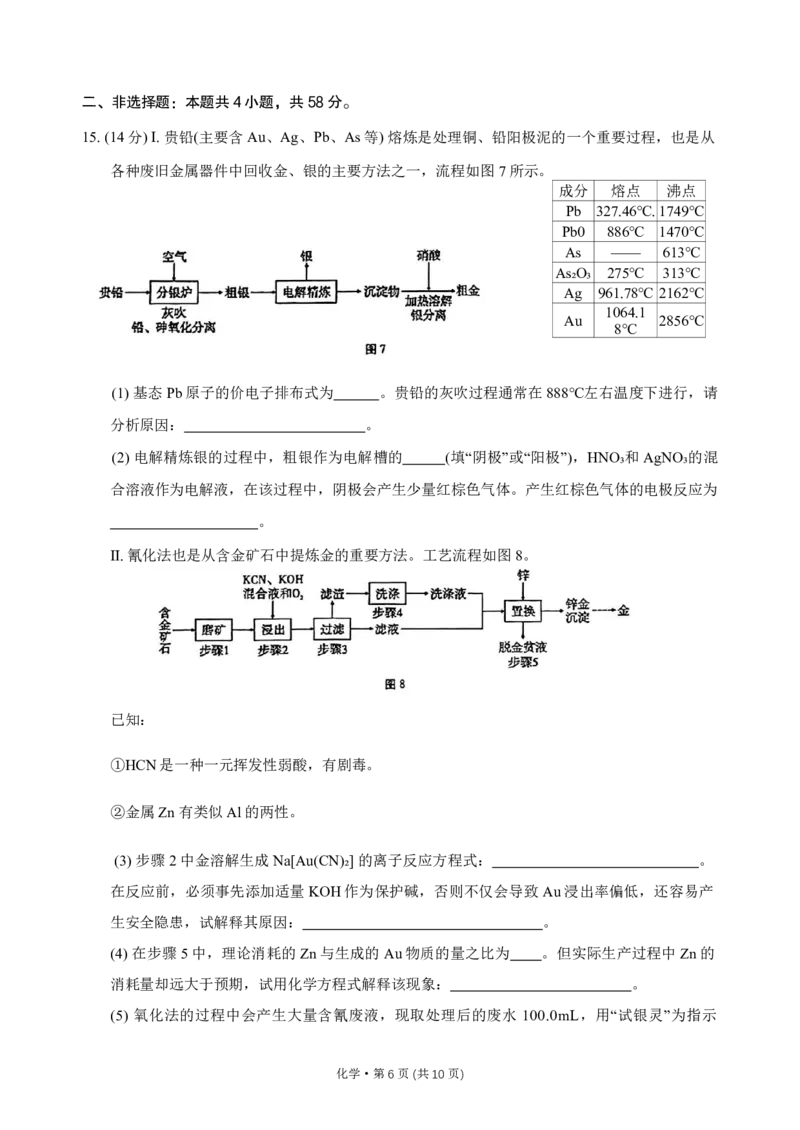
11.采用空气和水通过电解法可制备H₂O₂,装置如图4所示。乙中管道将d极产生的气体通过管道
送至c极。已知溶液的pH过高时H₂O₂会分解。下列说法错误的是
A.甲中b极为正极,电极反应为
O₂+4e⁻+4H⁺ =2H₂O
B.乙为电解池装置,其中d电极是阳极
C.若甲中燃料是乙烷,a电极反应为
− − 2−
C2H6−14e +18OH =2CO3 +12H2O
D.反应进行一段时间后,乙中c极附近溶液pH明显增大
12. 在2L刚性密闭容器中充入3mol X(g) 和3mol Y(g),发生反应: Z(g) ΔH。在不
∆
同温度下,X的转化率与时间的关系如图5甲所示;反应速率3X与g时+间Y的g关
⇌
系如图乙所示。
下列说法错误的是
化学·第4页(共10页)A.加入合适催化剂,不能提高X的平衡转化率
B.υ :a点