文档内容
第三章 晶体结构与性质
第三节 金属晶体与离子晶体
第1课时 金属晶体 离子晶体
培优第一阶——基础过关练
1.(2022·河北邢台·高二阶段练习)下列关于金属及金属键的说法正确的是
A.金属键具有方向性与饱和性
B.金属具有光泽是因为金属阳离子吸收并放出可见光
C.金属能导电是因为金属在外加电场作用下产生了自由电子
D.金属键是金属阳离子与自由电子间的相互作用
【答案】D
【详解】A.金属键不是存在于相邻原子之间的作用力,而是属于整块金属,因此没有方向性和饱和性,A
错误;
B.金属具有光泽是因为自由电子能够吸收可见光,但不能放出可见光,B错误;
C.金属中存在金属阳离子和自由电子,当给金属通电时,自由电子定向移动而导电,C错误;
D.金属键是存在于金属阳离子和自由电子之间的强的相互作用,这些自由电子为所有的阳离子所共用,D
正确;
答案选D。
2.(2022·江苏·响水县第二中学高二期中)关于晶体的下列说法正确的是
A.任何晶体中,若含有阳离子就一定有阴离子
B.氯化钠溶于水时晶体中的离子键被破坏
C.晶体中分子间作用力越大,分子越稳定
D.离子晶体中只含有离子键,不含有共价键
【答案】B
【详解】A.晶体中如果含有阳离子,可能不含阴离子,如:金属晶体是由金属阳离子和自由电子构成的,
故A错误;
B.氯化钠溶于水电离为氯离子和钠离子,晶体中的离子键被破坏,故B正确;
C.分子的稳定性取决于分子内原子间共价键的键能大小,与分子间作用力无关,故C错误;
D.离子晶体可能含有共价键,如NaOH,故D错误;
故选:B。
3.(2022·北京东城·高二期末)氯化铯的晶胞结构如图所示。下列说法不正确的是A.氯化铯晶体属于离子晶体
B.氯化铯晶胞中有3套平行棱,3套平行面
C.在氯化铯晶体中,每个Cl-周围紧邻1个Cs+
D.在氯化铯晶体中,每个Cs+周围与它最近且等距离的Cs+共有6个
【答案】C
【详解】A.氯化铯晶体是由氯离子和铯离子通过离子键结合而成的,属于离子晶体,故A正确;
B.从图中可以看出,氯化铯晶胞中有3套平行棱,3套平行面,故B正确;
C.晶胞是晶体的最小结构单元,从图中可以看出,在氯化铯晶体中,每个Cl-周围紧邻8个Cs+,故C错
误;
D.从图中可以看出,在氯化铯晶体中,每个Cs+周围与它最近且等距离的Cs+共有6个,故D正确;
故选C。
4.(2022·陕西·西安市阎良区关山中学高二阶段练习)金晶体采用面心立方最密堆积方式,其晶胞如图所
示。设金原子的直径为d,用N 表示阿伏加德罗常数的值,M表示金的摩尔质量。则下列说法错误的是
A
A.每个晶胞中含有4个Au原子
B.金属键无方向性,金属原子尽可能采取紧密堆积
C.一个晶胞的体积是16 d3
D.晶体中Au的配位数为12
【答案】C
【详解】A.金晶胞中含有8× +6× =4个Au原子,A正确;
B.金属键无方向性和饱和性,在空间允许的情况下金属原子尽可能采取紧密堆积,B正确;
C.面心立方最密堆积方式的晶胞中,各个面的对角线上3个Au原子两两相切,Au原子的直径为d,故面
对角线长度为2d,棱长为 ×2d= d,故晶胞的体积为( d)3=2 d3,C错误;
D.面心立方最密堆积方式的配位数为12,D正确;故选C。
5.(2022·福建三明·高二期中)表中所列数据是对应物质的熔点,据此判断下列选项正确的是
物质 NaO Na AlF AlCl Al O BCl CO SiO
2 3 3 2 3 3 2 2
熔点(℃) 920 97.8 1291 190 2073 -107 -57 1723
A.含有金属元素的晶体一定是离子晶体
B.AlF 和AlCl 晶体熔化时,克服的微粒间作用力类型相同
3 3
C.同族元素的氧化物不可能形成不同类型的晶体
D.金属晶体的熔点不一定比分子晶体的高
【答案】D
【详解】A.金属晶体中含有金属元素,AlCl 是分子晶体,其也含有金属元素,所以含有金属元素的晶体
3
不一定是离子晶体,故A错误;
B. 属于分子晶体,熔点较低,熔化时破坏分子间作用力, 属于离子晶体,熔点较高,熔化时破
坏离子键,故B错误;
C.C和 同主族,但其最高价氧化物的晶体类型不同, 晶体和 晶体分别属于分子晶体和共价晶
体,所以同族元素的最高价氧化物可能形成不同类型的晶体,故C错误;
D.金属晶体的熔点有的很高,有的很低,如常温下汞呈液态,所以金属晶体的熔点不一定比分子晶体的
高,故D正确;
答案D。
6.(2022·陕西西安·高二期末)金属晶体的堆积方式、空间利用率和配位数关系正确的是
A.锌 ——镁型——68%——8 B.钠 ——钾型——74%——12
C.钋 ——简单立方堆积——52%——6 D.银 ——铜型——74%——8
【答案】C
【详解】A. 为镁型,属于六方堆积,空间利用率为74%,配位数为12,故A错误;
B. 为钾型,属于体心立方堆积,空间利用率为68%,配位数为8,故B错误;
C. 属于简单立方堆积,空间利用率为52%,配位数为6,故C正确;
D. 为铜型,属于面心立方堆积,空间利用率为74%,配位数为12,故D错误;
答案选C。
7.(2022·云南省石屏县第一中学高二阶段练习)下列有关金属键的叙述正确的是
A.金属键有饱和性和方向性
B.金属键是金属阳离子和自由电子之间存在的强烈的静电吸引作用
C.金属键中的自由电子属于整块金属
D.金属的性质和金属固体的形成都与金属键无关
【答案】C【详解】A.金属键不是存在于相邻原子之间的作用力,而是属于整块金属,因此没有方向性和饱和性,
故A错误;
B.金属键是金属阳离子和自由电子之间存在的强烈的静电作用,包括吸引和排斥作用,故B错误;
C.金属中的电子可以在整块金属中自由移动,金属键中的自由电子属于整块金属,故C正确;
D.金属键的强弱决定金属的熔沸点等物理性质,故D错误;
正确答案是C。
8.(2022·陕西·西安市阎良区关山中学高二阶段练习)下图是金属晶体内部的电子气理论示意图。电子气
理论可以用来解释金属的性质,其中正确的是
A.金属能导电是因为金属阳离子在外加电场作用下定向移动
B.金属能导热是因为自由电子在热的作用下相互碰撞,从而发生热的传导
C.金属具有延展性是因为在外力的作用下,金属中各原子层间会出现相对滑动,但自由电子可以起到润
滑剂的作用,使金属不会断裂
D.合金与纯金属相比,由于增加了不同的金属或非金属,使电子数目增多,所以合金的延展性比纯金属
强,硬度比纯金属小
【答案】C
【详解】A.金属能导电是因为自由电子在外加电场作用下定向移动,故A错误;
B.金属能导热是因为自由电子在热的作用下与金属阳离子发生碰撞,从而发生热的传导,故B错误;
C.金属具有延展性是因为在外力的作用下,金属中各原子层间会出现相对滑动,而自由电子起到润滑剂
的作用,使得金属不会断裂,故C正确;
D.合金与纯金属相比,由于增加了不同的金属或非金属,相当于填补了金属阳离子之间的空隙,所以一
般情况下合金的延展性比纯金属弱,硬度比纯金属大,故D错误;
综上所述,答案为C。
9.(2022·辽宁大连·高二期末)有关晶体的结构如图所示,下列说法不正确的是
A. 晶体中,每个 周围等距且紧邻的 有6个B. 晶体中,每个 被8个 包围
C.钛酸钙的化学式为
D.在金刚石晶体中,碳原子与碳碳键的个数之比为
【答案】A
【详解】A.从NaCl的晶胞图可以看出,在 NaCl 晶胞中,顶点 周围等距且紧邻的 位于面心,有
个,A项错误;
B.以最上面面心钙离子为例,它被上面4个和下面4个 包围,即 晶体中,每个 被8个 包围,
B项正确;
C.钛酸钙晶胞中,Ca位于顶点,每个晶胞中有 =1个Ca,Ti位于体心,每个晶胞有1个Ti,O位于
面心,每个晶胞有 =3个O,则钛酸钙的化学式为 CaTiO ,C项正确;
3
D.在金刚石晶体中,每个碳原子都和4个碳原子形成4个碳碳键,每个碳碳键被2个碳原子共用,所以每
个碳原子平均连有2个碳碳键,则碳原子与碳碳键的个数之比为 1:2,D项正确;
答案选A。
10.(2022·江苏·苏州市相城区陆慕高级中学高二阶段练习)钡在氧气中燃烧时得到一种钡的氧化物晶体,
其晶胞的结构如图所示,下列有关说法错误的是
A.该晶体属于离子晶体
B.晶体的化学式为BaO
2
C.该晶体的晶胞结构与NaCl的相似
D.与每个Ba2+距离相等且最近的Ba2+共有8个
【答案】D
【详解】A. 该晶胞是由金属阳离子钡离子和阴离子过氧根离子构成的,为离子晶体,故A正确;
B. 该晶胞中钡离子和过氧根离子个数之比为4:4=1:1,其化学式为BaO,故B正确;
2
C. 该晶胞中钡离子配位数是6,过氧根离子配位数是6,NaCl中离子配位数是6,该晶胞结构和氯化钠
结构相似,故C正确;
D. 与每个Ba2+距离相等且最近的Ba2+个数12,故D错误;
故选D。11.(2022·北京市第十二中学高二阶段练习)锂辉石的主要成分氧化锂的晶胞结构如图所示。下列说法正
确的是
A.氧化锂的化学式为LiO
B.每个晶胞中含有14个
C.每个 周围距离最近且等距的 有8个
D.和钠同主族的锂在空气中燃烧会生成过氧化锂
【答案】C
【详解】A.由晶胞结构可知,晶胞中位于顶点和面心的氧离子个数为8× +6× =4,位于体内的锂离子
为8,则氧化锂的化学式为Li2O,故A错误;
B.由晶胞结构可知,晶胞中位于顶点和面心的氧离子个数为8× +6× =4,故B错误;
C.由晶胞结构可知,晶胞中位于顶点的氧离子与位于体对角线 处的锂离子的距离最近,则每个氧离子
周围距离最近且等距的锂离子有8个,故C正确;
D.锂的金属性弱于钠,则和钠同主族的锂在空气中燃烧只能生成氧化锂,故D错误;
故选C。
培优第二阶——拓展培优练
12.(2022·新疆·乌鲁木齐市第三十一中学高二期中)下列有关离子晶体的叙述错误的是
A. 氯化钠晶体中有 个 分子
B.氯化钠晶体中,每个 周围与它距离相等且最近的 有 个
C.氯化铯晶体中,每个 周围紧邻 个
D.平均每个 晶胞中有 个 、 个
【答案】A
【详解】A.氯化钠为离子化合物,不存在 分子,故A错误;
B.由 晶胞结构可知,钠离子在棱心和体心时,顶点和面心为氯离子,则每个 周围距离相等的
共有 个,故B正确;
C.氯化铯晶体中,铯离子在体心,氯离子在顶点,每个 周围紧邻 个 ,故C正确;D.由 晶胞结构可知,钠离子在棱心和体心时,顶点和面心为氯离子,则由 分析可知,平均每个
晶胞中有 个 、 个 ,故D正确;
故答案为A。
13.(2022·新疆兵团农六师芳草湖农场中学高二期末)下面的排序不正确的是
A.晶体沸点由低到高:CF<CCl <CBr B.晶格能由大到小: NaF> NaCl> NaBr
4 4 4
C.硬度由大到小:金刚石>碳化硅>晶体硅D.熔点由高到低:Na>Mg>Al
【答案】D
【详解】A.四种分子晶体的组成和结构相似,分子的相对分子质量越大,分子间作用力越大,则晶体的
熔沸点越高,则晶体熔点由低到高; CF<CCl <CBr , 故A正确;
4 4 4
B.先比较电荷数的晶格能大,而如果电荷数一样多比较核间距,核间距大的晶格能小,即离子半径小的
晶格能大,则晶格能由大到小; NaF> NaCl> NaBr,故B正确;
C.原子半径Si > C>N ,三者都为原子晶体,原子半径越大,共价键的键能越小,则硬度越小,即硬度由
大到小;刚石>碳化硅>晶体硅,故C正确;
D.Na、Mg、Al原子半径依次减小,属离子电荷逐渐增多,金属键逐渐增强,则熔点由高到低: Al> Mg
> Na, 故D错误。
故选D。
14.(2022·黑龙江齐齐哈尔·高二期末)下列有关晶体的叙述中错误的是
A.干冰晶体中,每个 分子周围紧邻12个 分子
B.氯化铯晶体中,每个 周围紧邻8个
C.氯化钠晶体中,每个 周围紧邻6个
D.金刚石晶体中,每个C原子周围紧邻4个C原子
【答案】C
【详解】A.干冰(CO)是分子晶体,晶胞属于面心立方堆积,故每个CO 分子周围紧邻12个CO 分子,
2 2 2
A正确;
B.氯化铯晶胞中,每个晶胞中含有一个铯离子,每个顶点上的氯离子被8个晶胞共用,故每个 Cs+ 周围
紧邻8个 Cl−,B正确;
C.在氯化钠晶胞中,钠离子在体心和棱心位置,距离体心位置的钠离子最近的钠离子是位于棱心的12个
钠离子,故每个钠离子周围紧邻12个钠离子,C错误;
D.金刚石晶体中,碳原子采用sp3杂化方式成键,故每个C原子周围紧邻4个C原子,D正确;
故选C。
15.(2022·广东·江门市棠下中学高二期中)晶体的熔点高低与微粒间的作用力大小有关,下列各组物质
中,熔点高低的顺序排列正确的是
A.Na>Mg>Al B.CsCl>KC1>NaCl
C. D.金刚石>碳化硅>晶体硅
【答案】D【详解】A.在金属晶体中,如果金属原子的价电子数越多,原子半径越小,自由电子与金属阳离子间的
作用力越大,金属的熔点越高,价电子数Al>Mg>Na,半径Na>Mg>Al,所以金属的熔点Al>Mg>
Na,A错误;
B.CsCl、KC1和NaCl 均属于离子晶体,离子半径Cs+>K+>Na+,则CsCl、KC1和NaCl的晶格能递增、
熔点CsCl<KC1<NaCl,B错误;
C.分子晶体的基本微粒是分子,分子晶体熔沸点由分子间作用力决定。 、 、 分子结构相
似,相对分子质量越小则分子间作用力越小、沸点越低,则氢化物的沸点高低顺序为 ,
C错误;
D.金刚石、碳化硅和晶体硅均属于共价晶体,键长C-C<C-Si<Si-Si,共价键牢固程度:C-C>C-Si>Si-
Si,则熔点:金刚石>碳化硅>晶体硅,D正确;
答案选D。
16.(2022·云南·曲靖市马龙区第一中学高二阶段练习)物质结构理论推出:金属键越强,其金属的硬度
越大,熔、沸点越高。且研究表明,一般来说,金属阳离子半径越小,所带电荷越多,则金属键越强,由
此判断下列说法错误的是
A.硬度:Mg>Al B.熔点:Mg>Ca
C.硬度:Mg>K D.熔点:Ca>K
【答案】A
【详解】A.Mg2+半径比Al3+大,带电荷数比Al3+少,则金属键能Mg<Al,硬度:Mg<Al,A错误;
B.Mg2+半径比Ca2+小,带电荷数相同,则金属键能Mg>Ca,熔点:Mg>Ca,B正确;
C.Mg2+半径比K+小,带电荷数比K+多,则金属键能Mg>K,硬度:Mg>K,C正确;
D.Ca2+半径比K+小,带电荷数比K+多,则金属键能Ca>K,熔点:Ca>K,D正确;
故选A。
17.(2022·四川省绵阳南山中学高二期中)下列各组固体物质熔化或升华所克服的粒子间作用属于同种类
型的是
A.NaO和晶体硅 B.碘和干冰 C.Mg和S D.氯化钠和蔗糖
2
【答案】B
【详解】A.NaO属于离子晶体,熔化克服离子键,硅属于原子晶体,需要克服共价键,类型不同,故A
2
错误;
B.碘和干冰升华均属于分子晶体,升华时均克服分子间作用力,类型相同,故B正确;
C.镁是金属晶体和硫是分子晶体熔化分别克服金属键、硫熔化克服分子间作用力,故C错误;
D.NaCl和蔗糖分别属于离子晶体、分子晶体,NaCl熔化克服离子键、蔗糖熔化克服分子间作用力,故D
错误;
故选:B。
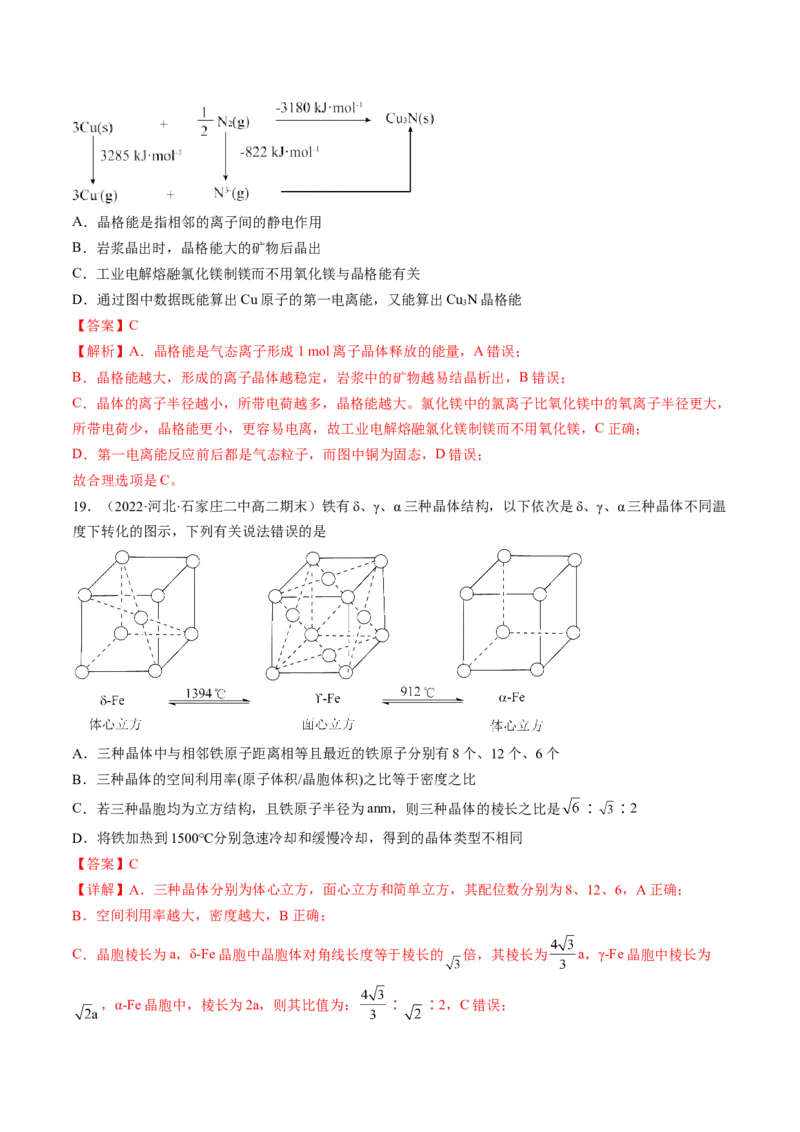
18.下列关于晶格能的叙述正确的是A.晶格能是指相邻的离子间的静电作用
B.岩浆晶出时,晶格能大的矿物后晶出
C.工业电解熔融氯化镁制镁而不用氧化镁与晶格能有关
D.通过图中数据既能算出Cu原子的第一电离能,又能算出Cu N晶格能
3
【答案】C
【解析】A.晶格能是气态离子形成1 mol离子晶体释放的能量,A错误;
B.晶格能越大,形成的离子晶体越稳定,岩浆中的矿物越易结晶析出,B错误;
C.晶体的离子半径越小,所带电荷越多,晶格能越大。氯化镁中的氯离子比氧化镁中的氧离子半径更大,
所带电荷少,晶格能更小,更容易电离,故工业电解熔融氯化镁制镁而不用氧化镁,C正确;
D.第一电离能反应前后都是气态粒子,而图中铜为固态,D错误;
故合理选项是C。
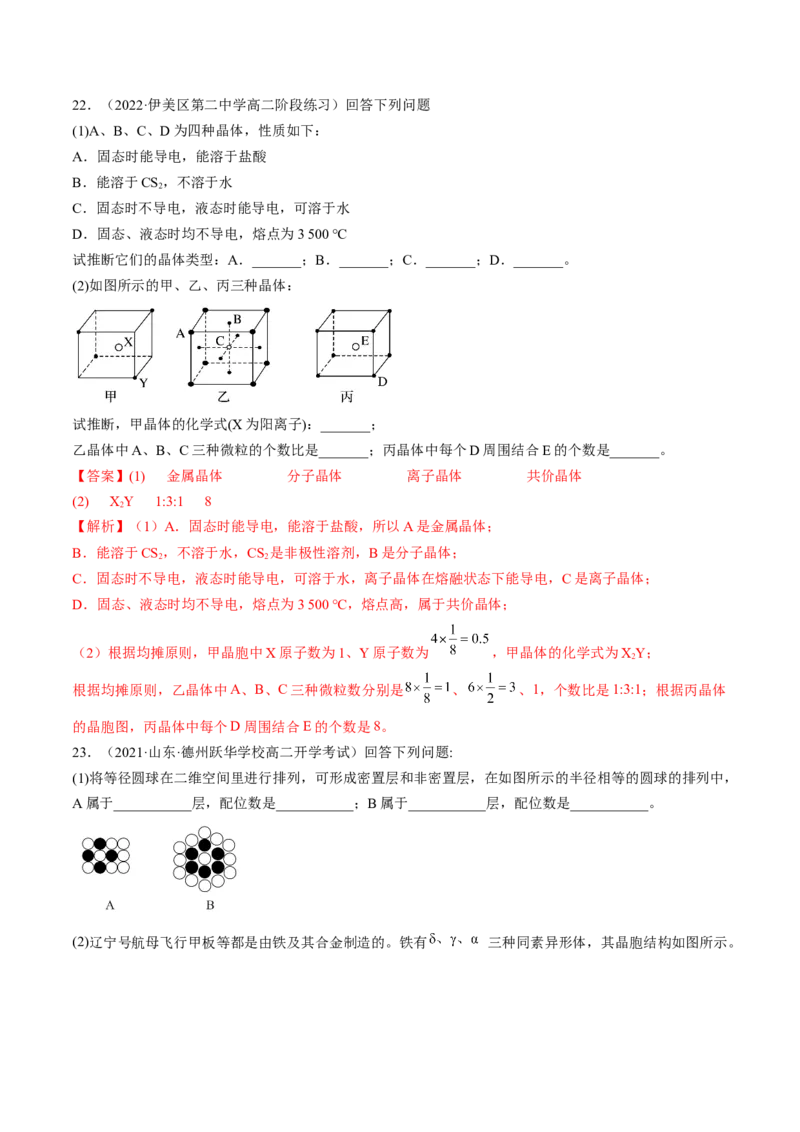
19.(2022·河北·石家庄二中高二期末)铁有δ、γ、α三种晶体结构,以下依次是δ、γ、α三种晶体不同温
度下转化的图示,下列有关说法错误的是
A.三种晶体中与相邻铁原子距离相等且最近的铁原子分别有8个、12个、6个
B.三种晶体的空间利用率(原子体积/晶胞体积)之比等于密度之比
C.若三种晶胞均为立方结构,且铁原子半径为anm,则三种晶体的棱长之比是 ∶ ∶2
D.将铁加热到1500℃分别急速冷却和缓慢冷却,得到的晶体类型不相同
【答案】C
【详解】A.三种晶体分别为体心立方,面心立方和简单立方,其配位数分别为8、12、6,A正确;
B.空间利用率越大,密度越大,B正确;
C.晶胞棱长为a,δ-Fe晶胞中晶胞体对角线长度等于棱长的 倍,其棱长为 a,γ-Fe晶胞中棱长为
,α-Fe晶胞中,棱长为2a,则其比值为: ∶ ∶2,C错误;D.将铁加热到1500℃分别急速冷却得到δ-Fe晶体,缓慢冷却得到α-Fe晶体,晶体类型不相同,D正确;
故选C。
20.金属键
(1)概念:在金属单质晶体中原子之间以_______之间强烈的相互作用。
电子气理论:金属原子脱落下来的_______形成遍布整块晶体的“_______”被所有原子所共用,从而把所
有的金属原子维系在一起。
(2)成键微粒:_______。
(3)存在:金属单质与_______中。
(4)金属键没有_______,也没有饱和性。
【答案】(1) 金属阳离子与自由电子 价电子 电子气
(2)金属阳离子和自由电子
(3)合金
(4)方向性
21.(2022·海南·儋州川绵中学高二阶段练习)按构成晶体的粒子和粒子间作用力的不同,将以下晶体进
行分类:
①氯化钡、②石英、③金刚砂、④水、⑤乙醇、⑥铜、⑦氯酸钾、⑧高锰酸钾、⑨稀有气体的晶体、⑩干
冰
(1)属于共价晶体的有:_______
(2)属于分子晶体的有:_______
(3)属于离子晶体的有:_______
(4)属于金属晶体的有:_______
【答案】(1)②③
(2)④⑤⑨⑩
(3)①⑦⑧
(4)⑥
【分析】氯化钡、氯酸钾、高锰酸钾属于离子晶体,石英和金刚砂属于共价晶体,水、乙醇、稀有气体的
晶体、干冰属于分子晶体,铜属于金属晶体。
【详解】(1)根据分析,属于共价晶体的有:②③;
(2)根据分析,属于分子晶体的有:④⑤⑨⑩;
(3)根据分析,属于离子晶体的有:①⑦⑧;
(4)根据分析,属于金属晶体的有:⑥。22.(2022·伊美区第二中学高二阶段练习)回答下列问题
(1)A、B、C、D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS,不溶于水
2
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3 500 ℃
试推断它们的晶体类型:A._______;B._______;C._______;D._______。
(2)如图所示的甲、乙、丙三种晶体:
试推断,甲晶体的化学式(X为阳离子):_______;
乙晶体中A、B、C三种微粒的个数比是_______;丙晶体中每个D周围结合E的个数是_______。
【答案】(1) 金属晶体 分子晶体 离子晶体 共价晶体
(2) XY 1:3:1 8
2
【解析】(1)A.固态时能导电,能溶于盐酸,所以A是金属晶体;
B.能溶于CS,不溶于水,CS 是非极性溶剂,B是分子晶体;
2 2
C.固态时不导电,液态时能导电,可溶于水,离子晶体在熔融状态下能导电,C是离子晶体;
D.固态、液态时均不导电,熔点为3 500 ℃,熔点高,属于共价晶体;
(2)根据均摊原则,甲晶胞中X原子数为1、Y原子数为 ,甲晶体的化学式为XY;
2
根据均摊原则,乙晶体中A、B、C三种微粒数分别是 、 、1,个数比是1:3:1;根据丙晶体
的晶胞图,丙晶体中每个D周围结合E的个数是8。
23.(2021·山东·德州跃华学校高二开学考试)回答下列问题:
(1)将等径圆球在二维空间里进行排列,可形成密置层和非密置层,在如图所示的半径相等的圆球的排列中,
A属于___________层,配位数是___________;B属于___________层,配位数是___________。
(2)辽宁号航母飞行甲板等都是由铁及其合金制造的。铁有 三种同素异形体,其晶胞结构如图所示。① 、 晶胞中含有的铁原子数之比为___________。
② 、 两种晶体中铁原子的配位数之比为___________。
③若 晶胞的边长为a cm, 晶胞的边长为b cm,则两种晶体的密度之比为___________。
【答案】(1) 非密置 4 密置 6
(2) 2∶1 4∶3 b3∶(4a3)
【解析】(1)密置层的排列最紧密,靠的最近,空隙最少,在图1所示的半径相等的圆球的排列中,A中
的排布不是最紧密,A属于非密置层,一个中心圆球周围有四个圆球,配位数是4;B中排布是最紧密的
结构,B属于密置层,一个中心圆球周围有六个圆球,配位数是6;
(2)① 晶胞中,Fe原子位于晶胞的8个顶点和6个面心,则含有的铁原子数 ; 晶
胞中,Fe原子位于晶胞的8个顶点和1个体心,则含有的铁原子数8×1/8+1×1=2,故答案为2∶1;
② 晶体中铁原子的配位数为8, 晶体中铁原子的配位数为6,故二者铁原子的配位数之比为
8∶6=4∶3;
③若 晶胞的边长为acm,其晶胞只含1个Fe原子,则晶体的密度为: ,若 晶胞
的边长为bcm,其晶胞中含有4个Fe原子,则晶体密度为 ,则两种晶体的密度之比
。