文档内容
3.3.2 影响盐类水解的主要因素 盐类水解的应用 练习(原卷版)
1.为使Na S溶液中c(Na+)/c(S2﹣)的值减小,可加入的物质是( )
2
盐酸 适量的NaOH溶液 适量的KOH溶液 适量的K S固体
2
①A. ② B. ③ C. ④ D.
2.在一①定②条件下,Na
2
S溶液②存在③水解平衡;S2﹣+H 2③O④HS﹣+OH﹣.下列说①法④正确的是( )
⇌
A.升高温度, 增大 B.加入CuSO 固体,HS﹣浓度增大
4
C.稀释溶液,水解平衡常数增大 D.加入NaOH固体,溶液pH减小
3.欲使NH Cl稀溶液中 比值增大,可在溶液中(恒温并忽略溶液体积的变化)加入少
4
量下列物质中的( )
通入HCl; H SO ; NH Cl固体; NH NO 固体 Ba(OH) 固体
2 4 4 4 3 2
①A. 或 或② B.③或 或 ④C. 或 或⑤ D. 或 或
4.在一②定条③件下④,Na
2
S溶液①存在水②解平④衡;S2﹣+H 2②O H③S﹣+O⑤H﹣.下列说①法正③确的⑤是( )
A.加入NaOH固体,溶液pH减小 B.稀⇌释溶液,水解平衡常数增大
C.加入CuSO 固体,HS﹣浓度增大 D.升高温度,c(HS﹣)/c(S2﹣)增大
4
5.在一定条件下,Na CO 溶液存在水解平衡:CO 2﹣+H O HCO ﹣+OH﹣.下列说法正确的是(
2 3 3 2 3
) ⇌
A.稀释溶液,水解平衡常数增大 B.通入CO ,平衡向正反应方向移动
2
C.升高温度, 减小 D.加入NaOH固体,溶液pH减小
6.一定条件下,Na CO 溶液中存在如下平衡:CO 2﹣+H O HCO ﹣+OH﹣,下列说法正确的是(
2 3 3 2 3
) ⇌
A.稀释溶液,平衡正向移动, 增大
B.通入CO ,平衡逆向移动,溶液pH减小
2
C.加入NaOH固体,平衡逆向移动,pH减小
D.升高温度, 增大
7.室温下,有两种溶液: 0.01mol•L﹣1 NH •H O 溶液、 0.01mol•L﹣1 NH Cl 溶液,下列操
3 2 4
① ②作可以使两种溶液中 c(NH +)都增大的是( )
4
A.通入少量 HCl 气体 B.加入少量 NaOH 固体
C.加入少量 H O D.适当升高温度
2
8.已知溶液中存在Cr O 2﹣+H O 2CrO 2﹣+2H+的平衡,其中Cr O 2﹣呈橙色,CrO 2﹣呈黄色,向
2 7 2 4 2 7 4
该平衡体系中滴加饱和NaOH溶⇌液时,颜色的变化情况是( )
A.黄色加深 B.橙色加深 C.颜色不变 D.颜色褪去
9.下列叙述中与盐类水解有关的是( )
A.自来水杀菌、消毒
B.实验室制H 时,在稀H SO 溶液中滴入少许CuSO 溶液
2 2 4 4
C.不能用玻璃瓶盛放NH F浓溶液
4
D.酸雨在空气中放置一段时间后,pH降低
10.下列物质的水溶液由于水解而呈碱性的是( )
A.NaF B.Na SO C.NaOH D.CuSO
2 4 4
11.已知酸性:HX>HY>HZ,物质的量浓度相同的三种钠盐NaX、NaY和NaZ的溶液,pH由大
到小的顺序是( )
A.NaX,NaZ,NaY B.NaZ,NaY,NaX
C.NaX,NaY,NaZ D.NaY,NaZ,NaX
12.下列有关物质的用途,直接与水解的性质有关的是( )
A.NaClO作漂白剂 B.用NH 制氮肥
3
C.明矾作净水剂 D.用食醋除水垢
13.下列实验现象或操作与盐类水解无关的是( )
A.0.1mol•L﹣1的醋酸溶液加水稀释,溶液的pH增大,导电能力减弱
B.用浓NaHCO 溶液与浓Al (SO ) 溶液混合作灭火剂
3 2 4 3
C.热的纯碱溶液有利于除去废铁屑表面的油污
D.配制FeCl 溶液时,将FeCl 固体溶解在浓盐酸中,然后再加水稀释到所需的浓度
3 3
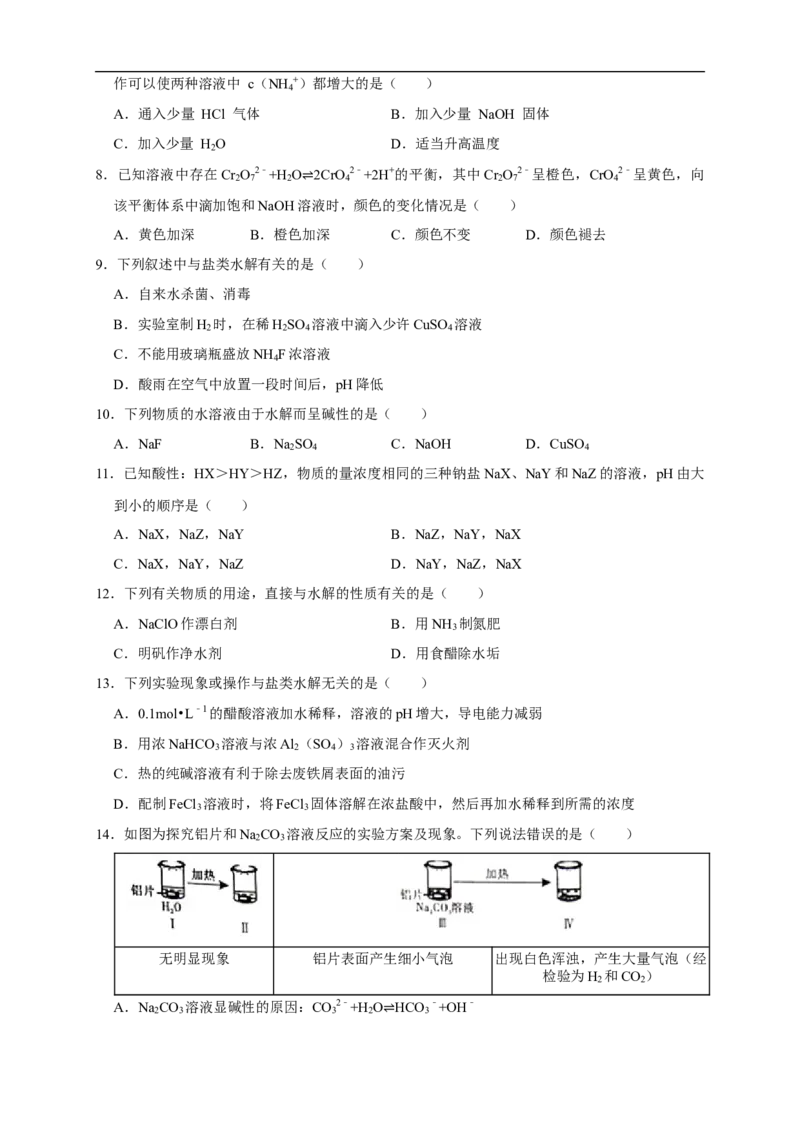
14.如图为探究铝片和Na CO 溶液反应的实验方案及现象。下列说法错误的是( )
2 3
无明显现象 铝片表面产生细小气泡 出现白色浑浊,产生大量气泡(经
检验为H 和CO )
2 2
A.Na CO 溶液显碱性的原因:CO 2﹣+H O HCO ﹣+OH﹣
2 3 3 2 3
⇌B.加热和H 逸出对CO 2﹣ 水解平衡移动方向的影响是相反的
2 3
C.对比实验Ⅰ、Ⅲ,说明Na CO 溶液能破坏铝表面的氧化膜
2 3
D.推测出现的白色沉淀可能是氢氧化铝
15.下列说法不正确的是( )
A.明矾能水解生成Al(OH) 胶体,可用作净水剂
3
B.水解反应NH ++H O NH •H O+H+达到平衡后,升高温度平衡逆向移动
4 2 3 2
C.草木灰与铵态氮肥不⇌宜混合使用
D.盐类水解反应的逆反应是中和反应
16.下列事实与盐类水解无关的是( )
A.明矾可以净水
B.使用热的纯碱溶液去除油污效果好
C.实验室配制FeCl 溶液时加入少量稀盐酸
2
D.向FeCl 溶液中加入KOH溶液产生红褐色沉淀
3
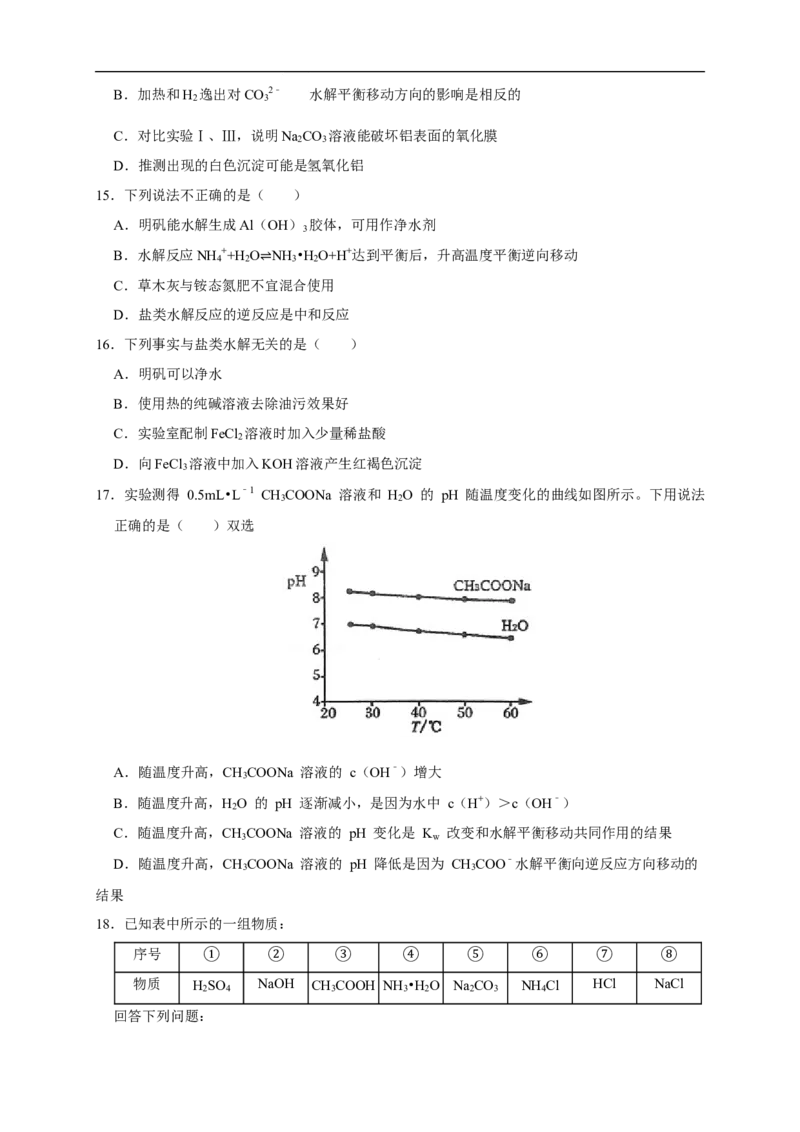
17.实验测得 0.5mL•L﹣1 CH COONa 溶液和 H O 的 pH 随温度变化的曲线如图所示。下用说法
3 2
正确的是( )双选
A.随温度升高,CH COONa 溶液的 c(OH﹣)增大
3
B.随温度升高,H O 的 pH 逐渐减小,是因为水中 c(H+)>c(OH﹣)
2
C.随温度升高,CH COONa 溶液的 pH 变化是 K 改变和水解平衡移动共同作用的结果
3 w
D.随温度升高,CH COONa 溶液的 pH 降低是因为 CH COO﹣水解平衡向逆反应方向移动的
3 3
结果
18.已知表中所示的一组物质:
序号
物质 H①SO N②aOH CH③COOH NH④•H O Na⑤CO NH⑥Cl H⑦Cl N⑧aCl
2 4 3 3 2 2 3 4
回答下列问题:(1)常温时,0.1mol•L﹣1的溶液呈碱性的是_______________。(填序号)
(2)标准状况下,5.6L HCl气体完全溶于蒸馏水中,形成2500mL溶液,则该溶液的pH=
_______________。
(3)常温时,pH=4的H SO 溶液中,由水电离出的c(H+)=______________,pH=9的
2 4
Na CO 溶液中由水电离出
2 3
的c( OH﹣)=___________________________。
(4)常温时,向CH COOH 溶液中加入少量NH Cl固体,电离平衡常数K _______________。
3 4 a
(填“增大”、“减小”或“不变”)
19.我们的生活离不开化学。化学物质在不同的领域发挥着重要的作用。
(1)明矾是常用的一种净水剂,用离子方程式和相应的文字叙述解释其净水的原理:
_______________________________________。
(2)化合物Mg Al (OH) (H O) 可作环保型阻燃材料,受热时发生如下分解反应:
5 3 19 2 4
2Mg Al (OH) (H O) 27H O+10MgO+3Al O 写出该化合物作阻燃剂的两条依据:
5 3 19 2 4 2 2 3
___________________________、____________________________。
(3)焦亚硫酸钠(Na S O )是一种常见的食品抗氧化剂,焦亚硫酸钠中硫元素的化合价为
2 2 5
_+4_。
(4)铵盐是重要的化肥,NH Cl溶液中离子浓度大小顺序是_______________。
4
(5)NaHCO 可以中和胃酸又是常用的食品添加剂,室温下pH=8的NaHCO 溶液中水电离出
3 3
的OH﹣浓度为_______________。
20.溶液中的化学反应大多是离子反应。根据要求回答下列问题:
(1)盐碱地(含较多Na CO 、NaCl)不利于植物生长,试用化学方程式表示:盐碱地产生碱
2 3
性的原因:______________;农业上用石膏降低其碱性的反应原理:______________。
(2)若取pH、体积均相等的NaOH溶液和氨水分别用水稀释m倍、n倍,稀释后pH仍相等,
则m_______________n(填“>”、“<”或“=”)
(3)常温下,在pH=6的CH COOH与CH COONa的混合溶液中水电离出来的c(OH﹣)=
3 3
_______________。
(4)25℃时,将amol/L氨水与0.01mol/L盐酸等体积混合,反应平衡时溶液中c(NH +)=c
4
(Cl﹣),则溶液显______________。(填“酸”“碱”或“中”)性
21.运用盐类水解知识回答下列问题:
(1)FeCl 溶液可用作净水剂,原理为(用必要的化学用语和相关文字说明)
3
_________________________________________。(2)由 FeCl •6H O 晶体得到纯的无水 FeCl 的合理方法是_______________。实验室配制
3 2 3
0.01mol•L﹣1FeCl 溶液时,为了抑制FeCl 水解使溶液中不产生沉淀,可加入少量盐酸至溶液pH
3 3
不大于______________。[Fe(OH) 的K =1.0×10﹣38]
3 sp
(3)泡沫灭火器灭火时发生反应的离子方程式是_______________。
(4)25℃时,pH=11的KOH溶液和pH=11的K CO 溶液中,由水电离出的c(OH﹣)的比值
2 3
为_______________。
22.根据氯化铁溶液回答下列问题:
(1)向FeCl 溶液中加入少量NaHCO ,产生的现象为___________________________,用离子
3 3
方程式表示其原因____________________________。
(2)不断加热FeCl 溶液蒸干其水分并灼烧,得到的固体是______________。
3
(3)在配制FeCl 溶液时,为防止溶液变浑浊,应加入______________________。
3