文档内容
第二课时 沉淀溶解平衡的应用基础练习题
1.欲除去混在BaSO 中的少量CaCO 杂质,下列措施正确的是 ( )
4 3
A.盐酸、过滤 B.稀硫酸、过滤 C.NaOH溶液、过滤 D.四氯化碳、分液
2.以MnO 为原料制得的MnCl 溶液中常含有少量Cu2+、Pb2+、Cd2+等金属离子,通过添加过量难溶电解质MnS,可使这
2 2
些金属离子形成硫化物沉淀,经过滤除去包括MnS在内的沉淀,再经蒸发、结晶,可得纯净的MnCl 根据上述实验事
2
实,可推知MnS具有的相关性质是 ( )
A.具有吸附性 B.溶解度与CuS、PbS、CdS等相同
C.溶解度大于CuS、PbS、CdS D.溶解度小于CuS、PbS、CdS
3.某pH=1的ZnCl 和HCl的混合溶液中含有FeCl 杂质,为了除去FeCl 杂质,需将溶液调至pH=4,在调节溶液pH时,
2 3 3
应选用的试剂是 ( )
A. NaOH B. ZnO C. Na CO D. Fe O
2 3 2 3
4.在2mL物质的量浓度相等的NaCl和NaI溶液中滴入几滴AgNO 溶液,发生的反应为 ( )
3
A.只有AgCl沉淀生成 B.只有AgI沉淀生成
C.生成等物质的量的AgCl和AgI沉淀 D.两种沉淀都有,但以AgI为主
5.下列有关说法正确的是 ( )
A.常温下,AgCl在等物质的量浓度的CaCl 和NaCl溶液中的溶解度相同
2
B.常温下,向饱和NaCO 溶液中加少量BaSO 粉末,过滤,向洗净的沉淀中加稀盐酸有气泡产生,说明常温下
2 3 4
Ksp(BaCO )c(Cl-)
7.已知同温度下的溶解度:Zn(OH) >ZnS,MgCO >Mg(OH) 就溶解或电离出S2-的能力而言,FeS>HS>CuS则下列离子
2 3 2 2
方程式错误的是 ( )
A. Mg2++2HCO-+2Ca2++4OH-=2HO+Mg(OH)↓+2CaCO ↓ B. Cu2++H S=CuS↓+2H+
3 2 2 3 2
C.Zn2++S2-+2H O=Zn(OH)↓+H S↑ D.FeS+2H+=Fe2++H S↑
2 2 2
8.实验:①0.1mol·L-1AgNO 溶液和0.1mol·L-1NaCl溶液等体积混合得到浊液a,过滤得到滤液b和白色沉淀c;②向滤液
3
b中滴加0.1mol/LKI溶液,出现浑浊;③向沉淀c中滴加0.1mol/LKI溶液,沉淀变为黄色。下列分析不正确的是 (
)
A.浊液a中存在沉淀溶解平衡:AgCl(s)=Ag+(aq)+Cl- (ag)
B.滤液b中不含有Ag+
C.③中颜色变化说明AgCl转化为AgI
D.实验可以证明AgI比AgCl更难溶
9.已知在pH为4~5的环境中,Cu2+、Fe2+几乎不水解,而Fe3+几乎完全水解。工业上制CuCl 溶液是将浓盐酸用蒸气加
2
热到80℃左右,再慢慢加入粗氧化铜(含少量杂质FeO),充分搅拌使之溶解。欲除去溶液中的杂质离子,下述方法中可
行的是 ( )
A.向溶液中通入Cl,再加入纯净的CuO粉末调节pH为4~5
2
B.向溶液中通入HS使Fe2+沉淀
2
C.向溶液中通入Cl,再通入NH ,调节pH为4~5
2 3
D.加入纯Cu将Fe2+还原为Fe
10.下列事实不能用平衡移动原理解释的是 ( )
A.Mg(OH) 不溶于水,但能溶于浓NH Cl溶液中
2 4
B.水垢中含有的CaSO,先用NaCO 溶液处理,使之转化为疏松、易溶于酸的CaCO ,再用酸除去
4 2 3 3
C.洗涤BaSO 沉淀时,用稀硫酸洗涤BaSO 沉淀比用蒸馏水洗涤损失少
4 4
D.FeCl 溶液中混有FeCl ,常加入少量的HO,使Fe2+氧化为Fe3+
3 2 2 2
11.自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO 溶液,向地下深层渗透,遇到难溶的ZnS或PbS,慢
4慢转变为铜蓝(CuS)。下列分析正确的是 ( )
A.CuS的溶解度大于PbS的溶解度
B.原生铜的硫化物具有还原性,而铜蓝没有还原性
C.CuSO 与ZnS反应的离子方程式是Cu2++S2-=CuS↓
4
D.整个过程涉及的反应类型有氧化还原反应和复分解反应
12.一定温度下,难溶电解质A B 在水溶液中达到沉淀溶解平衡时,其平衡常数Ksp=cm(An+)·cn(Bm-)称为难溶电解质的
m n
溶度积。已知下表数据:
物质 Fe(OH) Cu(OH) Fe(OH)
3 2 3
Ksp (25℃) 8.0×10-16 2.2×10-20 4.0×10-38
完全沉淀时的pH范围 ≥9.6 ≥6.4 ≥3
下列关于含有等物质的量的CuSO 、FeSO 、Fe (SO ) 的混合溶液的说法正确的是( )
4 4 2 4 3
A.向该混合溶液中逐滴加入NaOH溶液,最先看到的是蓝色沉淀
B.该混合溶液中c(SO 2-):[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5:4
4
C.向该混合溶液中加入适量氯水,调节pH到4~5后过滤,可获得纯净的CuSO 溶液
4
D.向该混合溶液中加入适量氨水,调节pH到9.6后过滤,将所得沉淀灼烧,可得到等物质的量的CuO、FeO、Fe O
2 3
三种固体的混合物
13.下列应用或现象主要体现的是沉淀溶解平衡原理的是( )
①热纯碱溶液洗涤油污的能力强②误将钡盐[BaCl 、Ba(NO )]当作食盐食用后,常用0.5%的NaSO 溶液解毒③溶洞
2 3 2 2 4
的形成④碳酸钡不能作“钡餐”而硫酸钡能⑤泡沫灭火器灭火
A.②③④ B.①②③ C.③④⑤ D.全部
14.已知 25℃时,电离常数 K(HF)=3.6×10-4,溶度积常数 Ksp(CaF )=1.46×10-10。现向 1L0.2mol·L-1HF 溶液中加入
a 2
1L0.2mol·L-1CaCl 溶液,则下列说法中正确的是 ( )
2
A.25℃时,0.1mol·L-1HF溶液中pH=1
B.Ksp(CaF)随温度和浓度的变化而变化
2
C.该体系中有CaF 沉淀产生
2
D.该体系中,K (CaF )=1/K(HF)
sp 2 a
15.已知:Ksp(CuS)=1.3×10-36,Ksp(MnS)=2.6×10-13。工业生产中常用MnS作为沉淀剂除去工业废水中的 Cu:Cu2+(aq)
+MnS(s) CuS(s)+Mn2+(aq)。下列说法错误的是 ( )
A.反应达平衡后,继续加入MnS,废水中的Cu2+的去除率增加
B.该反应可将工业废水中的Cu2+沉淀完全
C.往平衡体系中加入少量CuSO 固体后,c(Mn2+)变大
4
D.该反应的平衡常数K=2.0×1023
16.Cu(OH) 在水中存在着如下沉淀溶解平衡:Cu(OH) (s) Cu2+(aq)+2OH-(aq),在常温下,Ksp=2×10-20。某CuSO
2 2 4
溶液中,c(Cu2+)=0.02mol·L-1,在常温下如果要生成Cu(OH) 沉淀,需要向CuSO 溶液加入碱溶液来调整pH,使溶液的
2 4
pH大于 ( )
A.2 B.3 C.4 D.5
17.已知几种难溶电解质的溶度积常数K (25℃)见下表:
sp
难溶电解质 AgCl AgBr AgI Ag SO Ag CrO
2 4 2 4
Ksp 1.8×10-10 5.4×10-13 8.5×10-17 1.4×10-5 1.12×10-12
下列叙述不正确的是( )
A.由溶度积常数可判断在相同条件下一些物质的溶解性大小
B.将等体积的4×10-3mol·L-1的AgNO 溶液和4×10-3mol·L-1的KCrO 溶液混合,有Ag CrO 沉淀产生
3 2 4 2 4
C.向AgCl的悬浊液中滴加饱和NaBr溶液可以得到黄色AgBr悬浊液
D.向100mL0.1mol·L-1的NaSO 溶液中加入1mL0.1mo·L-1的AgNO 溶液,有白色沉淀生成
2 4 3
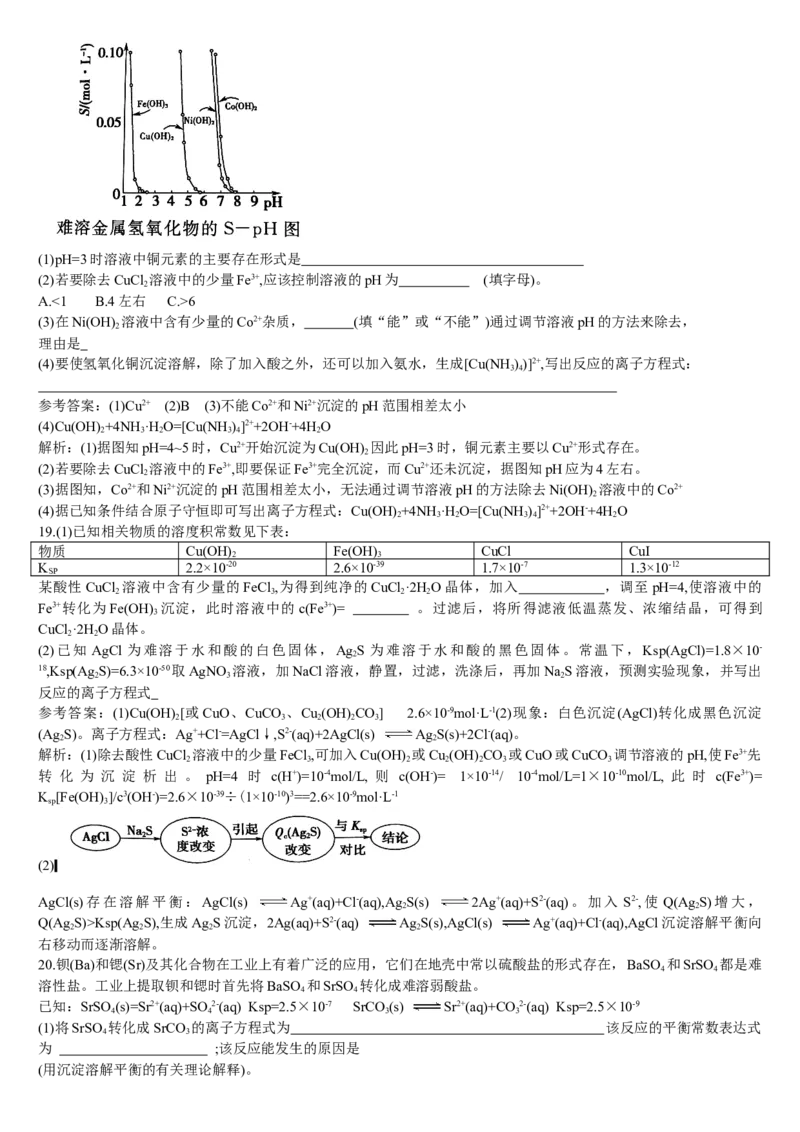
18.金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的 pH,以达到分离金属离子的目的。难溶金属
的氢氧化物在不同pH下的溶解度[S/(mol·L-1)]如图所示。(1)pH=3时溶液中铜元素的主要存在形式是
(2)若要除去CuCl 溶液中的少量Fe3+,应该控制溶液的pH为 (填字母)。
2
A.<1 B.4左右 C.>6
(3)在Ni(OH) 溶液中含有少量的Co2+杂质, (填“能”或“不能”)通过调节溶液pH的方法来除去,
2
理由是
(4)要使氢氧化铜沉淀溶解,除了加入酸之外,还可以加入氨水,生成[Cu(NH ))]2+,写出反应的离子方程式:
3 4
19.(1)已知相关物质的溶度积常数见下表:
物质 Cu(OH) Fe(OH) CuCl CuI
2 3
K 2.2×10-20 2.6×10-39 1.7×10-7 1.3×10-12
SP
某酸性CuCl 溶液中含有少量的FeCl ,为得到纯净的CuCl ·2H O晶体,加入 ,调至pH=4,使溶液中的
2 3 2 2
Fe3+转化为Fe(OH) 沉淀,此时溶液中的c(Fe3+)= 。过滤后,将所得滤液低温蒸发、浓缩结晶,可得到
3
CuCl ·2H O晶体。
2 2
(2)已知 AgCl 为难溶于水和酸的白色固体,Ag S 为难溶于水和酸的黑色固体。常温下,Ksp(AgCl)=1.8×10-
2
18,Ksp(Ag S)=6.3×10-50取AgNO 溶液,加NaCl溶液,静置,过滤,洗涤后,再加NaS溶液,预测实验现象,并写出
2 3 2
反应的离子方程式
20.钡(Ba)和锶(Sr)及其化合物在工业上有着广泛的应用,它们在地壳中常以硫酸盐的形式存在,BaSO 和SrSO 都是难
4 4
溶性盐。工业上提取钡和锶时首先将BaSO 和SrSO 转化成难溶弱酸盐。
4 4
已知:SrSO (s)=Sr2+(aq)+SO2-(aq) Ksp=2.5×10-7 SrCO (s) Sr2+(aq)+CO 2-(aq) Ksp=2.5×10-9
4 4 3 3
(1)将SrSO 转化成SrCO 的离子方程式为 该反应的平衡常数表达式
4 3
为 ;该反应能发生的原因是
(用沉淀溶解平衡的有关理论解释)。
(2)对于上述反应,实验证明增大CO2-的浓度或降低温度都有利于提高SrSO 的转化率。判断在下列两种情况下,平衡
3 4
常数K的变化情况(填“增大”“减小”或“不变”)。
①升高温度,平衡常数K将
②增大CO2-的浓度,平衡常数K将
3
(3)已知,SrSO 和SrCO 在酸中的溶解度与BaSO 和BaCO 类似,设计实验证明上述过程中 SrSO 是否完全转化成
4 3 4 3 4
SrCO 。实验所用的试剂为 ;实验现象及其相
3
应结论为第二课时 沉淀溶解平衡的应用基础练习题解析版
1.欲除去混在BaSO 中的少量CaCO 杂质,下列措施正确的是 ( )
4 3
A.盐酸、过滤 B.稀硫酸、过滤 C.NaOH溶液、过滤 D.四氯化碳、分液
解析:A项,CaCO +2HCl=CaCl +CO ↑+H O,BaSO 不溶于盐酸,故可行;B项,CaSO 微溶,阻止反应进一步进行;
3 2 2 2 4 4
C项, CaCO 与NaOH不反应;D项,CaCO 不溶于CCl 。答案:A
3 3 4
2.以MnO 为原料制得的MnCl 溶液中常含有少量Cu2+、Pb2+、Cd2+等金属离子,通过添加过量难溶电解质MnS,可使这
2 2
些金属离子形成硫化物沉淀,经过滤除去包括MnS在内的沉淀,再经蒸发、结晶,可得纯净的MnCl 根据上述实验事
2
实,可推知MnS具有的相关性质是 ( )
A.具有吸附性 B.溶解度与CuS、PbS、CdS等相同
C.溶解度大于CuS、PbS、CdS D.溶解度小于CuS、PbS、CdS
解析:本题考查了沉淀的转化,MnS与Cu2+、Pb2+、Cd2+生成溶解度更小的硫化物。答案:C
3.某pH=1的ZnCl 和HCl的混合溶液中含有FeCl 杂质,为了除去FeCl 杂质,需将溶液调至pH=4,在调节溶液pH时,
2 3 3
应选用的试剂是 ( )
A. NaOH B. ZnO C. Na CO D. Fe O
2 3 2 3
解析:加入的物质应该能消耗溶液中的H+而促使Fe3+成为沉淀,过滤除去,但同时要注意不能引入新的杂质离子,故
选B。
4.在2mL物质的量浓度相等的NaCl和NaI溶液中滴入几滴AgNO 溶液,发生的反应为 ( )
3
A.只有AgCl沉淀生成 B.只有AgI沉淀生成
C.生成等物质的量的AgCl和AgI沉淀 D.两种沉淀都有,但以AgI为主
解析:在同浓度的NaCl和NaI溶液中c(Cl-)=c(I-),但滴入几滴AgNO 溶液后,由于Ksp(AgI)Ksp(BaSO ),但存在
2 3 4
BaSO(s) Ba2+(aq)+SO2-(aq),因为 NaCO 溶液浓度大,也有可能生成少部分 BaCO 沉淀,错误;D 选项,
4 4 2 3 3
Ag CrO 的溶解度大,错误。答案:C
2 4
6.已知常温下,Ksp(AgCl)=1.8×10-10,K(AgI)=8.5×10-17,下列叙述中正确的是 ( )
A.常温下,AgCl在饱和NaCl溶液中的Ksp比在纯水中的Ksp小
B.将0.001mol·L-1AgNO 溶液滴入KCl和KI的混合溶液中,一定产生AgI沉淀
3
C.向AgCl的悬浊液中加入KI溶液,沉淀由白色转化为黄色
D.向AgCl的饱和溶液中加入NaCl晶体,有AgCl析出且溶液中c(Ag+)>c(Cl-)
解析:Ksp 只与温度有关,A 错误;若溶液中 c(Ag+)·c(I-)Ksp(AgI),故向AgCl的悬浊液中加入KI溶液时,白色沉淀AgCl将转化为黄色沉淀AgI,C正确;向AgCl的
饱和溶液中加入NaCl晶体时有AgCl析出,使溶液中c(Ag+)ZnS,MgCO >Mg(OH) 就溶解或电离出S2-的能力而言,FeS>HS>CuS则下列离子
2 3 2 2
方程式错误的是 ( )
A. Mg2++2HCO-+2Ca2++4OH-=2HO+Mg(OH)↓+2CaCO ↓ B. Cu2++H S=CuS↓+2H+
3 2 2 3 2
C.Zn2++S2-+2H O=Zn(OH)↓+H S↑ D.FeS+2H+=Fe2++H S↑
2 2 2
解析:就溶解度而言,反应向着生成溶解度更小的方向进行;就电离而言,反应向着难电离的方向进行。答案:C
8.实验:①0.1mol·L-1AgNO 溶液和0.1mol·L-1NaCl溶液等体积混合得到浊液a,过滤得到滤液b和白色沉淀c;②向滤液
3
b中滴加0.1mol/LKI溶液,出现浑浊;③向沉淀c中滴加0.1mol/LKI溶液,沉淀变为黄色。下列分析不正确的是 (
)
A.浊液a中存在沉淀溶解平衡:AgCl(s)=Ag+(aq)+Cl- (ag)
B.滤液b中不含有Ag+C.③中颜色变化说明AgCl转化为AgI
D.实验可以证明AgI比AgCl更难溶
解析:注意“0.1mol·L-1AgNO 溶液和0.1mol/LNaCl溶液等体积混合”,即二者恰好完全反应,是分析、解答本题的关
3
键。A.向二者恰好反应后的滤液b中滴加0.1mol·L-1KI溶液出现碘化银沉淀,则说明浊液a中存在沉淀溶解平衡,正
确。B.向滤液b中加入0.1mol·L-1KI溶液,出现浑浊,则说明b中含有Ag+,错误。C.③中颜色变化是沉淀进行了转化,
即AgCl转化为AgI,正确。D.因AgCl沉淀能转化为AgI沉淀,所以Ksp(AgI)Cu知,D
2 4
错误。答案:A
10.下列事实不能用平衡移动原理解释的是 ( )
A.Mg(OH) 不溶于水,但能溶于浓NH Cl溶液中
2 4
B.水垢中含有的CaSO,先用NaCO 溶液处理,使之转化为疏松、易溶于酸的CaCO ,再用酸除去
4 2 3 3
C.洗涤BaSO 沉淀时,用稀硫酸洗涤BaSO 沉淀比用蒸馏水洗涤损失少
4 4
D.FeCl 溶液中混有FeCl ,常加入少量的HO,使Fe2+氧化为Fe3+
3 2 2 2
解析:Mg(OH) 不溶于水,但由于NH Cl是强酸弱碱盐,在溶液中存在水解平衡:NH ++H O NH ·H O+H+,使溶
2 4 4 2 3 2
液显酸性,所以能溶于浓NH Cl溶液中由于消耗溶液中的氢离子,故可以使水解平衡正向移动,可以用平衡移动原理
4
解释,A不选;水垢中含有的CaSO,在溶液中存在沉淀溶解平衡:CaSO(s) Ca2+(aq)+SO2-(aq),先用NaCO 溶液
4 4 4 2 3
处理,Ca2+就会与溶液中的CO2-结合形成难溶性的CaCO 沉淀,发生沉淀的转化,使之转化为疏松、易溶于酸的
3 3
CaCO ,再加入稀盐酸,发生反应:CaCO +2H+=Ca2++CO ↑+H O,转化为可溶性的物质,可以用平衡移动原理解释,B
3 3 2 2
不选;洗涤BaSO 沉淀时,BaSO 在溶液中存在沉淀溶解平衡:BaSO(s) Ba2+(aq)+ SO 2- (aq),若用稀硫酸洗涤
4 4 4 4
BaSO 沉淀,由于增大了溶液中c(SO 2-),使沉淀溶解平衡逆向移动,溶解的硫酸钡的物质的量比用蒸馏水洗涤少,所
4 4
以损失减少,可以用平衡移动原理解释,C不选;FeCl 溶液中混有FeCl ,常加入少量的HO,会发生反应:2Fe2+
3 2 2 2
+H O+2H+=2Fe3++2H O,达到了除杂的目的,与化学平衡无关,故使Fe2+氧化为Fe3+不能用平衡移动原理解释,D符合
2 2 2
题意。答案:D
11.自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO 溶液,向地下深层渗透,遇到难溶的ZnS或PbS,慢
4
慢转变为铜蓝(CuS)。下列分析正确的是 ( )
A.CuS的溶解度大于PbS的溶解度
B.原生铜的硫化物具有还原性,而铜蓝没有还原性
C.CuSO 与ZnS反应的离子方程式是Cu2++S2-=CuS↓
4
D.整个过程涉及的反应类型有氧化还原反应和复分解反应
解析:CuSO 与PbS反应可以生成CuS所以CuS的溶解度小于PbS的,A错误;硫化物中硫的化合价为-2,具有还原性,
4
B错误;ZnS难溶于水,不能写成离子形式,C错误;铜的硫化物首先被氧化成CuSO ,然后硫酸铜与ZnS、PbS发生
4
复分解反应生成更难溶的CuS,D正确。答案:D
12.一定温度下,难溶电解质A B 在水溶液中达到沉淀溶解平衡时,其平衡常数Ksp=cm(An+)·cn(Bm-)称为难溶电解质的
m n
溶度积。已知下表数据:
物质 Fe(OH) Cu(OH) Fe(OH)
3 2 3
Ksp (25℃) 8.0×10-16 2.2×10-20 4.0×10-38
完全沉淀时的pH范围 ≥9.6 ≥6.4 ≥3
下列关于含有等物质的量的CuSO 、FeSO 、Fe (SO ) 的混合溶液的说法正确的是( )
4 4 2 4 3
A.向该混合溶液中逐滴加入NaOH溶液,最先看到的是蓝色沉淀
B.该混合溶液中c(SO 2-):[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5:4
4
C.向该混合溶液中加入适量氯水,调节pH到4~5后过滤,可获得纯净的CuSO 溶液
4
D.向该混合溶液中加入适量氨水,调节pH到9.6后过滤,将所得沉淀灼烧,可得到等物质的量的CuO、FeO、Fe O
2 3三种固体的混合物
解析:在滴加NaOH溶液的过程中,先生成Fe(OH) 沉淀,故最先看到的是Fe(OH) 红褐色沉淀,A项错误;假设
3 3
Cu2+、Fe2+、Fe3+均不水解,则c(SO 2-):[c(Cu2+)+c(Fe2+)+c(Fe3+)]=5:4,而这三种阳离子都可以水解,所以c(SO 2-):[c(Cu2+)
4 4
+c(Fe2+)+c(Fe3+)]>5:4,B项正确;氯水可将Fe2+氧化为Fe3+,pH=4~5时,Fe3+被完全沉淀,因为加入了氯水,所以还引入
了Cl-,C项错误;灼烧后得不到FeO,因为在灼烧过程中,铁元素会完全转化为Fe O,D项错误。答案:B
2 3
13.下列应用或现象主要体现的是沉淀溶解平衡原理的是( )
①热纯碱溶液洗涤油污的能力强②误将钡盐[BaCl 、Ba(NO )]当作食盐食用后,常用0.5%的NaSO 溶液解毒③溶洞
2 3 2 2 4
的形成④碳酸钡不能作“钡餐”而硫酸钡能⑤泡沫灭火器灭火
A.②③④ B.①②③ C.③④⑤ D.全部
答案:A
14.已知 25℃时,电离常数 K(HF)=3.6×10-4,溶度积常数 Ksp(CaF )=1.46×10-10。现向 1L0.2mol·L-1HF 溶液中加入
a 2
1L0.2mol·L-1CaCl 溶液,则下列说法中正确的是 ( )
2
A.25℃时,0.1mol·L-1HF溶液中pH=1
B.Ksp(CaF)随温度和浓度的变化而变化
2
C.该体系中有CaF 沉淀产生
2
D.该体系中,K (CaF )=1/K(HF)
sp 2 a
解析:A项错误,若HF为强酸,则0.1mol/LHF溶液pH=1,实际HF是弱酸,所以pH>1;B项错误,K不随浓度的变化
而 变 化 ; C 项 正 确 , 等 体 积 混 合 后 HF 电 离 出 的 c(H+)=c(F-)=6×10-2mol/L , c(Ca2+)=0.1mol/L , 此 时
Q(CaF )=c(Ca2+)•c2(F-)=3.6×10-4>Ksp(CaF),所以有沉淀生成。答案:C
2 2
15.已知:Ksp(CuS)=1.3×10-36,Ksp(MnS)=2.6×10-13。工业生产中常用MnS作为沉淀剂除去工业废水中的 Cu:Cu2+(aq)
+MnS(s) CuS(s)+Mn2+(aq)。下列说法错误的是 ( )
A.反应达平衡后,继续加入MnS,废水中的Cu2+的去除率增加
B.该反应可将工业废水中的Cu2+沉淀完全
C.往平衡体系中加入少量CuSO 固体后,c(Mn2+)变大
4
D.该反应的平衡常数K=2.0×1023
解析:A项,达到平衡后,增加MnS的使用量,平衡不移动,废水中的Cu2+的去除率不再改变,故A错误;B项,利
用此反应可将工业废水中的Cu2+沉淀完全,故B项正确;项,c(Cu2+)增大,平衡正向移动,所以c(Mn2+)变大,故C正
确;D项,该反应的平衡常数 K=c(Mn2+)/ c(Cu2+)=Ksp(MnS)/ Ksp(CuS)=2.0×1023,故D正确。答案:A
16.Cu(OH) 在水中存在着如下沉淀溶解平衡:Cu(OH) (s) Cu2+(aq)+2OH-(aq),在常温下,Ksp=2×10-20。某CuSO
2 2 4
溶液中,c(Cu2+)=0.02mol·L-1,在常温下如果要生成Cu(OH) 沉淀,需要向CuSO 溶液加入碱溶液来调整pH,使溶液的
2 4
pH大于 ( )
A.2 B.3 C.4 D.5
解析:[Cu(OH) (s) Cu2+(aq)+2OH-(aq),其中 Ksp=c(Cu2+)·c2(OH-),要使 Cu(OH) 沉淀需达到其 Ksp,故,c(OH-)>
2 2
故c(OH-)>1×10-9mol·L-1,则c(H+)<1×10-5mol·L-1,因此pH应大于5.答案:D
17.已知几种难溶电解质的溶度积常数K (25℃)见下表:
sp
难溶电解质 AgCl AgBr AgI Ag SO Ag CrO
2 4 2 4
Ksp 1.8×10-10 5.4×10-13 8.5×10-17 1.4×10-5 1.12×10-12
下列叙述不正确的是( )
A.由溶度积常数可判断在相同条件下一些物质的溶解性大小
B.将等体积的4×10-3mol·L-1的AgNO 溶液和4×10-3mol·L-1的KCrO 溶液混合,有Ag CrO 沉淀产生
3 2 4 2 4
C.向AgCl的悬浊液中滴加饱和NaBr溶液可以得到黄色AgBr悬浊液
D.向100mL0.1mol·L-1的NaSO 溶液中加入1mL0.1mo·L-1的AgNO 溶液,有白色沉淀生成
2 4 3
解析:D项,混合溶液中c(Ag+)=0.1mol·L-1× ≈0.001mol·L-1,c2(Ag+)·c(SO 2-)=0.0012×0.1=1×10-7 <1.4×10-5,故不
4
会产生沉淀。答案:D
18.金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的 pH,以达到分离金属离子的目的。难溶金属
的氢氧化物在不同pH下的溶解度[S/(mol·L-1)]如图所示。(1)pH=3时溶液中铜元素的主要存在形式是
(2)若要除去CuCl 溶液中的少量Fe3+,应该控制溶液的pH为 (填字母)。
2
A.<1 B.4左右 C.>6
(3)在Ni(OH) 溶液中含有少量的Co2+杂质, (填“能”或“不能”)通过调节溶液pH的方法来除去,
2
理由是
(4)要使氢氧化铜沉淀溶解,除了加入酸之外,还可以加入氨水,生成[Cu(NH ))]2+,写出反应的离子方程式:
3 4
参考答案:(1)Cu2+ (2)B (3)不能Co2+和Ni2+沉淀的pH范围相差太小
(4)Cu(OH) +4NH·H O=[Cu(NH )]2++2OH-+4H O
2 3 2 3 4 2
解析:(1)据图知pH=4~5时,Cu2+开始沉淀为Cu(OH) 因此pH=3时,铜元素主要以Cu2+形式存在。
2
(2)若要除去CuCl 溶液中的Fe3+,即要保证Fe3+完全沉淀,而Cu2+还未沉淀,据图知pH应为4左右。
2
(3)据图知,Co2+和Ni2+沉淀的pH范围相差太小,无法通过调节溶液pH的方法除去Ni(OH) 溶液中的Co2+
2
(4)据已知条件结合原子守恒即可写出离子方程式:Cu(OH) +4NH·H O=[Cu(NH )]2++2OH-+4H O
2 3 2 3 4 2
19.(1)已知相关物质的溶度积常数见下表:
物质 Cu(OH) Fe(OH) CuCl CuI
2 3
K 2.2×10-20 2.6×10-39 1.7×10-7 1.3×10-12
SP
某酸性CuCl 溶液中含有少量的FeCl ,为得到纯净的CuCl ·2H O晶体,加入 ,调至pH=4,使溶液中的
2 3 2 2
Fe3+转化为Fe(OH) 沉淀,此时溶液中的c(Fe3+)= 。过滤后,将所得滤液低温蒸发、浓缩结晶,可得到
3
CuCl ·2H O晶体。
2 2
(2)已知 AgCl 为难溶于水和酸的白色固体,Ag S 为难溶于水和酸的黑色固体。常温下,Ksp(AgCl)=1.8×10-
2
18,Ksp(Ag S)=6.3×10-50取AgNO 溶液,加NaCl溶液,静置,过滤,洗涤后,再加NaS溶液,预测实验现象,并写出
2 3 2
反应的离子方程式
参考答案:(1)Cu(OH) [或CuO、CuCO 、Cu (OH) CO] 2.6×10-9mol·L-1(2)现象:白色沉淀(AgCl)转化成黑色沉淀
2 3 2 2 3
(Ag S)。离子方程式:Ag++Cl-=AgCl↓,S2-(aq)+2AgCl(s) Ag S(s)+2Cl-(aq)。
2 2
解析:(1)除去酸性CuCl 溶液中的少量FeCl ,可加入Cu(OH) 或Cu (OH) CO 或CuO或CuCO 调节溶液的pH,使Fe3+先
2 3 2 2 2 3 3
转 化 为 沉 淀 析 出 。 pH=4 时 c(H+)=10-4mol/L, 则 c(OH-)= 1×10-14/ 10-4mol/L=1×10-10mol/L, 此 时 c(Fe3+)=
K [Fe(OH) ]/c3(OH-)=2.6×10-39÷(1×10-10)3==2.6×10-9mol·L-1
sp 3
(2)
AgCl(s)存在溶解平衡:AgCl(s) Ag+(aq)+Cl-(aq),Ag S(s) 2Ag+(aq)+S2-(aq)。加入 S2-,使 Q(Ag S)增大,
2 2
Q(Ag S)>Ksp(Ag S),生成Ag S沉淀,2Ag(aq)+S2-(aq) Ag S(s),AgCl(s) Ag+(aq)+Cl-(aq),AgCl沉淀溶解平衡向
2 2 2 2
右移动而逐渐溶解。
20.钡(Ba)和锶(Sr)及其化合物在工业上有着广泛的应用,它们在地壳中常以硫酸盐的形式存在,BaSO 和SrSO 都是难
4 4
溶性盐。工业上提取钡和锶时首先将BaSO 和SrSO 转化成难溶弱酸盐。
4 4
已知:SrSO (s)=Sr2+(aq)+SO2-(aq) Ksp=2.5×10-7 SrCO (s) Sr2+(aq)+CO 2-(aq) Ksp=2.5×10-9
4 4 3 3
(1)将SrSO 转化成SrCO 的离子方程式为 该反应的平衡常数表达式
4 3
为 ;该反应能发生的原因是
(用沉淀溶解平衡的有关理论解释)。(2)对于上述反应,实验证明增大CO2-的浓度或降低温度都有利于提高SrSO 的转化率。判断在下列两种情况下,平衡
3 4
常数K的变化情况(填“增大”“减小”或“不变”)。
①升高温度,平衡常数K将
②增大CO2-的浓度,平衡常数K将
3
(3)已知,SrSO 和SrCO 在酸中的溶解度与BaSO 和BaCO 类似,设计实验证明上述过程中 SrSO 是否完全转化成
4 3 4 3 4
SrCO 。实验所用的试剂为 ;实验现象及其相
3
应结论为
解析:(1)SrSO 转化成SrCO 的离子反应为SrSO (s)+CO2-(aq) SrCO (s)+SO 2-(aq),平衡常数表达式为K=c(SO2-)/
4 3 4 3 3 4 4
c(CO2- )根据沉淀转化的原理,该反应能够发生,是因为Ksp(SrCO )< Ksp(SrSO )。
3 3 4
(2)①降低温度有利于提高SrSO 的转化率,说明降温平衡向正反应方向移动,因此升高温度,平衡向逆反应方向移动,
4
故平衡常数K减小。②平衡常数只与温度有关,增大CO2-的浓度,平衡常数不变。
3
(3)根据提供的信息,可以推断SrSO 难溶于盐酸,而SrCO 可溶于盐酸,因此向溶液中加入盐酸,若沉淀全部溶解,
4 3
则SrSO 完全转化成SrCO ,若沉淀没有全部溶解,则SrSO 没有完全转化成SrCO ,需要注意的是,不能选择稀硫酸,
4 3 4 3
因为SrCO 与稀硫酸反应生成SrSO 。
3 4
参考答案:(1)SrSO (s)+c(CO2-)(aq) SrCO (s)+SO 2-(aq) K=c(SO2-)/ c(CO2- ) Ksp(SrCO )