文档内容
第一课时 难溶电解质的沉淀溶解平衡基础练习题解析版
1.室温下向饱和AgC1溶液中加水,下列叙述正确的是( )
A.AgCl的溶解度增大
B.AgCl的溶解度、K 均不变
sp
C.AgCl的K 增大
sp
D.AgCl的溶解度、K 均增大
sp
2.下列说法中,正确的是 ( )
A.难溶电解质在水溶液中达到沉淀溶解平衡时,沉淀和溶解均停止
B.K越小,难溶电解质在水中的溶解能力一定越弱
C.K的大小与离子浓度无关,只与难溶电解质的性质和温度有关
D.相同温度下,AgCl在水中的溶解能力与在NaCl溶液中的相同
3.25℃时,已知K (AgCl)=1.8×10-10,K (AgBr)=7.8×10-13。现向等浓度NaCl和NaBr的混合溶液中逐滴加入稀AgNO
sp sp 3
溶液,先沉淀的是( )
A.AgCI B.AgBr C.同时沉淀 D.无法判断
4.25℃时,在含有大量PbI 的饱和溶液中存在着平衡:PbI (s) Pb2+(aq)+2I-(aq), 加入KI溶液,下列说法正确的
2 2
是 ( )
A.溶液中Pb2+和I-浓度都增大 B.溶度积常数K 增大 C.沉淀溶解平衡向左移动 D.溶液中Pb2+浓度增大
sp
5.已知CaCO 的K =2.8×10-9,现将浓度为2×10-4mol·L-1的NaCO 溶液与CaCl 溶液等体积混合,若要产生沉淀,则所
3 sp 2 3 2
用CaCl 溶液的浓度至少应为 ( )
2
A.2.8×10-2mol·L-1 B.1.4×10-5mol·L-1 C.2.8×10-5mol·L-1 6×10-5mol·L-1
6.向含有MgCO 固体的溶液中滴加少许浓盐酸(忽略体积变化),下列数值变小的是( )
3
A. c(H+) B. c(Mg2+) C. c(CO2-) D. Ksp(MgCO )
3 3
7.(双选)已知25℃时,K(HF)=3.6×10-4,K(CaF )=1.46×10-10,现向1L0.2mol·L-1HF溶液中加入1L0.2mol·L-1CaCl 溶液,则
a 2 2
下列说法中,正确的是( )
A.25℃时,0.1mol·L-1HF溶液中pH>1 B.K (CaF )随温度和浓度的变化而变化
SP 2
C.该体系中没有沉淀产生 D.该体系中HF与CaCl 反应产生沉淀
2
8. (双选)在25℃时,FeS的K =6.3×10-18,CuS的K =1.3×10-36,ZnS的K =1.3×10-24,下列有关说法中正确的是( )
SP SP sp
A.FeS的溶解度大于CuS的溶解度
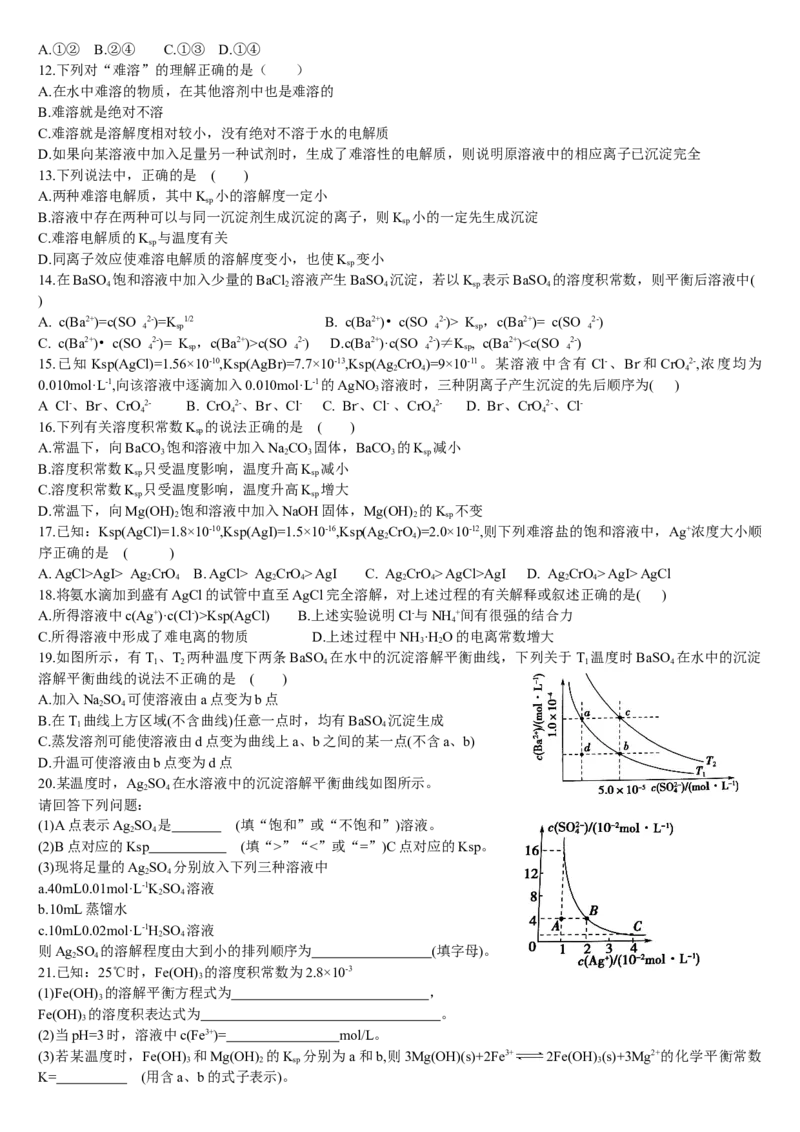
B.饱和CuS溶液中Cu2+浓度为 mol/L
C.向物质的量浓度相同的FeCl 、ZnCl 的混合液中加入少量NaS,只有FeS沉淀生成
2 2 2
D.向饱和ZnS溶液中加入少量ZnCl 固体,ZnS的K 变大
2 SP
9.电离常数(K、K)、水解常数(K )、溶度积常数(K )等常数是表示、判断物质性质的重要常数,下列关于这些常数的
a b h sp
说法中正确的是( )
A.当温度升高时,弱酸、弱碱的电离常数(K、K)均变大
a b
B.K(HCN)K (BaCO)
4 sp 4 sp 3
D.水解常数的大小与温度、浓度有关,与溶液的酸碱性无关
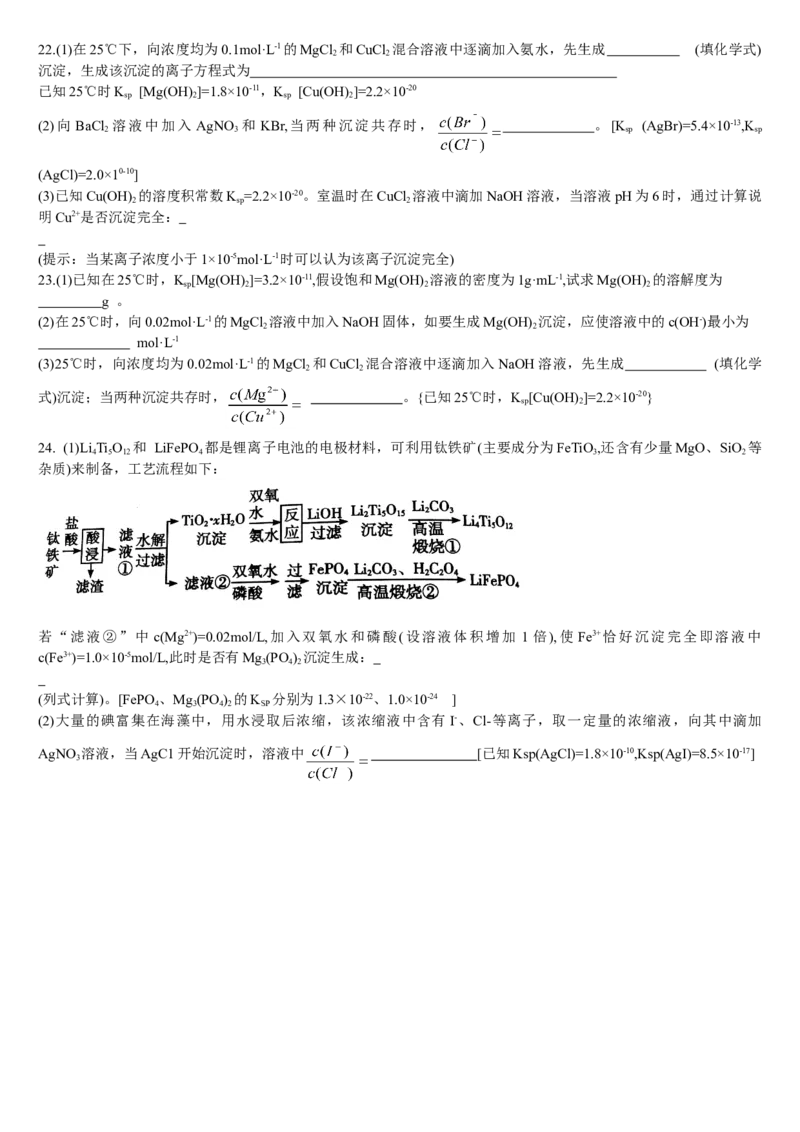
10.已知:图甲是由某温度下 Fe(OH) (s)、Cu(OH) (s)分别在溶液
3 2
中达到沉淀溶解平衡后,改变溶液 pH,金属阳离子浓度的变化图。
图乙是常温下向 100mL0.1mol/LHA 溶液中逐滴加入 0.2mol/
LKOH溶液,混合溶液的pH变化图。如图所示与推测的结论相
符的是( )
A.由图甲知:K [Fe(OH) ]c(A-)>c(OH-)
11.下列物质的溶解度随温度升高而减小的是( )
①KNO ②Ca(OH) ③BaSO ④CO
3 2 4 2A.①② B.②④ C.①③ D.①④
12.下列对“难溶”的理解正确的是( )
A.在水中难溶的物质,在其他溶剂中也是难溶的
B.难溶就是绝对不溶
C.难溶就是溶解度相对较小,没有绝对不溶于水的电解质
D.如果向某溶液中加入足量另一种试剂时,生成了难溶性的电解质,则说明原溶液中的相应离子已沉淀完全
13.下列说法中,正确的是 ( )
A.两种难溶电解质,其中K 小的溶解度一定小
sp
B.溶液中存在两种可以与同一沉淀剂生成沉淀的离子,则K 小的一定先生成沉淀
sp
C.难溶电解质的K 与温度有关
sp
D.同离子效应使难溶电解质的溶解度变小,也使K 变小
sp
14.在BaSO 饱和溶液中加入少量的BaCl 溶液产生BaSO 沉淀,若以K 表示BaSO 的溶度积常数,则平衡后溶液中(
4 2 4 sp 4
)
A. c(Ba2+)=c(SO 2-)=K 1/2 B. c(Ba2+)• c(SO 2-)> K ,c(Ba2+)= c(SO 2-)
4 sp 4 sp 4
C. c(Ba2+)• c(SO 2-)= K ,c(Ba2+)>c(SO 2-) D.c(Ba2+)·c(SO 2-)≠K , c(Ba2+)AgI> Ag CrO B. AgCl> Ag CrO> AgI C. Ag CrO> AgCl>AgI D. Ag CrO> AgI> AgCl
2 4 2 4 2 4 2 4
18.将氨水滴加到盛有AgCl的试管中直至AgCl完全溶解,对上述过程的有关解释或叙述正确的是( )
A.所得溶液中c(Ag+)·c(Cl-)>Ksp(AgCl) B.上述实验说明Cl-与NH +间有很强的结合力
4
C.所得溶液中形成了难电离的物质 D.上述过程中NH ·H O的电离常数增大
3 2
19.如图所示,有T 、T 两种温度下两条BaSO 在水中的沉淀溶解平衡曲线,下列关于T 温度时BaSO 在水中的沉淀
1 2 4 1 4
溶解平衡曲线的说法不正确的是 ( )
A.加入NaSO 可使溶液由a点变为b点
2 4
B.在T 曲线上方区域(不含曲线)任意一点时,均有BaSO 沉淀生成
1 4
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
D.升温可使溶液由b点变为d点
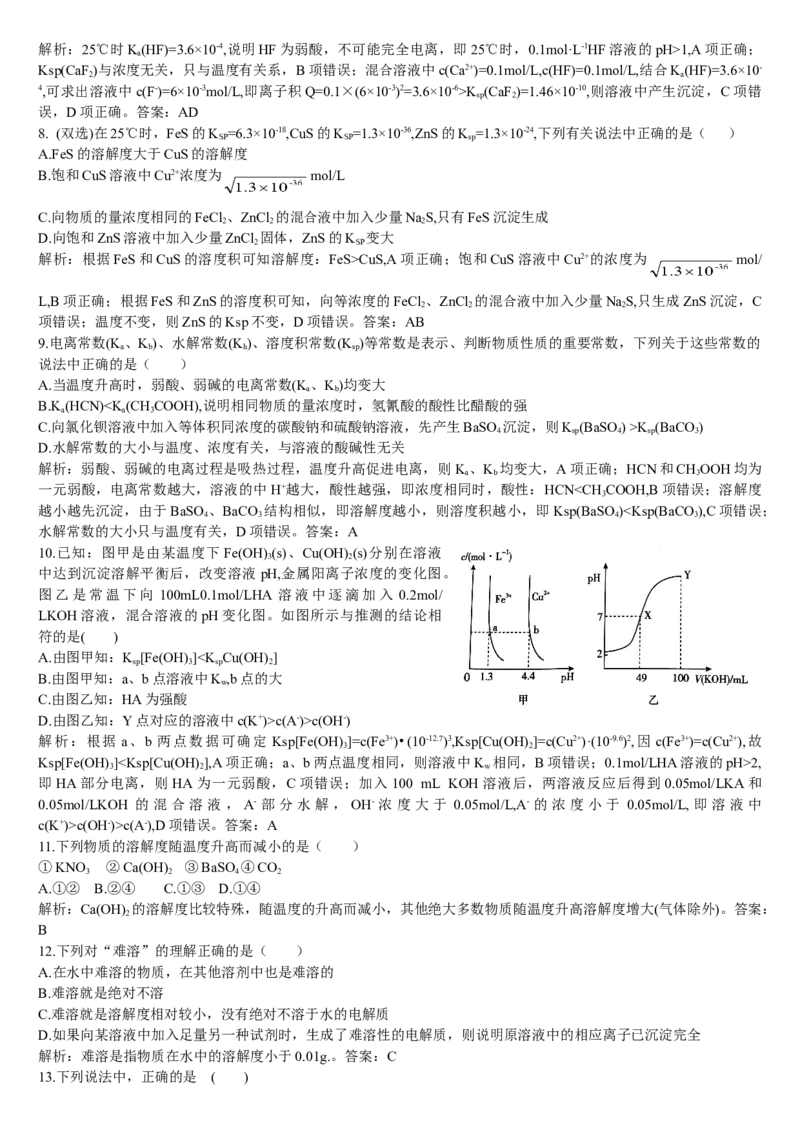
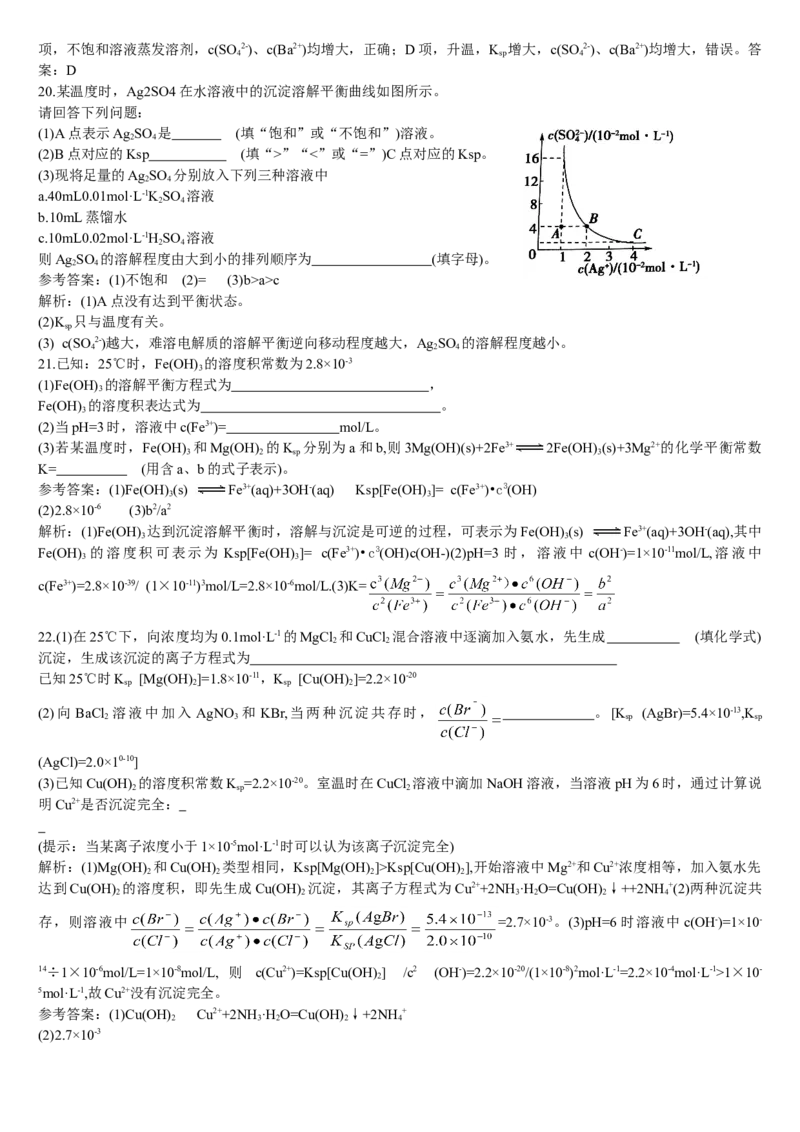
20.某温度时,Ag SO 在水溶液中的沉淀溶解平衡曲线如图所示。
2 4
请回答下列问题:
(1)A点表示Ag SO 是 (填“饱和”或“不饱和”)溶液。
2 4
(2)B点对应的Ksp (填“>”“<”或“=”)C点对应的Ksp。
(3)现将足量的Ag SO 分别放入下列三种溶液中
2 4
a.40mL0.01mol·L-1KSO 溶液
2 4
b.10mL蒸馏水
c.10mL0.02mol·L-1HSO 溶液
2 4
则Ag SO 的溶解程度由大到小的排列顺序为 (填字母)。
2 4
21.已知:25℃时,Fe(OH) 的溶度积常数为2.8×10-3
3
(1)Fe(OH) 的溶解平衡方程式为 ,
3
Fe(OH) 的溶度积表达式为 。
3
(2)当pH=3时,溶液中c(Fe3+)= mol/L。
(3)若某温度时,Fe(OH) 和Mg(OH) 的K 分别为a和b,则3Mg(OH)(s)+2Fe3+ 2Fe(OH) (s)+3Mg2+的化学平衡常数
3 2 sp 3
K= (用含a、b的式子表示)。22.(1)在25℃下,向浓度均为0.1mol·L-1的MgCl 和CuCl 混合溶液中逐滴加入氨水,先生成 (填化学式)
2 2
沉淀,生成该沉淀的离子方程式为
已知25℃时K [Mg(OH) ]=1.8×10-11,K [Cu(OH) ]=2.2×10-20
sp 2 sp 2
(2)向 BaCl 溶液中加入 AgNO 和 KBr,当两种沉淀共存时, 。[K (AgBr)=5.4×10-13,K
2 3 sp sp
(AgCl)=2.0×10-10]
(3)已知Cu(OH) 的溶度积常数K =2.2×10-20。室温时在CuCl 溶液中滴加NaOH溶液,当溶液pH为6时,通过计算说
2 sp 2
明Cu2+是否沉淀完全:
(提示:当某离子浓度小于1×10-5mol·L-1时可以认为该离子沉淀完全)
23.(1)已知在25℃时,K [Mg(OH) ]=3.2×10-11,假设饱和Mg(OH) 溶液的密度为1g·mL-1,试求Mg(OH) 的溶解度为
sp 2 2 2
g 。
(2)在25℃时,向0.02mol·L-1的MgCl 溶液中加入NaOH固体,如要生成Mg(OH) 沉淀,应使溶液中的c(OH-)最小为
2 2
mol·L-1
(3)25℃时,向浓度均为0.02mol·L-1的MgCl 和CuCl 混合溶液中逐滴加入NaOH溶液,先生成 (填化学
2 2
式)沉淀;当两种沉淀共存时, 。{已知25℃时,K [Cu(OH) ]=2.2×10-20}
sp 2
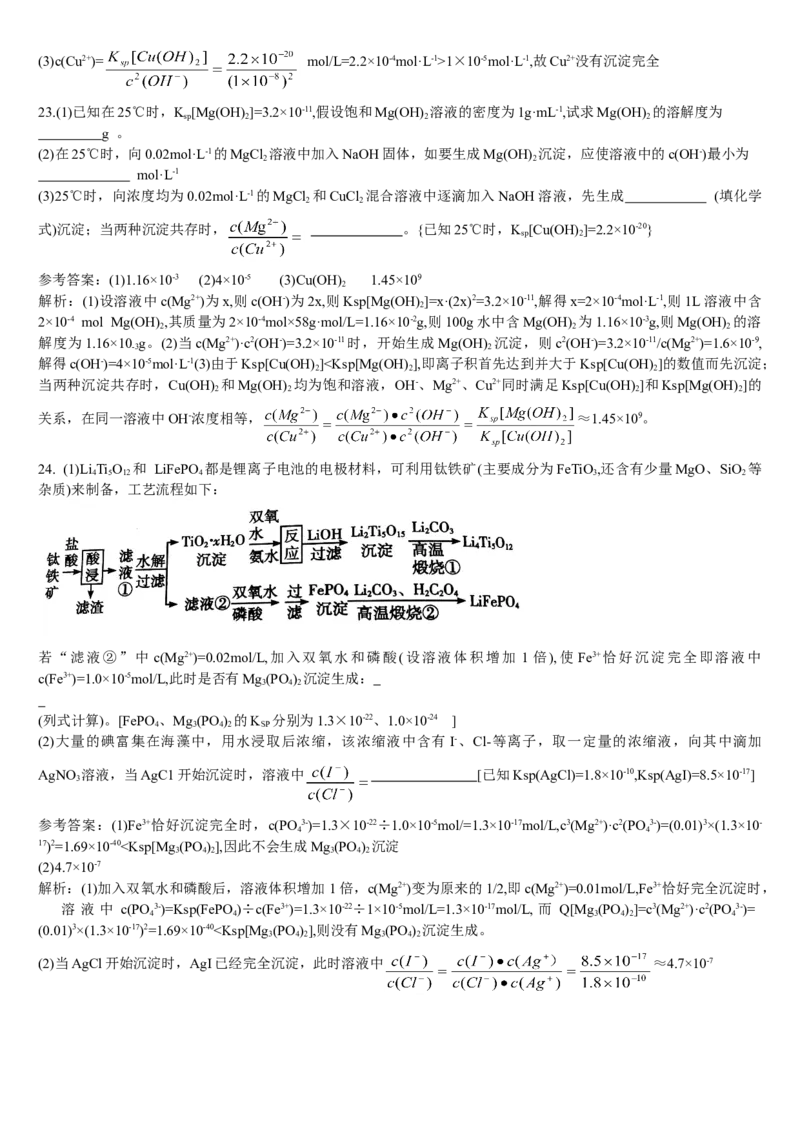
24. (1)Li Ti O 和 LiFePO 都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO,还含有少量MgO、SiO 等
4 5 12 4 3 2
杂质)来制备,工艺流程如下:
若“滤液②”中 c(Mg2+)=0.02mol/L,加入双氧水和磷酸(设溶液体积增加 1 倍),使 Fe3+恰好沉淀完全即溶液中
c(Fe3+)=1.0×10-5mol/L,此时是否有Mg(PO ) 沉淀生成:
3 4 2
(列式计算)。[FePO 、Mg(PO ) 的K 分别为1.3×10-22、1.0×10-24 ]
4 3 4 2 SP
(2)大量的碘富集在海藻中,用水浸取后浓缩,该浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加
AgNO 溶液,当AgC1开始沉淀时,溶液中 [已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17]
3第一课时 难溶电解质的沉淀溶解平衡基础练习题解析版
1.室温下向饱和AgC1溶液中加水,下列叙述正确的是( )
A.AgCl的溶解度增大
B.AgCl的溶解度、K 均不变
sp
C.AgCl的K 增大
sp
D.AgCl的溶解度、K 均增大
sp
解析:物质的溶解度和溶度积都是温度的函数,与溶液的浓度无关。所以向饱和 AgCl溶液中加水,AgCl的溶解度和
K 都不变,故B项正确。答案:B
sp
2.下列说法中,正确的是 ( )
A.难溶电解质在水溶液中达到沉淀溶解平衡时,沉淀和溶解均停止
B.K越小,难溶电解质在水中的溶解能力一定越弱
C.K的大小与离子浓度无关,只与难溶电解质的性质和温度有关
D.相同温度下,AgCl在水中的溶解能力与在NaCl溶液中的相同
解析:沉淀溶解平衡是动态平衡,沉淀和溶解速率相同,A项错误;K 可用来判断相同类型化合物在水中溶解度的大
sp
小,但化合物的类型不同,就不能进行直接判断,B项错误;K 的大小只与难溶电解质的性质和温度有关,C项正确;
sp
NaCl溶液对AgCl的溶解有抑制作用,即相同温度下,AgCl在水中的溶解能力比在NaCl溶液中大,D项错误。答案:
C
3.25℃时,已知K (AgCl)=1.8×10-10,K (AgBr)=7.8×10-13。现向等浓度NaCl和NaBr的混合溶液中逐滴加入稀AgNO
sp sp 3
溶液,先沉淀的是( )
A.AgCI B.AgBr C.同时沉淀 D.无法判断
解析:由于Ksp(AgCl)>Ksp(AgBr),等浓度的NaCl和NaBr混合溶液中逐滴加入AgNO 溶液,先达到AgBr的溶度积,
3
先析出AgBr沉淀。。答案:B
4.25℃时,在含有大量PbI 的饱和溶液中存在着平衡:PbI (s) Pb2+(aq)+2I-(aq), 加入KI溶液,下列说法正确的
2 2
是 ( )
A.溶液中Pb2+和I-浓度都增大
B.溶度积常数K 增大
sp
C.沉淀溶解平衡向左移动
D.溶液中Pb2+浓度增大
解析:加入KI溶液,c(I-)增大,沉淀溶解平衡逆向移动,c(Pb2+)减小,A、D项错误,C项正确;溶度积常数K 只与
sp
温度有关,B项错误。答案:C
5.已知CaCO 的K =2.8×10-9,现将浓度为2×10-4mol·L-1的NaCO 溶液与CaCl 溶液等体积混合,若要产生沉淀,则所
3 sp 2 3 2
用CaCl 溶液的浓度至少应为 ( )
2
A.2.8×10-2mol·L -1
B.1.4×10-5mol·L-1
C.2.8×10-5mol·L-1
D.5.6×10-5mol·L-1
解析:等体积混合后c(Na CO)=1×10-4mol/L,即溶液中c(CO2-)=1×10-4mol/L,根据Ksp= c(CO2-)·c(Ca2+)=2.8×10-9可知,
2 3 3 3
c(Ca2+)=2.8×10-9 / 1×10-4mol/L=2.8×10-5mol/L,则原溶液中CaCl 的最小浓度为混合溶液中c(Ca2+)的2倍,为2×2.8×10-
2
5mol/L=5.6×10-5mol/L。答案:B
6.向含有MgCO 固体的溶液中滴加少许浓盐酸(忽略体积变化),下列数值变小的是( )
3
A. c(H+) B. c(Mg2+) C. c(CO2-) D. Ksp(MgCO )
3 3
解析:MgCO 固体在溶液中存在溶解平衡:MgCO (s) Mg2+(aq)+CO 2-(aq),滴加少许浓盐酸,溶液中c(H+)增大,
3 3 3
A项错误;H+与CO2-反应,c(CO2-)减小,促使平衡正向移动,c(Mg2+)增大,B项错误,C项正确;K (MgCO )只与
3 3 sp 3
温度有关,数值保持不变,D项错误。答案:C
7.(双选)已知25℃时,K(HF)=3.6×10-4,K(CaF )=1.46×10-10,现向1L0.2mol·L-1HF溶液中加入1L0.2mol·L-1CaCl 溶液,则
a 2 2
下列说法中,正确的是( )
A.25℃时,0.1mol·L-1HF溶液中pH>1 B.K (CaF )随温度和浓度的变化而变化
SP 2
C.该体系中没有沉淀产生 D.该体系中HF与CaCl 反应产生沉淀
2解析:25℃时K(HF)=3.6×10-4,说明HF为弱酸,不可能完全电离,即25℃时,0.1mol·L-1HF溶液的pH>1,A项正确;
a
Ksp(CaF )与浓度无关,只与温度有关系,B项错误;混合溶液中c(Ca2+)=0.1mol/L,c(HF)=0.1mol/L,结合K(HF)=3.6×10-
2 a
4,可求出溶液中c(F-)=6×10-3mol/L,即离子积Q=0.1×(6×10-3)2=3.6×10-6>K (CaF )=1.46×10-10,则溶液中产生沉淀,C项错
sp 2
误,D项正确。答案:AD
8. (双选)在25℃时,FeS的K =6.3×10-18,CuS的K =1.3×10-36,ZnS的K =1.3×10-24,下列有关说法中正确的是( )
SP SP sp
A.FeS的溶解度大于CuS的溶解度
B.饱和CuS溶液中Cu2+浓度为 mol/L
C.向物质的量浓度相同的FeCl 、ZnCl 的混合液中加入少量NaS,只有FeS沉淀生成
2 2 2
D.向饱和ZnS溶液中加入少量ZnCl 固体,ZnS的K 变大
2 SP
解析:根据FeS和CuS的溶度积可知溶解度:FeS>CuS,A项正确;饱和CuS溶液中Cu2+的浓度为 mol/
L,B项正确;根据FeS和ZnS的溶度积可知,向等浓度的FeCl 、ZnCl 的混合液中加入少量NaS,只生成ZnS沉淀,C
2 2 2
项错误;温度不变,则ZnS的Ksp不变,D项错误。答案:AB
9.电离常数(K、K)、水解常数(K )、溶度积常数(K )等常数是表示、判断物质性质的重要常数,下列关于这些常数的
a b h sp
说法中正确的是( )
A.当温度升高时,弱酸、弱碱的电离常数(K、K)均变大
a b
B.K(HCN)K (BaCO)
4 sp 4 sp 3
D.水解常数的大小与温度、浓度有关,与溶液的酸碱性无关
解析:弱酸、弱碱的电离过程是吸热过程,温度升高促进电离,则K、K 均变大,A项正确;HCN和CHOOH均为
a b 3
一元弱酸,电离常数越大,溶液的中 H+越大,酸性越强,即浓度相同时,酸性:HCNc(A-)>c(OH-)
解析:根据 a、b 两点数据可确定 Ksp[Fe(OH) ]=c(Fe3+)•(10-12.7)3,Ksp[Cu(OH) ]=c(Cu2+)·(10-9.6)2,因 c(Fe3+)=c(Cu2+),故
3 2
Ksp[Fe(OH) ]2,
3 2 w
即HA部分电离,则HA为一元弱酸,C项错误;加入100 mL KOH溶液后,两溶液反应后得到 0.05mol/LKA和
0.05mol/LKOH 的混合溶液, A-部分水解, OH-浓度大于 0.05mol/L,A-的浓度小于 0.05mol/L, 即溶液中
c(K+)>c(OH-)>c(A-),D项错误。答案:A
11.下列物质的溶解度随温度升高而减小的是( )
①KNO ②Ca(OH) ③BaSO ④CO
3 2 4 2
A.①② B.②④ C.①③ D.①④
解析:Ca(OH) 的溶解度比较特殊,随温度的升高而减小,其他绝大多数物质随温度升高溶解度增大(气体除外)。答案:
2
B
12.下列对“难溶”的理解正确的是( )
A.在水中难溶的物质,在其他溶剂中也是难溶的
B.难溶就是绝对不溶
C.难溶就是溶解度相对较小,没有绝对不溶于水的电解质
D.如果向某溶液中加入足量另一种试剂时,生成了难溶性的电解质,则说明原溶液中的相应离子已沉淀完全
解析:难溶是指物质在水中的溶解度小于0.01g.。答案:C
13.下列说法中,正确的是 ( )A.两种难溶电解质,其中K 小的溶解度一定小
sp
B.溶液中存在两种可以与同一沉淀剂生成沉淀的离子,则K 小的一定先生成沉淀
sp
C.难溶电解质的K 与温度有关
sp
D.同离子效应使难溶电解质的溶解度变小,也使K 变小
sp
解析: K 只与难溶电解质的性质和温度有关。答案:C
sp
14.在BaSO 饱和溶液中加入少量的BaCl 溶液产生BaSO 沉淀,若以K 表示BaSO 的溶度积常数,则平衡后溶液中(
4 2 4 sp 4
) A. c(Ba2+)=c(SO 2-)=K 1/2
4 sp
B. c(Ba2+)• c(SO 2-)> K ,c(Ba2+)= c(SO 2-)
4 sp 4
C. c(Ba2+)• c(SO 2-)= K ,c(Ba2+)>c(SO 2-)
4 sp 4
D.c(Ba2+)·c(SO 2-)≠K , c(Ba2+)c(SO 2-)。答案:C
4 4 4
15.已知 Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13,Ksp(Ag CrO)=9×10-11。某溶液中含有 Cl-、Br-和 CrO2-,浓度均为
2 4 4
0.010mol·L-1,向该溶液中逐滴加入0.010mol·L-1的AgNO 溶液时,三种阴离子产生沉淀的先后顺序为( )
3
A Cl-、Br-、CrO2- B. CrO2-、Br-、Cl- C. Br-、Cl- 、CrO2- D. Br-、CrO2-、Cl-
4 4 4 4
解析:析出沉淀时,AgCl溶液中c(Ag+)=Ksp(AgCI)÷c(Cl- ) =1.56×10-10÷0.01mol·L-1=1.56×10-8mol·L-1;AgBr溶液中
Ksp(AgBr) ÷c(Br- )=7.7×10-13÷0.01mol·L-1=7.7×10-11mol/L;Ag CrO 溶 液 中 , c(Ag+)=
2 4
=3×10-4.5mol/L ,c(Ag+)越小越先生成沉淀,所以三种阴离子产生沉淀的先后顺
序为Br-、Cl-、CrO2- 答案:C
4
16.下列有关溶度积常数K 的说法正确的是 ( )
sp
A.常温下,向BaCO 饱和溶液中加入NaCO 固体,BaCO 的K 减小
3 2 3 3 sp
B.溶度积常数K 只受温度影响,温度升高K 减小
sp sp
C.溶度积常数K 只受温度影响,温度升高K 增大
sp sp
D.常温下,向Mg(OH) 饱和溶液中加入NaOH固体,Mg(OH) 的K 不变
2 2 sp
解析:温度不变,溶度积常数不变,故A项不正确、D项正确;大多数的难溶物温度升高,Ksp增大,但也有少数物
质相反如Ca(OH) ,故B、C均不正确。答案:D
2
17.已知:Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,Ksp(Ag CrO)=2.0×10-12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺
2 4
序正确的是 ( )
B. AgCl>AgI> Ag CrO B. AgCl> Ag CrO> AgI C. Ag CrO> AgCl>AgI D. Ag CrO> AgI> AgCl
2 4 2 4 2 4 2 4
解析:AgCl和AgI的结构相似,由Ksp可知AgCl饱和溶液中的c(Ag+)大于AgI饱和溶液中的c(Ag+);AgCl饱和溶液中
的 c2(Ag+)=Ksp=1.8×10-10,Ag CrO (s)=2 Ag+ (aq)+CrO2-(aq)的 Ksp=c2(Ag+)·c(CrO2-)=1/2c3(Ag+)=2.0×10-12,可得 Ag CrO
2 4 4 4 2 4
饱和溶液中的c(Ag+)大于AgCl饱和溶中的c(Ag+)。答案:C
18.将氨水滴加到盛有AgCl的试管中直至AgCl完全溶解,对上述过程的有关解释或叙述正确的是( )
A.所得溶液中c(Ag+)·c(Cl-)>Ksp(AgCl)
B.上述实验说明Cl-与NH +间有很强的结合力
4
C.所得溶液中形成了难电离的物质
D.上述过程中NH ·H O的电离常数增大
3 2
解析:一水合氨和溶解的AgCl反应生成络合物[Ag(NH)]OH,故A错误;反应生成[Ag(NH)]OH,说明Ag+和NH 有很
3 2 3 2 3
强的结合力,故B错误;一水合氨和溶解的AgCl反应生成络合物[Ag(NH)]OH,说明[Ag(NH)]OH比AgCl更难电离,
3 2 3 2
故C正确;弱电解质的电离平衡常数只与温度有关,温度不变,一水合氨电离平衡常数不变,故D错误。答案:C
19.如图所示,有T 、T 两种温度下两条BaSO 在水中的沉淀溶解平衡曲线,下列关于T 温度时BaSO 在水中的沉淀
1 2 4 1 4
溶解平衡曲线的说法不正确的是 ( )
A.加入NaSO 可使溶液由a点变为b点
2 4
B.在T 曲线上方区域(不含曲线)任意一点时,均有BaSO 沉淀生成
1 4
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
D.升温可使溶液由b点变为d点
解析:A项,加入NaSO ,c(SO 2-)增大,K 不变,c(Ba2+)减小,正确;B项,
2 4 4 sp
在T 曲线上方任意一点,由于Q>K ,所以均有BaSO 沉淀生成,正确;C
1 sp 4项,不饱和溶液蒸发溶剂,c(SO 2-)、c(Ba2+)均增大,正确;D项,升温,K 增大,c(SO 2-)、c(Ba2+)均增大,错误。答
4 sp 4
案:D
20.某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示。
请回答下列问题:
(1)A点表示Ag SO 是 (填“饱和”或“不饱和”)溶液。
2 4
(2)B点对应的Ksp (填“>”“<”或“=”)C点对应的Ksp。
(3)现将足量的Ag SO 分别放入下列三种溶液中
2 4
a.40mL0.01mol·L-1KSO 溶液
2 4
b.10mL蒸馏水
c.10mL0.02mol·L-1HSO 溶液
2 4
则Ag SO 的溶解程度由大到小的排列顺序为 (填字母)。
2 4
参考答案:(1)不饱和 (2)= (3)b>a>c
解析:(1)A点没有达到平衡状态。
(2)K 只与温度有关。
sp
(3) c(SO 2-)越大,难溶电解质的溶解平衡逆向移动程度越大,Ag SO 的溶解程度越小。
4 2 4
21.已知:25℃时,Fe(OH) 的溶度积常数为2.8×10-3
3
(1)Fe(OH) 的溶解平衡方程式为 ,
3
Fe(OH) 的溶度积表达式为 。
3
(2)当pH=3时,溶液中c(Fe3+)= mol/L。
(3)若某温度时,Fe(OH) 和Mg(OH) 的K 分别为a和b,则3Mg(OH)(s)+2Fe3+ 2Fe(OH) (s)+3Mg2+的化学平衡常数
3 2 sp 3
K= (用含a、b的式子表示)。
参考答案:(1)Fe(OH) (s) Fe3+(aq)+3OH-(aq) Ksp[Fe(OH) ]= c(Fe3+)•c3(OH)
3 3
(2)2.8×10-6 (3)b2/a2
解析:(1)Fe(OH) 达到沉淀溶解平衡时,溶解与沉淀是可逆的过程,可表示为Fe(OH) (s) Fe3+(aq)+3OH-(aq),其中
3 3
Fe(OH) 的溶度积可表示为 Ksp[Fe(OH) ]= c(Fe3+)•c3(OH)c(OH-)(2)pH=3 时,溶液中 c(OH-)=1×10-11mol/L,溶液中
3 3
c(Fe3+)=2.8×10-39/ (1×10-11)3mol/L=2.8×10-6mol/L.(3)K=
22.(1)在25℃下,向浓度均为0.1mol·L-1的MgCl 和CuCl 混合溶液中逐滴加入氨水,先生成 (填化学式)
2 2
沉淀,生成该沉淀的离子方程式为
已知25℃时K [Mg(OH) ]=1.8×10-11,K [Cu(OH) ]=2.2×10-20
sp 2 sp 2
(2)向 BaCl 溶液中加入 AgNO 和 KBr,当两种沉淀共存时, 。[K (AgBr)=5.4×10-13,K
2 3 sp sp
(AgCl)=2.0×10-10]
(3)已知Cu(OH) 的溶度积常数K =2.2×10-20。室温时在CuCl 溶液中滴加NaOH溶液,当溶液pH为6时,通过计算说
2 sp 2
明Cu2+是否沉淀完全:
(提示:当某离子浓度小于1×10-5mol·L-1时可以认为该离子沉淀完全)
解析:(1)Mg(OH) 和Cu(OH) 类型相同,Ksp[Mg(OH) ]>Ksp[Cu(OH) ],开始溶液中Mg2+和Cu2+浓度相等,加入氨水先
2 2 2 2
达到Cu(OH) 的溶度积,即先生成Cu(OH) 沉淀,其离子方程式为Cu2++2NH·H O=Cu(OH) ↓++2NH +(2)两种沉淀共
2 2 3 2 2 4
存,则溶液中 =2.7×10-3。(3)pH=6时溶液中c(OH-)=1×10-
14÷1×10-6mol/L=1×10-8mol/L, 则 c(Cu2+)=Ksp[Cu(OH) ] /c2 (OH-)=2.2×10-20/(1×10-8)2mol·L-1=2.2×10-4mol·L-1>1×10-
2
5mol·L-1,故Cu2+没有沉淀完全。
参考答案:(1)Cu(OH) Cu2++2NH·H O=Cu(OH) ↓+2NH+
2 3 2 2 4
(2)2.7×10-3(3)c(Cu2+)= mol/L=2.2×10-4mol·L-1>1×10-5mol·L-1,故Cu2+没有沉淀完全
23.(1)已知在25℃时,K [Mg(OH) ]=3.2×10-11,假设饱和Mg(OH) 溶液的密度为1g·mL-1,试求Mg(OH) 的溶解度为
sp 2 2 2
g 。
(2)在25℃时,向0.02mol·L-1的MgCl 溶液中加入NaOH固体,如要生成Mg(OH) 沉淀,应使溶液中的c(OH-)最小为
2 2
mol·L-1
(3)25℃时,向浓度均为0.02mol·L-1的MgCl 和CuCl 混合溶液中逐滴加入NaOH溶液,先生成 (填化学
2 2
式)沉淀;当两种沉淀共存时, 。{已知25℃时,K [Cu(OH) ]=2.2×10-20}
sp 2
参考答案:(1)1.16×10-3 (2)4×10-5 (3)Cu(OH) 1.45×109
2
解析:(1)设溶液中c(Mg2+)为x,则c(OH-)为2x,则Ksp[Mg(OH) ]=x·(2x)2=3.2×10-11,解得x=2×10-4mol·L-1,则1L溶液中含
2
2×10-4 mol Mg(OH) ,其质量为2×10-4mol×58g·mol/L=1.16×10-2g,则100g水中含Mg(OH) 为1.16×10-3g,则Mg(OH) 的溶
2 2 2
解度为1.16×10 g。(2)当c(Mg2+)·c2(OH-)=3.2×10-11时,开始生成Mg(OH) 沉淀,则c2(OH-)=3.2×10-11/c(Mg2+)=1.6×10-9,
-3 2
解得c(OH-)=4×10-5mol·L-1(3)由于Ksp[Cu(OH) ]