文档内容
第二课时 化学电源同步基础练习题
1.关于铅蓄电池的说法中正确的是 ( )
A.在放电时,正极发生的反应是:Pb+SO2-=PbSO+2e-
4 4
B.在放电时,该电池的负极材料是铅板
C.在充电时,电池中硫酸的浓度不断变小
D.在充电时,阳极发生的反应是:PbSO +2e-=Pb+ SO 2-
4 4
2.爱迪生蓄电池在充电和放电时发生的反应为Fe+NiO +2H O Fe(OH) +Ni(OH) ,下列对该蓄电池的推断错误的是(
2 2 2 2
)
①放电时,Fe参与负极反应,NiO 参与正极反应
2
②放电时,电解质溶液中的阴离子向正极移动
③放电时,负极上的电极反应式为Fe+2H O-2e-=Fe(OH) +2H+
2 2
④该蓄电池的电极必须浸入某种碱性电解质溶液中
A.①② B.②③ C.①③ D.③④
3.镍-镉电池是一种可充电的“干电池”,使用寿命长达10~15年。其总反应为Cd+2NiO(OH)+2H O
2
2Ni(OH) +Cd(OH) 。下列说法不正确的是( )
2 2
A.放电时,负极发生了氧化反应,反应为Cd+2OH-+2e-=Cd(OH)
2
B.放电时,正极反应为NiO(OH)+H O +e- = Ni(OH) - +OH-
2 2
C.电池工作时,负极区pH增大,正极区pH减小
D.该电池充电时将电能转化为化学能
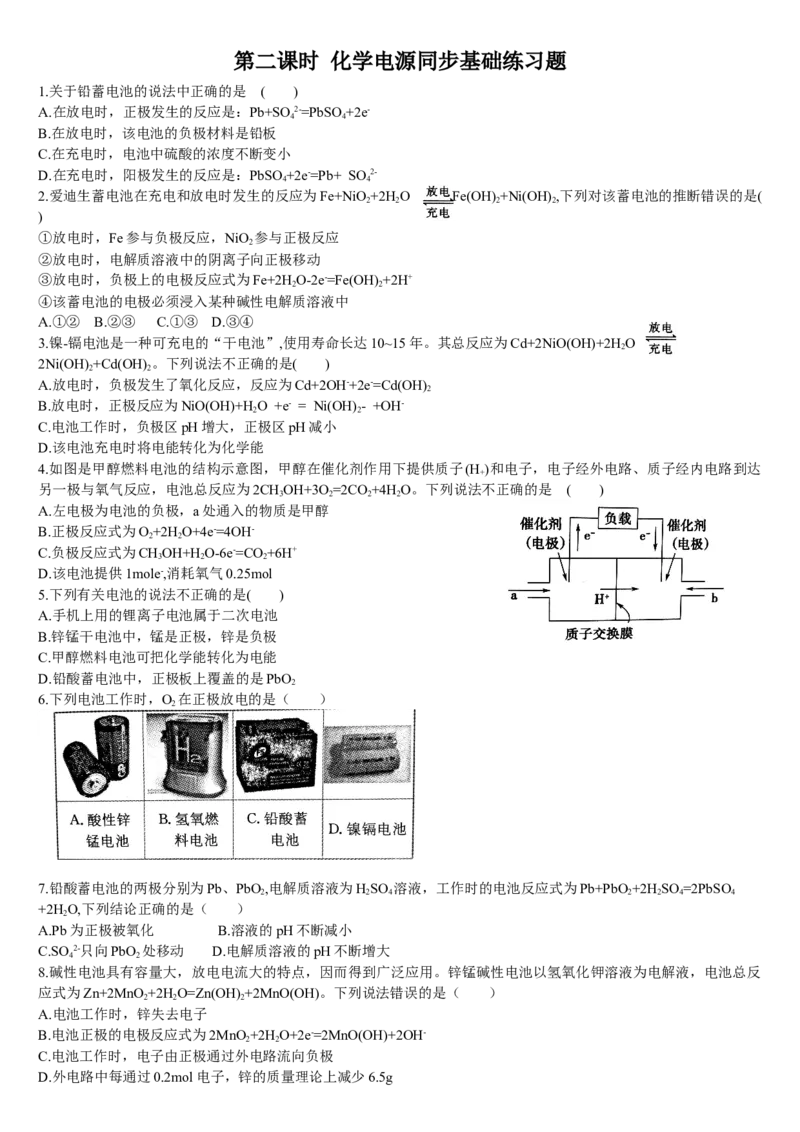
4.如图是甲醇燃料电池的结构示意图,甲醇在催化剂作用下提供质子(H )和电子,电子经外电路、质子经内电路到达
+
另一极与氧气反应,电池总反应为2CHOH+3O =2CO +4H O。下列说法不正确的是 ( )
3 2 2 2
A.左电极为电池的负极,a处通入的物质是甲醇
B.正极反应式为O+2H O+4e-=4OH-
2 2
C.负极反应式为CHOH+H O-6e-=CO +6H+
3 2 2
D.该电池提供1mole-,消耗氧气0.25mol
5.下列有关电池的说法不正确的是( )
A.手机上用的锂离子电池属于二次电池
B.锌锰干电池中,锰是正极,锌是负极
C.甲醇燃料电池可把化学能转化为电能
D.铅酸蓄电池中,正极板上覆盖的是PbO
2
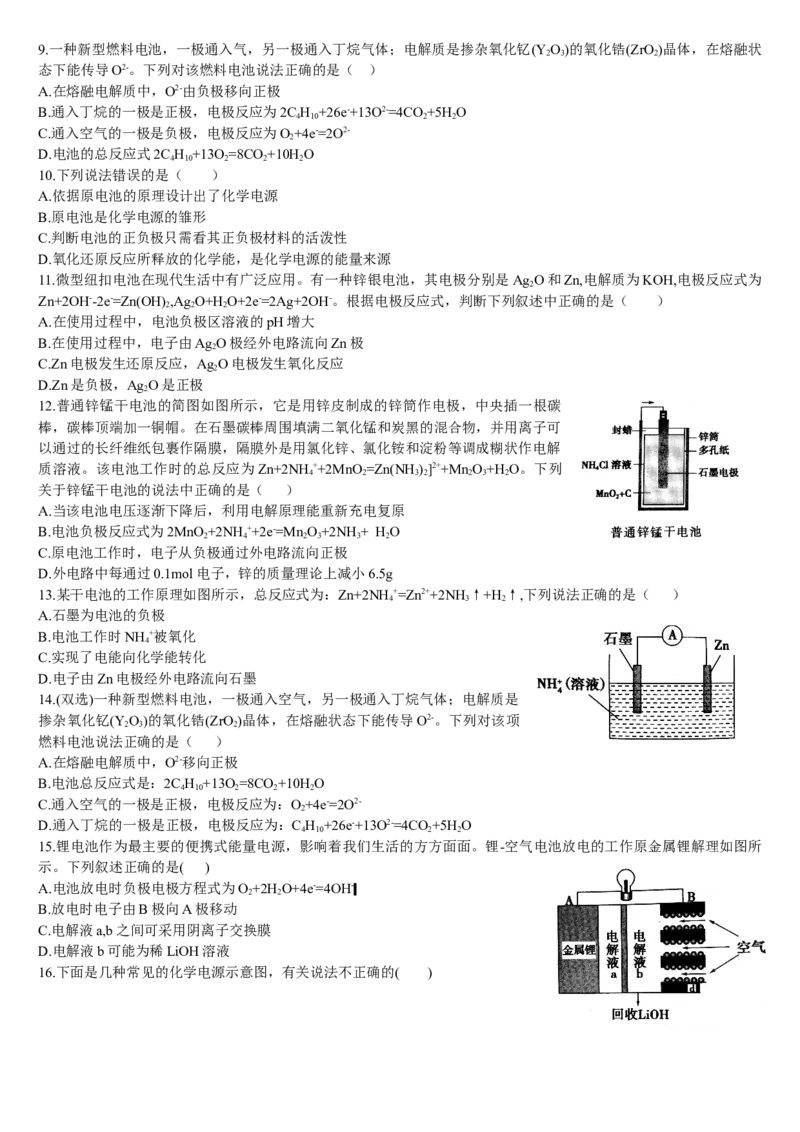
6.下列电池工作时,O 在正极放电的是( )
2
7.铅酸蓄电池的两极分别为Pb、PbO ,电解质溶液为HSO 溶液,工作时的电池反应式为Pb+PbO+2H SO =2PbSO
2 2 4 2 2 4 4
+2H O,下列结论正确的是( )
2
A.Pb为正极被氧化 B.溶液的pH不断减小
C.SO 2-只向PbO 处移动 D.电解质溶液的pH不断增大
4 2
8.碱性电池具有容量大,放电电流大的特点,因而得到广泛应用。锌锰碱性电池以氢氧化钾溶液为电解液,电池总反
应式为Zn+2MnO +2H O=Zn(OH) +2MnO(OH)。下列说法错误的是( )
2 2 2
A.电池工作时,锌失去电子
B.电池正极的电极反应式为2MnO +2H O+2e-=2MnO(OH)+2OH-
2 2
C.电池工作时,电子由正极通过外电路流向负极
D.外电路中每通过0.2mol电子,锌的质量理论上减少6.5g9.一种新型燃料电池,一极通入气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y O)的氧化锆(ZrO)晶体,在熔融状
2 3 2
态下能传导O2-。下列对该燃料电池说法正确的是( )
A.在熔融电解质中,O2-由负极移向正极
B.通入丁烷的一极是正极,电极反应为2C H +26e-+13O2-=4CO+5HO
4 10 2 2
C.通入空气的一极是负极,电极反应为O+4e-=2O2-
2
D.电池的总反应式2C H +13O =8CO +10H O
4 10 2 2 2
10.下列说法错误的是( )
A.依据原电池的原理设计出了化学电源
B.原电池是化学电源的雏形
C.判断电池的正负极只需看其正负极材料的活泼性
D.氧化还原反应所释放的化学能,是化学电源的能量来源
11.微型纽扣电池在现代生活中有广泛应用。有一种锌银电池,其电极分别是Ag O和Zn,电解质为KOH,电极反应式为
2
Zn+2OH--2e-=Zn(OH) ,Ag O+HO+2e-=2Ag+2OH-。根据电极反应式,判断下列叙述中正确的是( )
2 2 2
A.在使用过程中,电池负极区溶液的pH增大
B.在使用过程中,电子由Ag O极经外电路流向Zn极
2
C.Zn电极发生还原反应,Ag O电极发生氧化反应
2
D.Zn是负极,Ag O是正极
2
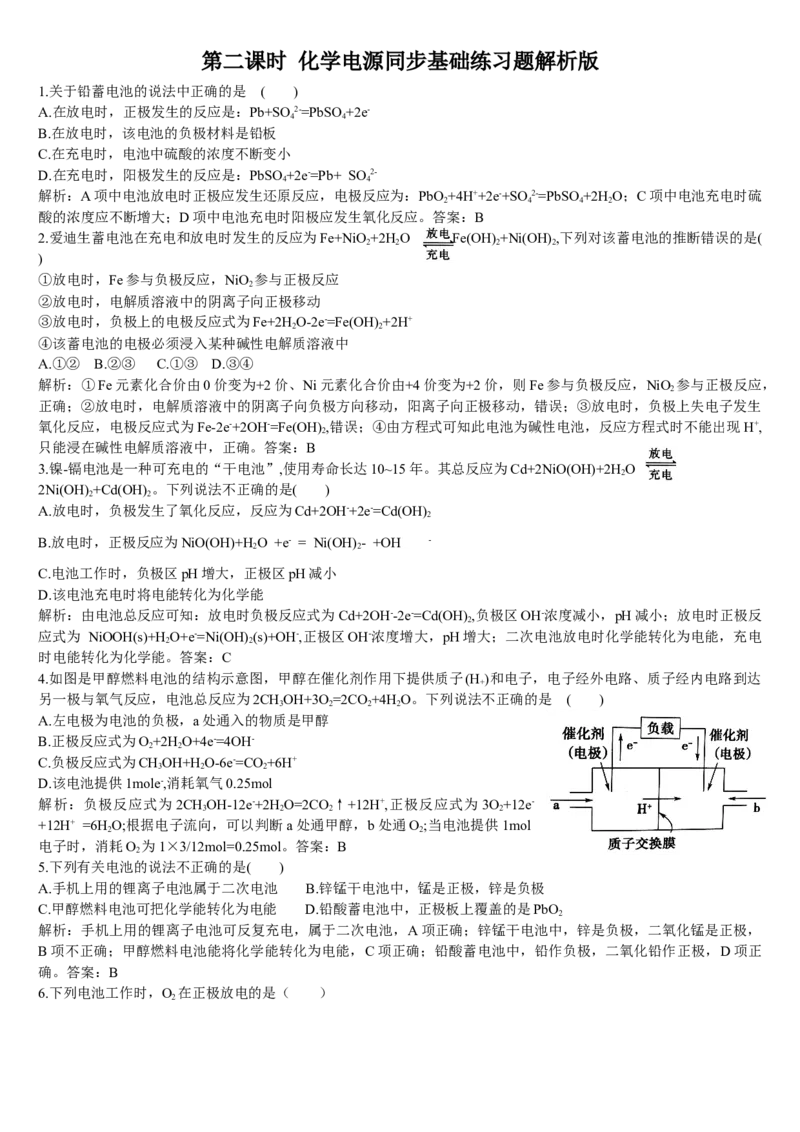
12.普通锌锰干电池的简图如图所示,它是用锌皮制成的锌筒作电极,中央插一根碳
棒,碳棒顶端加一铜帽。在石墨碳棒周围填满二氧化锰和炭黑的混合物,并用离子可
以通过的长纤维纸包裹作隔膜,隔膜外是用氯化锌、氯化铵和淀粉等调成糊状作电解
质溶液。该电池工作时的总反应为Zn+2NH ++2MnO=Zn(NH)]2++Mn O+H O。下列
4 2 3 2 2 3 2
关于锌锰干电池的说法中正确的是( )
A.当该电池电压逐渐下降后,利用电解原理能重新充电复原
B.电池负极反应式为2MnO +2NH++2e-=Mn O+2NH + HO
2 4 2 3 3 2
C.原电池工作时,电子从负极通过外电路流向正极
D.外电路中每通过0.1mol电子,锌的质量理论上减小6.5g
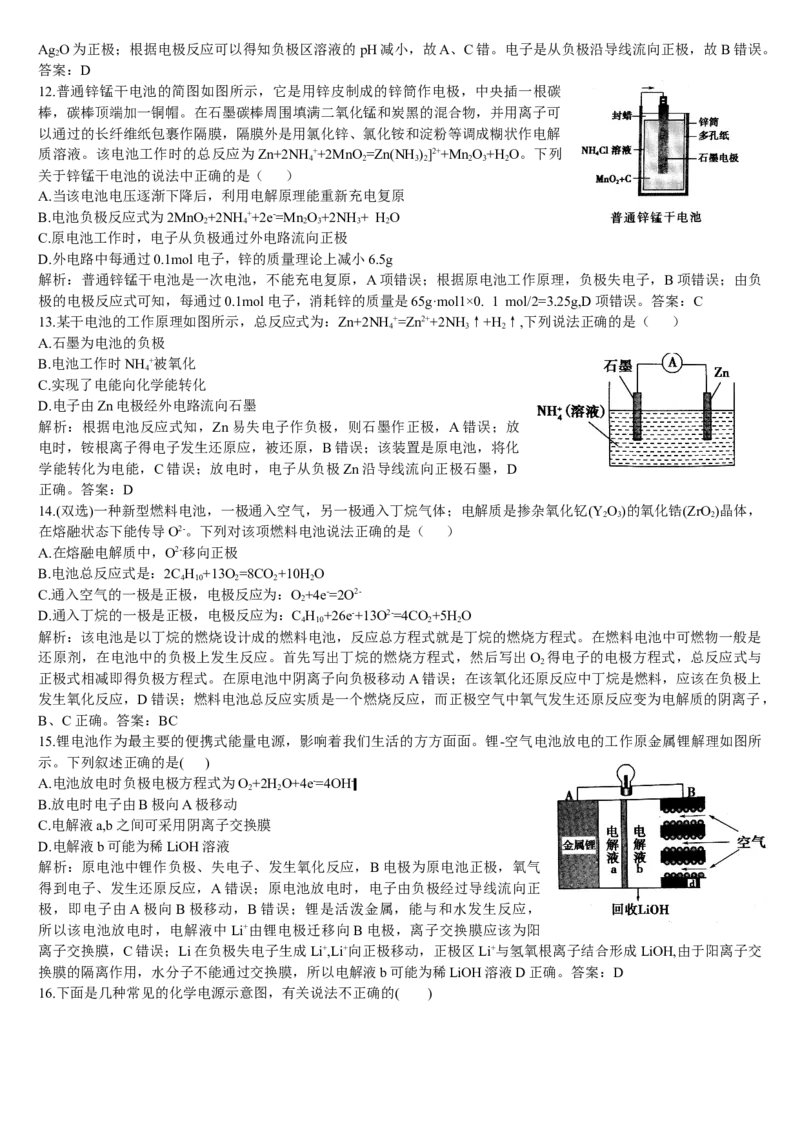
13.某干电池的工作原理如图所示,总反应式为:Zn+2NH +=Zn2++2NH↑+H ↑,下列说法正确的是( )
4 3 2
A.石墨为电池的负极
B.电池工作时NH +被氧化
4
C.实现了电能向化学能转化
D.电子由Zn电极经外电路流向石墨
14.(双选)一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是
掺杂氧化钇(Y O)的氧化锆(ZrO)晶体,在熔融状态下能传导O2-。下列对该项
2 3 2
燃料电池说法正确的是( )
A.在熔融电解质中,O2-移向正极
B.电池总反应式是:2C H +13O =8CO +10H O
4 10 2 2 2
C.通入空气的一极是正极,电极反应为:O+4e-=2O2-
2
D.通入丁烷的一极是正极,电极反应为:C H +26e-+13O2-=4CO+5H O
4 10 2 2
15.锂电池作为最主要的便携式能量电源,影响着我们生活的方方面面。锂-空气电池放电的工作原金属锂解理如图所
示。下列叙述正确的是( )
A.电池放电时负极电极方程式为O
2
+2H
2
O+4e-=4OH-
B.放电时电子由B极向A极移动
C.电解液a,b之间可采用阴离子交换膜
D.电解液b可能为稀LiOH溶液
16.下面是几种常见的化学电源示意图,有关说法不正确的( )A.上述电池分别属于一次电池、二次电池和燃料电池
B.干电池在长时间使用后,锌筒被破坏
C.铅蓄电池工作过程中,每通过2mol电子,负极质量减轻207g
D.氢氧燃料电池是一种具有应用前景的绿色电源
17.镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式
进行:
Cd+2NiO(OH)+2H O Cd(OH) +2Ni(OH) 。有关该电池的说法正确的是( )
2 2 2
A. 放电时,正极反应为NiO(OH)+H O +e- = Ni(OH) - +OH-
2 2
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH向正极移动
18.一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为 CHCHOH-4e-+H O=CHCOOH+4H+。下列有关说
3 2 2 3
法正确的是( )
A.检测时,电解质溶液中的H+向负极移动
B.若有0.4mol电子转移,则在标准状况下消耗4.48L氧气
C.电池反应的化学方程式为CHCHOH+O =CHCOOH+H O
3 2 2 3 2
D.正极上发生的反应为O+4e-+2H O=4OH-
2 2
19.燃料电池是利用燃料(如CO、H、CH 等)与氧气反应,将反应产生的化学能转变为电能的装置,通常用氢氧化钾溶
2 4
液作为电解质溶液。完成下列关于甲烷(CH)燃料电池的填空:
4
(1)甲烷与氧气反应的化学方程式为
(2)已知燃料电池的总反应式为CH+2O +2KOH=K CO+3H O,电池中有一极的电极反应为CH+10H--8e-=CO 2-+7H O,这
4 2 2 3 2 4 3 2
个电极是燃料电池的 (填“正极”或“负极”),另一个电极上的电极反应式为
(3)随着电池不断放电,电解质溶液的碱性 (填 “增大”“减小”或“不变”)。
(4)通常情况下,甲烷燃料电池的能量利用率 (填“大于”“小于”或“等于”)甲烷燃烧的能量利用率。
20.化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)Zn-MnO 干电池应用广泛,其电解质溶液是ZnCl-NH Cl混合溶液。该电池的负极材料是 ,电池工作
2 2 4
时,电子流向 (填“正极”或“负极”)。若ZnCl-NH Cl混合溶液中含有杂质Cu2+,会加速某电极的反应,
2 4
其主要原因是
(2)铅酸蓄电池是常用的化学电源,其电极材料分别是 Pb 和PbO ,电解液为硫酸。该电池总反应式为 Pb+ PbO
2 2
+2H SO =2PbSO +2H O
2 4 4 2
请根据上述情况判断:
该蓄电池放电时,电解质溶液中阴离子移向 (填“正极”或“负极”);正极附近溶液的酸性
(填“增强”“减弱”或“不变”);放电时,负极的电极反应式为
(3)氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅酸蓄电池。若电解质为 KOH溶液,则氢氧燃料电池
的负极反应式为 。该电池工作时,外电路每流过2mole-,消耗标准状况下氧气 L
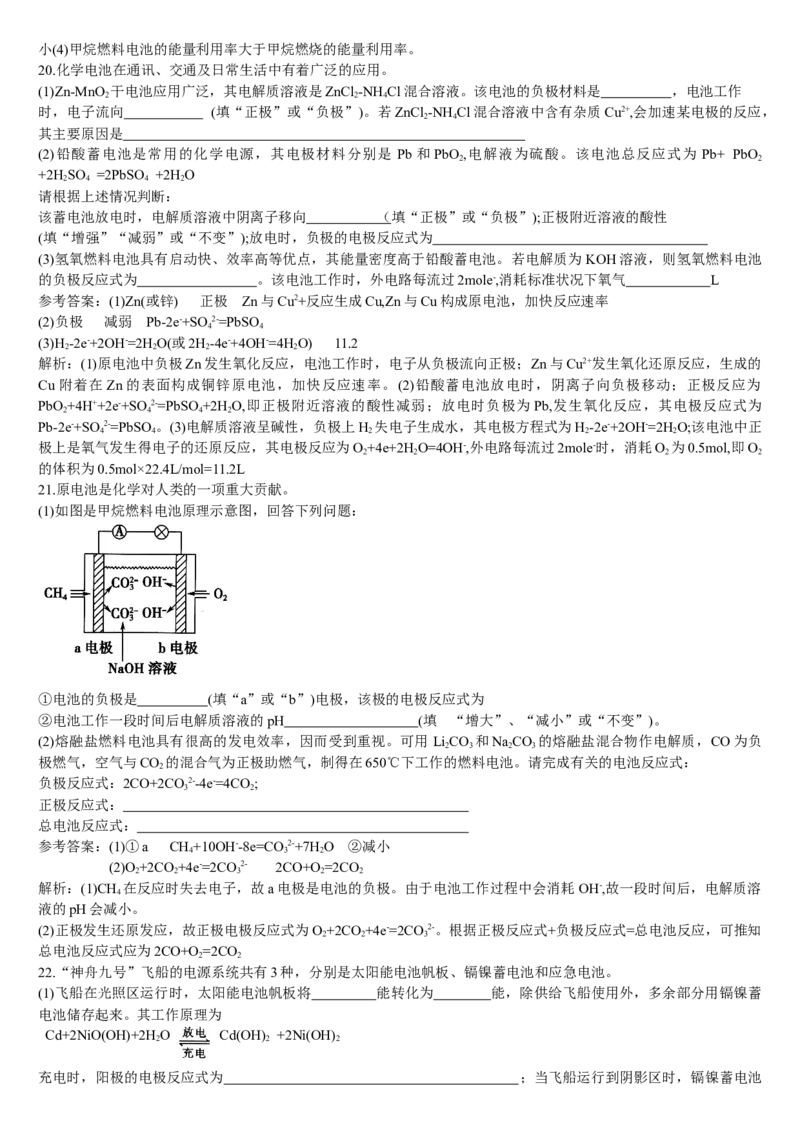
21.原电池是化学对人类的一项重大贡献。
(1)如图是甲烷燃料电池原理示意图,回答下列问题:①电池的负极是 (填“a”或“b”)电极,该极的电极反应式为
②电池工作一段时间后电解质溶液的pH (填 “增大”、“减小”或“不变”)。
(2)熔融盐燃料电池具有很高的发电效率,因而受到重视。可用 LiCO 和NaCO 的熔融盐混合物作电解质,CO为负
2 3 2 3
极燃气,空气与CO 的混合气为正极助燃气,制得在650℃下工作的燃料电池。请完成有关的电池反应式:
2
负极反应式:2CO+2CO2--4e-=4CO ;
3 2
正极反应式:
总电池反应式:
22.“神舟九号”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。
(1)飞船在光照区运行时,太阳能电池帆板将 能转化为 能,除供给飞船使用外,多余部分用镉镍蓄
电池储存起来。其工作原理为
Cd+2NiO(OH)+2H O Cd(OH) +2Ni(OH)
2 2 2
充电时,阳极的电极反应式为 ;当飞船运行到阴影区时,镉镍蓄电池
开始为飞船供电,此时负极附近溶液的碱性 (填“增大”“减小”或“不变”)。
(2)紧急状况下,应急电池会自动启动,工作原理为Zn+Ag O+HO 2Ag+Zn(OH) ,负极的电极反应式为
2 2 2第二课时 化学电源同步基础练习题解析版
1.关于铅蓄电池的说法中正确的是 ( )
A.在放电时,正极发生的反应是:Pb+SO2-=PbSO+2e-
4 4
B.在放电时,该电池的负极材料是铅板
C.在充电时,电池中硫酸的浓度不断变小
D.在充电时,阳极发生的反应是:PbSO +2e-=Pb+ SO 2-
4 4
解析:A项中电池放电时正极应发生还原反应,电极反应为:PbO +4H++2e-+SO2-=PbSO+2HO;C项中电池充电时硫
2 4 4 2
酸的浓度应不断增大;D项中电池充电时阳极应发生氧化反应。答案:B
2.爱迪生蓄电池在充电和放电时发生的反应为Fe+NiO +2H O Fe(OH) +Ni(OH) ,下列对该蓄电池的推断错误的是(
2 2 2 2
)
①放电时,Fe参与负极反应,NiO 参与正极反应
2
②放电时,电解质溶液中的阴离子向正极移动
③放电时,负极上的电极反应式为Fe+2H O-2e-=Fe(OH) +2H+
2 2
④该蓄电池的电极必须浸入某种碱性电解质溶液中
A.①② B.②③ C.①③ D.③④
解析:①Fe元素化合价由0价变为+2价、Ni元素化合价由+4价变为+2价,则Fe参与负极反应,NiO 参与正极反应,
2
正确;②放电时,电解质溶液中的阴离子向负极方向移动,阳离子向正极移动,错误;③放电时,负极上失电子发生
氧化反应,电极反应式为Fe-2e-+2OH-=Fe(OH) ,错误;④由方程式可知此电池为碱性电池,反应方程式时不能出现H+,
2
只能浸在碱性电解质溶液中,正确。答案:B
3.镍-镉电池是一种可充电的“干电池”,使用寿命长达10~15年。其总反应为Cd+2NiO(OH)+2H O
2
2Ni(OH) +Cd(OH) 。下列说法不正确的是( )
2 2
A.放电时,负极发生了氧化反应,反应为Cd+2OH-+2e-=Cd(OH)
2
B.放电时,正极反应为NiO(OH)+H O +e- = Ni(OH) - +OH -
2 2
C.电池工作时,负极区pH增大,正极区pH减小
D.该电池充电时将电能转化为化学能
解析:由电池总反应可知:放电时负极反应式为Cd+2OH--2e-=Cd(OH) ,负极区OH-浓度减小,pH减小;放电时正极反
2
应式为 NiOOH(s)+H O+e-=Ni(OH) (s)+OH-,正极区OH-浓度增大,pH增大;二次电池放电时化学能转化为电能,充电
2 2
时电能转化为化学能。答案:C
4.如图是甲醇燃料电池的结构示意图,甲醇在催化剂作用下提供质子(H )和电子,电子经外电路、质子经内电路到达
+
另一极与氧气反应,电池总反应为2CHOH+3O =2CO +4H O。下列说法不正确的是 ( )
3 2 2 2
A.左电极为电池的负极,a处通入的物质是甲醇
B.正极反应式为O+2H O+4e-=4OH-
2 2
C.负极反应式为CHOH+H O-6e-=CO +6H+
3 2 2
D.该电池提供1mole-,消耗氧气0.25mol
解析:负极反应式为2CHOH-12e-+2H O=2CO↑+12H+,正极反应式为3O+12e-
3 2 2 2
+12H+ =6H O;根据电子流向,可以判断a处通甲醇,b处通O;当电池提供1mol
2 2
电子时,消耗O 为1×3/12mol=0.25mol。答案:B
2
5.下列有关电池的说法不正确的是( )
A.手机上用的锂离子电池属于二次电池 B.锌锰干电池中,锰是正极,锌是负极
C.甲醇燃料电池可把化学能转化为电能 D.铅酸蓄电池中,正极板上覆盖的是PbO
2
解析:手机上用的锂离子电池可反复充电,属于二次电池,A项正确;锌锰干电池中,锌是负极,二氧化锰是正极,
B项不正确;甲醇燃料电池能将化学能转化为电能,C项正确;铅酸蓄电池中,铅作负极,二氧化铅作正极,D项正
确。答案:B
6.下列电池工作时,O 在正极放电的是( )
2解析:A项正极上放电的为NH +,错误;B项H 在负极发生氧化反应,O 在正极发生还原反应,正确;C项正极上放
4 2 2
电的为PbO ,错误;D项电解质溶液为KOH溶液时,正极上放电的为NiO(OH),D错误。答案:B
2
7.铅酸蓄电池的两极分别为Pb、PbO ,电解质溶液为HSO 溶液,工作时的电池反应式为Pb+PbO+2H SO =2PbSO
2 2 4 2 2 4 4
+2H O,下列结论正确的是( )
2
A.Pb为正极被氧化 B.溶液的pH不断减小
C.SO 2-只向PbO 处移动 D.电解质溶液的pH不断增大
4 2
解析:由化合价变化可知Pb是负极被氧化,A项错误;由总反应式可看出HSO 不断被消耗,溶液pH不断增大,B
2 4
项错误,D项正确;该电池工作时,SO 2-等阴离子向负极移动,由于PbO 是正极,Pb是负极,即SO 2-向Pb电极移动,
4 2 4
C项错误。答案:D
8.碱性电池具有容量大,放电电流大的特点,因而得到广泛应用。锌锰碱性电池以氢氧化钾溶液为电解液,电池总反
应式为Zn+2MnO +2H O=Zn(OH) +2MnO(OH)。下列说法错误的是( )
2 2 2
A.电池工作时,锌失去电子
B.电池正极的电极反应式为2MnO +2H O+2e-=2MnO(OH)+2OH-
2 2
C.电池工作时,电子由正极通过外电路流向负极
D.外电路中每通过0.2mol电子,锌的质量理论上减少6.5g
解析:总反Zn+2MnO +2H O=Zn(OH) +2MnO(OH)中锌元素被氧化,可判断Zn为负极,A项正确;根据总反应和化
2 2 2
合价变化可写出正极反应为2MnO +2H O+2e-=2MnO(OH)+2OH-,B项正确;电子从负极流出经外电路流向正极,C项
2 2
错误,当外电路中通过0.2mol电子,参加反应的锌理论上为0.1mol,其质量减少6.5g,D项正确。答案:C
9.一种新型燃料电池,一极通入气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y O)的氧化锆(ZrO)晶体,在熔融状
2 3 2
态下能传导O2-。下列对该燃料电池说法正确的是( )
A.在熔融电解质中,O2-由负极移向正极
B.通入丁烷的一极是正极,电极反应为2C H +26e-+13O2-=4CO+5HO
4 10 2 2
C.通入空气的一极是负极,电极反应为O+4e-=2O2-
2
D.电池的总反应式2C H +13O =8CO +10H O
4 10 2 2 2
解析:燃料电池中,通入丁烷的电极为极,通入空气的电极为正极。原电池中,O2-等阴离子向负极移动,A项错误;
丁烷在负极发生氧化反应,其电极反应式为2C H -26e-+13O2-=4CO+5HO,B项错误;正极是O 得电子被还原为O2-,其
4 10 2 2 2
电极反应式为O+4e-=2O2-,C项错误;电池总反应与丁烷燃烧的化学方程式相同,均为 2C H +13O =8CO +10H O,D项
2 4 10 2 2 2
正确。答案:D
10.下列说法错误的是( )
A.依据原电池的原理设计出了化学电源
B.原电池是化学电源的雏形
C.判断电池的正负极只需看其正负极材料的活泼性
D.氧化还原反应所释放的化学能,是化学电源的能量来源
解析:判断电池的正负极不仅与电极材料有关,还与电解质溶液有关误;电子是从负极沿导线流向正极,故 B错误。
答案:C
11.微型纽扣电池在现代生活中有广泛应用。有一种锌银电池,其电极分别是Ag O和Zn,电解质为KOH,电极反应式为
2
Zn+2OH--2e-=Zn(OH) ,Ag O+HO+2e-=2Ag+2OH-。根据电极反应式,判断下列叙述中正确的是( )
2 2 2
A.在使用过程中,电池负极区溶液的pH增大
B.在使用过程中,电子由Ag O极经外电路流向Zn极
2
C.Zn电极发生还原反应,Ag O电极发生氧化反应
2
D.Zn是负极,Ag O是正极
2
解析:根据原电池原理:负极失去电子发生氧化反应,正极得到电子发生还原反应,可以判断该原电池中 Zn为负极,Ag O为正极;根据电极反应可以得知负极区溶液的pH减小,故A、C错。电子是从负极沿导线流向正极,故B错误。
2
答案:D
12.普通锌锰干电池的简图如图所示,它是用锌皮制成的锌筒作电极,中央插一根碳
棒,碳棒顶端加一铜帽。在石墨碳棒周围填满二氧化锰和炭黑的混合物,并用离子可
以通过的长纤维纸包裹作隔膜,隔膜外是用氯化锌、氯化铵和淀粉等调成糊状作电解
质溶液。该电池工作时的总反应为Zn+2NH ++2MnO=Zn(NH)]2++Mn O+H O。下列
4 2 3 2 2 3 2
关于锌锰干电池的说法中正确的是( )
A.当该电池电压逐渐下降后,利用电解原理能重新充电复原
B.电池负极反应式为2MnO +2NH++2e-=Mn O+2NH + HO
2 4 2 3 3 2
C.原电池工作时,电子从负极通过外电路流向正极
D.外电路中每通过0.1mol电子,锌的质量理论上减小6.5g
解析:普通锌锰干电池是一次电池,不能充电复原,A项错误;根据原电池工作原理,负极失电子,B项错误;由负
极的电极反应式可知,每通过0.1mol电子,消耗锌的质量是65g·mol1×0. 1 mol/2=3.25g,D项错误。答案:C
13.某干电池的工作原理如图所示,总反应式为:Zn+2NH +=Zn2++2NH↑+H ↑,下列说法正确的是( )
4 3 2
A.石墨为电池的负极
B.电池工作时NH +被氧化
4
C.实现了电能向化学能转化
D.电子由Zn电极经外电路流向石墨
解析:根据电池反应式知,Zn易失电子作负极,则石墨作正极,A错误;放
电时,铵根离子得电子发生还原应,被还原,B错误;该装置是原电池,将化
学能转化为电能,C错误;放电时,电子从负极Zn沿导线流向正极石墨,D
正确。答案:D
14.(双选)一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y O)的氧化锆(ZrO)晶体,
2 3 2
在熔融状态下能传导O2-。下列对该项燃料电池说法正确的是( )
A.在熔融电解质中,O2-移向正极
B.电池总反应式是:2C H +13O =8CO +10H O
4 10 2 2 2
C.通入空气的一极是正极,电极反应为:O+4e-=2O2-
2
D.通入丁烷的一极是正极,电极反应为:C H +26e-+13O2-=4CO+5H O
4 10 2 2
解析:该电池是以丁烷的燃烧设计成的燃料电池,反应总方程式就是丁烷的燃烧方程式。在燃料电池中可燃物一般是
还原剂,在电池中的负极上发生反应。首先写出丁烷的燃烧方程式,然后写出O 得电子的电极方程式,总反应式与
2
正极式相减即得负极方程式。在原电池中阴离子向负极移动 A错误;在该氧化还原反应中丁烷是燃料,应该在负极上
发生氧化反应,D错误;燃料电池总反应实质是一个燃烧反应,而正极空气中氧气发生还原反应变为电解质的阴离子,
B、C正确。答案:BC
15.锂电池作为最主要的便携式能量电源,影响着我们生活的方方面面。锂-空气电池放电的工作原金属锂解理如图所
示。下列叙述正确的是( )
A.电池放电时负极电极方程式为O
2
+2H
2
O+4e-=4OH-
B.放电时电子由B极向A极移动
C.电解液a,b之间可采用阴离子交换膜
D.电解液b可能为稀LiOH溶液
解析:原电池中锂作负极、失电子、发生氧化反应,B电极为原电池正极,氧气
得到电子、发生还原反应,A错误;原电池放电时,电子由负极经过导线流向正
极,即电子由A极向B极移动,B错误;锂是活泼金属,能与和水发生反应,
所以该电池放电时,电解液中Li+由锂电极迁移向B电极,离子交换膜应该为阳
离子交换膜,C错误;Li在负极失电子生成Li+,Li+向正极移动,正极区Li+与氢氧根离子结合形成LiOH,由于阳离子交
换膜的隔离作用,水分子不能通过交换膜,所以电解液b可能为稀LiOH溶液D正确。答案:D
16.下面是几种常见的化学电源示意图,有关说法不正确的( )A.上述电池分别属于一次电池、二次电池和燃料电池
B.干电池在长时间使用后,锌筒被破坏
C.铅蓄电池工作过程中,每通过2mol电子,负极质量减轻207g
D.氢氧燃料电池是一种具有应用前景的绿色电源
解析:在干电池中,Zn作负极,被氧化,B正确;C项忽略了硫酸铅在该极上析出,该极质量应该增加而非减小;氢
氧燃料电池不需要将还原剂和氧化剂全部储藏在电池内,且工作的最终产物是水,故氢氧燃料电池是一种具有应用前
景的绿色电源,D正确。答案:C
17.镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式
进行:
Cd+2NiO(OH)+2H O Cd(OH) +2Ni(OH) 。有关该电池的说法正确的是( )
2 2 2
A. 放电时,正极反应为NiO(OH)+H O +e- = Ni(OH) - +OH-
2 2
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH向正极移动
解析:充电过程是电能转化为化学能的过程,B项错误;放电时负极反应式为Cd-2e-+2OH-=Cd(OH) ,附近溶液的碱性
2
减弱,因Cd2+结合了溶液中的OH-,同时溶液中的OH-向负极移动,C、D项错误。答案:A
18.一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为 CHCHOH-4e-+H O=CHCOOH+4H+。下列有关说
3 2 2 3
法正确的是( )
A.检测时,电解质溶液中的H+向负极移动
B.若有0.4mol电子转移,则在标准状况下消耗4.48L氧气
C.电池反应的化学方程式为CHCHOH+O =CHCOOH+H O
3 2 2 3 2
D.正极上发生的反应为O+4e-+2H O=4OH-
2 2
解析:在原电池中,电解质溶液中的离子应向正极移动,A错;每消耗1molO ,转移4mol电子,若有0.4mol电子转移
2
则在标准状况下消耗2.24LO ,B错;根据题意,电解质溶液呈酸性,正极的电极反应为O+4H++4e-=2H O,D错。答案:
2 2 2
C
19.燃料电池是利用燃料(如CO、H、CH 等)与氧气反应,将反应产生的化学能转变为电能的装置,通常用氢氧化钾溶
2 4
液作为电解质溶液。完成下列关于甲烷(CH)燃料电池的填空:
4
(1)甲烷与氧气反应的化学方程式为
(2)已知燃料电池的总反应式为CH+2O +2KOH=K CO+3H O,电池中有一极的电极反应为CH+10H--8e-=CO 2-+7H O,这
4 2 2 3 2 4 3 2
个电极是燃料电池的 (填“正极”或“负极”),另一个电极上的电极反应式为
(3)随着电池不断放电,电解质溶液的碱性 (填 “增大”“减小”或“不变”)。
(4)通常情况下,甲烷燃料电池的能量利用率 (填“大于”“小于”或“等于”)甲烷燃烧的能量利用率。
参考答案:(1)CH +2O 点燃 CO+2H O
4 2 2 2
(2)负极 2O+4H O+8e-=8OH-
2 2
(3)减小
(4)大于
解析:(1)可燃性气体甲烷,与氧气反应的化学方程式为CH+2O 点燃 CO+2H O。(2)电极反应CH+10H--8e-=CO 2-
4 2 2 2 4 3
+7H O中,CH 失电子发生氧化反应,为燃料电池的负极;另一电极上 O 得电子,发生还原反应,其电极反应式为
2 4 2
2O+4H O+8e-=8OH-。(3)根据总反应式可知随着电池不断放电,KOH溶液浓度逐渐减小,即电解质溶液的碱性逐渐减
2 2小(4)甲烷燃料电池的能量利用率大于甲烷燃烧的能量利用率。
20.化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)Zn-MnO 干电池应用广泛,其电解质溶液是ZnCl-NH Cl混合溶液。该电池的负极材料是 ,电池工作
2 2 4
时,电子流向 (填“正极”或“负极”)。若ZnCl-NH Cl混合溶液中含有杂质Cu2+,会加速某电极的反应,
2 4
其主要原因是
(2)铅酸蓄电池是常用的化学电源,其电极材料分别是 Pb 和PbO ,电解液为硫酸。该电池总反应式为 Pb+ PbO
2 2
+2H SO =2PbSO +2H O
2 4 4 2
请根据上述情况判断:
该蓄电池放电时,电解质溶液中阴离子移向 (填“正极”或“负极”);正极附近溶液的酸性
(填“增强”“减弱”或“不变”);放电时,负极的电极反应式为
(3)氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅酸蓄电池。若电解质为 KOH溶液,则氢氧燃料电池
的负极反应式为 。该电池工作时,外电路每流过2mole-,消耗标准状况下氧气 L
参考答案:(1)Zn(或锌) 正极 Zn与Cu2+反应生成Cu,Zn与Cu构成原电池,加快反应速率
(2)负极 减弱 Pb-2e-+SO2-=PbSO
4 4
(3)H -2e-+2OH-=2H O(或2H-4e-+4OH-=4H O) 11.2
2 2 2 2
解析:(1)原电池中负极Zn发生氧化反应,电池工作时,电子从负极流向正极;Zn与Cu2+发生氧化还原反应,生成的
Cu附着在Zn的表面构成铜锌原电池,加快反应速率。(2)铅酸蓄电池放电时,阴离子向负极移动;正极反应为
PbO +4H++2e-+SO2-=PbSO+2HO,即正极附近溶液的酸性减弱;放电时负极为Pb,发生氧化反应,其电极反应式为
2 4 4 2
Pb-2e-+SO2-=PbSO。(3)电解质溶液呈碱性,负极上H 失电子生成水,其电极方程式为H-2e-+2OH-=2HO;该电池中正
4 4 2 2 2
极上是氧气发生得电子的还原反应,其电极反应为O+4e+2HO=4OH-,外电路每流过2mole-时,消耗O 为0.5mol,即O
2 2 2 2
的体积为0.5mol×22.4L/mol=11.2L
21.原电池是化学对人类的一项重大贡献。
(1)如图是甲烷燃料电池原理示意图,回答下列问题:
①电池的负极是 (填“a”或“b”)电极,该极的电极反应式为
②电池工作一段时间后电解质溶液的pH (填 “增大”、“减小”或“不变”)。
(2)熔融盐燃料电池具有很高的发电效率,因而受到重视。可用 LiCO 和NaCO 的熔融盐混合物作电解质,CO为负
2 3 2 3
极燃气,空气与CO 的混合气为正极助燃气,制得在650℃下工作的燃料电池。请完成有关的电池反应式:
2
负极反应式:2CO+2CO2--4e-=4CO ;
3 2
正极反应式:
总电池反应式:
参考答案:(1)①a CH+10OH--8e=CO 2-+7H O ②减小
4 3 2
(2)O +2CO +4e-=2CO2- 2CO+O=2CO
2 2 3 2 2
解析:(1)CH 在反应时失去电子,故a电极是电池的负极。由于电池工作过程中会消耗 OH-,故一段时间后,电解质溶
4
液的pH会减小。
(2)正极发生还原发应,故正极电极反应式为O+2CO +4e-=2CO 2-。根据正极反应式+负极反应式=总电池反应,可推知
2 2 3
总电池反应式应为2CO+O=2CO
2 2
22.“神舟九号”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。
(1)飞船在光照区运行时,太阳能电池帆板将 能转化为 能,除供给飞船使用外,多余部分用镉镍蓄
电池储存起来。其工作原理为
Cd+2NiO(OH)+2H O Cd(OH) +2Ni(OH)
2 2 2
充电时,阳极的电极反应式为 ;当飞船运行到阴影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性 (填“增大”“减小”或“不变”)。
(2)紧急状况下,应急电池会自动启动,工作原理为Zn+Ag O+HO 2Ag+Zn(OH) ,负极的电极反应式为
2 2 2
参考答案:(1)太阳 电 Ni(OH) -e-+OH-=NiO(OH)+H O 减小
2 2
(2)Zn-2e-+2OH-=Zn(OH)
2
解析:阳极是失电子发生氧化反应的一极,Ni(OH) 为阳极;放电时负极反应为Cd-2e-+2OH-=Cd(OH) ,溶液的碱性减
2 2
小。