文档内容
第二单元 海水中的重要元素——钠和氯
第三节 物质的量(三)
一、基础巩固
1.溶液浓度是常用的物理量,下列说法中正确的是( )
A.将5.85g NaCl固体溶于1L水,所得NaCl溶液物质的量浓度为1mo/L
B.配制480mL 0.2mol/L NaOH溶液,需称量NaOH固体质量为3.84克
C.98%浓硫酸和等体积水混合后,质量分数大于49%
D.50mL 0.1mo/L NaCl溶液和25mL 0.1mol/L MgCl 溶液的Cl﹣浓度相同
2
2.将等物质的量钠、过氧化钠、氧化钠、氢氧化钠加入到足量且等量的水中,形成溶液质量分数分别为
X、Y、Z、W,下列关系正确的是( )
A.X<W<Y<Z B.W<X<Y<Z C.W<X<Y=Z D.W<X<Y<Z
3.下列溶液中Cl﹣物质的量浓度最大的是( )
A.10mL 0.1mol/L的AlCl 溶液
3
B.20mL 0.2mol/L的CaCl 溶液
2
C.20mL 0.5mol/L的KClO 溶液
3
D.10mL 0.25mol/L的NaCl溶液
4.在配制一定物质的量浓度的盐酸时,下列错误操作可使所配制溶液的浓度偏高的是( )
A.定容时俯视容量瓶瓶颈刻度线
B.溶解搅拌时有液体飞溅
C.用量筒量取浓盐酸时俯视量筒刻度进行读数
D.摇匀后见液面下降,再加水至刻度线
5.(1)配制500mL浓度为0.2mol•L﹣1NaOH溶液,需称取NaOH固体 g.然后再加入适量水,将上
述固体溶解,待 后,再转移到 中,定容,摇匀。
(2)在实验(1)中,其他操作均正确,但定容时俯视刻度线,会导致所配制的溶液中溶质的物质的
量浓度 (填“大于“小于”或“等于”下同)0.2 mol•L﹣1。
(3)在实验(1)中,转移NaOH溶液至容量瓶中时洒落少许,则所配制的溶液中溶质的物质的量浓度 0.2mol•L﹣1。
6.根据所学知识,回答下列问题:
(1)将12.5g CuSO •5H O溶于水中形成1L溶液,溶质的物质的量浓度为 mol•L﹣1。
4 2
(2)氢原子的物质的量相等的四种气体HCl、H 、NH 、CH ,在同温同压下,此四种气体体积之比V
2 3 4
(HCl):V(H ):V(NH ):V(CH )= 。
2 3 4
(3)配制100mL 1.00mol•L﹣1H SO 溶液,需要用量筒量取浓硫酸(密度为1.84g•cm﹣3,溶质质量分数
2 4
为98%)的体积为 (精确到0.1)mL。
(4)反应2K S+K SO +3H SO ═3S↓+3K SO +3H O中,氧化剂与还原剂的物质的量之比为 ,
2 2 3 2 4 2 4 2
若反应生成0.6mol S,则反应中转移的电子为 mol。
7. 实验室需要0.1 mol/L NaOH溶液450mL和0.5 mol/L H SO 溶液450mL.根据这两种溶液的配制情况回
2 4
答下列问题:
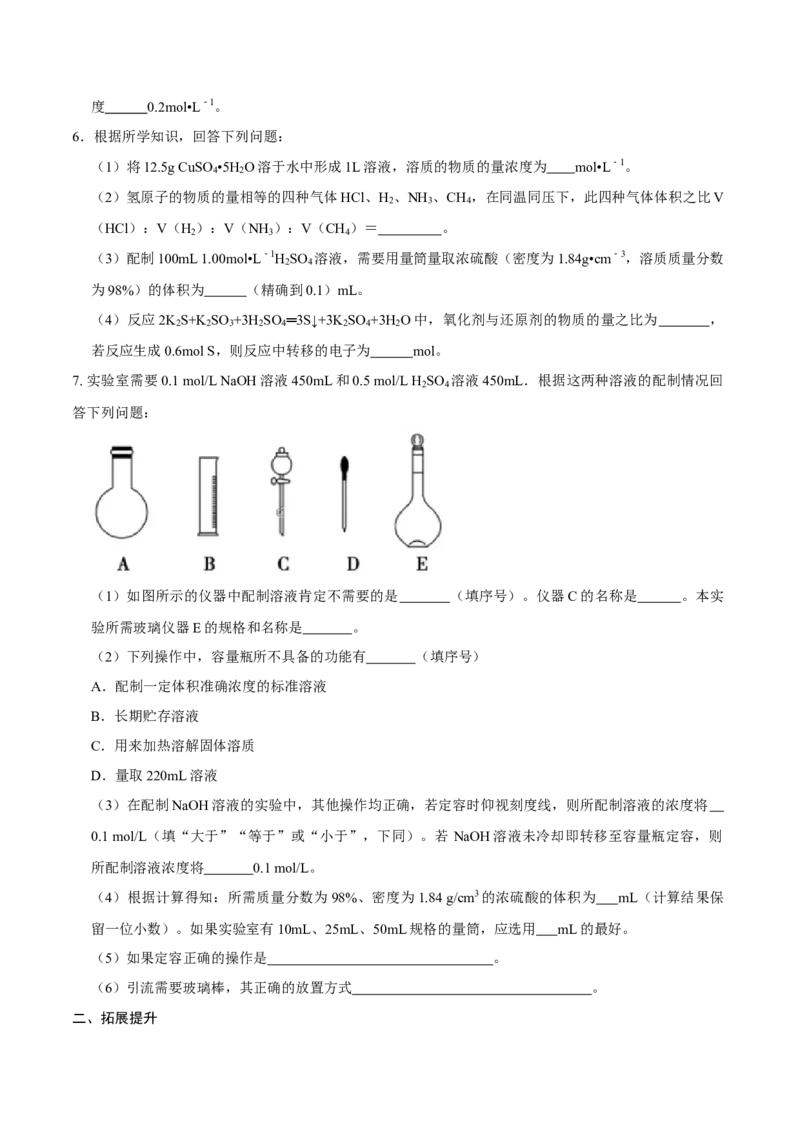
(1)如图所示的仪器中配制溶液肯定不需要的是 (填序号)。仪器C的名称是 。本实
验所需玻璃仪器E的规格和名称是 。
(2)下列操作中,容量瓶所不具备的功能有 (填序号)
A.配制一定体积准确浓度的标准溶液
B.长期贮存溶液
C.用来加热溶解固体溶质
D.量取220mL溶液
(3)在配制NaOH溶液的实验中,其他操作均正确,若定容时仰视刻度线,则所配制溶液的浓度将
0.1 mol/L(填“大于”“等于”或“小于”,下同)。若 NaOH溶液未冷却即转移至容量瓶定容,则
所配制溶液浓度将 0.1 mol/L。
(4)根据计算得知:所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为 mL(计算结果保
留一位小数)。如果实验室有10mL、25mL、50mL规格的量筒,应选用 mL的最好。
(5)如果定容正确的操作是 。
(6)引流需要玻璃棒,其正确的放置方式 。
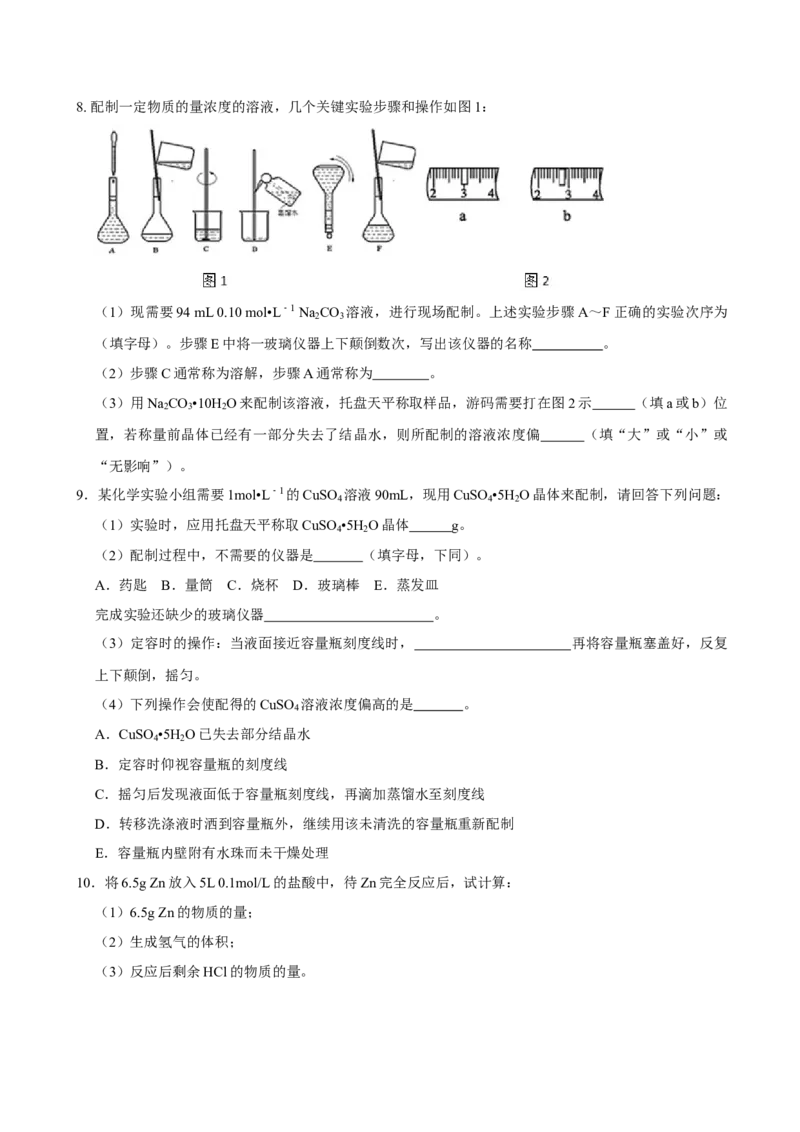
二、拓展提升8. 配制一定物质的量浓度的溶液,几个关键实验步骤和操作如图1:
(1)现需要94 mL 0.10 mol•L﹣1 Na CO 溶液,进行现场配制。上述实验步骤A~F正确的实验次序为
2 3
(填字母)。步骤E中将一玻璃仪器上下颠倒数次,写出该仪器的名称 。
(2)步骤C通常称为溶解,步骤A通常称为 。
(3)用Na CO •10H O来配制该溶液,托盘天平称取样品,游码需要打在图2示 (填a或b)位
2 3 2
置,若称量前晶体已经有一部分失去了结晶水,则所配制的溶液浓度偏 (填“大”或“小”或
“无影响”)。
9.某化学实验小组需要1mol•L﹣1的CuSO 溶液90mL,现用CuSO •5H O晶体来配制,请回答下列问题:
4 4 2
(1)实验时,应用托盘天平称取CuSO •5H O晶体 g。
4 2
(2)配制过程中,不需要的仪器是 (填字母,下同)。
A.药匙 B.量筒 C.烧杯 D.玻璃棒 E.蒸发皿
完成实验还缺少的玻璃仪器 。
(3)定容时的操作:当液面接近容量瓶刻度线时, 再将容量瓶塞盖好,反复
上下颠倒,摇匀。
(4)下列操作会使配得的CuSO 溶液浓度偏高的是 。
4
A.CuSO •5H O已失去部分结晶水
4 2
B.定容时仰视容量瓶的刻度线
C.摇匀后发现液面低于容量瓶刻度线,再滴加蒸馏水至刻度线
D.转移洗涤液时洒到容量瓶外,继续用该未清洗的容量瓶重新配制
E.容量瓶内壁附有水珠而未干燥处理
10.将6.5g Zn放入5L 0.1mol/L的盐酸中,待Zn完全反应后,试计算:
(1)6.5g Zn的物质的量;
(2)生成氢气的体积;
(3)反应后剩余HCl的物质的量。