文档内容
兰州一中 2024-2025-1 学期 12 月月考试题
高一化学
说明:本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分100分,考试时间75
分钟。答案写在答题卡上,交卷时只交答题卡。
可能用到的相对原子质量:H:1 C:12 O: 16 Mg:24 Al:27 Ca:40 Cu:64 Zn:65
第I卷(单项选择题 共42分)
1.下列生活中常见的现象中,不涉及氧化还原反应的是( )
A.钟乳石的形成 B.铁锅生锈 C.金属的冶炼 D.天然气燃烧
2.物质的性质决定用途,下列两者对应关系不正确的是( )
A.硬铝密度小、强度高,可用作制造飞机的材料
B.金属钠导热性好,可用作传热介质
C.NaClO 溶液呈碱性,可用作消毒剂
D.Fe O 呈红色,可用作颜料
2 3
3.科学家开发出一种低成本光伏材料——蜂窝状石墨烯,生产原理为:NaO + 2CO = NaCO + C(石
2 2 3
墨烯)。下列说法正确的是( )
A.该生产石墨烯的反应属于置换反应
B.石墨烯和金刚石是同素异形体
C.CO 在该反应中只做还原剂
D.NaO 属于碱性氧化物,CO 属于酸性氧化物
2
4.设N 表示阿伏加德罗常数的值。下列说法正确的是( )
A
A.1 mol/L HCl 溶液中,Cl- 的数目为N
A
B.标准状况下,0.1 mol Cl 溶于水,转移的电子数目为0.1 N
2 A
C.C.标准状况下,11.2 L CHCHOH中含有的分子数目为0.5 N
3 2 A
D.常温常压下,18 g HO中含有的原子总数为3 N
2 A
5.下列关于化学与职业的表述不正确的是( )
A.科技考古研究人员依靠自身丰富的经验来断定文物的精确年代
B.化学科研工作者是指从事与化学有关的基础研究和应用研究的专业技术人员
C.水质检验员是指对天然水、工业用水、生活用水等进行检测和评定的专业技术人员
D.金属材料研究机构的测试工程师可以通过化学检测仪器或化学检测方法来确定不锈钢的等级
6.下列溶液中,可以大量共存的离子组是( )
A.使石蕊试液变红的溶液中 K+、Cl-、ClO-、Na+B.加入铝粉能放出氢气的溶液:Na+、Cl-、SO 2-、NO -
4 3
C.含有NaSO 的溶液中:Ba2+、NH +、Al3+、Cl-
2 4 4
D.透明溶液中:Fe3+、Na+、SCN-、Cl-
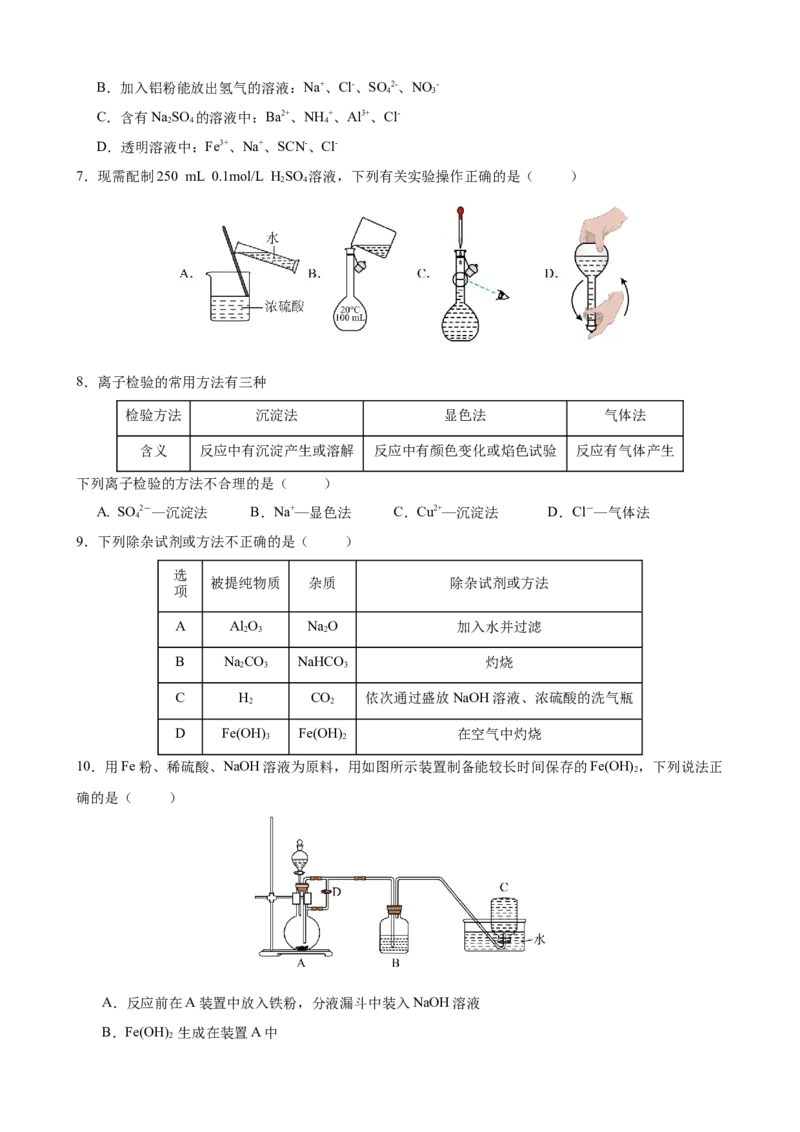
7.现需配制250 mL 0.1mol/L HSO 溶液,下列有关实验操作正确的是( )
2 4
8.离子检验的常用方法有三种
检验方法 沉淀法 显色法 气体法
含义 反应中有沉淀产生或溶解 反应中有颜色变化或焰色试验 反应有气体产生
下列离子检验的方法不合理的是( )
A. SO 2-—沉淀法 B.Na+—显色法 C.Cu2+—沉淀法 D.Cl-—气体法
4
9.下列除杂试剂或方法不正确的是( )
选
被提纯物质 杂质 除杂试剂或方法
项
A Al O NaO 加入水并过滤
2 3 2
B NaCO NaHCO 灼烧
2 3 3
C H CO 依次通过盛放NaOH溶液、浓硫酸的洗气瓶
2 2
D Fe(OH) Fe(OH) 在空气中灼烧
3 2
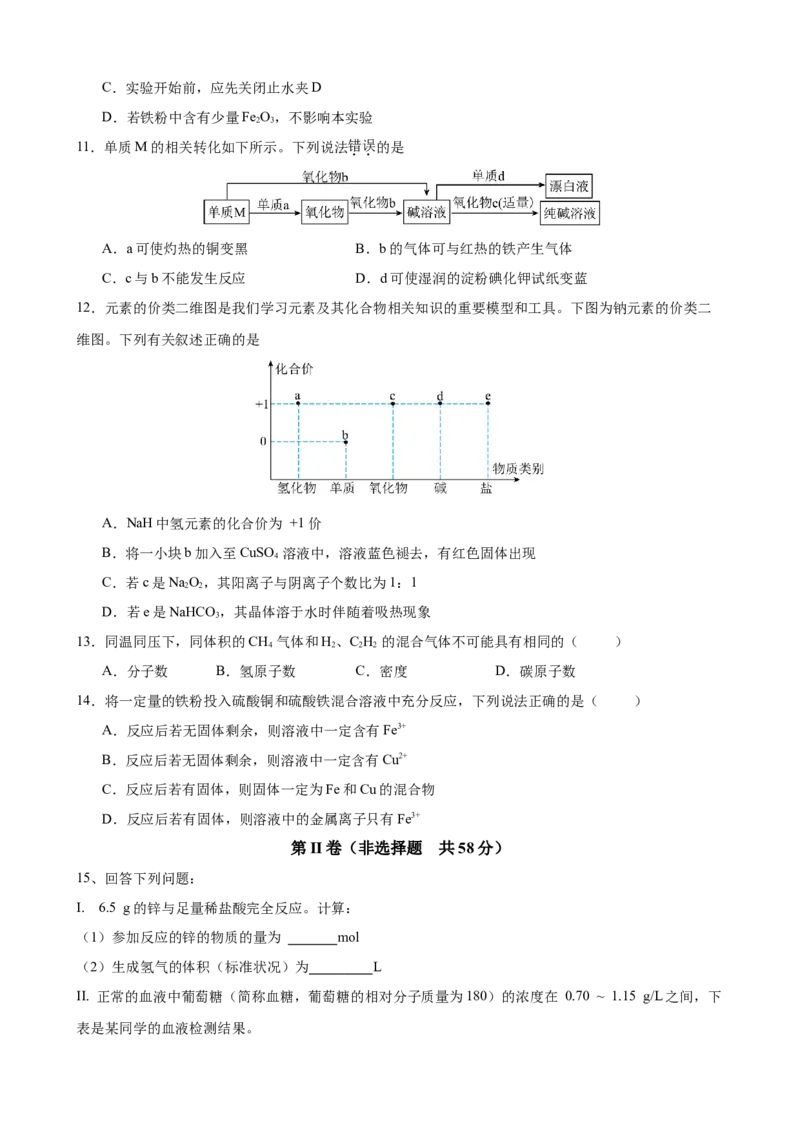
10.用Fe粉、稀硫酸、NaOH溶液为原料,用如图所示装置制备能较长时间保存的Fe(OH) ,下列说法正
2
确的是( )
A.反应前在A装置中放入铁粉,分液漏斗中装入NaOH溶液
B.Fe(OH) 生成在装置A中
2C.实验开始前,应先关闭止水夹D
D.若铁粉中含有少量Fe O,不影响本实验
2 3
11.单质M的相关转化如下所示。下列说法错误的是
A.a可使灼热的铜变黑 B.b的气体可与红热的铁产生气体
C.c与b不能发生反应 D.d可使湿润的淀粉碘化钾试纸变蓝
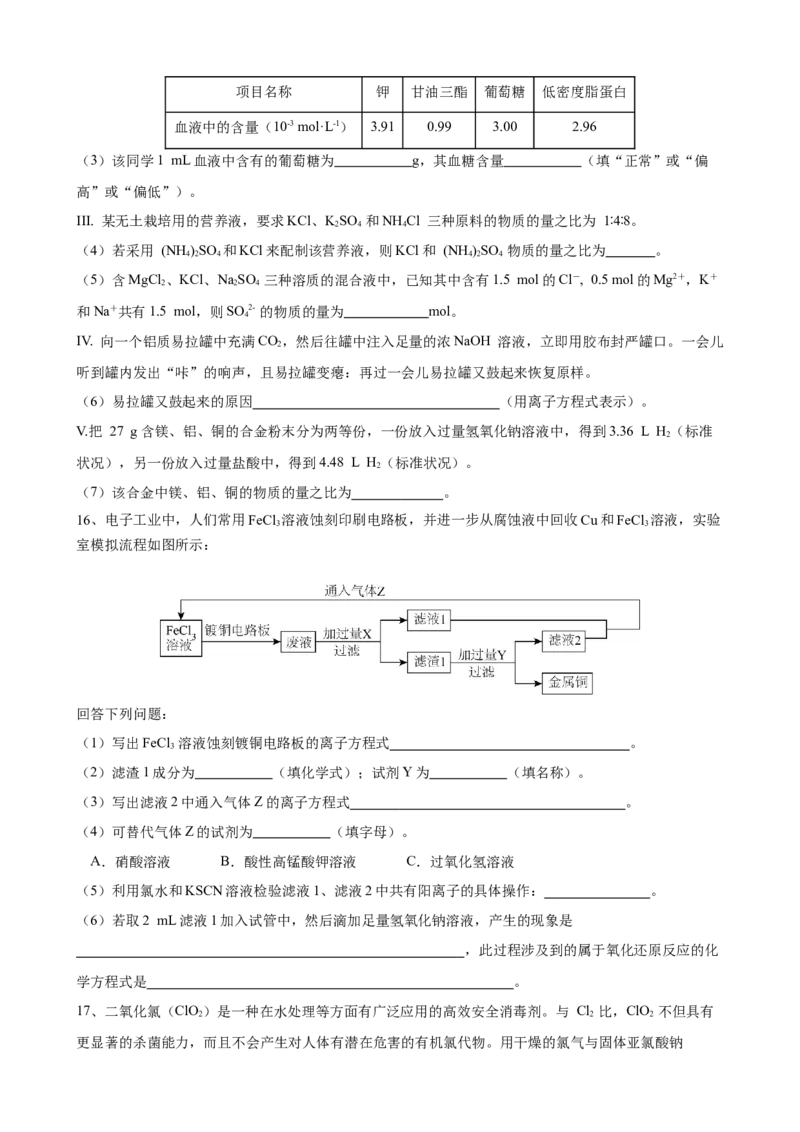
12.元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具。下图为钠元素的价类二
维图。下列有关叙述正确的是
A.NaH中氢元素的化合价为 +1价
B.将一小块b加入至CuSO 溶液中,溶液蓝色褪去,有红色固体出现
4
C.若c是NaO,其阳离子与阴离子个数比为1:1
2 2
D.若e是NaHCO ,其晶体溶于水时伴随着吸热现象
3
13.同温同压下,同体积的CH 气体和H、C H 的混合气体不可能具有相同的( )
4 2 2 2
A.分子数 B.氢原子数 C.密度 D.碳原子数
14.将一定量的铁粉投入硫酸铜和硫酸铁混合溶液中充分反应,下列说法正确的是( )
A.反应后若无固体剩余,则溶液中一定含有Fe3+
B.反应后若无固体剩余,则溶液中一定含有Cu2+
C.反应后若有固体,则固体一定为Fe和Cu的混合物
D.反应后若有固体,则溶液中的金属离子只有Fe3+
第II卷(非选择题 共58分)
15、回答下列问题:
I. 6.5 g的锌与足量稀盐酸完全反应。计算:
(1)参加反应的锌的物质的量为 mol
(2)生成氢气的体积(标准状况)为 L
II. 正常的血液中葡萄糖(简称血糖,葡萄糖的相对分子质量为180)的浓度在 0.70 ~ 1.15 g/L之间,下
表是某同学的血液检测结果。项目名称 钾 甘油三酯 葡萄糖 低密度脂蛋白
血液中的含量(10-3 mol·L-1) 3.91 0.99 3.00 2.96
(3)该同学1 mL血液中含有的葡萄糖为 g,其血糖含量 (填“正常”或“偏
高”或“偏低”)。
III. 某无土栽培用的营养液,要求KCl、KSO 和NH Cl 三种原料的物质的量之比为 1∶4∶8。
2 4 4
(4)若采用 (NH )SO 和KCl来配制该营养液,则KCl和 (NH )SO 物质的量之比为 。
4 2 4 4 2 4
(5)含MgCl 、KCl、NaSO 三种溶质的混合液中,已知其中含有1.5 mol的Cl-, 0.5 mol的Mg2+,K+
2 2 4
和Na+共有1.5 mol,则SO 2- 的物质的量为 mol。
4
IV. 向一个铝质易拉罐中充满CO,然后往罐中注入足量的浓NaOH 溶液,立即用胶布封严罐口。一会儿
2
听到罐内发出“咔”的响声,且易拉罐变瘪:再过一会儿易拉罐又鼓起来恢复原样。
(6)易拉罐又鼓起来的原因 (用离子方程式表示)。
V.把 27 g含镁、铝、铜的合金粉末分为两等份,一份放入过量氢氧化钠溶液中,得到3.36 L H(标准
2
状况),另一份放入过量盐酸中,得到4.48 L H(标准状况)。
2
(7)该合金中镁、铝、铜的物质的量之比为 。
16、电子工业中,人们常用FeCl 溶液蚀刻印刷电路板,并进一步从腐蚀液中回收Cu和FeCl 溶液,实验
3 3
室模拟流程如图所示:
回答下列问题:
(1)写出FeCl 溶液蚀刻镀铜电路板的离子方程式 。
3
(2)滤渣1成分为 (填化学式);试剂Y为 (填名称)。
(3)写出滤液2中通入气体Z的离子方程式 。
(4)可替代气体Z的试剂为 (填字母)。
A.硝酸溶液 B.酸性高锰酸钾溶液 C.过氧化氢溶液
(5)利用氯水和KSCN溶液检验滤液1、滤液2中共有阳离子的具体操作: 。
(6)若取2 mL滤液1加入试管中,然后滴加足量氢氧化钠溶液,产生的现象是
,此过程涉及到的属于氧化还原反应的化
学方程式是 。
17、二氧化氯(ClO )是一种在水处理等方面有广泛应用的高效安全消毒剂。与 Cl 比,ClO 不但具有
2 2 2
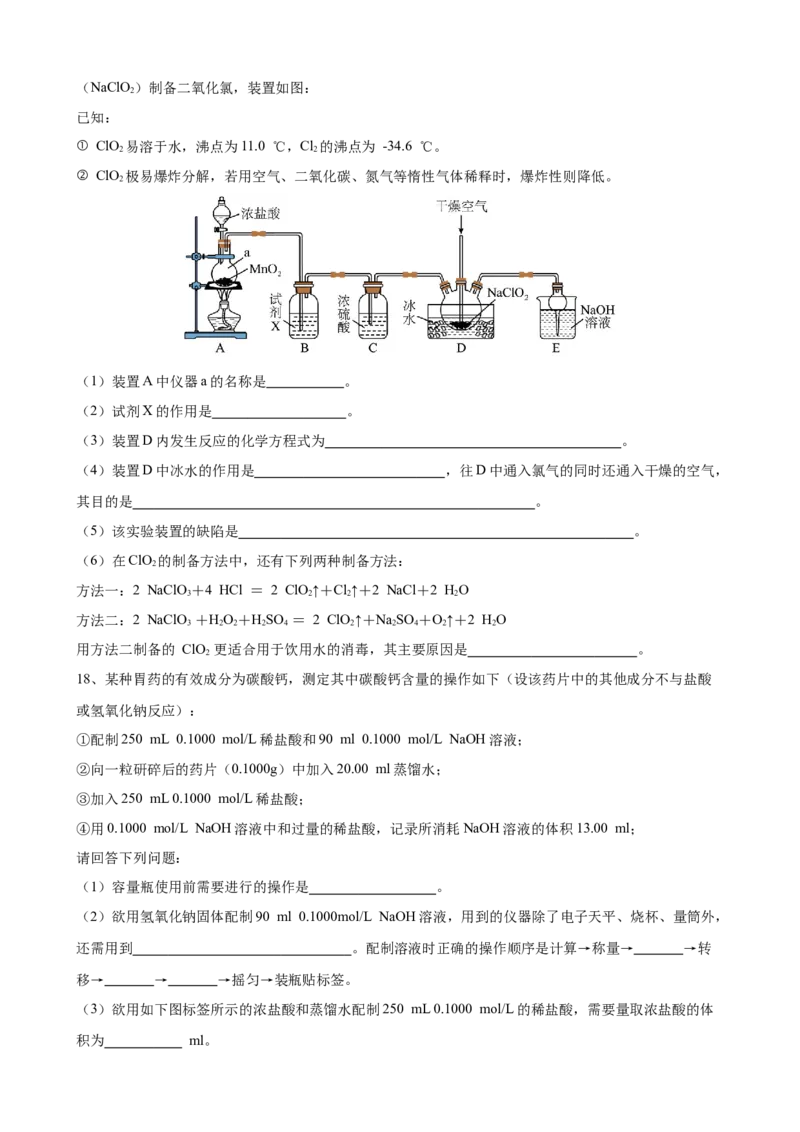
更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。用干燥的氯气与固体亚氯酸钠(NaClO)制备二氧化氯,装置如图:
2
已知:
① ClO 易溶于水,沸点为11.0 ℃,Cl 的沸点为 -34.6 ℃。
2 2
② ClO 极易爆炸分解,若用空气、二氧化碳、氮气等惰性气体稀释时,爆炸性则降低。
2
(1)装置A中仪器a的名称是 。
(2)试剂X的作用是 。
(3)装置D内发生反应的化学方程式为 。
(4)装置D中冰水的作用是 ,往D中通入氯气的同时还通入干燥的空气,
其目的是 。
(5)该实验装置的缺陷是 。
(6)在ClO 的制备方法中,还有下列两种制备方法:
2
方法一:2 NaClO+4 HCl = 2 ClO ↑+Cl↑+2 NaCl+2 HO
3 2 2 2
方法二:2 NaClO +HO+HSO = 2 ClO ↑+NaSO +O↑+2 HO
3 2 2 2 4 2 2 4 2 2
用方法二制备的 ClO 更适合用于饮用水的消毒,其主要原因是 。
2
18、某种胃药的有效成分为碳酸钙,测定其中碳酸钙含量的操作如下(设该药片中的其他成分不与盐酸
或氢氧化钠反应):
①配制250 mL 0.1000 mol/L稀盐酸和90 ml 0.1000 mol/L NaOH溶液;
②向一粒研碎后的药片(0.1000g)中加入20.00 ml蒸馏水;
③加入250 mL 0.1000 mol/L稀盐酸;
④用0.1000 mol/L NaOH溶液中和过量的稀盐酸,记录所消耗NaOH溶液的体积13.00 ml;
请回答下列问题:
(1)容量瓶使用前需要进行的操作是 。
(2)欲用氢氧化钠固体配制90 ml 0.1000mol/L NaOH溶液,用到的仪器除了电子天平、烧杯、量筒外,
还需用到 。配制溶液时正确的操作顺序是计算→称量→ →转
移→ → →摇匀→装瓶贴标签。
(3)欲用如下图标签所示的浓盐酸和蒸馏水配制250 mL 0.1000 mol/L的稀盐酸,需要量取浓盐酸的体
积为 ml。盐酸
分子式:
相对分子质量:36.5
密度:
质量分数:
(4)下列操作导致所配制的稀盐酸物质的量浓度偏低的是_______(选填序号)。
A.未洗涤烧杯和玻璃棒
B.容量瓶用蒸馏水洗后未干燥
C.定容时俯视看到刻度线
D.将容量瓶用瓶塞盖好,颠倒摇匀后发现液面低于刻度线,再加水直至刻度线
(5)这种药片中碳酸钙的质量分数 (CaCO )
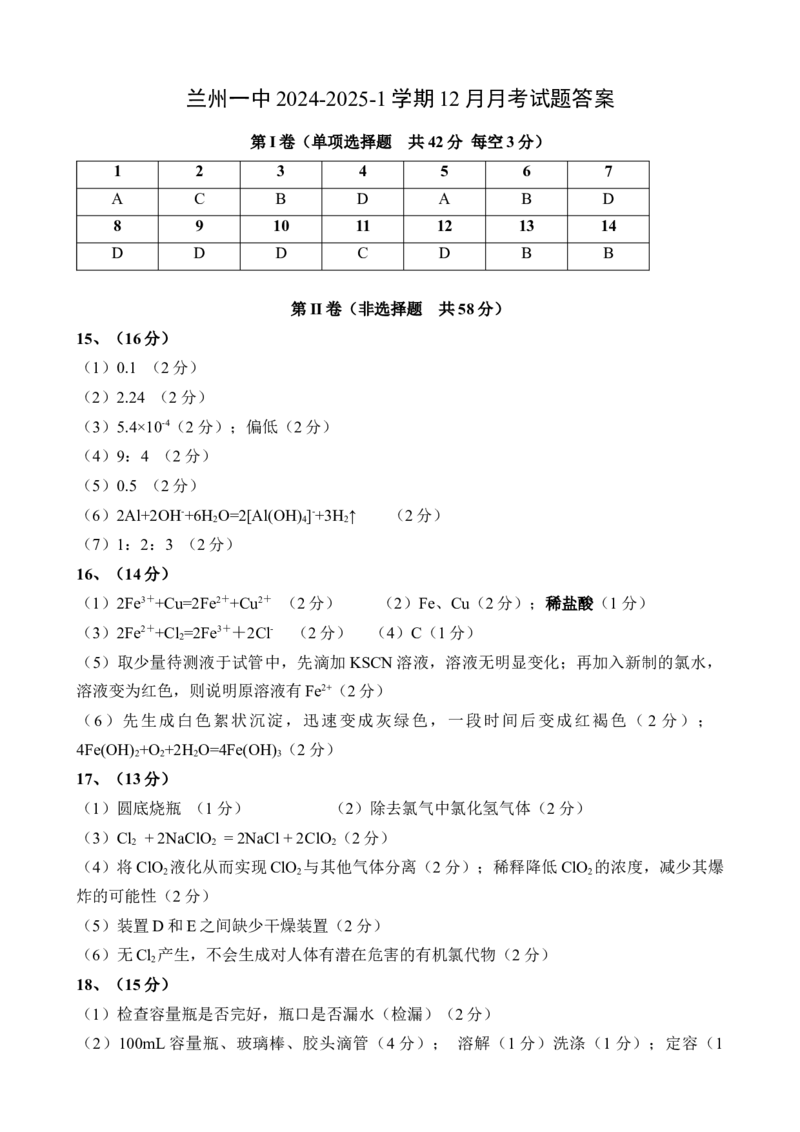
3兰州一中 2024-2025-1 学期 12 月月考试题答案
第I卷(单项选择题 共42分 每空3分)
1 2 3 4 5 6 7
A C B D A B D
8 9 10 11 12 13 14
D D D C D B B
第II卷(非选择题 共58分)
15、(16分)
(1)0.1 (2分)
(2)2.24 (2分)
(3)5.4×10-4(2分);偏低(2分)
(4)9:4 (2分)
(5)0.5 (2分)
(6)2Al+2OH-+6H O=2[Al(OH) ]-+3H ↑ (2分)
2 4 2
(7)1:2:3 (2分)
16、(14分)
(1)2Fe3++Cu=2Fe2++Cu2+ (2分) (2)Fe、Cu(2分);稀盐酸(1分)
(3)2Fe2++Cl =2Fe3++2Cl- (2分) (4)C(1分)
2
(5)取少量待测液于试管中,先滴加 KSCN溶液,溶液无明显变化;再加入新制的氯水,
溶液变为红色,则说明原溶液有Fe2+(2分)
(6)先生成白色絮状沉淀,迅速变成灰绿色,一段时间后变成红褐色(2 分);
4Fe(OH) +O +2H O=4Fe(OH) (2分)
2 2 2 3
17、(13分)
(1)圆底烧瓶 (1分) (2)除去氯气中氯化氢气体(2分)
(3)Cl + 2NaClO = 2NaCl + 2ClO (2分)
2 2 2
(4)将ClO 液化从而实现ClO 与其他气体分离(2分);稀释降低ClO 的浓度,减少其爆
2 2 2
炸的可能性(2分)
(5)装置D和E之间缺少干燥装置(2分)
(6)无Cl 产生,不会生成对人体有潜在危害的有机氯代物(2分)
2
18、(15分)
(1)检查容量瓶是否完好,瓶口是否漏水(检漏)(2分)
(2)100mL容量瓶、玻璃棒、胶头滴管(4分); 溶解(1分)洗涤(1分);定容(1分)
(3)2.1 (2分) (4)AD (2分) (5)60%(2分)