文档内容
高一化学上学期第一次月考-(基础 B 卷)
班级___________ 姓名___________ 学号____________ 分数____________
(考试时间:90分钟 试卷满分:100分)
考试范围:第一章 物质及其变化 难度:★★★☆☆
注意事项:
1.本试卷分第I卷(选择题)和第II卷(非选择题)两部分。答卷前,考生务必将自己的班级、姓名、
学号填写在试卷上。
2.回答第I卷时,选出每小题答案后,将答案填在选择题上方的答题表中。
3.回答第II卷时,将答案直接写在试卷上。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18
答案
第Ⅰ卷(选择题 54 分)
一、选择题:本题共18个小题,每小题3分,共54分。在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.纪录片《我在故宫修文物》表现了文物修复者穿越古今与百年之前的人进行对话的职业体验,让我们
领略到历史与文化的传承。下列文物修复和保护的过程中涉及化学变化的是( )
A B C D
银器用除锈剂除锈 变形的金属香炉复原 古画水洗除尘 木器表面擦拭烫蜡
【答案】A
【解析】A.银器表面的锈蚀物大多数为氧化银、氯化银、硫化银等,除此外还常会有银合金里所含铜元素
的腐蚀产物,对于锈层含较多铜元素锈蚀产物的,可以考虑使用甲酸溶液,甲酸能有效地除去铜元素锈蚀
产物,而对银不起作用,对于银器表面变色较深、锈层较厚重的,要考虑用电化学还原的方法处理,以上过
程涉及了化学变化,A项正确;B.变形的金属香炉复原主要原理是通过施加外力使器物恢复原状,未涉及
化学变化,B项错误;C.古画水洗除尘是用羊毛排笔蘸温水淋于画上,等画完全浸透进水,再用毛巾蘸干
画上的水分,如此进行多次,直到毛巾中挤出的水由浑浊变得澄清透明为止,未涉及化学变化,C项错误;
D. 木器表面擦拭烫蜡利用了蜂蜡熔点很低的性质,可以用吹风机对固体蜂蜡吹一会,蜂蜡会有稍微软化,此时把软化的蜂蜡大致涂到木头上,再用吹风机的热风吹涂好蜂蜡的木器,使蜂蜡融化并完全覆盖木器,
然后用棉布把多余的蜂蜡擦掉,再用热风吹使蜂蜡更好地渗入木头当中,该过程未涉及化学变化,D项错
误;
2.物质分类是化学研究的重要方法之一。化学工作者经常根据物质的组成对物质进行分类研究。近年来
发现,在金星大气层中存在三氧化二碳(C O)。下列物质与C O 属于同一类物质的是( )
2 3 2 3
A.KOH、Mg(OH) B.HSO 、HCO
2 2 4 2 3
C.SO 、NO D.NaSO 、KClO
2 2 3 3
【答案】C
【解析】A.KOH、Mg(OH) 属于碱,与C O 不同类,A不符合题意;B.HSO 、HCO 属于酸,与C O
2 2 3 2 4 2 3 2 3
不同类,B不符合题意;C.SO 、NO属于氧化物,与C O 同类,C符合题意;D.NaSO 、KClO 属于盐,
2 2 3 2 3 3
与C O 不同类,D不符合题意;
2 3
3.血液属于胶体,透析是除去肾衰竭病人血液中的毒性物质、从而拯救病人生命的重要方法。透析的原
理是( )
A.蒸发 B.电泳 C.过滤 D.渗析
【答案】D
【解析】血液属于胶体,透析是除去肾衰竭病人血液中的毒性物质,透析的原理为胶体的提纯方法——渗
析,答案选D。
4.下列有关FeCl 溶液和Fe(OH) 胶体的叙述正确的是( )
3 3
A.将饱和FeCl 溶液滴加到NaOH溶液中可制得Fe(OH) 胶体
3 3
B.Fe(OH) 胶体带正电,FeCl 溶液呈电中性
3 3
C.两种分散系的分散质具有相同的粒子直径
D.利用丁达尔效应可将两种液体区分开
【答案】D
【解析】
A.将饱和FeCl 溶液滴加到NaOH溶液中生成氢氧化铁沉淀,得不到氢氧化铁胶体,故A错误;B.胶体
3
不带电,带电的是胶粒,故B错误;C.分散系根据分散质粒子直径的不同分为溶液、胶体和浊液,即溶
液、胶体的分散质粒子直径不同,故C错误;D.溶液无丁达尔效应,胶体有丁达尔效应,故当两种液体
一种是胶体一种是溶液时,可以用丁达尔效应来区分,故D正确;5.雾霾、PM2.5已经成为公众耳熟能详的热词。“PM2.5”是指大气中直径小于或等于2.5微米的细小颗粒
物,也称为可入肺颗粒物。下列有关说法中,错误的是( )
A.雾霾有可能产生丁达尔效应
B.雾霾的形成与工业排放的烟气和汽车尾气有关系
C.“PM2.5”分散在大气中形成气溶胶,性质稳定,没有必要纳入空气质量评价指标
D.雾霾天气严重危害人体健康
【答案】C
【解析】A.“PM2.5”是指大气中直径小于或等于2.5微米的细小颗粒物,若直径在1~100nm之间也能形
成胶体,产生丁达尔现象,故A正确;B.工业排放的烟气是形成灰霾天气的最大元凶,故B正确;C.
PM2.5是指大气中直径小于或等于2.5微米的颗粒物,主要来自于化石燃料的燃烧,化石燃料燃烧产生有
害气体,能影响空气质量,要纳入空气质量评价指标,故C错误;D.PM2.5是指大气中直径小于或等于
2.5微米的颗粒物,主要来自于化石燃料的燃烧,化石燃料燃烧产生有害气体,能影响空气质量,严重危
害人体健康,故D正确;
5.铁、稀盐酸、澄清石灰水、氯化铜溶液是初中化学中常见的物质,四种物质间的反应关系如图所示。
图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应四个反应类型的说法正确的是( )
A.复分解反应、复分解反应、化合反应、置换反应
B.中和反应、置换反应、复分解反应、置换反应
C.复分解反应、复分解反应、置换反应、置换反应
D.分解反应、复分解反应、置换反应、置换反应
【答案】C
【解析】酸碱中和反应属于两种化合物相互交换成分生成另外两种化合物的反应,为复分解反应,氢氧化
钙和稀盐酸反应生成氯化钙和水,所以A为复分解反应、中和反应;B的反应属于两种化合物相互交换成分生成另外两种化合物的反应,为复分解反应,氢氧化钙和氯化铜反应生成氢氧化铜沉淀和氯化钙,所以
B为复分解反应;C的反应为一种单质和一种化合物反应生成另外的单质和化合物的反应,属于置换反应,
Fe和氯化铜反应生成Cu和氯化亚铁,所以C属于置换反应;D的反应为一种单质和一种化合物反应生成
另外的单质和化合物的反应,属于置换反应,铁和稀盐酸反应生成氯化亚铁和氢气,所以D属于置换反应;
故答案为C。
6.下列各选项中,不能满足如图一步关系选项是( )
A.X为铜、Y为氧化铜、Z为硫酸铜 B.X为二氧化碳、Y氧气、Z为一氧化碳
C.X为碳酸钙、Y氧化钙、Z为氢氧化钙 D.X为氢氧化钠、Y氯化钠、Z为碳酸钠
【答案】D
【解析】A.铜与氧气反应生成氧化铜,氧化铜能与硫酸反应生成硫酸铜,硫酸铜溶液与铁反应生成铜,故
A不选;B.二氧化碳发生光合作用生成氧气,氧气与碳反应可生成一氧化碳,CO继续燃烧生成CO,故B
2
不选;C.碳酸钙高温分解生成氧化钙,氧化钙与水反应生成氢氧化钙,氢氧化钙与CO 反应生成碳酸钙,
2
故C不选;D.氢氧化钠与盐酸反应生成氯化钠,氯化钠不能直接转化生成碳酸钠,故D选。
7.下列说法正确的是( )
A.将 AgCl 放入水中不能导电,故 AgCl 不是电解质
B.CO 溶于水得到的溶液能导电,所以 CO 是电解质
2 2
C.固态的 NaCl 不导电,熔融态的 NaCl 能导电,NaCl 是电解质
D.金属能导电,所以金属是电解质
【答案】C
【解析】A. AgCl的溶解度很小,导致将AgCl放入水中不能导电,但氯化银在熔融态能电离出自由移动的
阴阳离子,所以是电解质,故A错误;B. 二氧化碳溶于水能导电,但电离出自由移动离子的是碳酸不是
二氧化碳,所以二氧化碳是非电解质,故B错误;C. 固态的NaCl不导电,熔融态的NaCl有自由移动的
离子,所以能导电,故NaCl是电解质,故C正确;D. 金属能导电,但金属不是化合物,所以既不是电解质也不是非电解质,故D错误;
8.下列物质中存在自由移动的Cl-的是:
A.熔融的KClO B.NaCl固体 C.液态HCl D.MgCl 溶液
3 2
【答案】D
【解析】A.熔融氯酸钾电离出自由移动氯酸根离子,不存在自由移动的氯离子,故A错误;B.NaCl中
含有氯离子但是不含自由移动的氯离子,故B错误;C.液态HCl以分子存在,不含自由移动的氯离子,
故C错误;D.氯化镁在水分子的作用下电离出自由移动的氯离子,所以氯化镁溶液中含有自由移动的氯
离子,故D正确;
9.下列反应的离子方程式不正确的是( )
A.铁与稀盐酸反应:2Fe+6H+= 2Fe3++3H↑
2
B.氢氧化钠溶液与盐酸反应:OH-+H+= H O
2
C.锌与硫酸铜溶液反应:Zn+Cu2+ = Zn2++Cu
D.氯化钡溶液与稀硫酸反应:Ba2++SO 2-= BaSO↓
4 4
【答案】A
【解析】铁和元素反应的生成物是氯化亚铁,正确的为Fe + 2H+=Fe2++ H ↑,所以答案是A。
2
10.下列各组反应中,不能用同一个离子方程式表示的是( )
A.盐酸分别与NaOH溶液、Ca(OH) 溶液反应
2
B.硫酸分别与NaOH溶液、Ba(OH) 溶液反应
2
C.硝酸分别与NaCO 溶液、KCO 溶液反应
2 3 2 3
D.锌分别与稀盐酸、稀硫酸反应
【答案】B
【解析】A. 盐酸分别与NaOH溶液、Ca(OH) 溶液反应,离子方程式均为H++OH-=H O;B.硫酸与氢氧化
2 2
钠溶液反应:H++OH-=H O;硫酸与氢氧化钡溶液反应:2H++SO 2-+2OH-+Ba2+=BaSO ↓+2HO,不
2 4 4 2
能用同一离子方程式表示;C. 硝酸分别与NaCO 溶液、KCO 溶液反应,离子方程式均为CO2-
2 3 2 3 3
+2H+=CO ↑+H O;D. 锌分别与稀盐酸、稀硫酸反应,离子方程式均为Zn+2H+=Zn2++H ↑。
2 2 2
11.水溶液中能大量共存的一组离子是
A.NH +、Ba2+、Br-、CO2- B.Cl-、SO 2-、Fe2+、H+
4 3 3C.K+、Na+、SO 2-、MnO - D.Na+、H+、NO -、HCO -
4 4 3 3
【答案】C
【解析】A、Ba2+和CO2-反应生成BaCO 沉淀,不能大量共存,A错误;B、SO 2-和H+反应生成SO ,不
3 3 3 2
能大量共存,B错误;C、四种离子不反应,可以大量共存,C正确;D、H+和HCO -会反应生成CO、
3 2
HO,不能大量共存,D错误;
2
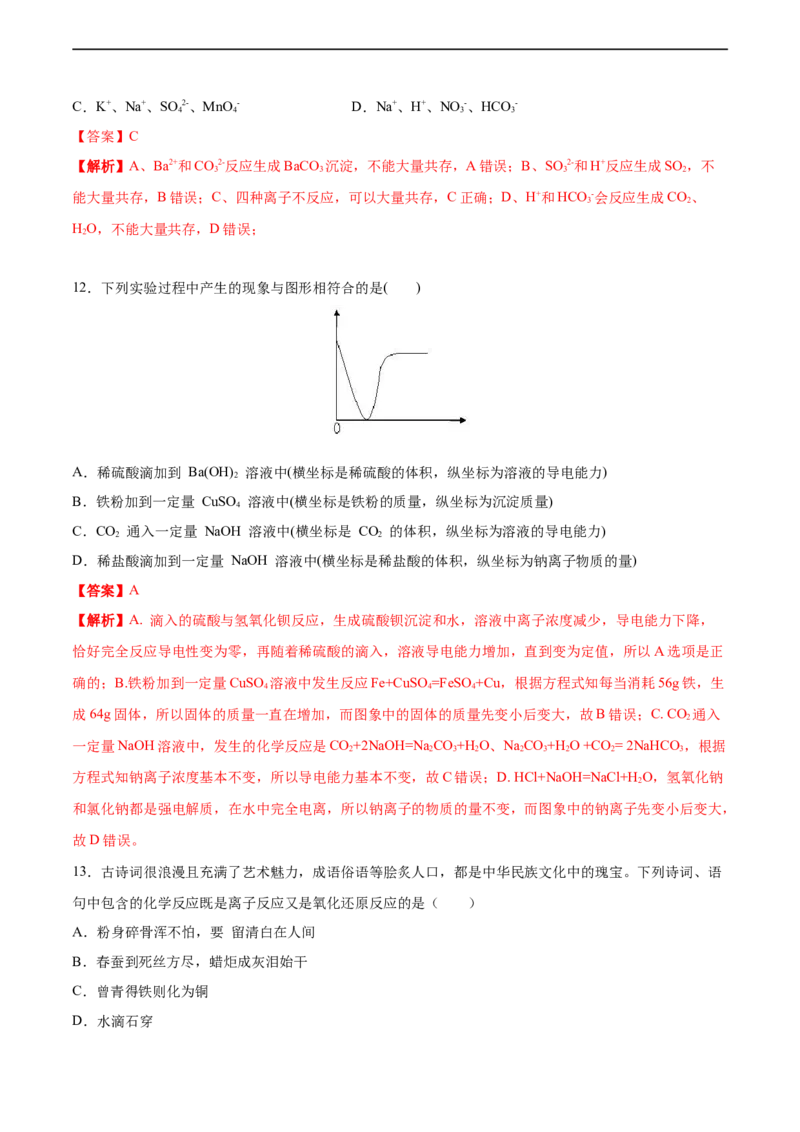
12.下列实验过程中产生的现象与图形相符合的是( )
A.稀硫酸滴加到 Ba(OH) 溶液中(横坐标是稀硫酸的体积,纵坐标为溶液的导电能力)
2
B.铁粉加到一定量 CuSO 溶液中(横坐标是铁粉的质量,纵坐标为沉淀质量)
4
C.CO 通入一定量 NaOH 溶液中(横坐标是 CO 的体积,纵坐标为溶液的导电能力)
2 2
D.稀盐酸滴加到一定量 NaOH 溶液中(横坐标是稀盐酸的体积,纵坐标为钠离子物质的量)
【答案】A
【解析】A. 滴入的硫酸与氢氧化钡反应,生成硫酸钡沉淀和水,溶液中离子浓度减少,导电能力下降,
恰好完全反应导电性变为零,再随着稀硫酸的滴入,溶液导电能力增加,直到变为定值,所以A选项是正
确的;B.铁粉加到一定量CuSO 溶液中发生反应Fe+CuSO=FeSO+Cu,根据方程式知每当消耗56g铁,生
4 4 4
成64g固体,所以固体的质量一直在增加,而图象中的固体的质量先变小后变大,故B错误;C. CO 通入
2
一定量NaOH溶液中,发生的化学反应是CO+2NaOH=Na CO+H O、NaCO+H O +CO = 2NaHCO ,根据
2 2 3 2 2 3 2 2 3
方程式知钠离子浓度基本不变,所以导电能力基本不变,故C错误;D. HCl+NaOH=NaCl+H O,氢氧化钠
2
和氯化钠都是强电解质,在水中完全电离,所以钠离子的物质的量不变,而图象中的钠离子先变小后变大,
故D错误。
13.古诗词很浪漫且充满了艺术魅力,成语俗语等脍炙人口,都是中华民族文化中的瑰宝。下列诗词、语
句中包含的化学反应既是离子反应又是氧化还原反应的是( )
A.粉身碎骨浑不怕,要 留清白在人间
B.春蚕到死丝方尽,蜡炬成灰泪始干
C.曾青得铁则化为铜
D.水滴石穿【答案】C
【解析】A.粉身碎骨浑不怕,要留清白在人间,此过程中发生碳酸钙受热分解的反应,没有元素化合价
的变化,不是氧化还原反应,A错误;B.曾青得铁则化为铜,Fe与硫酸铜溶液反应生成Cu和硫酸亚铁,
在溶液中的反应属于离子反应,Cu、Fe元素的化合价变化属于氧化还原反应,B正确;C.春蚕到死丝方
尽,蜡炬成灰泪始干,是石蜡的燃烧属于氧化还原反应,不是离子反应,C错误;D.水滴石穿,过程中
存在二氧化碳、水与碳酸钙的反应,不存在化合价的变化,不是氧化还原反应,D错误,答案选B。
14.在下列变化中,需要加入合适的氧化剂才能实现的是( )
A.HCl→H B.CO→CO
2 2
C.Fe O→Fe D.Br-→Br
2 3 2
【答案】D
【解析】A、氢元素化合价降低,发生了还原反应,需要加入还原剂才能实现,错误;B、碳元素化合价降
低,发生了还原反应,需加入还原剂才能实现,错误;C、铁元素化合价降低,发生了还原反应,需要加
入还原剂才能实现,错误;D、溴元素化合价升高,发生氧化反应,需加氧化剂才能实现,正确,
15.氢化钙可以作为生氢剂(其中CaH 中氢元素为-1价),反应方程式如下:CaH+2H O=Ca(OH) +2H ↑,
2 2 2 2 2
其中水的作用是( )
A.既不是氧化剂也不是还原剂
B.是氧化剂
C.是还原剂
D.既是氧化剂又是还原剂
【答案】B
【解析】根据反应前后元素的化合价变化来看,Ca和O的化合价均没有变化,其中CaH 中H的化合价
2
由-1价升高到0价,被氧化,作还原剂;HO中H的化合价由+1价降低到0价,被还原,作氧化剂;氢气
2
既是氧化产物,又是还原产物;答案选B。
16.某温度下将Cl 通入KOH溶液里,反应后得到KCl、KClO、KClO 的混合溶液,经测定ClO-与ClO -
2 3 3
的物质的量浓度之比为11∶1,则Cl 与KOH反应时,被还原的氯元素和被氧化的氯元素的物质的量之比
2
为( )
A.1∶3 B.4∶3 C.2∶1 D.3∶1
【答案】B【解析】 Cl 生成ClO−与ClO −是被氧化的过程,化合价分别由0价升高为+1价和+5价,ClO−与ClO −的物
2 3 3
质的量浓度之比为11:1,则可设ClO−为11mol,ClO −为1mol,被氧化的Cl共为12mol,失去电子的总物
3
质的量为11mol×(1−0)+1mol×(5−0)=16mol,氧化还原反应中氧化剂和还原剂之间得失电子数目相等,则
Cl 生成KCl是被还原的过程,化合价由0价降低为−1价,则得到电子的物质的量也应为16mol,则被还原
2
的Cl的物质的量为16mol,所以被还原的氯元素和被氧化的氯元素的物质的量之比为16mol:12mol=4:3,
故选B。
17.已知还原性:HSO (SO ) >I->Fe2+>NO,据此判断下列反应不能发生的是
2 3 2
A.HSO +I +H O=2HI+ H SO B.NO+SO =NO+SO
2 3 2 2 2 4 3 2 2
C.2FeCl +2HI= 2FeCl +2HCl+I D.3FeCl +4HNO =2FeCl +NO↑+2H O+Fe(NO )
3 2 2 2 3 3 2 3 3
【答案】B
【解析】A.因该反应中S元素的化合价升高,I元素的化合价降低,则SO 为还原剂,还原性强弱为SO
2 2
>HI,与已知的还原性强弱一致,反应能发生,故A不选;
B.因该反应中N元素的化合价升高,S元素的化合价降低,则NO为还原剂,还原性强弱为NO>SO ,
2
与已知的还原性强弱不一致,不能发生,故B选;
C.因该反应中I元素的化合价升高,Fe元素的化合价降低,则I-为还原剂,还原性强弱为I->Fe2+,与已
知的还原性强弱一致,反应能发生,故C不选;
D.因该反应中N元素的化合价降低,Fe元素的化合价升高,则Fe2+为还原剂,还原性强弱为Fe2+>NO,
与已知的还原性强弱一致,能发生,故D不选。
18.已知Co O 在酸性溶液中易被还原成Co2+,Co O 、Cl 、FeCl 、I 的氧化性依次减弱,下列反应在水
2 3 2 3 2 3 2
溶液中不可能发生的是( )
A.3Cl+6FeI===2FeCl +4FeI
2 2 3 3
B.Cl+2KI===2KCl+I
2 2
C.Co O+6HCl===2CoCl +Cl↑+3HO
2 3 2 2 2
D.2FeCl +Cl===2FeCl
2 2 3
【答案】 A
【解析】 A 项,根据反应:3Cl +6FeI===2FeCl +4FeI ,得出氧化性:Cl>FeCl ,但是氧化性是
2 2 3 3 2 3
FeCl >I ,还原性是碘离子强于亚铁离子,碘离子会先被氯气氧化,和题意不相符合,不可能发生,故 A
3 2
选;B项,根据反应:Cl +2KI===2KCl+I ,得出氧化性:Cl>I ,和题意相符合,反应可能发生,故B
2 2 2 2
不选;C项,根据反应:Co O +6HCl===2CoCl +Cl↑+3HO,得出氧化性:Co O>Cl ,和题意相符合,
2 3 2 2 2 2 3 2
反应可能发生,故C不选;D项,根据反应:2FeCl +Cl===2FeCl ,得出氧化性:Cl>FeCl ,和题意相符
2 2 3 2 3
合,反应可能发生,故D不选。
第 II 卷(非选择题 46 分)二、(非选择题46分)
19.(6分)对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。
Ⅰ.现有以下物质:①HO ②Cu ③BaCO ④Fe(OH) 胶体 ⑤酒精 ⑥CO ⑦稀硫酸
2 3 3 2
(1)以上物质中属于混合物的是________(填序号,下同),属于电解质的是________。
(2)向④中逐滴滴加⑦,可观察到的现象是_____________________。
Ⅱ.虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(3)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是________(填字母)。
(4)有同学认为所有酸碱中和反应均可表示为H++OH-=H O。请举个例子反驳上述观点(用离子方程式表
2
示)_____________。
【答案】(1)④⑦ ①③
(2) 先出现红褐色沉淀,后沉淀溶解,得到黄色溶液
(3) C Ba2++2OH-+2H++SO2-=BaSO ↓+2H O
4 4 2
【解析】I.(1)由多种物质组成的是混合物,④⑦是混合物;在水溶液中或熔融状态下能导电的化合物为电
解质,①③为电解质;②Cu是金属单质,不属于电解质,也不是非电解质;⑤酒精和⑥CO 都是化合物,
2
二者都属于非电解质;故属于混合物的是④⑦;属于电解质的是①③;
(2)电解质溶液能使胶体发生聚沉,故向氢氧化铁胶体中加入稀硫酸能发生胶体聚沉产生氢氧化铁红褐色沉
淀;继续滴加稀硫酸,则氢氧化铁沉淀与硫酸发生酸碱中和反应产生可溶性的Fe (SO ) 而使沉淀溶解,得
2 4 3
到黄色溶液,故反应现象是先出现红褐色沉淀,后沉淀溶解,得到黄色溶液;
Ⅱ.(3)所有的置换反应全是氧化还原反应,与氧化还原反应的关系是被包含和包含的关系,所以A是氧化还
原反应,B是置换反应,离子反应有的是氧化还原反应,有的是置换反应,所以C是离子反应;
(4)离子反应H++OH-=H O表示强酸、强碱混合生成可溶性强电解质和弱电解质水的反应,若是弱酸、弱碱
2
发生的中和反应,或者酸碱中和反应生成的盐是难溶性的沉淀,则不能用此离子方程式来表示,例如
HSO 、Ba(OH) 发生的中和反应的离子方程式为Ba2++2OH-+2H++SO2-=BaSO ↓+2H O。
2 4 2 4 4 2
20.(10分)有A、B、C、D四种化合物,分别由K+、Ba2+、SO 2—、CO2−、OH—中的两种组成,它们
4 3
具有下列性质:
①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无刺激性气味的气体E;③C的水溶液呈
碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
(1)推断A、B、C、D的化学式。A、________,B、________,C、________,D、________。
(2)写出下列反应的离子方程式。
B与盐酸反应:_______________________________________________,
C与硫酸反应:_______________________________________________,
E(少量)与澄清石灰水反应:____________________________________。
【答案】(1)BaSO BaCO Ba(OH) K CO
4 3 2 2 3
(2) 2H++BaCO ===CO ↑+H O+Ba2+ Ba2++2OH−+2H++ SO 2−===BaSO ↓+2H O Ca2++2OH−
3 2 2 4 4 2
+CO ===CaCO ↓+H O
2 3 2
【解析】(1) ①常见的“不溶于水和盐酸”的物质是氯化银和硫酸钡,结合所给离子知A是硫酸钡;②B
不溶于水,但溶于盐酸并放出无色无刺激性气味的气体,则B是碳酸钡,E是二氧化碳;③C的水溶液呈
碱性,与硫酸反应生成硫酸钡,则C是氢氧化钡;④D可溶于水,与硫酸作用时放出气体CO,则D是碳
2
酸钾。
因此,本题正确答案是:BaSO;BaCO ; Ba(OH) ; KCO;
4 3 2 2 3
(2)碳酸钡和盐酸反应:2HCl+BaCO ===CO ↑+HO+BaCl ;离子方程式:2H++BaCO ===CO ↑+HO+
3 2 2 2 3 2 2
Ba2+,氢氧化钡和硫酸反应:Ba(OH) +HSO ===BaSO ↓+2HO,离子方程式:Ba2++2OH-+2H++SO
2 2 4 4 2
===BaSO ↓+2HO 二氧化碳和足量澄清石灰水反应:Ca(OH)+CO===CaCO ↓+HO;离子方程式:
4 2 2 2 3 2
Ca2++2OH-+CO===CaCO ↓+HO。因此,本题正确答案是:2H++BaCO ===CO ↑+HO+Ba2+ ;Ba2
2 3 2 3 2 2
++2OH-+2H++SO ===BaSO ↓+2HO ;Ca2++2OH-+CO===CaCO ↓+HO。
4 2 2 3 2
21.(10分)现有甲、乙、丙三名同学分别进行Fe(OH) 胶体的制备实验。
3
I 甲同学向氯化铁溶液中加入少量的NaOH溶液;
II 乙同学直接加热饱和FeCl 溶液;
3
III 丙同学向25mL沸水中逐滴加入5~6滴FeCl 饱和溶液,继续煮沸至溶液呈红褐色,停止加热。
3
(1)其中操作正确的同学是______;他的操作中涉及到的化学反应方程式为 。
(2)证明有Fe(OH) 胶体生成的现象是 。
3
(3)丁同学将所制得的Fe(OH) 胶体分成两份,并进行下列实验:
3
①将其中一份装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,
这表明 。
②向另一份中不断滴加稀硫酸,观察到的现象是 。
【答案】(1)丙(2) 激光笔照射,有一条明亮的光路,则有胶体生成
(3) Fe(OH) 胶粒带正电 先生成红褐色的沉淀,后溶解为黄色溶液
3
【解析】(1)实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时
立即停止加热,即丙同学操作正确,反应的化学方程式为 ,故
答案为:丙; ;
(2)胶体具有丁达尔效应,当用激光笔照射时,会有一道明亮的光路,故答案为:用激光笔照射,有一
条明亮的光路,则有胶体生成;
(3)①Fe(OH) 胶粒带正电,通电时带正电荷的粒子向阴极移动,阴极附的颜色逐渐变深,故答案为:
3
Fe(OH) 胶粒带正电;
3
②向氢氧化铁胶体中逐滴加入过量HSO 溶液,HSO 电离出的SO 2-使Fe(OH) 胶体发生聚沉,H+使
2 4 2 4 4 3
Fe(OH) 沉淀溶解,会观察到先出现红褐色沉淀,后沉淀消失,故答案为:先生成红褐色的沉淀,后溶解
3
为黄色溶液。
22.(10分)按要求填空。
(1)在S2-、Fe2+、Fe3+、Mg2+、S、I-、H+中,只有氧化性的是________________,只有还原性的是
______________,既有氧化性又有还原性的是______________。
(2)某同学写出以下三个化学方程式:(未配平)
①NO+HNO→NO+HO
3 2 3 2
②NH +NO→HNO +HO
3 2 2
③NO+HO→HNO +HNO
2 4 2 3 2
其中你认为不可能实现的是__________________。
(3)下列三个氧化还原反应中,氧化性最强的物质的是______________。若溶质中Cl-与I-共存,为了氧化
I-而Cl-不被氧化,除单质外,还应用上述反应中的________________作氧化剂。
①2FeCl +2KI=2FeCl +2KCl+I
3 2 2
②2FeCl +Cl=2FeCl
2 2 3
③2KMnO +16HCl(浓)=2KCl+2MnCl +5Cl↑+8HO
4 2 2 2
【答案】(1)Fe3+、Mg2+、H+ S2-、I- Fe2+、S
(2)②(3)KMnO FeCl
4 3
【解析】(1)Fe3+、Mg2+、H+中的化合价都是最高价态,所以都只有氧化性;
S2-、I-中的化合价都是最低价态,所以都只有还原性;
Fe2+、S中的化合价是中间价态,所以既有氧化性又有还原性;
(2)氧化还原反应的特征是元素化合价的升降,②中N元素化合价只升高,不符合,故选②;
(3)根据氧化剂的氧化性大于氧化产物的氧化性,由①可知氧化性FeCl >I,②Cl>FeCl ,③KMnO
3 2 2 3 4
>Cl,则氧化性最强的为KMnO ,则若溶质中Cl-与I-共存,为了氧化I-而Cl-不被氧化,除单质外,还
2 4
可应用上述反应中的FeCl 。
3
23.(10分)根据反应8NH +3Cl=6NHCl+N ,回答下列问题。
3 2 4 2
(1)氧化剂______,还原剂________
(2)氧化产物______,还原产物_______
(3)氧化剂与还原剂的物质的量之比:_________________________
(4)用单线桥的方法表示该反应的电子转移情况。________________________
(5)用双线桥的方法表示该反应的电子转移情况。_________________________
【答案】(1)Cl NH
2 3
(2) N NH Cl
2 4
(3) 3:2
(4)
(5)
【解析】
(1)根据分析氧化剂为Cl,还原剂为NH ;
2 3
(2)氧化产物为N,还原产物为NH Cl;
2 4
(3)氧化剂为Cl,氨气作还原剂,但只有两个氮元素化合价升高,所以氧化剂和还原剂的物质的量之比为
2
3:2;
(4) N元素化合价由-3价变为0价,化合价升高,每个氮原子失去3个电子,但只有两个氮原子化合价升高,
即失去6个电子,氯元素化合价由0价变为-1价,化合价降低,得到电子,用单线桥表示为:;
(5) N元素化合价由-3价变为0价,化合价升高,每个氮原子失去3个电子,但只有两个氮原子化合价升高,
氯元素化合价由0价变为-1价,化合价降低,得到电子,用双线桥表示为: ;
(6)当有8mol NH 参加反应时,化合价变化的NH 只有2mol,N元素化合价由-3价变为0价,所以转移的
3 3
电子数目为6mol。