文档内容
五年(2021-2025)高考化学真题分类汇编
专题05 化学计量
考点 五年考情(2021-2025) 命题趋势
2025·湖南卷、2025·河北卷、2025·黑吉辽蒙
卷、2025·云南卷、2025·广东卷、2024·福建
卷、2024·海南卷、2024·贵州卷、2024·广东
卷、2024·河北卷、2024·吉林卷、2023·河北
考点01 有关阿伏加德
卷、2023·福建卷、2023·重庆卷、2022·辽宁
罗常数的判断
卷、2023·海南卷、2023·广东卷、2023·浙江 有关化学吉林的考查常以选择
卷、2023·辽宁卷、2023·全国甲卷、2022·重庆 题形式出现,题目中等难度,
卷、2022·福建卷、2022·河北卷、2022·海南 常结合物质结构、盐类水解、
卷、2022·浙江卷、2022·全国甲卷 可逆反应等知识综合考查;以
物质的量为核心,依据化学方
考点02 阿伏加德罗定
2021·山东卷 程式的有关计算主要在非选择
律
题中出现,难度稍大。预计未
来有关阿伏加德罗常数类试题
热度有所降低,有关化学方程
考点03 物质的量浓度 2025·江苏卷、2021·广东卷
式中定量关系的计算考
查力度会有所加大。
考点04 一定物质的量 2025·山东卷、2025·云南卷、2024·广西卷、
浓度溶液的配制 2024·甘肃卷、2024·全国甲卷、2023·全国甲卷
考点05 物质的量的综
2024·江西卷、2024·北京卷、2024·浙江卷
合应用
考点 01 有关阿伏加德罗常数的判断
1 / 13
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司1.(2025·湖南卷)加热时,浓硫酸与木炭发生反应: (浓) 。设 为
阿伏加德罗常数的值。下列说法正确的是
A. 含质子数为
B.常温常压下, 含σ键数目为
C. 的稀硫酸中含 数目为
D. 与 充分反应得到 的分子数为
2.(2025·河北卷)设 是阿伏加德罗常数的值,下列说法错误的是
A. 晶体内氢键的数目为
B. 的NaF溶液中阳离子总数为
C.28g环己烷和戊烯的混合物中碳原子的数目为
D.铅酸蓄电池负极增重96g,理论上转移电子数为
3.(2025·黑吉辽蒙卷)钠及其化合物的部分转化关系如图。设 为阿伏加德罗常数的值,下列说法正
确的是
A.反应①生成的气体,每11.2L(标准状况)含原子的数目为
B.反应②中2.3gNa完全反应生成的产物中含非极性键的数目为
C.反应③中 与足量 反应转移电子的数目为
D. 溶液中, 的数目为
4.(2025·云南卷) 为阿伏加德罗常数的值。下列说法正确的是
A. 中原子的数目为
B. 所含中子的数目为
C. 粉和足量S完全反应,转移电子的数目为
D. 盐酸与足量 反应,生成 的数目为
5.(2025·广东卷)设 为阿伏加德罗常数的值。下列说法正确的是
A. 的中子数,比 的多
B. 与水蒸气完全反应,生成 的数目为
C.在 的 溶液中, 的数目为
2 / 13
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司D.标准状况下的 与足量 反应,形成的共价键数目为
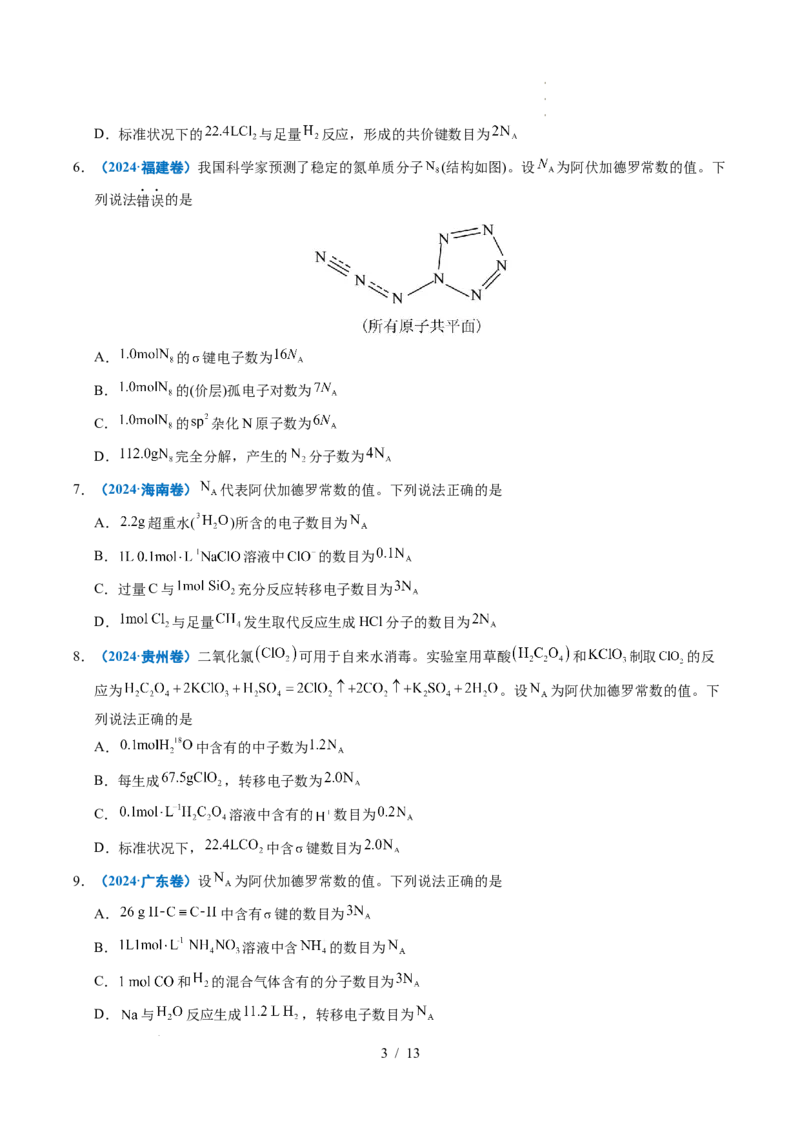
6.(2024·福建卷)我国科学家预测了稳定的氮单质分子 (结构如图)。设 为阿伏加德罗常数的值。下
列说法错误的是
A. 的 键电子数为
B. 的(价层)孤电子对数为
C. 的 杂化N原子数为
D. 完全分解,产生的 分子数为
7.(2024·海南卷) 代表阿伏加德罗常数的值。下列说法正确的是
A. 超重水( )所含的电子数目为
B. 溶液中 的数目为
C.过量C与 充分反应转移电子数目为
D. 与足量 发生取代反应生成HCl分子的数目为
8.(2024·贵州卷)二氧化氯 可用于自来水消毒。实验室用草酸 和 制取 的反
应为 。设 为阿伏加德罗常数的值。下
列说法正确的是
A. 中含有的中子数为
B.每生成 ,转移电子数为
C. 溶液中含有的 数目为
D.标准状况下, 中含 键数目为
9.(2024·广东卷)设 为阿伏加德罗常数的值。下列说法正确的是
A. 中含有 键的数目为
B. 溶液中含 的数目为
C. 和 的混合气体含有的分子数目为
D. 与 反应生成 ,转移电子数目为
3 / 13
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司10.(2024·河北卷)超氧化钾 可用作潜水或宇航装置的 吸收剂和供氧剂,反应为
, 为阿伏加德罗常数的值。下列说法正确的是
A. 中 键的数目为
B. 晶体中离子的数目为
C. 溶液中 的数目为
D.该反应中每转移 电子生成 的数目为
11.(2024·吉林卷)硫及其化合物部分转化关系如图。设 为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下, 中原子总数为
B. 溶液中, 数目为
C.反应①每消耗 ,生成物中硫原子数目为
D.反应②每生成 还原产物,转移电子数目为
12.(2023·河北卷) 为阿伏加德罗常数的值,下列说法正确的是
A. 的 溶液中含 个
B.反应 生成 ,转移 个电子
C. 号元素的原子一定含有 个质子、 个中子
D. 组成为 的烃一定含有 个双键
13.(2023·福建卷)我国新一代载人飞船使用的绿色推进剂硝酸羟胺 在催化剂作用下可
完全分解为 和 。 为阿伏加德罗常数的值,下列说法正确的是
A. 含有的质子数为
B. 固态硝酸羟胺含有的离子数为
C. 硝酸羟胺含有的 键数为
D.硝酸羟胺分解产生 (已折算为标况)的同时,生成 分子数为
14.(2023·重庆卷)已知反应: , 为阿伏加德罗常数的值,若消耗
(标准状况) ,下列叙述错误的是
A.转移的电子数为 B.生成的 质量为
4 / 13
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司C.生成的氧化产物分子数为 D.生成的 含有孤电子对数为
15.(2022·辽宁卷)设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.标准状况下,22.4LHCl气体中H+数目为N
A
B.28gC H 分子中含有的 键数目为4N
2 4 A
C.1.8g18O中含有的中子数为N
A
D.pH=12的NaCO 溶液中 数目为0.01N
2 3 A
16.(2023·海南卷) 代表阿伏加德罗常数的值。下列说法正确的是
A.2.4g镁条在空气中充分燃烧,转移的电子数目为
B.5.6g铁粉与 的HCl的溶液充分反应,产生的气体分子数目为
C.标准状况下, 与 充分反应,生成的 分子数目为
D. 完全溶于 所得溶液, 微粒数目为
17.(2023·广东卷)设 为阿伏加德罗常数的值。侯氏制碱法涉及 和 等物质。下
列叙述正确的是
A. 含有的共价键数目为
B. 完全分解,得到的 分子数目为
C.体积为 的 溶液中, 数目为
D. 和 的混合物中含 ,则混合物中质子数为
18.(2023·浙江卷)N 为阿伏加德罗常数的值,下列说法正确的是
A
A.4.4gC HO中含有σ键数目最多为0.7N
2 4 A
B.1.7gHO 中含有氧原子数为0.2N
2 2 A
C.向1L0.1mol/LCHCOOH溶液通氨气至中性,铵根离子数为0.1N
3 A
D.标准状况下,11.2LCl 通入水中,溶液中氯离子数为0.5N
2 A
19.(2023·辽宁卷)我国古代四大发明之一黑火药的爆炸反应为: 。
设 为阿伏加德罗常数的值,下列说法正确的是
A. 含 键数目为 B.每生成 转移电子数目为
C. 晶体中含离子数目为 D. 溶液中含 数目为
20.(2023·全国甲卷) 为阿伏加德罗常数的值。下列叙述正确的是
A. 异丁烷分子中共价键的数目为
B.标准状况下, 中电子的数目为
C. 的 溶液中 的数目为
5 / 13
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司D. 的 溶液中 的数目为
21.(2022·重庆卷)工业上用N 和H 合成NH ,N 代表阿伏加德罗常数的值,下列说法正确的是
2 2 3 A
A.消耗14gN 生成NH 分子数为2 N
2 3 A
B.消耗1molH ,生成N-H键数为2 N
2 A
C.生成标准状况下22.4LNH ,电子转移数为2 N
3 A
D.氧化1molNH 生成NO,需O 分子数为2 N
3 2 A
22.(2022·福建卷)常温常压下,电化学还原制氨气的总反应方程式: ,
设 为阿伏加德罗常数的值,下列说法正确的是
A. 水中含有的孤电子对数为
B.每产生 失去的电子数为
C. 氨水中,含有的 分子数少于
D.消耗 (已折算为标况)时,产生的 分子数为
23.(2022·河北卷)N 是阿伏加德罗常数的值。下列说法正确的是
A
A.3.9gNaO 与足量水反应,转移电子个数为0.1N
2 2 A
B.1.2gMg在空气中燃烧生成MgO和MgN,转移电子个数为0.1N
3 2 A
C.2.7gAl与足量NaOH溶液反应,生成H 的个数为0.1N
2 A
D.6.0gSiO 与足量NaOH溶液反应,所得溶液中SiO 的个数为0.1N
2 A
24.(2022·海南卷)在2.8gFe中加入100mL3mol/LHCl,Fe完全溶解。N 代表阿伏加德罗常数的值,下
A
列说法正确的是
A.反应转移电子为0.1mol B.HCl溶液中 数为3N
A
C. 含有的中子数为1.3N D.反应生成标准状况下气体3.36L
A
25.(2022·浙江卷) 为阿伏加德罗常数的值,下列说法正确的是
A. 中含有 个阳离子
B. 乙烷和丙烯的混合气体中所含碳氢键数为
C. 含有中子数为
D. 和 于密闭容器中充分反应后, 分子总数为
26.(2022·全国甲卷) 为阿伏加德罗常数的值,下列说法正确的是
A.25℃, 下, 氢气中质子的数目为
B .溶液中, 的数目为
6 / 13
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司C. 苯甲酸完全燃烧,生成 的数目为
D.电解熔融 ,阴极增重 ,外电路中通过电子的数目为
27.(2021·重庆卷)葡萄酒中含有CHCHOH、CHCOOH、 SO 和CO 等多种成分。若N 代表阿伏加
3 2 3 2 2 A
德罗常数的值,下列说法正确的是
A.46gCHCHOH中含有C-H键数为5N
3 2 A
B.1L1 mol·L-1CHCOOH溶液中含有氢离子数为N
3 A
C.1 mol SO 与1 mol O 完全反应转移的电子数为4 N
2 2 A
D.11.2L (标准状况) CO 完全溶于水后溶液中HCO 分子数为0.5N
2 2 3 A
28.(2022·浙江卷)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
B.1.8g重水(D O)中所含质子数为N
2 A
C.足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 A
D.32g甲醇的分子中含有C—H键的数目为4N
A
29.(2021·福建卷)设 为阿伏加德罗常数的值.下列说法正确的是
A. 所含极性共价键的数目为
B. 晶体中阴、阳离子总数为
C. 与足量 反应生成 的分子数为
D.电解熔融 制 ,电路中通过的电子数为
30.(2021·海南卷) 代表阿伏加德罗常数的值。下列说法正确的是
A. 中含有的电子数为1.3
B. 中含有的共价键的数目为0.1
C. 肼 含有的孤电子对数为0.2
D. ,生成 乙烷时断裂的共价键总数为
31.(2021·湖北卷)N 为阿伏加德罗常数的值。下列说法错误的是
A
A.23gCHCHOH中sp3杂化的原子数为N
3 2 A
B.0.5molXeF 中氙的价层电子对数为3N
4 A
C.1mol[Cu(H O) ]2+中配位键的个数为4N
2 4 A
D.标准状况下,11.2LCO和H 的混合气体中分子数为0.5N
2 A
32.(2021·天津卷)设N 为阿伏加德罗常数的值,下列叙述正确的是
A
A.1mol/LHCl溶液中,HCl分子的数目为N
A
B.22.4L氢气中,H 分子的数目为N
2 A
C.180g葡萄糖中,C原子的数目为6N
A
7 / 13
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司D.1molN 中,σ键的数目为3N
2 A
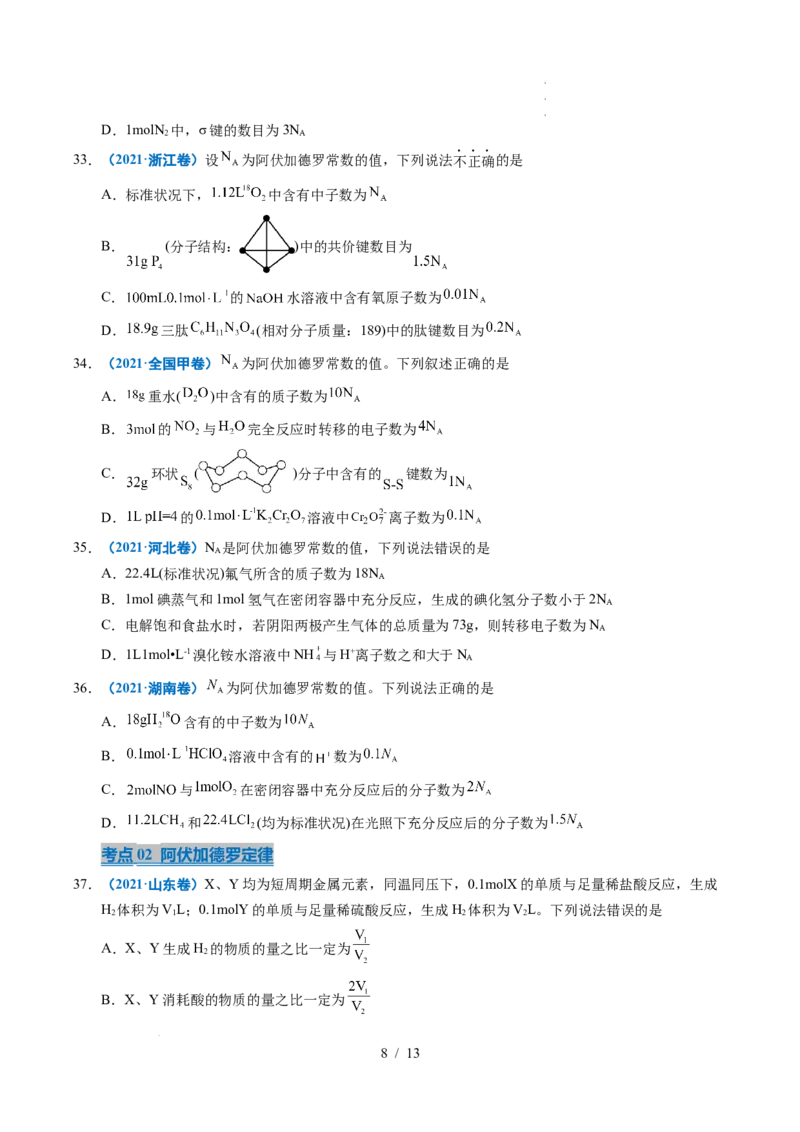
33.(2021·浙江卷)设 为阿伏加德罗常数的值,下列说法不正确的是
A.标准状况下, 中含有中子数为
B. (分子结构: )中的共价键数目为
C. 的 水溶液中含有氧原子数为
D. 三肽 (相对分子质量:189)中的肽键数目为
34.(2021·全国甲卷) 为阿伏加德罗常数的值。下列叙述正确的是
A. 重水( )中含有的质子数为
B. 的 与 完全反应时转移的电子数为
C. 环状 ( )分子中含有的 键数为
D. 的 溶液中 离子数为
35.(2021·河北卷)N 是阿伏加德罗常数的值,下列说法错误的是
A
A.22.4L(标准状况)氟气所含的质子数为18N
A
B.1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2N
A
C.电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为N
A
D.1L1mol•L-1溴化铵水溶液中NH 与H+离子数之和大于N
A
36.(2021·湖南卷) 为阿伏加德罗常数的值。下列说法正确的是
A. 含有的中子数为
B. 溶液中含有的 数为
C. 与 在密闭容器中充分反应后的分子数为
D. 和 (均为标准状况)在光照下充分反应后的分子数为
考点 02 阿伏加德罗定律
37.(2021·山东卷)X、Y均为短周期金属元素,同温同压下,0.1molX的单质与足量稀盐酸反应,生成
H 体积为VL;0.1molY的单质与足量稀硫酸反应,生成H 体积为VL。下列说法错误的是
2 1 2 2
A.X、Y生成H 的物质的量之比一定为
2
B.X、Y消耗酸的物质的量之比一定为
8 / 13
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司C.产物中X、Y化合价之比一定为
D.由 一定能确定产物中X、Y的化合价
考点 03 物质的量浓度
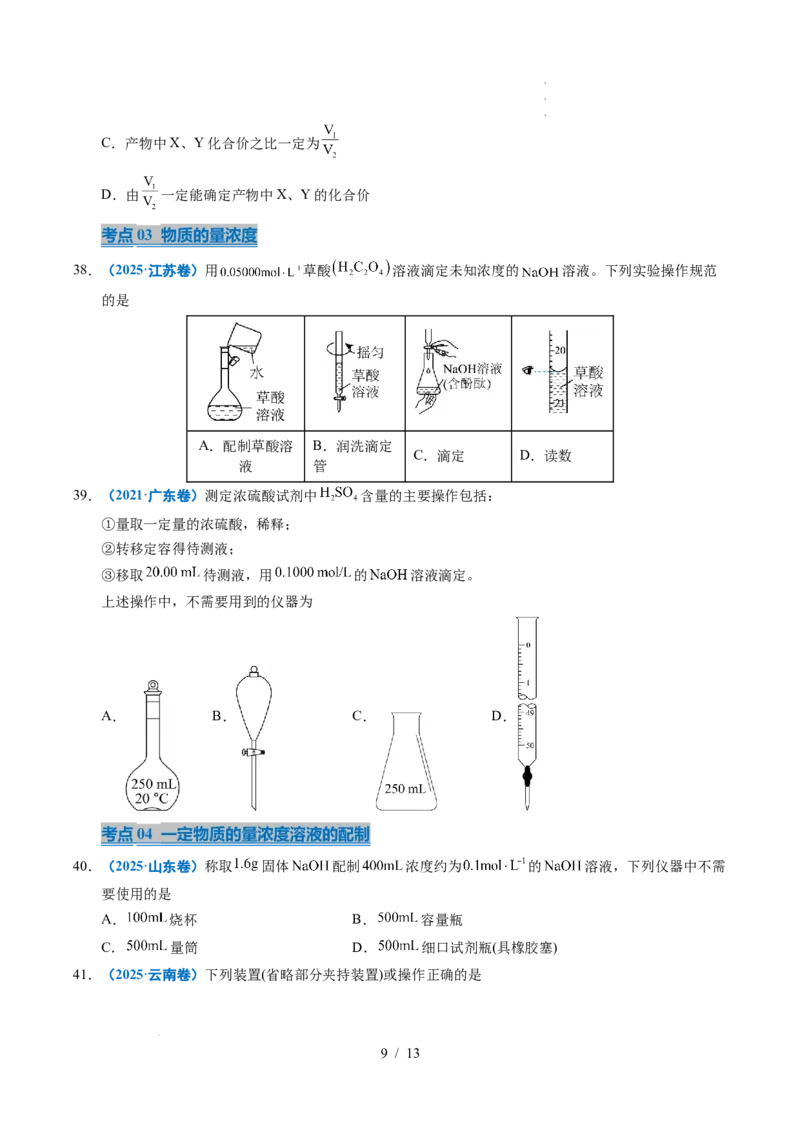
38.(2025·江苏卷)用 草酸 溶液滴定未知浓度的 溶液。下列实验操作规范
的是
A.配制草酸溶 B.润洗滴定
C.滴定 D.读数
液 管
39.(2021·广东卷)测定浓硫酸试剂中 含量的主要操作包括:
①量取一定量的浓硫酸,稀释;
②转移定容得待测液;
③移取 待测液,用 的 溶液滴定。
上述操作中,不需要用到的仪器为
A. B. C. D.
考点 04 一定物质的量浓度溶液的配制
40.(2025·山东卷)称取 固体 配制 浓度约为 的 溶液,下列仪器中不需
要使用的是
A. 烧杯 B. 容量瓶
C. 量筒 D. 细口试剂瓶(具橡胶塞)
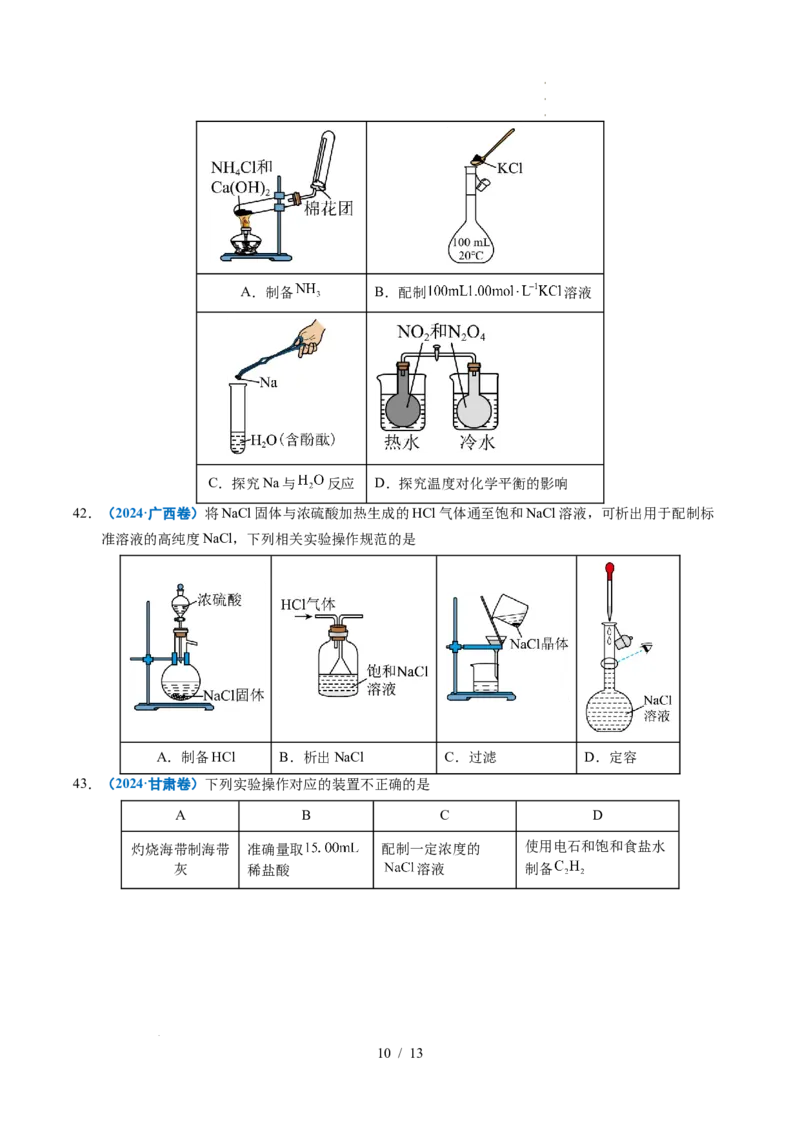
41.(2025·云南卷)下列装置(省略部分夹持装置)或操作正确的是
9 / 13
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A.制备 B.配制 溶液
C.探究Na与 反应 D.探究温度对化学平衡的影响
42.(2024·广西卷)将NaCl固体与浓硫酸加热生成的HCl气体通至饱和NaCl溶液,可析出用于配制标
准溶液的高纯度NaCl,下列相关实验操作规范的是
A.制备HCl B.析出NaCl C.过滤 D.定容
43.(2024·甘肃卷)下列实验操作对应的装置不正确的是
A B C D
灼烧海带制海带 准确量取 配制一定浓度的 使用电石和饱和食盐水
灰 稀盐酸 溶液 制备
10 / 13
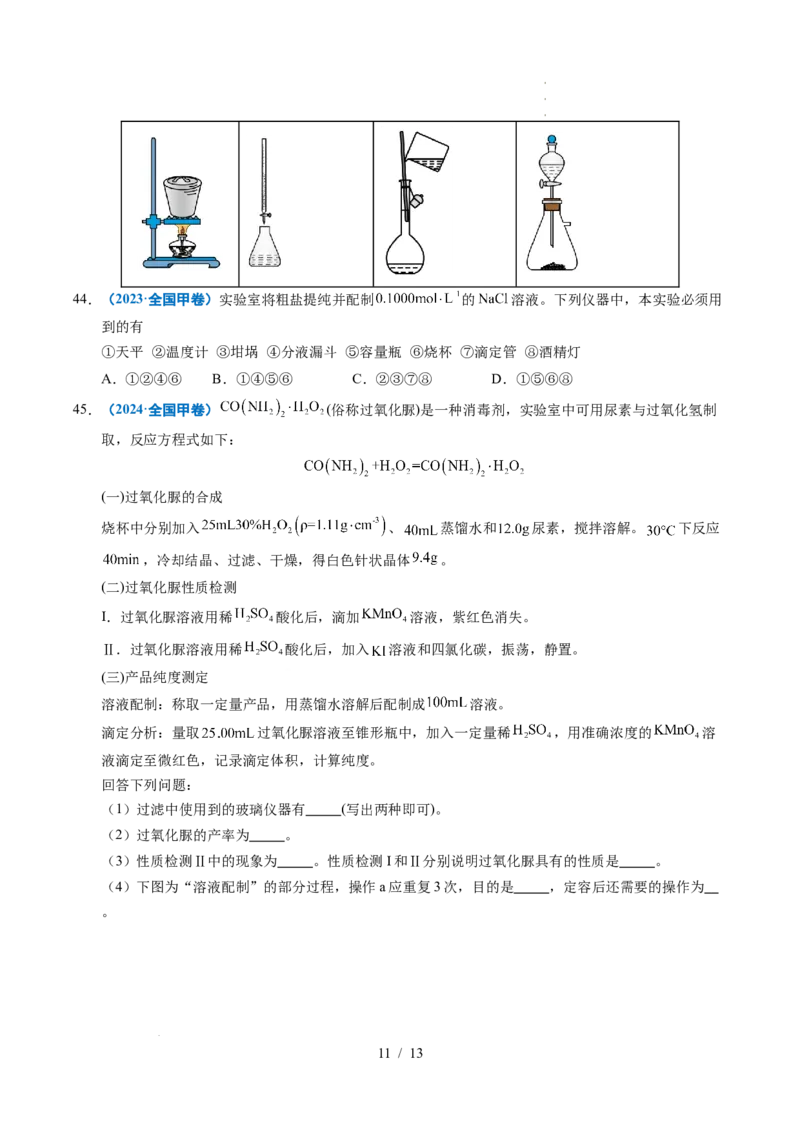
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司44.(2023·全国甲卷)实验室将粗盐提纯并配制 的 溶液。下列仪器中,本实验必须用
到的有
①天平 ②温度计 ③坩埚 ④分液漏斗 ⑤容量瓶 ⑥烧杯 ⑦滴定管 ⑧酒精灯
A.①②④⑥ B.①④⑤⑥ C.②③⑦⑧ D.①⑤⑥⑧
45.(2024·全国甲卷) (俗称过氧化脲)是一种消毒剂,实验室中可用尿素与过氧化氢制
取,反应方程式如下:
(一)过氧化脲的合成
烧杯中分别加入 、 蒸馏水和 尿素,搅拌溶解。 下反应
,冷却结晶、过滤、干燥,得白色针状晶体 。
(二)过氧化脲性质检测
I.过氧化脲溶液用稀 酸化后,滴加 溶液,紫红色消失。
Ⅱ.过氧化脲溶液用稀 酸化后,加入 溶液和四氯化碳,振荡,静置。
(三)产品纯度测定
溶液配制:称取一定量产品,用蒸馏水溶解后配制成 溶液。
滴定分析:量取 过氧化脲溶液至锥形瓶中,加入一定量稀 ,用准确浓度的 溶
液滴定至微红色,记录滴定体积,计算纯度。
回答下列问题:
(1)过滤中使用到的玻璃仪器有 (写出两种即可)。
(2)过氧化脲的产率为 。
(3)性质检测Ⅱ中的现象为 。性质检测I和Ⅱ分别说明过氧化脲具有的性质是 。
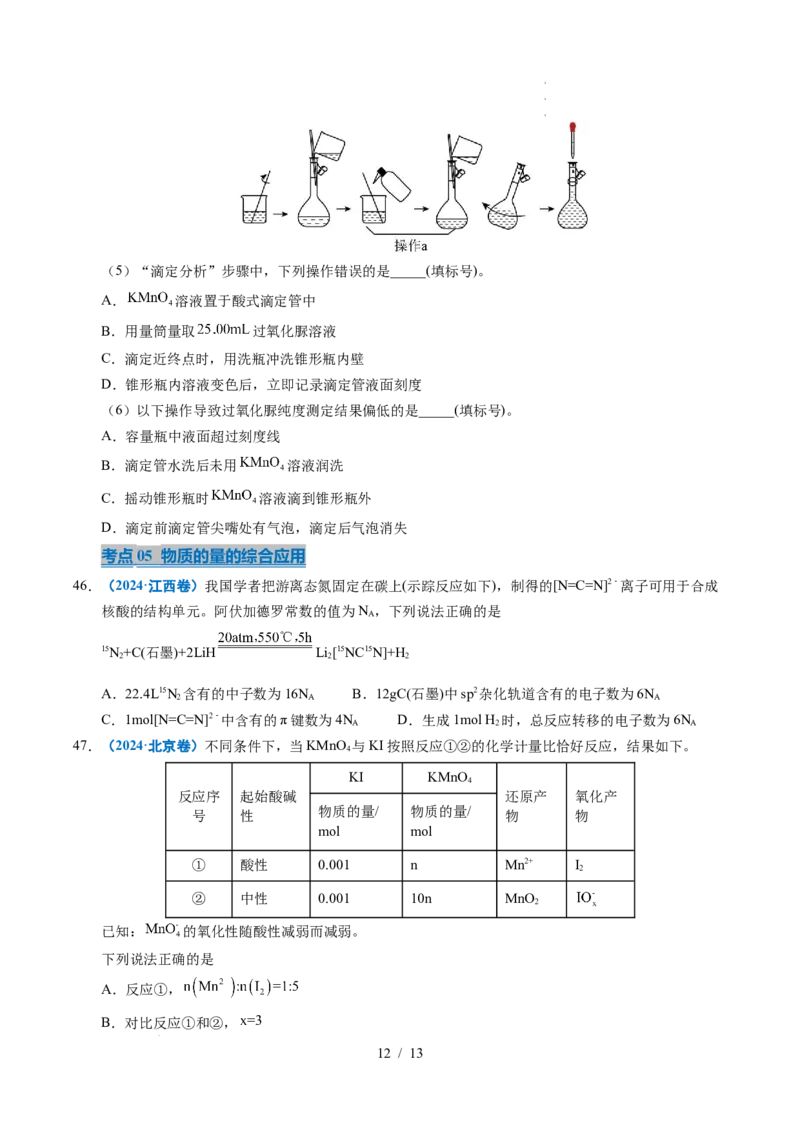
(4)下图为“溶液配制”的部分过程,操作a应重复3次,目的是 ,定容后还需要的操作为
。
11 / 13
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司(5)“滴定分析”步骤中,下列操作错误的是_____(填标号)。
A. 溶液置于酸式滴定管中
B.用量筒量取 过氧化脲溶液
C.滴定近终点时,用洗瓶冲洗锥形瓶内壁
D.锥形瓶内溶液变色后,立即记录滴定管液面刻度
(6)以下操作导致过氧化脲纯度测定结果偏低的是_____(填标号)。
A.容量瓶中液面超过刻度线
B.滴定管水洗后未用 溶液润洗
C.摇动锥形瓶时 溶液滴到锥形瓶外
D.滴定前滴定管尖嘴处有气泡,滴定后气泡消失
考点 05 物质的量的综合应用
46.(2024·江西卷)我国学者把游离态氮固定在碳上(示踪反应如下),制得的[N=C=N]2﹣离子可用于合成
核酸的结构单元。阿伏加德罗常数的值为N ,下列说法正确的是
A
15N+C(石墨)+2LiH Li[15NC15N]+H
2 2 2
A.22.4L15N 含有的中子数为16N B.12gC(石墨)中sp2杂化轨道含有的电子数为6N
2 A A
C.1mol[N=C=N]2﹣中含有的π键数为4N D.生成1mol H 时,总反应转移的电子数为6N
A 2 A
47.(2024·北京卷)不同条件下,当KMnO 与KI按照反应①②的化学计量比恰好反应,结果如下。
4
KI KMnO
4
反应序 起始酸碱 还原产 氧化产
物质的量/ 物质的量/
号 性 物 物
mol mol
① 酸性 0.001 n Mn2+ I
2
② 中性 0.001 10n MnO
2
已知: 的氧化性随酸性减弱而减弱。
下列说法正确的是
A.反应①,
B.对比反应①和②,
12 / 13
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司C.对比反应①和②, 的还原性随酸性减弱而减弱
D.随反应进行,体系 变化:①增大,②不变
48.(2024·浙江卷)利用 可将废水中的 转化为对环境无害的物质后排放。反应原理为:
(未配平)。下列说法正确的是
A.X表示
B.可用 替换
C.氧化剂与还原剂物质的量之比为
D.若生成标准状况下的 气体 ,则反应转移的电子数为 ( 表示阿伏加德罗常数的值)
13 / 13
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司