文档内容
五年(2021-2025)高考化学真题分类汇编
专题05 化学计量
考点 五年考情(2021-2025) 命题趋势
2025·湖南卷、2025·河北卷、2025·黑吉辽蒙
卷、2025·云南卷、2025·广东卷、2024·福建
卷、2024·海南卷、2024·贵州卷、2024·广东
卷、2024·河北卷、2024·吉林卷、2023·河北
考点01 有关阿伏加德
卷、2023·福建卷、2023·重庆卷、2022·辽宁
罗常数的判断
卷、2023·海南卷、2023·广东卷、2023·浙江 有关化学吉林的考查常以选择
卷、2023·辽宁卷、2023·全国甲卷、2022·重庆 题形式出现,题目中等难度,
卷、2022·福建卷、2022·河北卷、2022·海南 常结合物质结构、盐类水解、
卷、2022·浙江卷、2022·全国甲卷 可逆反应等知识综合考查;以
物质的量为核心,依据化学方
考点02 阿伏加德罗定
2021·山东卷 程式的有关计算主要在非选择
律
题中出现,难度稍大。预计未
来有关阿伏加德罗常数类试题
热度有所降低,有关化学方程
考点03 物质的量浓度 2025·江苏卷、2021·广东卷
式中定量关系的计算考
查力度会有所加大。
考点04 一定物质的量 2025·山东卷、2025·云南卷、2024·广西卷、
浓度溶液的配制 2024·甘肃卷、2024·全国甲卷、2023·全国甲卷
考点05 物质的量的综
2024·江西卷、2024·北京卷、2024·浙江卷
合应用
考点 01 有关阿伏加德罗常数的判断
1.(2025·湖南卷)加热时,浓硫酸与木炭发生反应: (浓) 。设 为
阿伏加德罗常数的值。下列说法正确的是
A. 含质子数为
B.常温常压下, 含σ键数目为
C. 的稀硫酸中含 数目为
D. 与 充分反应得到 的分子数为
【答案】A
【解析】A.12g的12C的物质的量为1mol,每个12C原子含有6个质子,因此总质子数为6N ,A正
A
1 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司确;
B.常温常压下,6.72L CO 的物质的量小于0.3mol,每个CO 分子含2个σ键,总σ键数小于0.6N ,
2 2 A
B错误;
C.pH=1的稀硫酸中, 浓度为0.1mol/L,1L溶液中 数目为0.1N ,而非0.2N ,C错误;
A A
D.SO 与O 生成SO 的反应为可逆反应,无法完全转化,实际生成的SO 分子数小于N ,D错误;
2 2 3 3 A
故选A。
2.(2025·河北卷)设 是阿伏加德罗常数的值,下列说法错误的是
A. 晶体内氢键的数目为
B. 的NaF溶液中阳离子总数为
C.28g环己烷和戊烯的混合物中碳原子的数目为
D.铅酸蓄电池负极增重96g,理论上转移电子数为
【答案】B
【解析】A.每个水分子在冰中形成4个氢键,但每个氢键被两个分子共享,故每个分子贡献2个氢
键。 ,氢键数目为 ,A正确;
B. 溶液中阳离子包括 。 ,根据电荷守恒:
,钠离子不会水解,并且水电离出少量氢离子,则有 ,所以阳离子总数大于
,B错误;
C.环己烷和戊烯的最简式均为 , 混合物含 单元,对应 碳原子,碳原子数目为
,C正确;
D.铅酸蓄电池负极反应为 。增重 对应生成 ,转移 电
子,数目为: ,D正确;
故选B。
3.(2025·黑吉辽蒙卷)钠及其化合物的部分转化关系如图。设 为阿伏加德罗常数的值,下列说法正
确的是
A.反应①生成的气体,每11.2L(标准状况)含原子的数目为
B.反应②中2.3gNa完全反应生成的产物中含非极性键的数目为
C.反应③中 与足量 反应转移电子的数目为
D. 溶液中, 的数目为
2 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司【答案】A
【解析】A.反应①电解熔融NaCl生成 ,标准状况下11.2L 为0.5mol,含0.5×2=1mol原子,即
,A正确;
B.2.3g Na(0.1mol)与氧气加热反应生成0.05mol ,每个 含1个O-O非极性键,所
以非极性键数目为 ,B错误;
C. 与水反应生成氢氧化钠和氧气,化学方程式为 ,1mol 与
水反应转移1mol电子,数目为 ,C错误;
D.ClO⁻在水中会水解,故 数目小于 ,D错误;
故选A。
4.(2025·云南卷) 为阿伏加德罗常数的值。下列说法正确的是
A. 中原子的数目为
B. 所含中子的数目为
C. 粉和足量S完全反应,转移电子的数目为
D. 盐酸与足量 反应,生成 的数目为
【答案】B
【解析】A.未指明气体是否处于标准状况,22.4L CH 的物质的量无法确定为1mol,因此原子数目无
4
法确定为5N ,A错误;
A
B.18O的中子数为18-8=10,1mol18O含10mol中子,数目为10N ,B正确;
A
C.28g Fe(0.5mol)与S反应生成FeS,Fe的氧化态为+2,转移电子数为0.5×2=1mol=1N ,而非
A
1.5N ,C错误;
A
D.浓盐酸与MnO 反应时,随反应进行浓度降低,反应停止,实际生成Cl 的物质的量小于理论值
2 2
0.3mol,D错误;
故选B。
5.(2025·广东卷)设 为阿伏加德罗常数的值。下列说法正确的是
A. 的中子数,比 的多
B. 与水蒸气完全反应,生成 的数目为
C.在 的 溶液中, 的数目为
D.标准状况下的 与足量 反应,形成的共价键数目为
【答案】D
【解析】A. 的中子数为10, 的中子数为8,每个O 分子含2个O原子,1mol 比1mol
2
3 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司多4N 个中子,A错误;
A
B.Fe与水蒸气反应生成Fe O 和H,1mol Fe生成 mol H,数目为 N ,B错误;
3 4 2 2 A
C. 在水中会水解,溶液中 的数目小于0.1N ,C错误;
A
D.1mol Cl 与H 反应生成2mol HCl,形成2mol H-Cl键,共价键数目为2N ,D正确;
2 2 A
故选D。
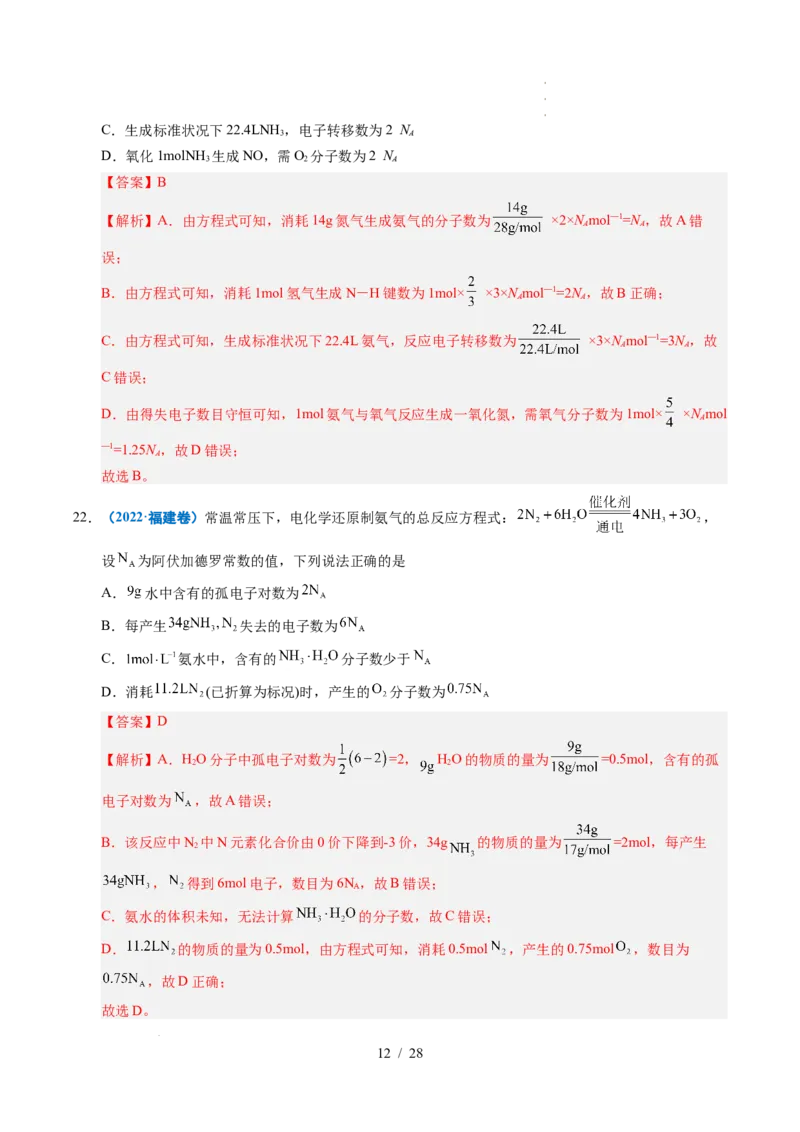
6.(2024·福建卷)我国科学家预测了稳定的氮单质分子 (结构如图)。设 为阿伏加德罗常数的值。下
列说法错误的是
A. 的 键电子数为
B. 的(价层)孤电子对数为
C. 的 杂化N原子数为
D. 完全分解,产生的 分子数为
【答案】B
【解析】A.1个 分子中有8个 键,每个 键含有2个电子,共16个电子, 的 键电子数
为 ,A正确;
B. 分子中所有原子共面可知 1个 分子1~6处的6个N原子采取sp2杂
化,7、8两处N原子采取sp杂化,其中8、1、3、4、5、6六处N原子各有一对孤电子对即1个 分
子有6对孤电子对, 的(价层)孤电子对数为 ,B错误;
C. 分子中所有原子共面可知 ,1个 分子有6个N原子采取sp2杂化,
的 杂化N原子数为 ,C正确;
D. 为 ,含有8molN,根据氮原子守恒, 完全分解产生4mol ,产
4 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司生的N 分子数为4N ,D正确;
2 A
故答案为:B。
7.(2024·海南卷) 代表阿伏加德罗常数的值。下列说法正确的是
A. 超重水( )所含的电子数目为
B. 溶液中 的数目为
C.过量C与 充分反应转移电子数目为
D. 与足量 发生取代反应生成HCl分子的数目为
【答案】A
【解析】A. 超重水( 为 )所含的电子为0.1mol×10=1mol,电子数目为 ,A
正确;
B.次氯酸根离子为弱酸根离子,水溶液中部分水解生成次氯酸和氢氧根离子,故
溶液中 的数目小于 ,B错误;
C.过量C与 充分生成硅单质和CO,硅化合价由+4变为0,则反应转移电子数目为4 ,C
错误;
D.甲烷与氯气发生取代反应为连锁反应,同时得到四种氯代产物和HCl,结合氯守恒, 与足
量 发生取代反应生成HCl分子的数目为 ,D错误;
故选A。
8.(2024·贵州卷)二氧化氯 可用于自来水消毒。实验室用草酸 和 制取 的反
应为 。设 为阿伏加德罗常数的值。下
列说法正确的是
A. 中含有的中子数为
B.每生成 ,转移电子数为
C. 溶液中含有的 数目为
D.标准状况下, 中含 键数目为
【答案】D
【解析】A. 分子中H原子无中子, 原子的中子数为10,则 中含有的中子数为
,故A错误;
B.由反应方程式 可知,每生成2mol
转移电子数为2mol,则每生成 ,即1mol 转移电子数为 ,故B错误;
5 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司C.未给出草酸溶液的体积,无法计算氢离子的物质的量,故C错误;
D.1个二氧化碳分子中含有2个 键和2个π键,则标准状况下 ,即1mol 中含 键数目
为 ,故D正确;
故选D。
9.(2024·广东卷)设 为阿伏加德罗常数的值。下列说法正确的是
A. 中含有 键的数目为
B. 溶液中含 的数目为
C. 和 的混合气体含有的分子数目为
D. 与 反应生成 ,转移电子数目为
【答案】A
【解析】A.26gC H 的物质的量为1mol,一个C H 分子中含有3个 键,故26gC H 中含有 键的数
2 2 2 2 2 2
目为3N ,A正确;
A
B. 在水溶液中发生水解,1L1mol⋅L-1NH NO 溶液中含 的数目小于N ,B错误;
4 3 A
C.CO和H 均由分子构成,1molCO和H 的混合气体含有的分子数目为N ,C错误;
2 2 A
D.Na与HO反应生成11.2LH ,由于未给出气体所处的状态,无法求出生成气体的物质的量,也无法
2 2
得出转移电子数目,D错误;
故选A。
10.(2024·河北卷)超氧化钾 可用作潜水或宇航装置的 吸收剂和供氧剂,反应为
, 为阿伏加德罗常数的值。下列说法正确的是
A. 中 键的数目为
B. 晶体中离子的数目为
C. 溶液中 的数目为
D.该反应中每转移 电子生成 的数目为
【答案】A
【解析】A. (即 ) 中 键的数目为 ,A正确;
B. 由 和 构成, 晶体中离子的数目为 ,B错误;
C. 在水溶液中会发生水解: ,故 溶液中 的数目
小于 ,C错误;
D.该反应中部分氧元素化合价由 价升至0价,部分氧元素化合价由 价降至 价,则每
参加反应转移 电子,每转移 电子生成 的数目为 ,D错误;
6 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司故选A。
11.(2024·吉林卷)硫及其化合物部分转化关系如图。设 为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下, 中原子总数为
B. 溶液中, 数目为
C.反应①每消耗 ,生成物中硫原子数目为
D.反应②每生成 还原产物,转移电子数目为
【答案】D
【解析】A.标况下SO 为气体,11.2L SO 为0.5mol,其含有1.5mol原子,原子数为1.5N ,A错
2 2 A
误;
B.SO 为弱酸阴离子,其在水中易发生水解,因此,100mL 0.1mol L-1 Na SO 溶液中SO 数目小于
2 3
0.01N ,B错误;
A
C.反应①的方程式为SO +2H S=3S +2H O,反应中每生成3mol S消耗2mol HS,3.4g HS为
2 2 2 2 2
0.1mol,故可以生成0.15mol S,生成的原子数目为0.15N ,C错误;
A
D.反应②的离子方程式为3S+6OH-=SO +2S2-+3H O,反应的还原产物为S2-,每生成2mol S2-共转移
2
4mol电子,因此,每生成1mol S2-,转移2mol电子,数目为2N ,D正确;
A
故答案选D。
12.(2023·河北卷) 为阿伏加德罗常数的值,下列说法正确的是
A. 的 溶液中含 个
B.反应 生成 ,转移 个电子
C. 号元素的原子一定含有 个质子、 个中子
D. 组成为 的烃一定含有 个双键
【答案】B
【解析】A. 即 ,故 的 溶液中含 的数目为 ,A错
误;
B. 中H的化合价由-1和+1归中到0价,转移1个电子,故生成 ,
转移 个电子,B正确;
C.6号元素为碳元素,碳定含有的质子数为6,但中子数却不一定为6,故 号元素的原子一定
7 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司含有 个质子、中子数不一定为 ,C错误;
D.通式 的有机物可能是单烯烃,也可能是环烷烃,为环烷烃时不含双键,D错误;
故选B。
13.(2023·福建卷)我国新一代载人飞船使用的绿色推进剂硝酸羟胺 在催化剂作用下可
完全分解为 和 。 为阿伏加德罗常数的值,下列说法正确的是
A. 含有的质子数为
B. 固态硝酸羟胺含有的离子数为
C. 硝酸羟胺含有的 键数为
D.硝酸羟胺分解产生 (已折算为标况)的同时,生成 分子数为
【答案】C
【解析】A. 含有的质子数为 ,A错误;
B. 固态硝酸羟胺含有的离子数为 ,B错误;
C. 硝酸羟胺含有的 键数为 ,C正确;
D.根据题意硝酸羟胺分解的化学方程式为 ,根据计量系数关系
可知硝酸羟胺分解产生标况下 ,同时生成 分子数为 ,D错误;
故选C。
14.(2023·重庆卷)已知反应: , 为阿伏加德罗常数的值,若消耗
(标准状况) ,下列叙述错误的是
A.转移的电子数为 B.生成的 质量为
C.生成的氧化产物分子数为 D.生成的 含有孤电子对数为
【答案】C
【解析】A.反应 中F的化合价由0价转化为-1价,O的化合价由-2
价变为+2价,转移电子数为4e-,若消耗 (标准状况) 即 =2mol,故转移的电子数为
,A正确;
B.根据反应 ,每消耗2molF 生成的 质量为2mol =
2
,B正确;
C.根据反应 可知反应生成的氧化产物为OF ,每消耗2molF 生成的
2 2
8 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司氧化产物OF 分子数为 ,C错误;
2
D.根据反应 可知,每消耗2molF 生成HO的物质的量为1mol,又
2 2
知1个HO中含有2对孤电子对,即生成的 含有孤电子对数为 ,D正确;
2
故答案为C。
15.(2022·辽宁卷)设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.标准状况下,22.4LHCl气体中H+数目为N
A
B.28gC H 分子中含有的 键数目为4N
2 4 A
C.1.8g18O中含有的中子数为N
A
D.pH=12的NaCO 溶液中 数目为0.01N
2 3 A
【答案】C
【解析】A.标准状况下,22.4LHCl的物质的量为1mol,HCl是共价化合物,没有H+,故A错误;
B.1个C H 中含有5个σ键,28gC H 分子中含有的σ键数目为 mol-1=5N ,故B错
2 4 2 4 A
误;
C.18O中子数为18-8=10,1.8g18O的物质的量为 ,含有的中子数为N ,故C正确;
A
D.未知溶液的体积,无法计算其离子数目,故D错误;
故选:C。
16.(2023·海南卷) 代表阿伏加德罗常数的值。下列说法正确的是
A.2.4g镁条在空气中充分燃烧,转移的电子数目为
B.5.6g铁粉与 的HCl的溶液充分反应,产生的气体分子数目为
C.标准状况下, 与 充分反应,生成的 分子数目为
D. 完全溶于 所得溶液, 微粒数目为
【答案】A
【解析】A.2.4g镁条在空气中充分燃烧,镁被氧化为+2价,故转移的电子数目为 ,故A正
确;
B.5.6g铁粉与 的HCl的溶液充分反应,产生的氢气的分子数目为 ,故B错误;
C.标准状况下, 与 充分反应,该反应为可逆反应,反应物不能完全转化为生成
物,故生成的 分子数目无法计算,故C错误;
D. 完全溶于 所得溶液,发生反应: ,生成的 微粒
数目小于 ,故D错误。
9 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司答案为:A。
17.(2023·广东卷)设 为阿伏加德罗常数的值。侯氏制碱法涉及 和 等物质。下
列叙述正确的是
A. 含有的共价键数目为
B. 完全分解,得到的 分子数目为
C.体积为 的 溶液中, 数目为
D. 和 的混合物中含 ,则混合物中质子数为
【答案】D
【解析】A.铵根中存在4个N-H共价键,1mol NH Cl 含有的共价键数目为4N ,A错误;
4 A
B.碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,1mol NaHCO 完全分解,得到0.5molCO 分子,B
3 2
错误;
C. , 会发生水解和电离,则1mol NaHCO 溶液中 数目小于
3
1N ,C错误;
A
D.NaCl 和NH Cl的混合物中含1molCl-,则混合物为1mol,质子数为28N ,D正确;
4 A
故答案为:D。
18.(2023·浙江卷)N 为阿伏加德罗常数的值,下列说法正确的是
A
A.4.4gC HO中含有σ键数目最多为0.7N
2 4 A
B.1.7gHO 中含有氧原子数为0.2N
2 2 A
C.向1L0.1mol/LCHCOOH溶液通氨气至中性,铵根离子数为0.1N
3 A
D.标准状况下,11.2LCl 通入水中,溶液中氯离子数为0.5N
2 A
【答案】A
【解析】A.1个C HO中含有6个σ键和1个π键(乙醛)或7个σ键(环氧乙烷),4.4gC HO的物质的
2 4 2 4
量为0.1mol,则含有σ键数目最多为0.7N ,A正确;
A
B.1.7gHO 的物质的量为 =0.05mol,则含有氧原子数为0.1N ,B不正确;
2 2 A
C.向1L0.1mol/LCHCOOH溶液通氨气至中性,溶液中存在电荷守恒关系:c(CHCOO-)
3 3
+c(OH-)=c(NH )+c(H+),中性溶液c(OH-)=c(H+),则c(CHCOO-)=c(NH ),再根据物料守恒:
3
n(CHCOO-)+n(CH COOH)=0.1mol,得出铵根离子数小于0.1N ,C不正确;
3 3 A
D.标准状况下,11.2LCl 的物质的量为0.5mol,通入水中后只有一部分Cl 与水反应生成H+、Cl-和
2 2
HClO,所以溶液中氯离子数小于0.5N ,D不正确;
A
故选A。
19.(2023·辽宁卷)我国古代四大发明之一黑火药的爆炸反应为: 。
设 为阿伏加德罗常数的值,下列说法正确的是
10 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A. 含 键数目为 B.每生成 转移电子数目为
C. 晶体中含离子数目为 D. 溶液中含 数目为
【答案】C
【解析】A. 分子含有2个 键,题中没有说是标况条件下,气体摩尔体积未知,无法计算 键个
数,A项错误;
B.2.8g 的物质的量 ,1mol 生成转移的电子数为12 ,则0.1mol 转
移的电子数为1.2 ,B项错误;
C.0.1mol 晶体含有离子为 、 ,含有离子数目为0.2 ,C项正确;
D.因为 水解使溶液中 的数目小于0.1 ,D项错误;
答案选C。
20.(2023·全国甲卷) 为阿伏加德罗常数的值。下列叙述正确的是
A. 异丁烷分子中共价键的数目为
B.标准状况下, 中电子的数目为
C. 的 溶液中 的数目为
D. 的 溶液中 的数目为
【答案】A
【解析】A.异丁烷的结构式为 ,1mol异丁烷分子含有13N 共价键,所以0.50mol
A
异丁烷分子中共价键的数目为6.5N ,A正确;
A
B.在标准状况下,SO 状态为固态,不能计算出2.24L SO 物质的量,故无法求出其电子数目,B错
3 3
误;
C.pH=2的硫酸溶液中氢离子浓度为c(H+)=0.01mol/L,则1.0L pH=2的硫酸溶液中氢离子数目为
0.01N ,C错误;
A
D. 属于强碱弱酸盐,在水溶液中CO 会发生水解,所以1.0L 1.0 mol/L的NaCO 溶液中CO
2 3
的数目小于1.0N ,D错误;
A
故选A。
21.(2022·重庆卷)工业上用N 和H 合成NH ,N 代表阿伏加德罗常数的值,下列说法正确的是
2 2 3 A
A.消耗14gN 生成NH 分子数为2 N
2 3 A
B.消耗1molH ,生成N-H键数为2 N
2 A
11 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司C.生成标准状况下22.4LNH ,电子转移数为2 N
3 A
D.氧化1molNH 生成NO,需O 分子数为2 N
3 2 A
【答案】B
【解析】A.由方程式可知,消耗14g氮气生成氨气的分子数为 ×2×N mol—1=N ,故A错
A A
误;
B.由方程式可知,消耗1mol氢气生成N-H键数为1mol× ×3×N mol—1=2N ,故B正确;
A A
C.由方程式可知,生成标准状况下22.4L氨气,反应电子转移数为 ×3×N mol—1=3N ,故
A A
C错误;
D.由得失电子数目守恒可知,1mol氨气与氧气反应生成一氧化氮,需氧气分子数为1mol× ×N mol
A
—1=1.25N ,故D错误;
A
故选B。
22.(2022·福建卷)常温常压下,电化学还原制氨气的总反应方程式: ,
设 为阿伏加德罗常数的值,下列说法正确的是
A. 水中含有的孤电子对数为
B.每产生 失去的电子数为
C. 氨水中,含有的 分子数少于
D.消耗 (已折算为标况)时,产生的 分子数为
【答案】D
【解析】A.HO分子中孤电子对数为 =2, HO的物质的量为 =0.5mol,含有的孤
2 2
电子对数为 ,故A错误;
B.该反应中N 中N元素化合价由0价下降到-3价,34g 的物质的量为 =2mol,每产生
2
, 得到6mol电子,数目为6N ,故B错误;
A
C.氨水的体积未知,无法计算 的分子数,故C错误;
D. 的物质的量为0.5mol,由方程式可知,消耗0.5mol ,产生的0.75mol ,数目为
,故D正确;
故选D。
12 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司23.(2022·河北卷)N 是阿伏加德罗常数的值。下列说法正确的是
A
A.3.9gNaO 与足量水反应,转移电子个数为0.1N
2 2 A
B.1.2gMg在空气中燃烧生成MgO和MgN,转移电子个数为0.1N
3 2 A
C.2.7gAl与足量NaOH溶液反应,生成H 的个数为0.1N
2 A
D.6.0gSiO 与足量NaOH溶液反应,所得溶液中SiO 的个数为0.1N
2 A
【答案】B
【解析】A.过氧化钠与水反应生成氢氧化钠和氧气,则3.9g过氧化钠与足量水反应,转移电子个数
为 ×1×N mol-1=0.05N ,故A错误;
A A
B.镁在空气中燃烧无论生成氧化镁,还是氮化镁,镁均转化为镁离子,则1.2gMg在空气中燃烧生成
氧化镁和氮化镁时,转移电子个数为 ×2×N mol-1=0.1N ,故B正确;
A A
C.铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,则2.7g铝与足量氢氧化钠溶液反应生成氢气的个数
为 × ×N mol-1=0.15N ,故C错误;
A A
D.二氧化硅与氢氧化钠溶液反应生成硅酸钠和水,硅酸钠在溶液中发生水解反应,则由原子个数守
恒可知,6.0g二氧化硅与足量氢氧化钠溶液反应所得溶液中硅酸根离子的个数小于
×N mol-1=0.1N ,故D错误;
A A
故选B。
24.(2022·海南卷)在2.8gFe中加入100mL3mol/LHCl,Fe完全溶解。N 代表阿伏加德罗常数的值,下
A
列说法正确的是
A.反应转移电子为0.1mol B.HCl溶液中 数为3N
A
C. 含有的中子数为1.3N D.反应生成标准状况下气体3.36L
A
【答案】A
【分析】2.8gFe的物质的量为0.05mol;100mL 3mol·L-1HCl中H+和Cl-的物质的量均为0.3mol,两者
发生反应后,Fe完全溶解,而盐酸过量。
【解析】A.Fe完全溶解生成Fe2+,该反应转移电子0.1mol,A正确;
B.HCl溶液中Cl-的物质的量为0.3mol,因此,Cl-数为0.3N ,B不正确;
A
C.56Fe 的质子数为26、中子数为30,2.8g56Fe的物质的量为0.05mol,因此,2.8g56Fe含有的中子数
为1.5N ,C不正确;
A
D.反应生成H 的物质的量为0.05mol,在标准状况下的体积为1.12L ,D不正确;
2
综上所述,本题A。
25.(2022·浙江卷) 为阿伏加德罗常数的值,下列说法正确的是
13 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A. 中含有 个阳离子
B. 乙烷和丙烯的混合气体中所含碳氢键数为
C. 含有中子数为
D. 和 于密闭容器中充分反应后, 分子总数为
【答案】C
【解析】A. 由钠离子和硫酸氢根离子构成,其中的阳离子只有钠离子, 的物
质的量为0.1mol,因此,其中只含有 个阳离子,A说法不正确;
B.没有指明气体的温度和压强,无法确定 乙烷和丙烯的混合气体的物质的量是多少,因此,无
法确定其中所含碳氢键的数目,B说法不正确;
C. 分子中有6个中子, 的物质的量为0.5mol,因此, 含有的中子数为 ,C说
法正确;
D. 和 发生反应生成 ,该反应是可逆反应,反应物不能完全转化为生成物,因此,
和 于密闭容器中充分反应后, 分子总数小于 ,D说法不正确。
综上所述,本题选C。
26.(2022·全国甲卷) 为阿伏加德罗常数的值,下列说法正确的是
A.25℃, 下, 氢气中质子的数目为
B .溶液中, 的数目为
C. 苯甲酸完全燃烧,生成 的数目为
D.电解熔融 ,阴极增重 ,外电路中通过电子的数目为
【答案】C
【解析】A.25℃、101kPa不是标准状况,不能用标况下的气体摩尔体积计算氢气的物质的量,故A
错误;
B.Al3+在溶液中会发生水解生成Al(OH) ,因此2.0L 1.0 mol/L的AlCl 溶液中Al3+数目小于2.0N ,故
3 3 A
B错误;
C.苯甲酸燃烧的化学方程式为 ,1mol苯甲酸燃烧生成
7molCO ,则0.2mol苯甲酸完全燃烧生成1.4molCO,数目为1.4N ,故C正确;
2 2 A
D.电解熔融CuCl 时,阳极反应为 ,阴极反应为 ,阴极增加的重量为Cu
2
的质量,6.4gCu的物质的量为0.1mol,根据阴极反应可知,外电路中通过电子的物质的量为0.2mol,
数目为0.2N ,故D错误;
A
答案选C。
14 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司27.(2021·重庆卷)葡萄酒中含有CHCHOH、CHCOOH、 SO 和CO 等多种成分。若N 代表阿伏加
3 2 3 2 2 A
德罗常数的值,下列说法正确的是
A.46gCHCHOH中含有C-H键数为5N
3 2 A
B.1L1 mol·L-1CHCOOH溶液中含有氢离子数为N
3 A
C.1 mol SO 与1 mol O 完全反应转移的电子数为4 N
2 2 A
D.11.2L (标准状况) CO 完全溶于水后溶液中HCO 分子数为0.5N
2 2 3 A
【答案】A
【解析】A.46gCHCHOH的物质的量为 ,1mol乙醇含有5molC-H键,含有
3 2
C-H键数为5N ,A正确;
A
B.1L1 mol·L-1CHCOOH的物质的量为n=cV=1mol,由于醋酸是弱酸,不能完全电离出氢离子,
3
1molCH COOH溶液中含有氢离子数小于N ,B错误;
3 A
C .SO 与O 反应 是可逆反应,不能完全转化,则1 mol SO 与1 mol O 完全反应
2 2 2 2
生成小于1mol SO ,S元素从+4升到+6价,转移的电子数小于2N ,C错误;
3 A
D.标准状况下11.2L CO 的物质的量为 ,0.5molCO 与水反应生成
2 2
0.5molHCO,由于溶液中HCO 部分电离,则HCO 分子数小于0.5N ,D错误;
2 3 2 3 2 3 A
故选:A。
28.(2022·浙江卷)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
B.1.8g重水(D O)中所含质子数为N
2 A
C.足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 A
D.32g甲醇的分子中含有C—H键的数目为4N
A
【答案】A
【解析】A.1LpH为12的Ba(OH) 溶液中含有OH-的浓度为0.01mol/L,物质的量0.01mol/L
2
1L=0.01mol,OH-的数目为0.01N ,A正确;
A
B.1.8g重水(D O)的物质的量为:0.09mol,所含质子数为0.9N ,B错误;
2 A
C.足量的浓盐酸与8.7gMnO(0.1mol)反应,+4价Mn转化生成Mn2+,转移电子的数目为0.2N ,C错
2 A
误;
D.甲醇的结构简式为:CHOH,32g (1mol)的分子中含有C—H键的数目为3N ,D错误;
3 A
答案选A。
29.(2021·福建卷)设 为阿伏加德罗常数的值.下列说法正确的是
A. 所含极性共价键的数目为
B. 晶体中阴、阳离子总数为
15 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司C. 与足量 反应生成 的分子数为
D.电解熔融 制 ,电路中通过的电子数为
【答案】B
【解析】A.没有标明气体的存在状态, 的物质的量不一定为0.5mol,故A错误;
B.硫酸氢钠晶体中存在钠离子和硫酸氢根离子,硫酸氢钠的摩尔质量为120g/mol,所以12g硫酸氢
钠晶体的物质的量为0.1mol,阴、阳离子总数为 ,故B正确;
C.甲烷与足量氯气反应生成一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳和氯化氢,因此
与足量 反应生成 的分子数小于 ,故C错误;
D.电解熔融的氯化镁生成金属镁,镁由+2价降低到0价,因此1mol氯化镁完全电解生成金属镁,转
移2mol电子,电解熔融 制 (物质的量为0.1mol),电路中通过的电子数为 ,故
D错误;
故选B。
30.(2021·海南卷) 代表阿伏加德罗常数的值。下列说法正确的是
A. 中含有的电子数为1.3
B. 中含有的共价键的数目为0.1
C. 肼 含有的孤电子对数为0.2
D. ,生成 乙烷时断裂的共价键总数为
【答案】C
【解析】A.1个 的电子数为10,故 中含有的电子数为1.0 ,故A错误;
B. 的电子式为 ,含有1个共价键, 的物质的量为
=0.05mol,故 中含有的共价键的数目为0.05 ,故B错误;
C.肼 中每个N原子上各有1个孤电子对,故 肼 含有的孤电子对数为
0.2 ,故C正确;
D.发生 反应时,C=C中的一个键和H-H键都断裂,故生成 乙烷时断
裂的共价键总数为2 ,故D错误;
故选C。
31.(2021·湖北卷)N 为阿伏加德罗常数的值。下列说法错误的是
A
A.23gCHCHOH中sp3杂化的原子数为N
3 2 A
B.0.5molXeF 中氙的价层电子对数为3N
4 A
16 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司C.1mol[Cu(H O) ]2+中配位键的个数为4N
2 4 A
D.标准状况下,11.2LCO和H 的混合气体中分子数为0.5N
2 A
【答案】A
【解析】A. 中C和O均为 杂化,23g乙醇为0.5mol, 杂化的原子数为 ,选项A
错误;
B. 中氙的孤电子对数为 ,价层电子对数为 ,则 中氙的价层电子
对数为 ,选项B正确;
C.1个 中含有4个配位键,1mol 含配位键的个数为 ,选项C正确;
D.标准状况下。11.2LCO和 的混合气体为0.5mol,分子数为 ,选项D正确。
答案选A。
32.(2021·天津卷)设N 为阿伏加德罗常数的值,下列叙述正确的是
A
A.1mol/LHCl溶液中,HCl分子的数目为N
A
B.22.4L氢气中,H 分子的数目为N
2 A
C.180g葡萄糖中,C原子的数目为6N
A
D.1molN 中,σ键的数目为3N
2 A
【答案】C
【解析】A.体积未知,HCl分子的数目不能计算,故A错误;
B.没有标准状态,不能计算H 分子的数目,故B错误;
2
C.葡萄糖的分子式为C H O,故180g葡萄糖的分子的物质的量为1mol,C原子的数目为6N ,故C
6 12 6 A
正确;
D.1molN 中有1molσ键,故σ键的数目为N ,故D错误;
2 A
故选C。
33.(2021·浙江卷)设 为阿伏加德罗常数的值,下列说法不正确的是
A.标准状况下, 中含有中子数为
B. (分子结构: )中的共价键数目为
C. 的 水溶液中含有氧原子数为
D. 三肽 (相对分子质量:189)中的肽键数目为
【答案】C
【解析】A.标准状况下, 的物质的量为:0.05mol,一个 中含有中子数为: 个,
所以 中含有中子数为 ,A正确;
17 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司B. 的物质的量为:0.25mol,根据白磷的分子结构可知一个白磷分子里含有六条共价键,所以
共价键数目为: ,B正确;
C. 的 水溶液中含有溶质氢氧化钠和溶剂水,氧原子数目为二者氧原子数目的
加和,C错误;
D. 三肽 的物质的量为:0.1mol,三分子氨基酸脱水缩合形成三肽,三肽中含有两个
肽键,所以 三肽 中的肽键数目为 ,D正确;
答案为:C。
34.(2021·全国甲卷) 为阿伏加德罗常数的值。下列叙述正确的是
A. 重水( )中含有的质子数为
B. 的 与 完全反应时转移的电子数为
C. 环状 ( )分子中含有的 键数为
D. 的 溶液中 离子数为
【答案】C
【解析】A. 的质子数为10,18g 的物质的量为 0.9mol, 则 重水( )中所含
质子数为 ,A错误;
B. 与 反应的化学方程式为:3NO +H O=2HNO +NO,该反应消耗3个NO 分子转移的电子
2 2 3 2
数为2个,则有3mol的NO 参与反应时,转移的电子数为 ,B错误;
2
C.一个 ( )分子中含有的 键数为8个,32gS 的物质的量为 mol,则
8
含有的 键数为 ,C正确;
D.酸性 溶液中存在: ,含Cr元素微粒有 和 ,则
的 溶液中 离子数应小于 ,D错误;
故选C。
35.(2021·河北卷)N 是阿伏加德罗常数的值,下列说法错误的是
A
A.22.4L(标准状况)氟气所含的质子数为18N
A
B.1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2N
A
C.电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为N
A
D.1L1mol•L-1溴化铵水溶液中NH 与H+离子数之和大于N
A
18 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司【答案】C
【解析】A.在标准状况下 氟气的物质的量为1mol,其质子数为1mol = ,A正
确;
B.碘蒸气与氢气发生的反应为: ,反应为可逆反应,有一定的限度,所以充
分反应,生成的碘化氢分子数小于 ,B正确;
C.电解饱和食盐水时电极总反应为:2NaCl+2H O 2NaOH+H ↑+Cl↑,若阴阳两极产生气体分别
2 2 2
是氢气与氯气,且物质的量之比为1:1,若气体的总质量为 ,则说明反应生成的氢气与氯气的物质
的量各自为1mol,根据关系式H 2e-可知,转移的电子数为 ,C错误;
2
D. 溴化铵水溶液存在电荷守恒,即c( )+c( )=c(Br-)+c(OH-),则物质的量也满足n(
)+n( )=n(Br-)+n(OH-),因为n(Br-)= ,所以该溶液中 与 离子数之和大
于 ,D正确;
故选C。
36.(2021·湖南卷) 为阿伏加德罗常数的值。下列说法正确的是
A. 含有的中子数为
B. 溶液中含有的 数为
C. 与 在密闭容器中充分反应后的分子数为
D. 和 (均为标准状况)在光照下充分反应后的分子数为
【答案】D
【解析】A. 的物质的量为 =0.9mol,1个 含0+(18-8)=10个中子,则
含有的中子数为 ,A错误;
B.未给溶液体积,无法计算,B错误;
C.存在2NO+O =2NO,2NO NO,因此 与 在密闭容器中充分反应后的分子数小
2 2 2 2 4
于 ,C错误;
D.甲烷和氯气在光照下发生取代,1mol氯气可取代1molH,同时产生1molHCl分子,分子数不变,
标准状况下 的物质的量为0.5mol, 的物质的量为1mol,在光照下充分反应后的分
子数为 ,D正确;
选D。
考点 02 阿伏加德罗定律
19 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司37.(2021·山东卷)X、Y均为短周期金属元素,同温同压下,0.1molX的单质与足量稀盐酸反应,生成
H 体积为VL;0.1molY的单质与足量稀硫酸反应,生成H 体积为VL。下列说法错误的是
2 1 2 2
A.X、Y生成H 的物质的量之比一定为
2
B.X、Y消耗酸的物质的量之比一定为
C.产物中X、Y化合价之比一定为
D.由 一定能确定产物中X、Y的化合价
【答案】D
【分析】设与1mol X反应消耗HCl的物质的量为amol,与1mol Y反应消耗HSO 的物质的量为
2 4
bmol,根据转移电子守恒以及H原子守恒可知 、 。
【解析】A.同温同压下,气体体积之比等于其物质的量之比,因此X、Y生成H 的物质的量之比一
2
定为 ,故A正确;
B. X、Y反应过程中消耗酸的物质的量之比为 ,因 ,因此 ,故B正确;
C.产物中X、Y化合价之比为 ,由B项可知 ,故C正确;
D.因短周期金属单质与盐酸或稀硫酸反应时,生成的盐中金属元素化合价有+1、+2、+3三种情况,
因此存在a=1,2,3,b=0.5,1的多种情况,由 可知,当a=1,b=0.5时, =1,当a=2,b=1
时, =1,两种情况下X、Y的化合价不同,因此根据 可能无法确定X、Y的化合价,故D错
误;
综上所述,错误的D项,故答案为D。
考点 03 物质的量浓度
38.(2025·江苏卷)用 草酸 溶液滴定未知浓度的 溶液。下列实验操作规范
的是
20 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A.配制草酸溶 B.润洗滴定
C.滴定 D.读数
液 管
【答案】D
【解析】A.定容时需要用玻璃棒引流,A错误;
B.润洗滴定管时应取少量标准液于滴定管中,倾斜着转动滴定管进行润洗,B错误;
C.滴定时,应手持锥形瓶上端轻微地摇动锥形瓶,不能手持锥形瓶底端摇动,C错误;
D.读数时,眼睛平视滴定管凹液面最低点,D正确;
答案选D。
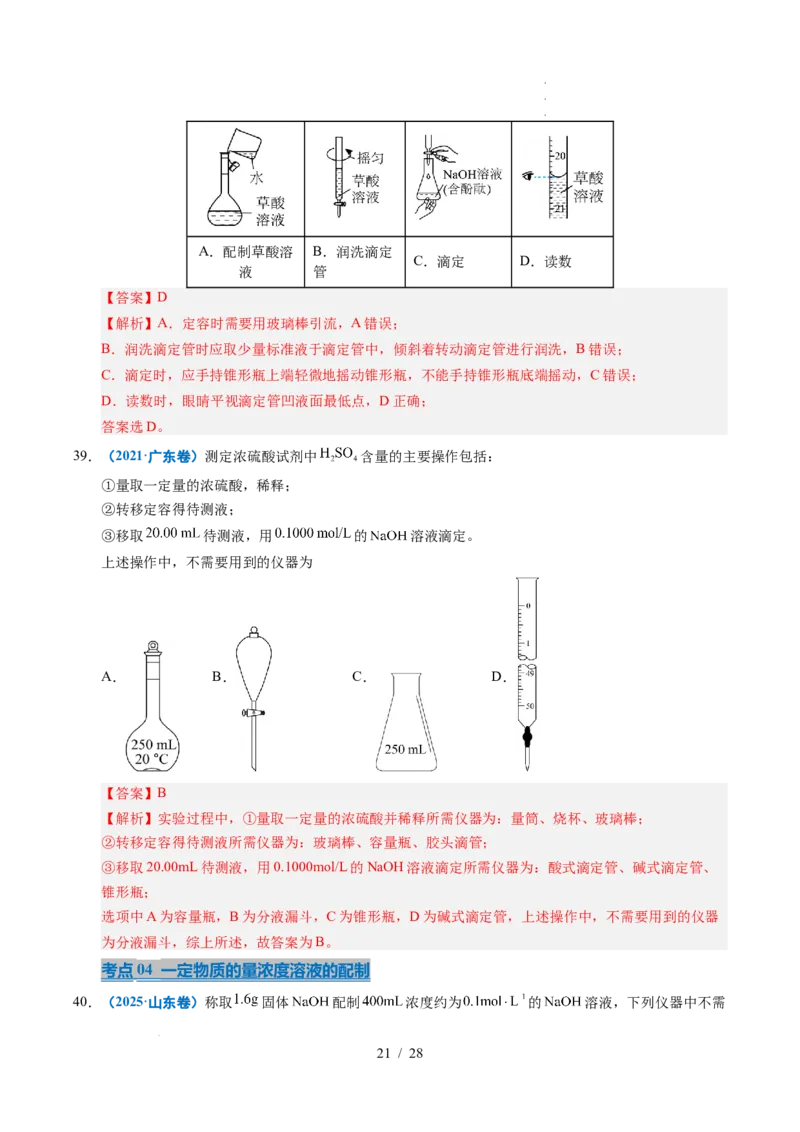
39.(2021·广东卷)测定浓硫酸试剂中 含量的主要操作包括:
①量取一定量的浓硫酸,稀释;
②转移定容得待测液;
③移取 待测液,用 的 溶液滴定。
上述操作中,不需要用到的仪器为
A. B. C. D.
【答案】B
【解析】实验过程中,①量取一定量的浓硫酸并稀释所需仪器为:量筒、烧杯、玻璃棒;
②转移定容得待测液所需仪器为:玻璃棒、容量瓶、胶头滴管;
③移取20.00mL待测液,用0.1000mol/L的NaOH溶液滴定所需仪器为:酸式滴定管、碱式滴定管、
锥形瓶;
选项中A为容量瓶,B为分液漏斗,C为锥形瓶,D为碱式滴定管,上述操作中,不需要用到的仪器
为分液漏斗,综上所述,故答案为B。
考点 04 一定物质的量浓度溶液的配制
40.(2025·山东卷)称取 固体 配制 浓度约为 的 溶液,下列仪器中不需
21 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司要使用的是
A. 烧杯 B. 容量瓶
C. 量筒 D. 细口试剂瓶(具橡胶塞)
【答案】B
【解析】A.溶解1.6g NaOH需要在烧杯中进行,故A需要;
B.1.6gNaOH的物质的量为 , ,即只需要溶解在400mL蒸馏
水中即可配制 浓度约为 的 溶液,无400mL容量瓶,准确配制500mL浓度为
的 溶液,需要 NaOH,即不需要 容量瓶,故B
不需要;
C.据B项分析可知,配制时需 量筒量取约400mL蒸馏水,故C需要;
D.NaOH溶液配制好后需要转移到试剂瓶中储存,氢氧化钠溶液呈碱性,能与玻璃中的二氧化硅反
应,不能选择玻璃塞,所以需要 细口试剂瓶(具橡胶塞),故D需要;
故选B。
41.(2025·云南卷)下列装置(省略部分夹持装置)或操作正确的是
A.制备 B.配制 溶液
C.探究Na与 反应 D.探究温度对化学平衡的影响
【答案】D
【解析】A. 和 固体混合物加热制取氨气,试管口要略向下倾斜,A错误;
B.配制 溶液,应在烧杯中溶解KCl固体,B错误;
C.金属钠与水反应剧烈,不能在试管中进行,应在烧杯中进行,且烧杯不能盛满水,C错误;
22 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司D.两个烧杯中分别盛有热水和冰水,可以通过观察气体的颜色深浅来探究温度对2NO (红棕色)
2
NO(无色)平衡的影响,D正确;
2 4
故选D。
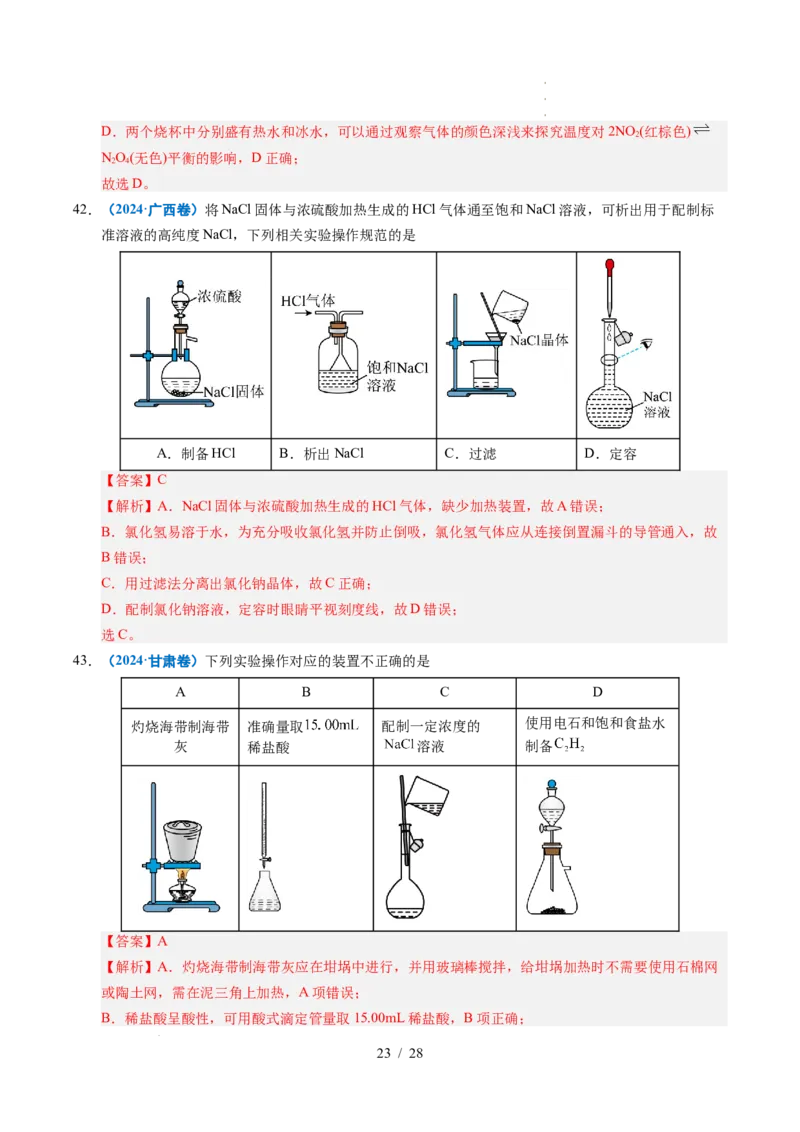
42.(2024·广西卷)将NaCl固体与浓硫酸加热生成的HCl气体通至饱和NaCl溶液,可析出用于配制标
准溶液的高纯度NaCl,下列相关实验操作规范的是
A.制备HCl B.析出NaCl C.过滤 D.定容
【答案】C
【解析】A.NaCl固体与浓硫酸加热生成的HCl气体,缺少加热装置,故A错误;
B.氯化氢易溶于水,为充分吸收氯化氢并防止倒吸,氯化氢气体应从连接倒置漏斗的导管通入,故
B错误;
C.用过滤法分离出氯化钠晶体,故C正确;
D.配制氯化钠溶液,定容时眼睛平视刻度线,故D错误;
选C。
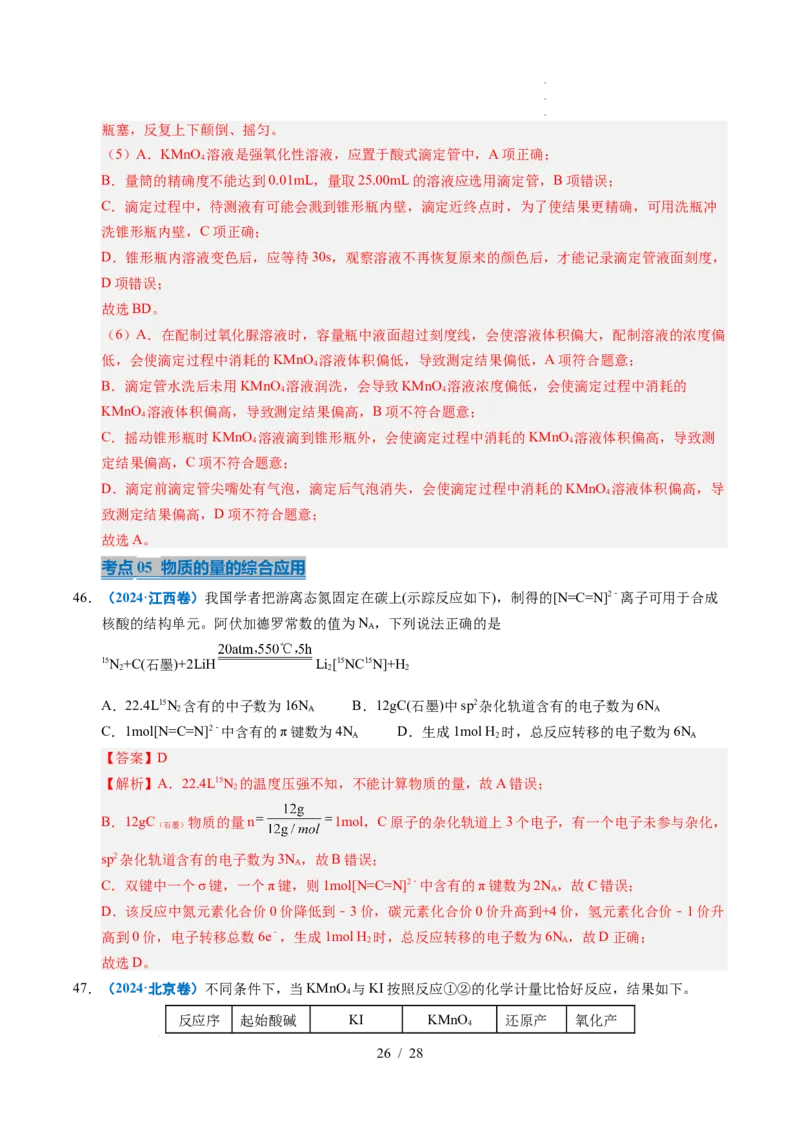
43.(2024·甘肃卷)下列实验操作对应的装置不正确的是
A B C D
灼烧海带制海带 准确量取 配制一定浓度的 使用电石和饱和食盐水
灰 稀盐酸 溶液 制备
【答案】A
【解析】A.灼烧海带制海带灰应在坩埚中进行,并用玻璃棒搅拌,给坩埚加热时不需要使用石棉网
或陶土网,需在泥三角上加热,A项错误;
B.稀盐酸呈酸性,可用酸式滴定管量取15.00mL稀盐酸,B项正确;
23 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司C.配制一定浓度的NaCl溶液时,需要将在烧杯中溶解得到的NaCl溶液通过玻璃棒引流转移到选定
规格的容量瓶中,C项正确;
D.电石的主要成分CaC 与水发生反应CaC +2H O→Ca(OH) +CH≡CH↑制取C H,该制气反应属于固
2 2 2 2 2 2
体与液体常温制气反应,分液漏斗中盛放饱和食盐水,具支锥形瓶中盛放电石,D项正确;
答案选A。
44.(2023·全国甲卷)实验室将粗盐提纯并配制 的 溶液。下列仪器中,本实验必须用
到的有
①天平 ②温度计 ③坩埚 ④分液漏斗 ⑤容量瓶 ⑥烧杯 ⑦滴定管 ⑧酒精灯
A.①②④⑥ B.①④⑤⑥ C.②③⑦⑧ D.①⑤⑥⑧
【答案】D
【解析】实验室将粗盐提纯时,需要将其溶于一定量的水中,然后将其中的硫酸根离子、钙离子、镁
离子依次用稍过量的氯化钡溶液、碳酸钠溶液和氢氧化钠溶液除去,该过程中有过滤操作,需要用到
烧杯、漏斗和玻璃棒;将所得滤液加适量盐酸酸化后蒸发结晶得到较纯的食盐,该过程要用到蒸发皿
和酒精灯;用提纯后得到的精盐配制溶液的基本步骤有称量、溶解、转移、洗涤、定容、摇匀等操
作,需要用到天平、容量瓶、烧杯、玻璃棒、胶头滴管等。综上所述,本实验必须用到的有①天平、
⑤容量瓶、⑥烧杯、⑧酒精灯,因此本题选D。
45.(2024·全国甲卷) (俗称过氧化脲)是一种消毒剂,实验室中可用尿素与过氧化氢制
取,反应方程式如下:
(一)过氧化脲的合成
烧杯中分别加入 、 蒸馏水和 尿素,搅拌溶解。 下反应
,冷却结晶、过滤、干燥,得白色针状晶体 。
(二)过氧化脲性质检测
I.过氧化脲溶液用稀 酸化后,滴加 溶液,紫红色消失。
Ⅱ.过氧化脲溶液用稀 酸化后,加入 溶液和四氯化碳,振荡,静置。
(三)产品纯度测定
溶液配制:称取一定量产品,用蒸馏水溶解后配制成 溶液。
滴定分析:量取 过氧化脲溶液至锥形瓶中,加入一定量稀 ,用准确浓度的 溶
液滴定至微红色,记录滴定体积,计算纯度。
回答下列问题:
(1)过滤中使用到的玻璃仪器有 (写出两种即可)。
(2)过氧化脲的产率为 。
(3)性质检测Ⅱ中的现象为 。性质检测I和Ⅱ分别说明过氧化脲具有的性质是 。
(4)下图为“溶液配制”的部分过程,操作a应重复3次,目的是 ,定容后还需要的操作为
24 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司。
(5)“滴定分析”步骤中,下列操作错误的是_____(填标号)。
A. 溶液置于酸式滴定管中
B.用量筒量取 过氧化脲溶液
C.滴定近终点时,用洗瓶冲洗锥形瓶内壁
D.锥形瓶内溶液变色后,立即记录滴定管液面刻度
(6)以下操作导致过氧化脲纯度测定结果偏低的是_____(填标号)。
A.容量瓶中液面超过刻度线
B.滴定管水洗后未用 溶液润洗
C.摇动锥形瓶时 溶液滴到锥形瓶外
D.滴定前滴定管尖嘴处有气泡,滴定后气泡消失
【答案】(1)烧杯、漏斗、玻璃棒,可任选两种作答
(2)50%
(3)液体分层,上层为无色,下层为紫红色 还原性、氧化性
(4)避免溶质损失 盖好瓶塞,反复上下颠倒、摇匀
(5)BD
(6)A
【解析】(1)过滤操作需要的玻璃仪器有烧杯、漏斗、玻璃棒,可任选两种作答。
(2)实验中加入尿素的质量为12.0g,物质的量为0.2mol,过氧化氢的质量为
,物质的量约为0.245mol,过氧化氢过量,产率应按照尿素的质量计
算,理论上可得到过氧化脲0.2mol,质量为0.2mol×94g/mol=18.8g,实验中实际得到过氧化脲9.4g,
故过氧化脲的产率为 。
(3)在过氧化脲的性质检测中,检测Ⅰ用稀硫酸酸化,加入高锰酸钾溶液,紫红色消失,说明过氧
化脲被酸性高锰酸钾氧化,体现了过氧化脲的还原性;检测Ⅱ用稀硫酸酸化,加入KI溶液和四氯化
碳溶液,过氧化脲会将KI氧化为I 单质,体现了过氧化脲的氧化性,生成的I 在四氯化碳中溶解度
2 2
大,会溶于四氯化碳溶液,且四氯化碳密度大于水,振荡,静置后出现的现象为:液体分层,上层为
无色,下层为紫红色。
(4)操作a为洗涤烧杯和玻璃棒,并将洗涤液转移到容量瓶中,目的是避免溶质损失;定容后应盖好
25 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司瓶塞,反复上下颠倒、摇匀。
(5)A.KMnO 溶液是强氧化性溶液,应置于酸式滴定管中,A项正确;
4
B.量筒的精确度不能达到0.01mL,量取25.00mL的溶液应选用滴定管,B项错误;
C.滴定过程中,待测液有可能会溅到锥形瓶内壁,滴定近终点时,为了使结果更精确,可用洗瓶冲
洗锥形瓶内壁,C项正确;
D.锥形瓶内溶液变色后,应等待30s,观察溶液不再恢复原来的颜色后,才能记录滴定管液面刻度,
D项错误;
故选BD。
(6)A.在配制过氧化脲溶液时,容量瓶中液面超过刻度线,会使溶液体积偏大,配制溶液的浓度偏
低,会使滴定过程中消耗的KMnO 溶液体积偏低,导致测定结果偏低,A项符合题意;
4
B.滴定管水洗后未用KMnO 溶液润洗,会导致KMnO 溶液浓度偏低,会使滴定过程中消耗的
4 4
KMnO 溶液体积偏高,导致测定结果偏高,B项不符合题意;
4
C.摇动锥形瓶时KMnO 溶液滴到锥形瓶外,会使滴定过程中消耗的KMnO 溶液体积偏高,导致测
4 4
定结果偏高,C项不符合题意;
D.滴定前滴定管尖嘴处有气泡,滴定后气泡消失,会使滴定过程中消耗的KMnO 溶液体积偏高,导
4
致测定结果偏高,D项不符合题意;
故选A。
考点 05 物质的量的综合应用
46.(2024·江西卷)我国学者把游离态氮固定在碳上(示踪反应如下),制得的[N=C=N]2﹣离子可用于合成
核酸的结构单元。阿伏加德罗常数的值为N ,下列说法正确的是
A
15N+C(石墨)+2LiH Li[15NC15N]+H
2 2 2
A.22.4L15N 含有的中子数为16N B.12gC(石墨)中sp2杂化轨道含有的电子数为6N
2 A A
C.1mol[N=C=N]2﹣中含有的π键数为4N D.生成1mol H 时,总反应转移的电子数为6N
A 2 A
【答案】D
【解析】A.22.4L15N 的温度压强不知,不能计算物质的量,故A错误;
2
B.12gC 物质的量n 1mol,C原子的杂化轨道上3个电子,有一个电子未参与杂化,
(石墨)
sp2杂化轨道含有的电子数为3N ,故B错误;
A
C.双键中一个σ键,一个π键,则1mol[N=C=N]2﹣中含有的π键数为2N ,故C错误;
A
D.该反应中氮元素化合价0价降低到﹣3价,碳元素化合价0价升高到+4价,氢元素化合价﹣1价升
高到0价,电子转移总数6e﹣,生成1mol H 时,总反应转移的电子数为6N ,故D正确;
2 A
故选D。
47.(2024·北京卷)不同条件下,当KMnO 与KI按照反应①②的化学计量比恰好反应,结果如下。
4
反应序 起始酸碱 KI KMnO 还原产 氧化产
4
26 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司号 性 物 物
物质的量/ 物质的量/
mol mol
① 酸性 0.001 n Mn2+ I
2
② 中性 0.001 10n MnO
2
已知: 的氧化性随酸性减弱而减弱。
下列说法正确的是
A.反应①,
B.对比反应①和②,
C.对比反应①和②, 的还原性随酸性减弱而减弱
D.随反应进行,体系 变化:①增大,②不变
【答案】B
【解析】A.反应①中Mn元素的化合价由+7价降至+2价,I元素的化合价由-1价升至0价,根据得
失电子守恒、原子守恒和电荷守恒,反应①的离子方程式是:10I-+2 +16H+=2Mn2++5I +8H O,
2 2
故n(Mn2+)∶n(I )=2∶5,A项错误;
2
B.根据反应①可得关系式10I-~2 ,可以求得n=0.0002,则反应②的n(I-)∶n(
)=0.001∶(10×0.0002)=1∶2,反应②中Mn元素的化合价由+7价降至+4价,反应②对应的关系式为I-~2
~MnO~ ~6e-, 中I元素的化合价为+5价,根据离子所带电荷数等于正负化合价的代数
2
和知x=3,反应②的离子方程式是:I-+2 +H O=2MnO ↓+ +2OH-,B项正确;
2 2
C.已知 的氧化性随酸性减弱而减弱,对比反应①和②的产物,I-的还原性随酸性减弱而增强,
C项错误;
D.根据反应①和②的离子方程式知,反应①消耗H+、产生水、pH增大,反应②产生OH-、消耗水、
pH增大,D项错误;
答案选B。
48.(2024·浙江卷)利用 可将废水中的 转化为对环境无害的物质后排放。反应原理为:
(未配平)。下列说法正确的是
A.X表示
B.可用 替换
C.氧化剂与还原剂物质的量之比为
D.若生成标准状况下的 气体 ,则反应转移的电子数为 ( 表示阿伏加德罗常数的值)
27 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司【答案】C
【解析】A.由题中信息可知,利用 可将废水中的 转化为对环境无害的物质X后排放,
则X表示 , 仍然是大气污染物,A不正确;
B. 中C元素的化合价由-2价升高到+4价, 是该反应的还原剂, 有强氧化性,通
常不能用作还原剂,故不可用 替换 ,B不正确;
C.该反应中,还原剂 中C元素的化合价由-2价升高到+4价,升高了6个价位,氧化剂
中N元素的化合价由+5价降低到0价,降低了5个价位,由电子转移守恒可知,氧化剂与还原剂的物
质的量之比为 ,C正确;
D. 中C元素的化合价由-2价升高到+4价,升高了6个价位,若生成标准状况下的 气体
,即生成0.5mol ,反应转移的电子数为0.5 ×6= ,D不正确;
综上所述,本题选C。
28 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司