文档内容
重庆市 2025 年普通高等学校招生统一考试
化学试题
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在
本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.可能用到的相对原子质量:Se-79 Ag-108 Cl-35.5 I-127 O-16 Na-23
一、选择题:本大题共 14小题,每小题3分,共42分,每题给出的四个选项中,只有一项
符合题目要求。
1. 抗日战争时期,我国军民同仇敌忾,利用简易装置制作了许多武器,下列制造过程中涉及氧化还原反应
的是
A. 用研磨法代替粉碎机碾碎硝化棉 B. 在陶缸中使用硫磺制作硫酸
C. 用蒸馏法将白酒制取工业酒精 D. 用水解法将植物油与熟石灰制备甘油
2. 下列实验对应物质性质、现象都正确的是
选
性质 现象
项
A 焰色反应 Na、K火焰都是紫色
B 漂白性 、 都可以使物质永久漂白
C 蛋白质变性 醋酸铅和甲醛都能让蛋白质变性
腐蚀印刷电 用氯化铁和浓硫酸在常温下都可以刻画电路
D
路 板
A. A B. B C. C D. D
3. 下列有关离子反应错误的是
A. 亚硫酸氢钠与石灰水反应:
.
B 与水反应:C. 与水反应:
D. 与NaBr溶液反应:
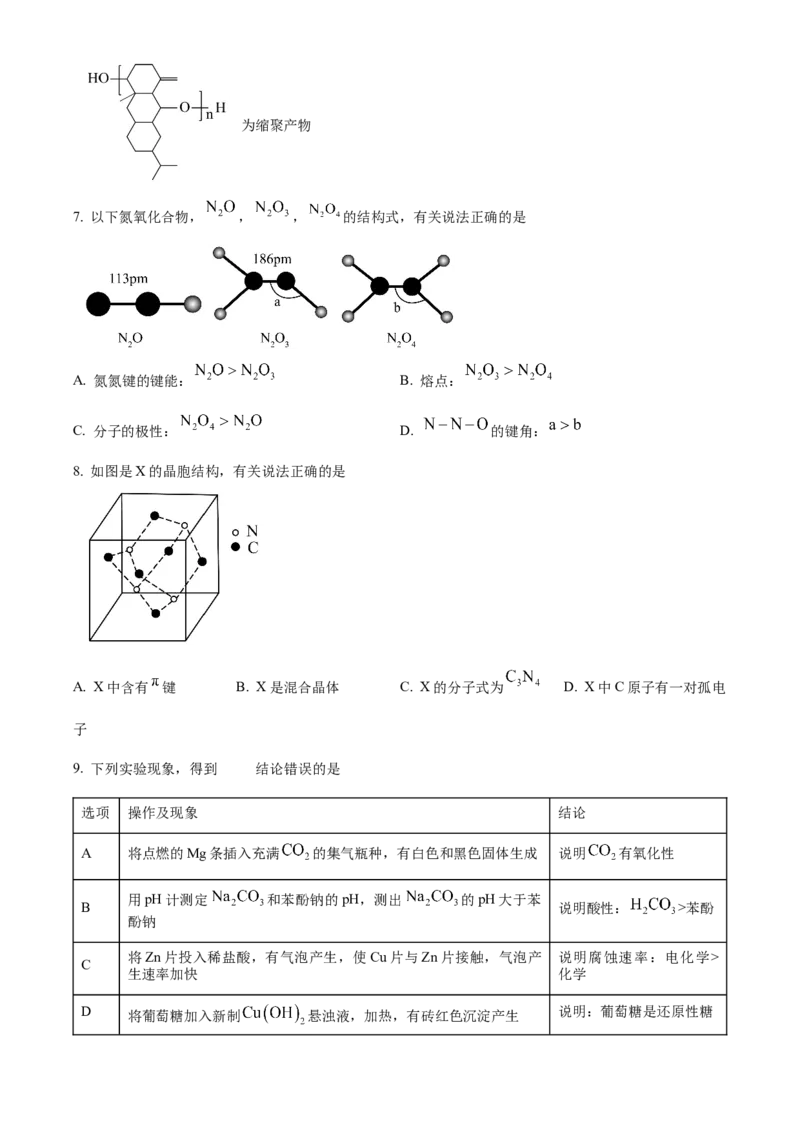
4. 下列实验操作及装置正确的是
A. 加热 B. 定容 C. 稀释 D. 滴定
5. 根据元素周期律,同时满足条件(ⅰ)和条件(ⅱ)的元素是
(ⅰ)电负性是同主族元素中最大;(ⅱ)第一电离能比同周期相邻主族元素大的。
A. Al B. Si C. B D. Be
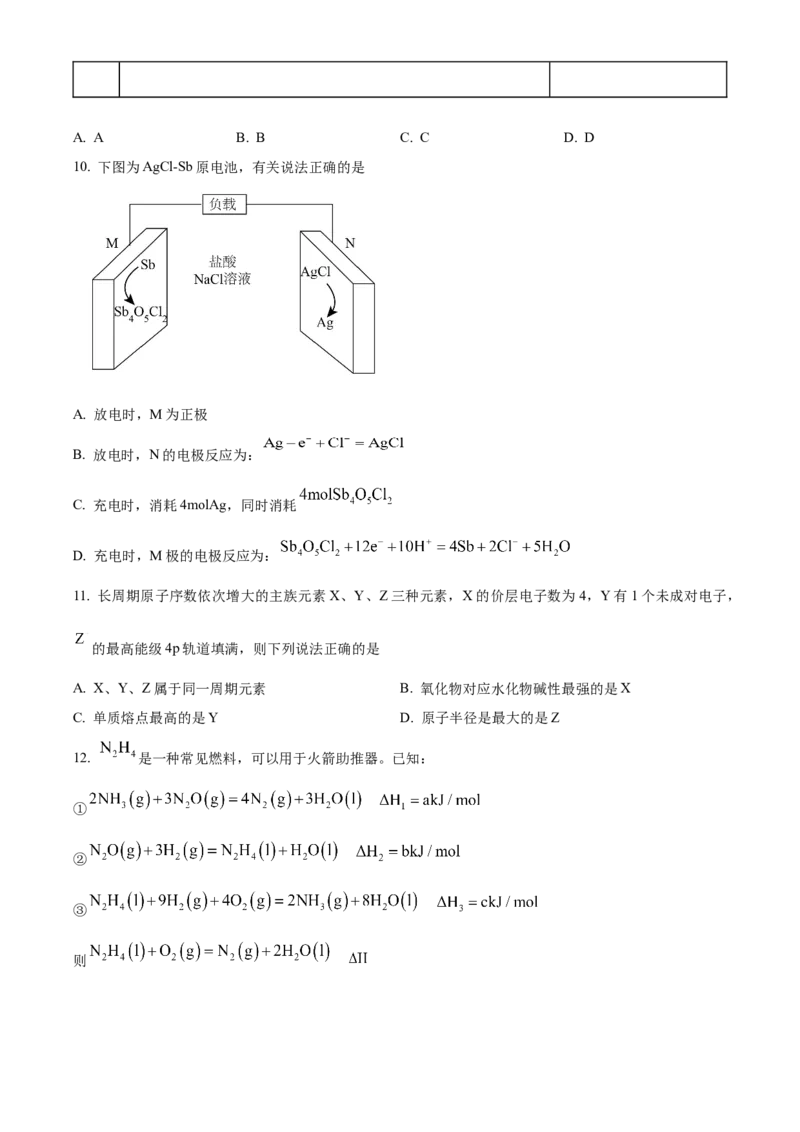
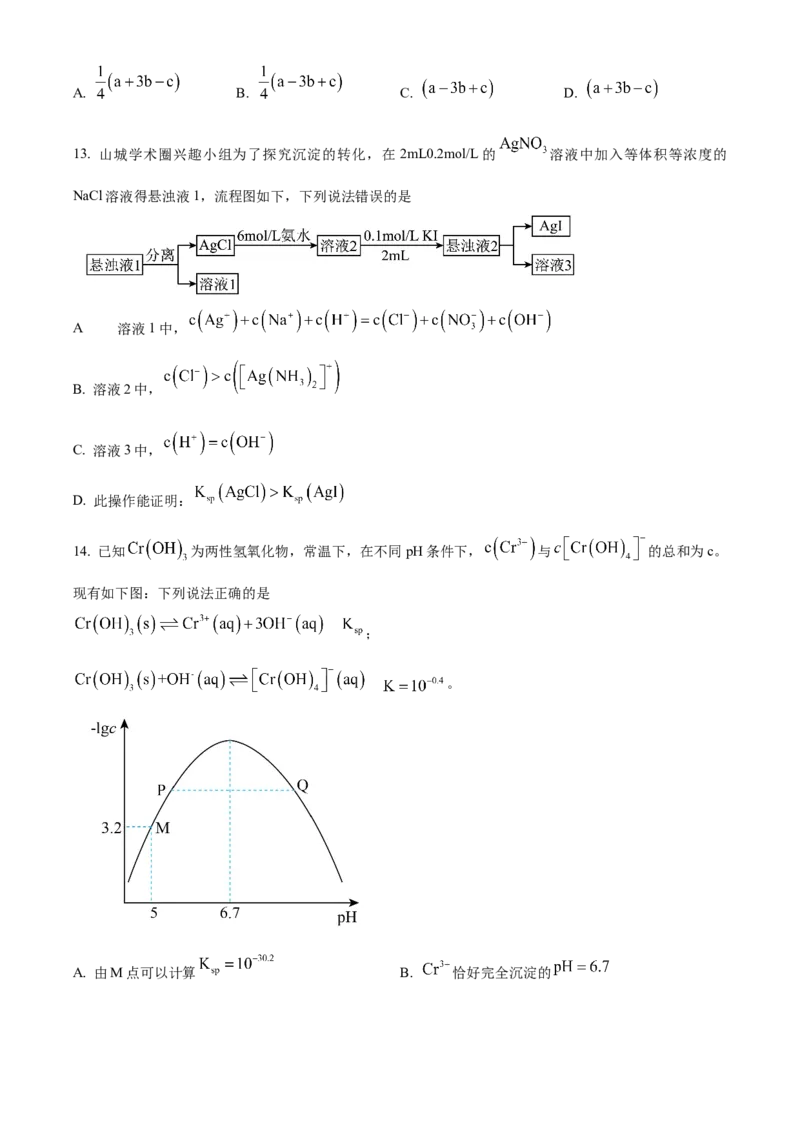
6. 如图为有机物结构式,有关说法正确的是
A. 分子式为 B. 手性碳有3个 C. 为加成产物 D.为缩聚产物
7. 以下氮氧化合物, , , 的结构式,有关说法正确的是
A. 氮氮键的键能: B. 熔点:
C. 分子的极性: D. 的键角:
8. 如图是X的晶胞结构,有关说法正确的是
A. X中含有 键 B. X是混合晶体 C. X的分子式为 D. X中C原子有一对孤电
子
的
9. 下列实验现象,得到 结论错误的是
选项 操作及现象 结论
A 将点燃的Mg条插入充满 的集气瓶种,有白色和黑色固体生成 说明 有氧化性
用pH计测定 和苯酚钠的pH,测出 的pH大于苯
B 说明酸性: >苯酚
酚钠
将Zn片投入稀盐酸,有气泡产生,使Cu片与Zn片接触,气泡产 说明腐蚀速率:电化学>
C
生速率加快 化学
D 将葡萄糖加入新制 悬浊液,加热,有砖红色沉淀产生 说明:葡萄糖是还原性糖A. A B. B C. C D. D
10. 下图为AgCl-Sb原电池,有关说法正确的是
A. 放电时,M为正极
B. 放电时,N的电极反应为:
C. 充电时,消耗4molAg,同时消耗
D. 充电时,M极的电极反应为:
11. 长周期原子序数依次增大的主族元素X、Y、Z三种元素,X的价层电子数为4,Y有1个未成对电子,
的最高能级4p轨道填满,则下列说法正确的是
A. X、Y、Z属于同一周期元素 B. 氧化物对应水化物碱性最强的是X
C. 单质熔点最高的是Y D. 原子半径是最大的是Z
12. 是一种常见燃料,可以用于火箭助推器。已知:
①
②
③
为
则A. B. C. D.
13. 山城学术圈兴趣小组为了探究沉淀的转化,在 2mL0.2mol/L的 溶液中加入等体积等浓度的
NaCl溶液得悬浊液1,流程图如下,下列说法错误的是
.
A 溶液1中,
B. 溶液2中,
C. 溶液3中,
D. 此操作能证明:
14. 已知 为两性氢氧化物,常温下,在不同pH条件下, 与 的总和为c。
现有如下图:下列说法正确的是
;
。
A. 由M点可以计算 B. 恰好完全沉淀的C. P点溶液质量小于Q点溶液质量 D. 随着pH的增大溶液中 比值先增大
后减小
二、非选择题:共58分。
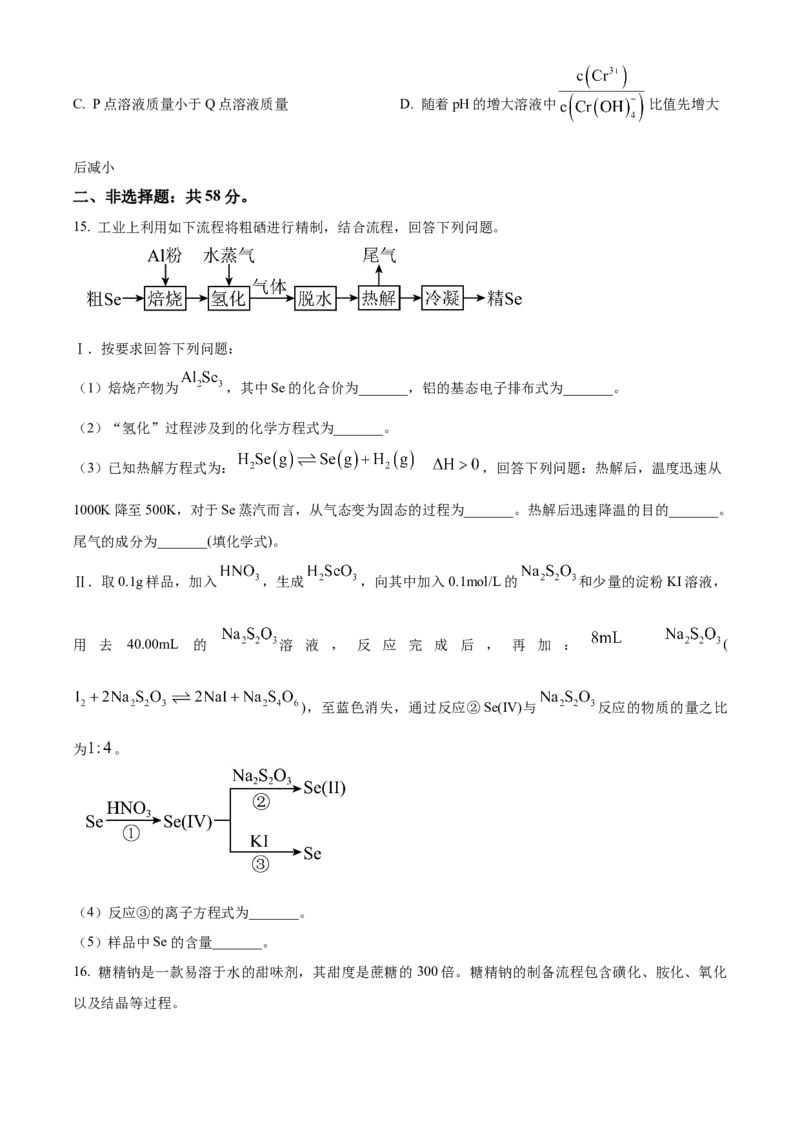
15. 工业上利用如下流程将粗硒进行精制,结合流程,回答下列问题。
Ⅰ.按要求回答下列问题:
(1)焙烧产物为 ,其中Se的化合价为_______,铝的基态电子排布式为_______。
(2)“氢化”过程涉及到的化学方程式为_______。
(3)已知热解方程式为: ,回答下列问题:热解后,温度迅速从
1000K降至500K,对于Se蒸汽而言,从气态变为固态的过程为_______。热解后迅速降温的目的_______。
尾气的成分为_______(填化学式)。
Ⅱ.取0.1g样品,加入 ,生成 ,向其中加入0.1mol/L的 和少量的淀粉KI溶液,
用 去 40.00mL 的 溶 液 , 反 应 完 成 后 , 再 加 : (
),至蓝色消失,通过反应②Se(IV)与 反应的物质的量之比
为 。
(4)反应③的离子方程式为_______。
(5)样品中Se的含量_______。
16. 糖精钠是一款易溶于水的甜味剂,其甜度是蔗糖的300倍。糖精钠的制备流程包含磺化、胺化、氧化
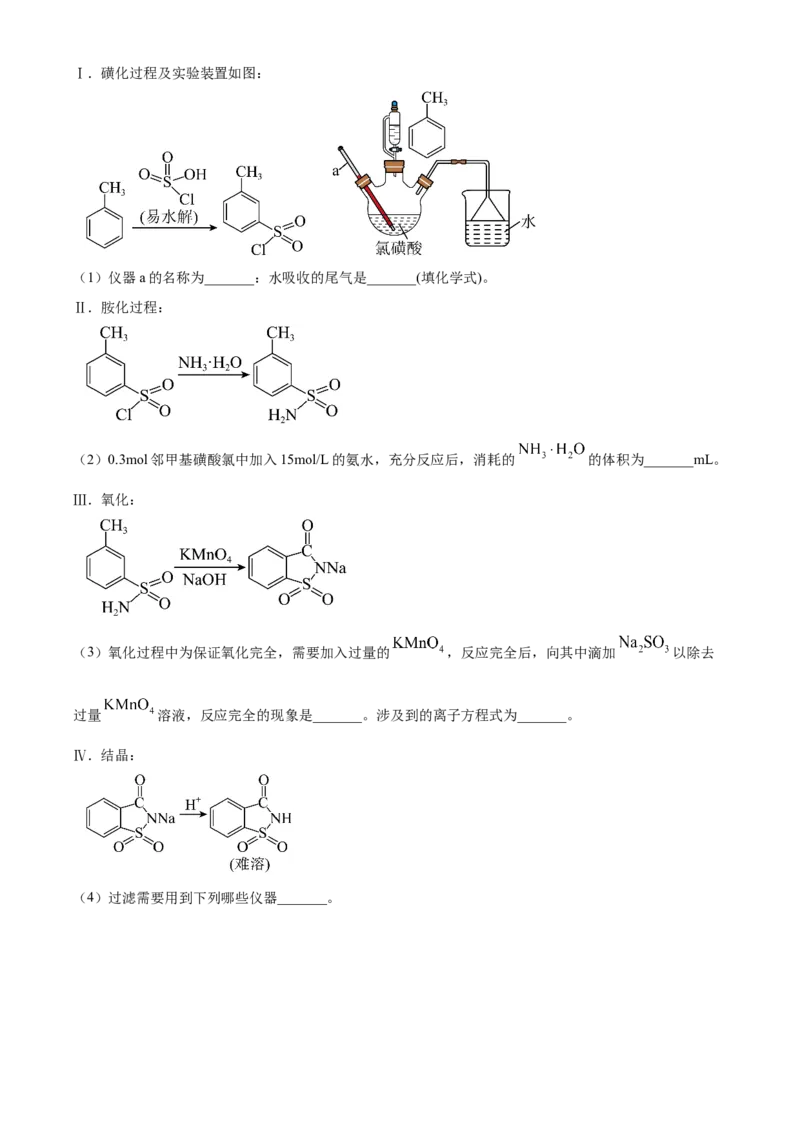
以及结晶等过程。Ⅰ.磺化过程及实验装置如图:
(1)仪器a的名称为_______:水吸收的尾气是_______(填化学式)。
Ⅱ.胺化过程:
(2)0.3mol邻甲基磺酸氯中加入15mol/L的氨水,充分反应后,消耗的 的体积为_______mL。
Ⅲ.氧化:
(3)氧化过程中为保证氧化完全,需要加入过量的 ,反应完全后,向其中滴加 以除去
过量 溶液,反应完全的现象是_______。涉及到的离子方程式为_______。
Ⅳ.结晶:
(4)过滤需要用到下列哪些仪器_______。(5) 与 反应,产生大量的气体,该气体是_______。当 完全反应,
趁热过滤,冷却结晶的后续操作是_______。
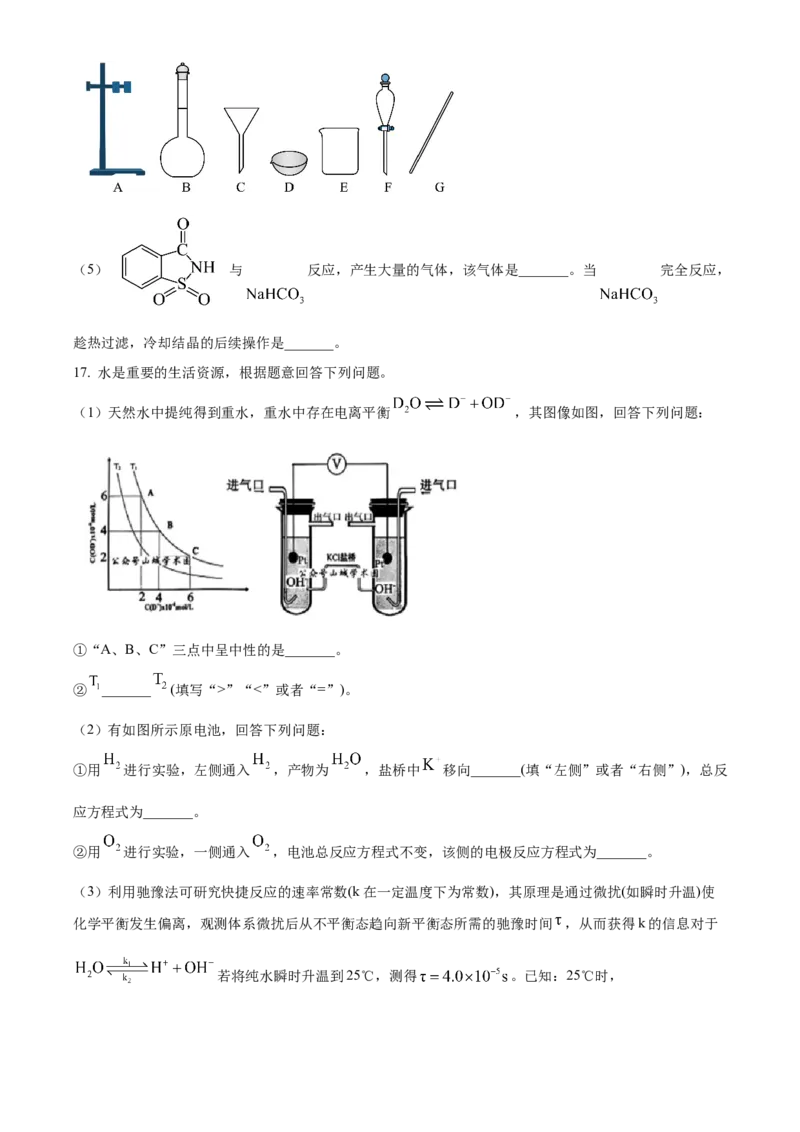
17. 水是重要的生活资源,根据题意回答下列问题。
(1)天然水中提纯得到重水,重水中存在电离平衡 ,其图像如图,回答下列问题:
①“A、B、C”三点中呈中性的是_______。
② _______ (填写“>”“<”或者“=”)。
(2)有如图所示原电池,回答下列问题:
①用 进行实验,左侧通入 ,产物为 ,盐桥中 移向_______(填“左侧”或者“右侧”),总反
应方程式为_______。
②用 进行实验,一侧通入 ,电池总反应方程式不变,该侧的电极反应方程式为_______。
(3)利用驰豫法可研究快捷反应的速率常数(k在一定温度下为常数),其原理是通过微扰(如瞬时升温)使
化学平衡发生偏离,观测体系微扰后从不平衡态趋向新平衡态所需的驰豫时间 ,从而获得k的信息对于
若将纯水瞬时升温到25℃,测得 。已知:25℃时,, , , ( 为 的
平衡浓度)。
①25℃时, ,的平衡常数 _______ (保留2位有效数字)。
②下列能正确表示瞬时升温后反应建立新平衡的过程示意图为_______。
③25℃时,计算得 为_______ 。
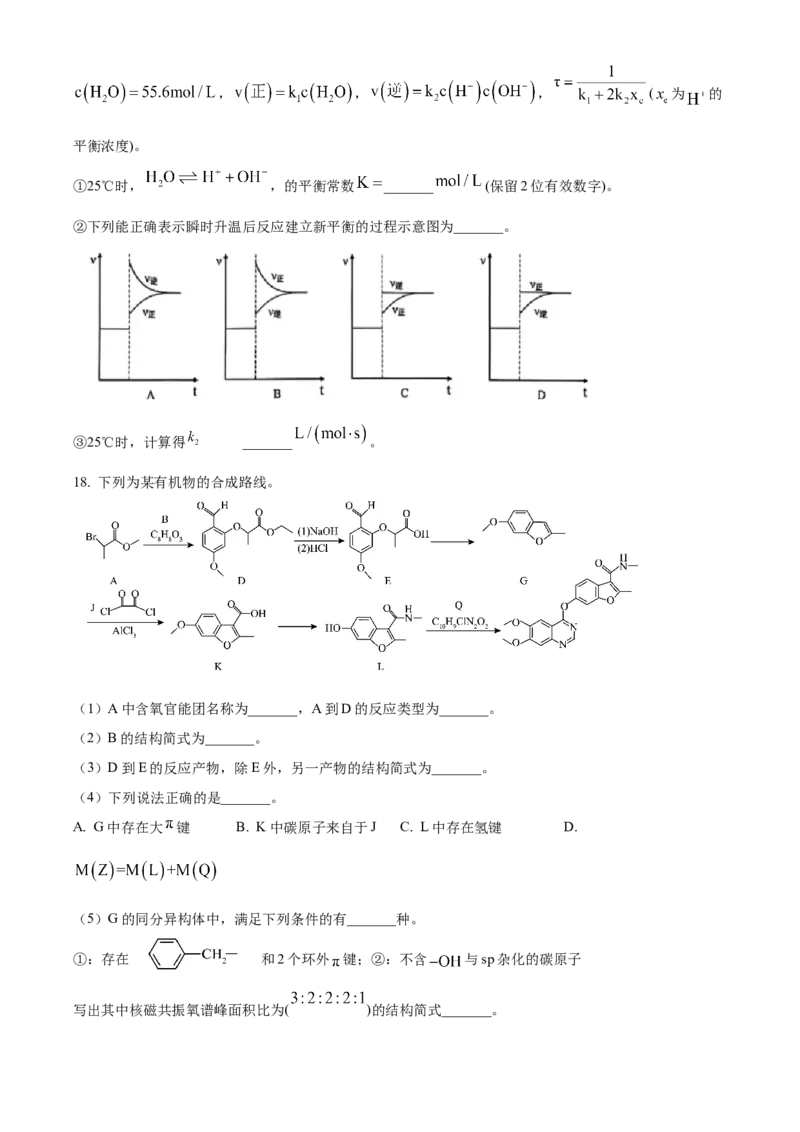
18. 下列为某有机物的合成路线。
(1)A中含氧官能团名称为_______,A到D的反应类型为_______。
(2)B的结构简式为_______。
(3)D到E的反应产物,除E外,另一产物的结构简式为_______。
(4)下列说法正确的是_______。
A. G中存在大 键 B. K中碳原子来自于J C. L中存在氢键 D.
(5)G的同分异构体中,满足下列条件的有_______种。
①:存在 和2个环外 键;②:不含 与sp杂化的碳原子
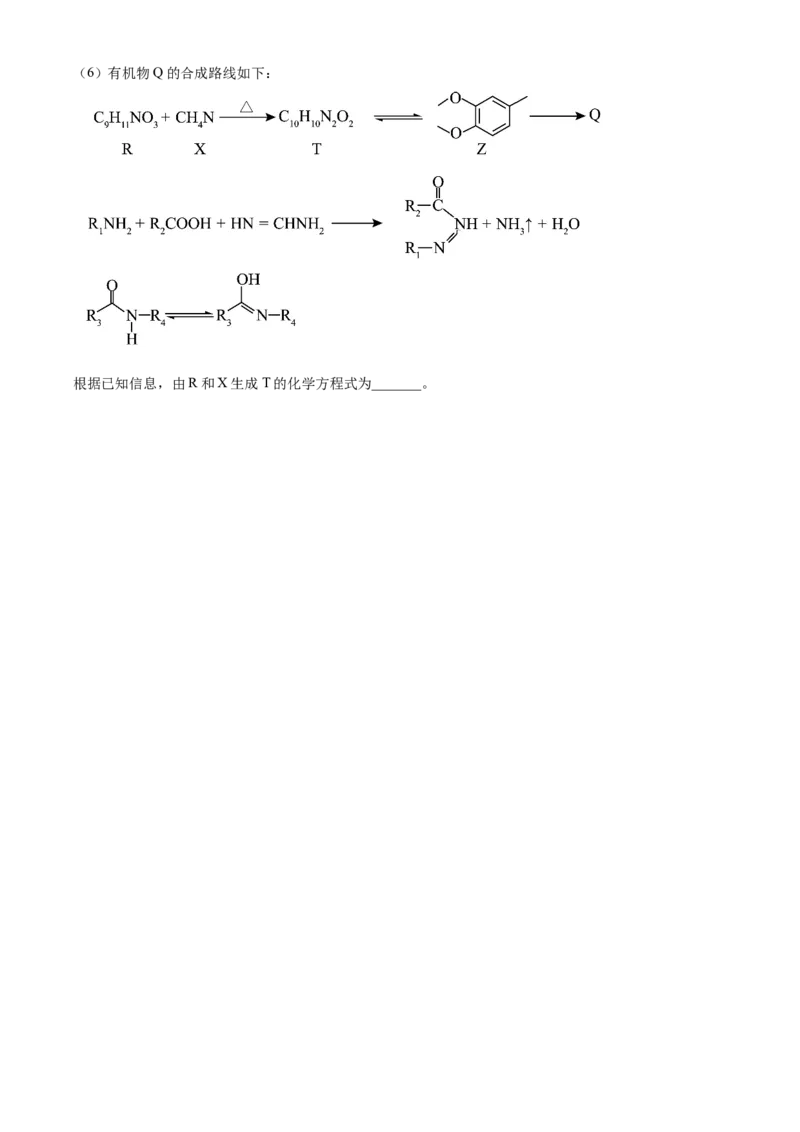
写出其中核磁共振氧谱峰面积比为( )的结构简式_______。(6)有机物Q的合成路线如下:
根据已知信息,由R和X生成T的化学方程式为_______。