文档内容
东城区 2019-2020 学年度第一学期期末统一检测
初三化学
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Cl-35.5
第一部分 选择题(共24分)
每小题只有1 个选项符合题意。每小题1分,共24分。
1. 空气成分中,体积分数最大的是( )
A. 氮气 B. 二氧化碳 C. 氧气 D. 稀有气体
2. 下列符号表示2个氢分子的是
A. H B. 2HO C. 2H D. 2H+
2 2 2
3. 地壳中含量最多的元素是( )
A. Si B. Al C. O D. Fe
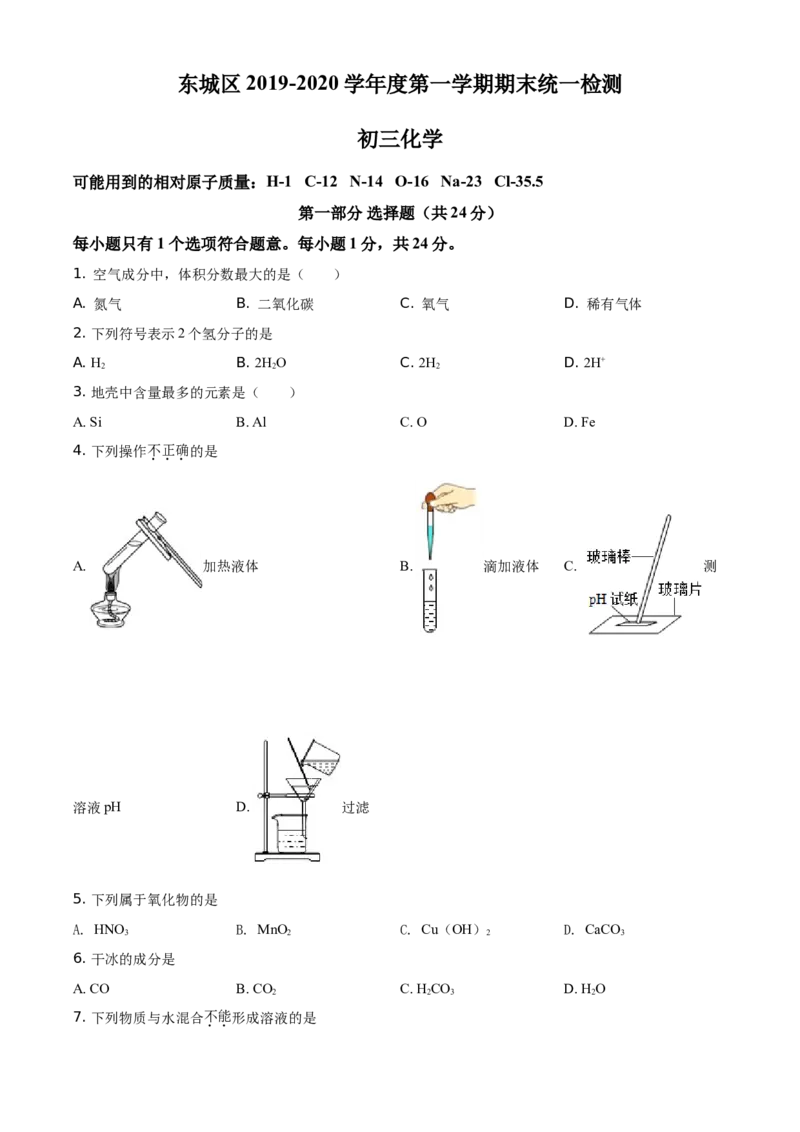
4. 下列操作不正确的是
A. 加热液体 B. 滴加液体 C. 测
溶液pH D. 过滤
5. 下列属于氧化物的是
A. HNO B. MnO C. Cu(OH) D. CaCO
3 2 2 3
6. 干冰的成分是
A. CO B. CO C. HCO D. H O
2 2 3 2
7. 下列物质与水混合不能形成溶液的是A. 蔗糖 B. 酒精 C. 食盐 D. 植物油
8. 下列物质的化学式书写不正确的是
A. 氯化锌 ZnCl B. 硫酸钙 CaSO
4
C. 氢氧化钾 KOH D. 氧化镁 MgO
9. 下列食物显碱性的是
食物 苹果汁 葡萄汁 牛奶 鸡蛋清
pH 2.9~3.3 3.5~4.5 6.3~6.6 7.6~8.0
A. 苹果汁 B. 葡萄汁 C. 牛奶 D. 鸡蛋清
10. 能闻到花香,说明分子的性质是
A. 分子的体积很小 B. 分子的质量很小
C. 分子在不断运动 D. 分子之间有间隔
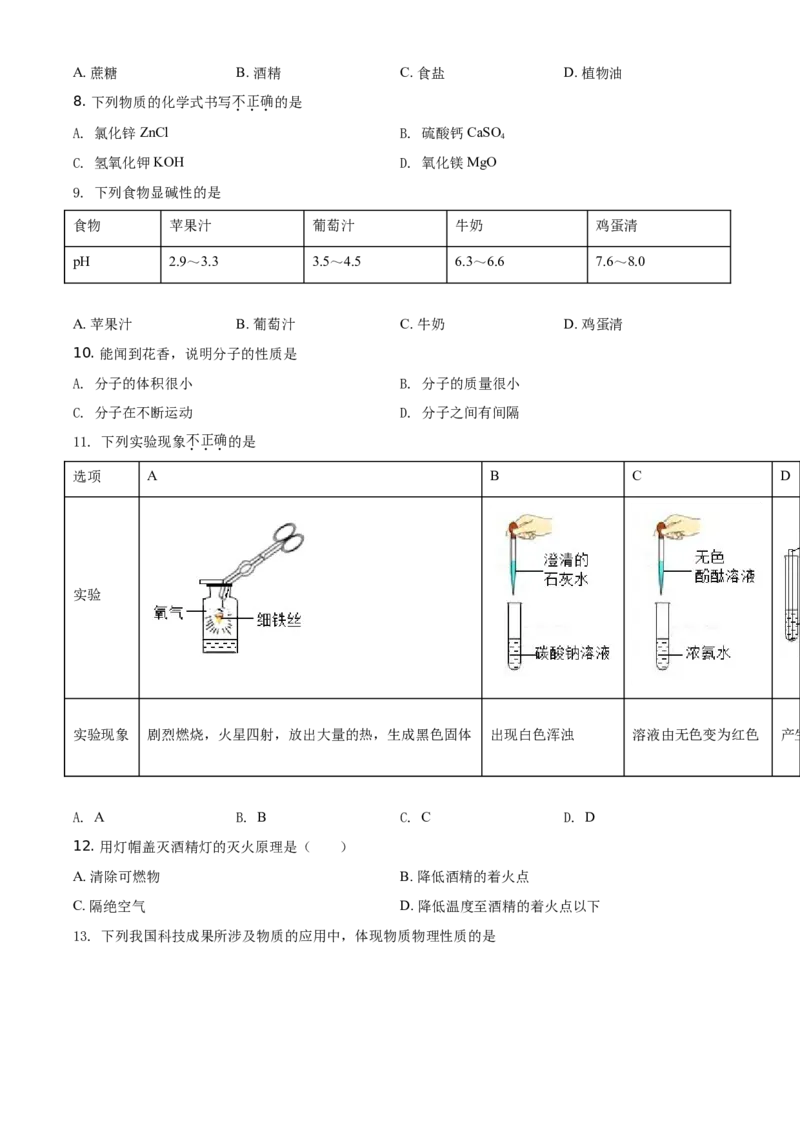
11. 下列实验现象不正确的是
选项 A B C D
实验
实验现象 剧烈燃烧,火星四射,放出大量的热,生成黑色固体 出现白色浑浊 溶液由无色变为红色 产生气泡,溶液变为浅绿色
A. A B. B C. C D. D
12. 用灯帽盖灭酒精灯的灭火原理是( )
A. 清除可燃物 B. 降低酒精的着火点
C. 隔绝空气 D. 降低温度至酒精的着火点以下
13. 下列我国科技成果所涉及物质的应用中,体现物质物理性质的是C 甲醇(CHOH) D 优化煤的综合利
A 利用石墨烯优异的导电性, B可燃冰 是天然气水合 3
低温制得氢气,用 用,发展煤制乙醇
制成新型电阻触摸屏的电极 物,作为新能源使用
于新能源汽车 (C HOH)技术
2 5
A. A B. B C. C D. D
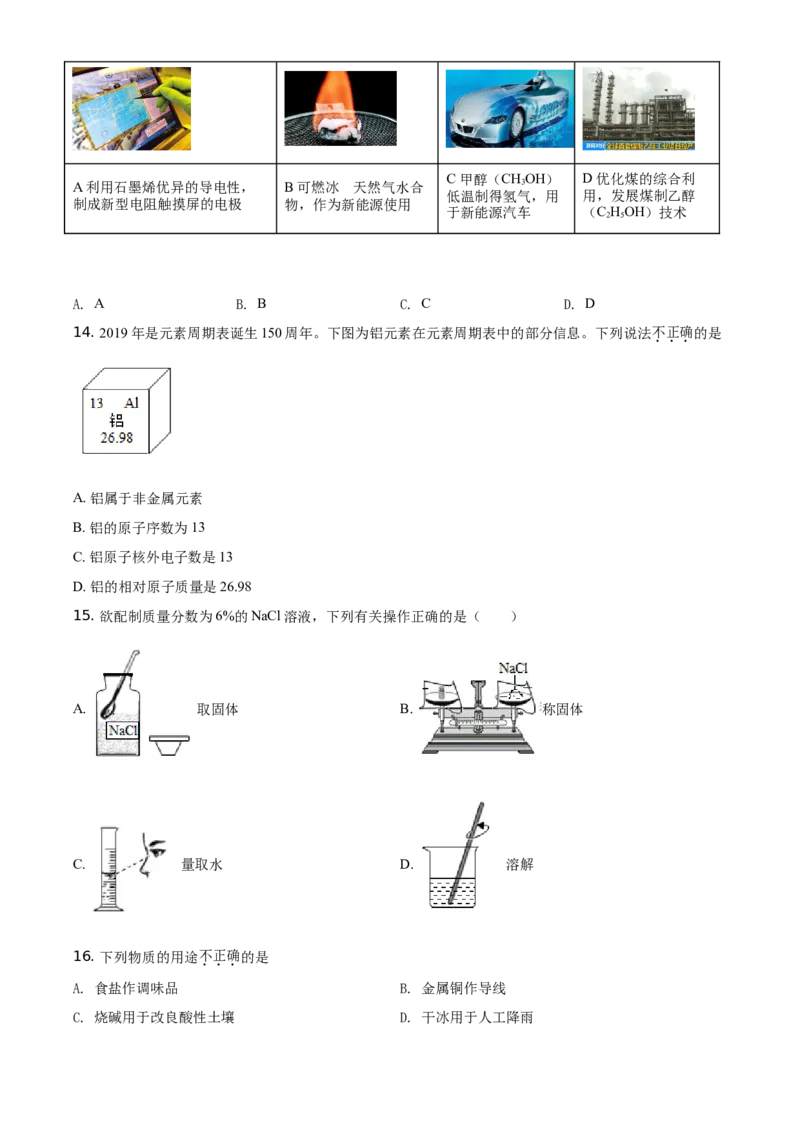
14. 2019年是元素周期表诞生150周年。下图为铝元素在元素周期表中的部分信息。下列说法不正确的是
A. 铝属于非金属元素
B. 铝的原子序数为13
C. 铝原子核外电子数是13
D. 铝的相对原子质量是26.98
15. 欲配制质量分数为6%的NaCl溶液,下列有关操作正确的是( )
A. 取固体 B. 称固体
C. 量取水 D. 溶解
16. 下列物质的用途不正确的是
A. 食盐作调味品 B. 金属铜作导线
C. 烧碱用于改良酸性土壤 D. 干冰用于人工降雨17. 利用氢氟酸(HF)蚀刻玻璃,发生的化学方程式为:SiO +4HF =X↑+2H O,物质X为
2 2
A. SiO B. SiF C. SiF D. F
4 2
依据实验和溶解度曲线回答以下小题:
20℃时,向下列5只盛有100g水的烧杯中,分别加入不同质量的固体,充分溶解。
18. 上述溶液为饱和溶液的是
A. ①②④ B. ①③⑤
C. ②③⑤ D. ③④⑤
19. ④中溶液的质量为
A. 80g B. 100g
C. 180g D. 190g
20. 下列温度中,KNO 比NaNO 溶解度大的是
3 3
A. 30℃ B. 50℃
C. 60℃ D. 90℃
21. 碳酸乙烯酯(C HO)可用作锂电池电解液。下列有关碳酸乙烯酯的说法不正确的是
3 4 3
A. 由碳、氢和氧三种元素组成B. 其中碳元素的质量分数最大
C. 其中氢元素与氧元素的质量比为1:12
D. 每个碳酸乙烯酯分子中含有10个原子
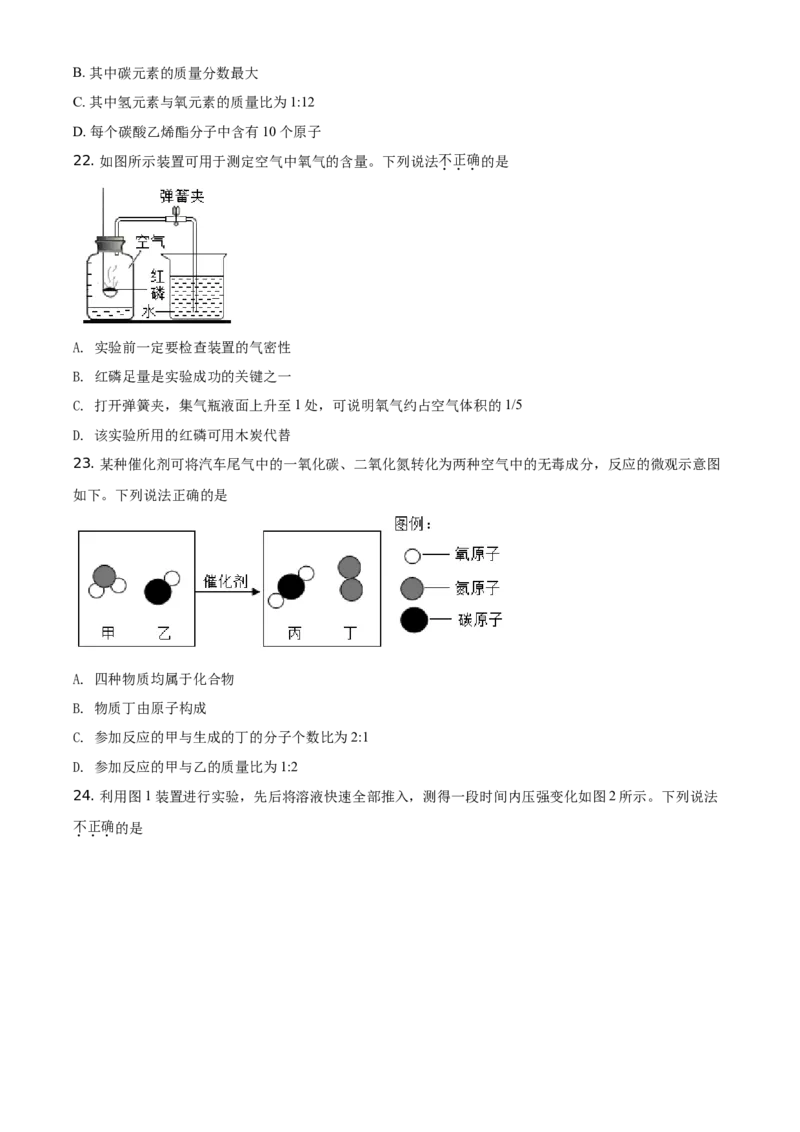
22. 如图所示装置可用于测定空气中氧气的含量。下列说法不正确的是
A. 实验前一定要检查装置的气密性
B. 红磷足量是实验成功的关键之一
C. 打开弹簧夹,集气瓶液面上升至1处,可说明氧气约占空气体积的1/5
D. 该实验所用的红磷可用木炭代替
23. 某种催化剂可将汽车尾气中的一氧化碳、二氧化氮转化为两种空气中的无毒成分,反应的微观示意图
如下。下列说法正确的是
A. 四种物质均属于化合物
B. 物质丁由原子构成
C. 参加反应的甲与生成的丁的分子个数比为2:1
D. 参加反应的甲与乙的质量比为1:2
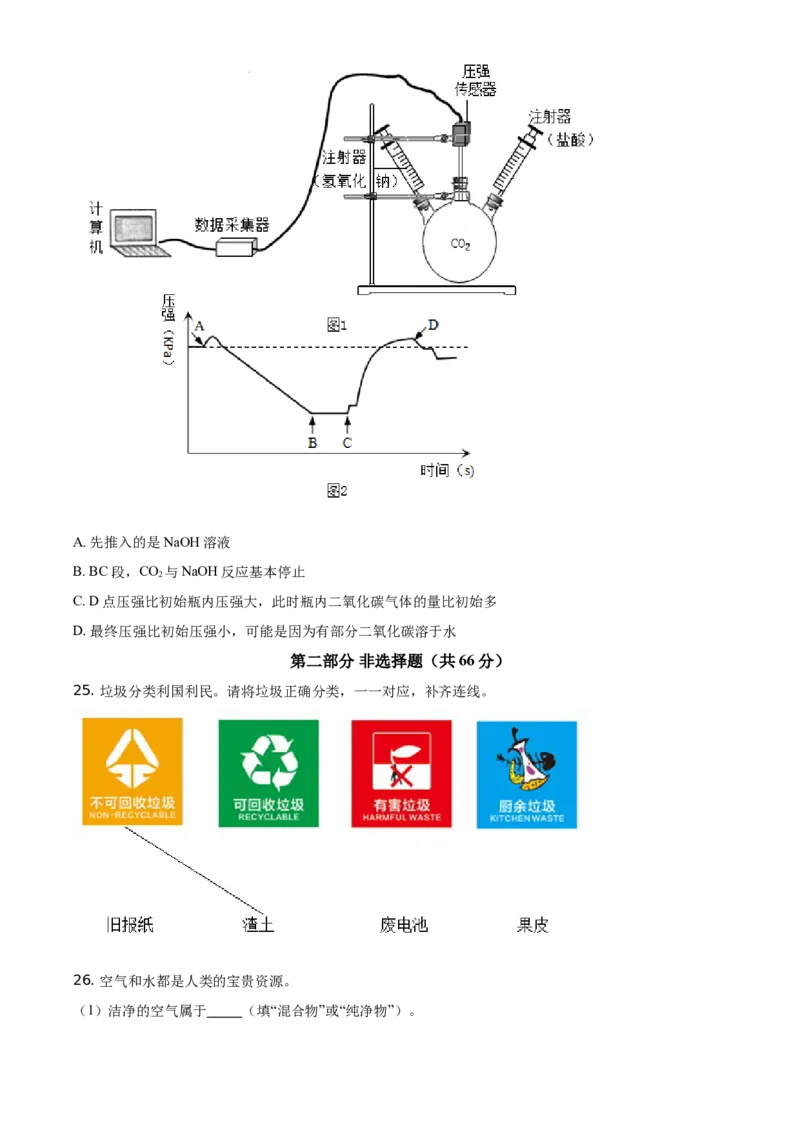
24. 利用图1装置进行实验,先后将溶液快速全部推入,测得一段时间内压强变化如图2所示。下列说法
不正确的是A. 先推入的是NaOH溶液
B. BC段,CO 与NaOH反应基本停止
2
C. D点压强比初始瓶内压强大,此时瓶内二氧化碳气体的量比初始多
D. 最终压强比初始压强小,可能是因为有部分二氧化碳溶于水
第二部分 非选择题(共66分)
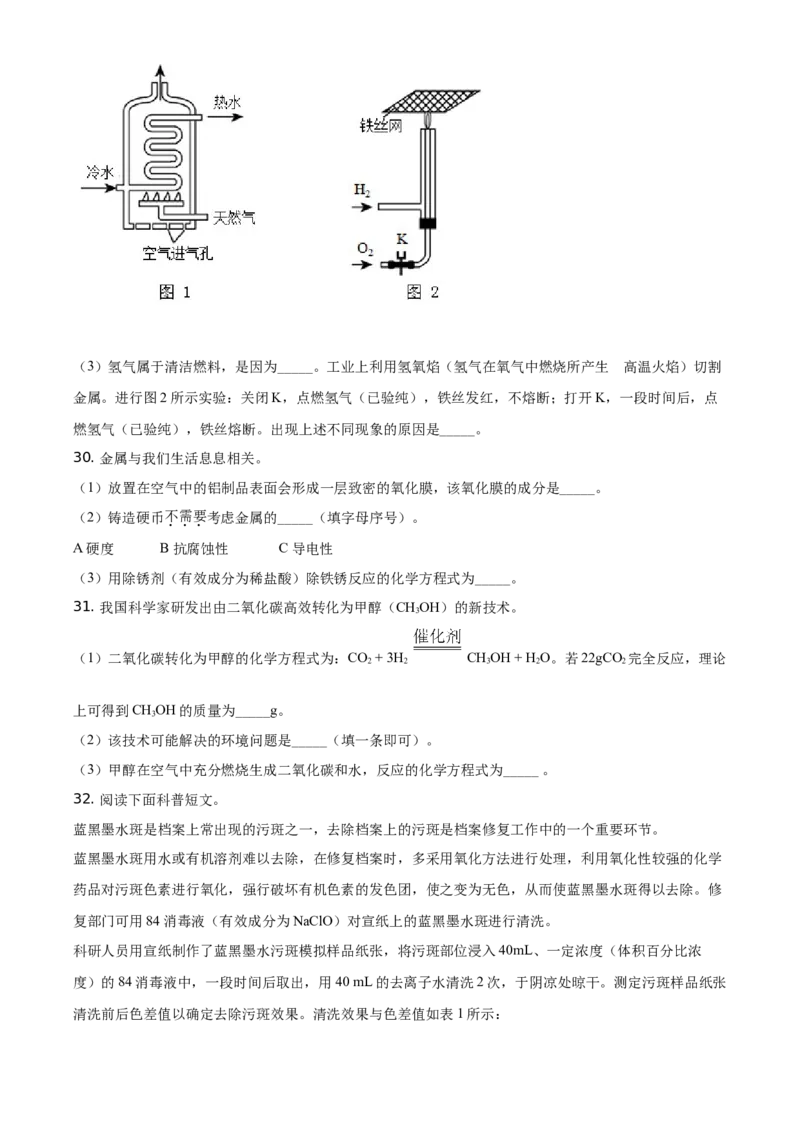
25. 垃圾分类利国利民。请将垃圾正确分类,一一对应,补齐连线。
26. 空气和水都是人类的宝贵资源。
(1)洁净的空气属于_____(填“混合物”或“纯净物”)。(2)人类的生命活动离不开空气,因为空气中的氧气能起到_____的作用。
(3)海水淡化可缓解淡水资源匮乏的问题。如图为太阳能海水淡化装置示意图。从微观的角度分析,海
水中的水变成水蒸气的过程中,没有改变的是_____,变化的是_____。
27. 家庭自制汽水时,需加入白糖、食用色素、小苏打、柠檬酸、凉开水等。
(1)汽水是溶液,其中加入的白糖是_____(填“溶质”或“溶剂”)。
(2)饮用汽水时,将瓶盖打开,会有大量气泡冒出,该气体的成分是_____,将该气体通入澄清石灰水中,
观察到_____,反应的化学方程式为_____。
28. 小寒是二十四节气之一。下面列举了一些民间小寒风俗食物。
(1)高钙羊肉中的钙是指钙_____(填“分子”、“原子”或“元素”);中老年人多吃含钙的食物能够预防
_____(填“骨质疏松”或“贫血”)。
(2)从营养均衡角度考虑,合理的食物搭配是_____(填字母序号)。
A ①②③ B ③④⑤ C ①③⑤
29. 人类的生产生活离不开燃料。
(1)化石燃料包括天然气、煤和_____,天然气的主要成分是_____。
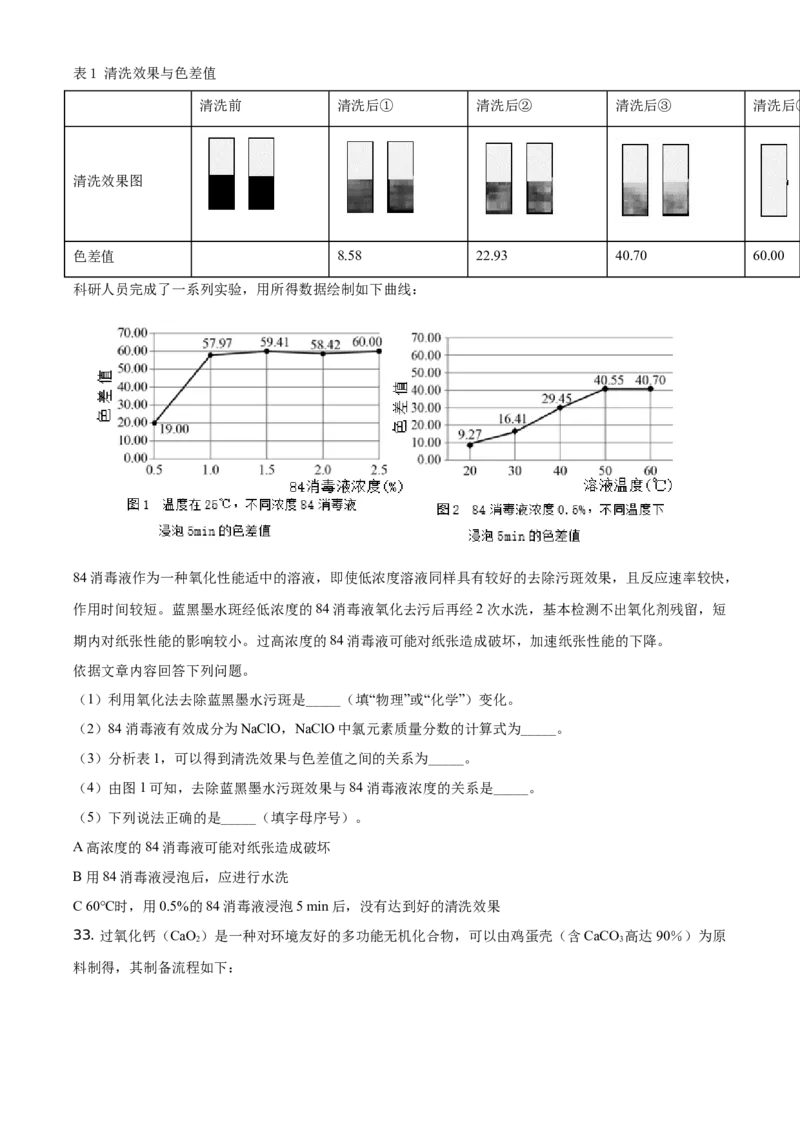
(2)家用燃气热水器的工作原理如图1所示,若“空气进气孔”被部分堵塞,导致天然气燃烧不充分,会产
生的有毒气体是_____。(3)氢气属于清洁燃料,是因为_____。工业上利用氢氧焰(氢气在氧气中燃烧所产生 的高温火焰)切割
金属。进行图2所示实验:关闭K,点燃氢气(已验纯),铁丝发红,不熔断;打开K,一段时间后,点
燃氢气(已验纯),铁丝熔断。出现上述不同现象的原因是_____。
30. 金属与我们生活息息相关。
(1)放置在空气中的铝制品表面会形成一层致密的氧化膜,该氧化膜的成分是_____。
(2)铸造硬币不需要考虑金属的_____(填字母序号)。
A 硬度 B 抗腐蚀性 C 导电性
(3)用除锈剂(有效成分为稀盐酸)除铁锈反应的化学方程式为_____。
31. 我国科学家研发出由二氧化碳高效转化为甲醇(CHOH)的新技术。
3
(1)二氧化碳转化为甲醇的化学方程式为:CO + 3H CH OH + H O。若22gCO 完全反应,理论
2 2 3 2 2
上可得到CHOH的质量为_____g。
3
(2)该技术可能解决的环境问题是_____(填一条即可)。
(3)甲醇在空气中充分燃烧生成二氧化碳和水,反应的化学方程式为_____ 。
32. 阅读下面科普短文。
蓝黑墨水斑是档案上常出现的污斑之一,去除档案上的污斑是档案修复工作中的一个重要环节。
蓝黑墨水斑用水或有机溶剂难以去除,在修复档案时,多采用氧化方法进行处理,利用氧化性较强的化学
药品对污斑色素进行氧化,强行破坏有机色素的发色团,使之变为无色,从而使蓝黑墨水斑得以去除。修
复部门可用84消毒液(有效成分为NaClO)对宣纸上的蓝黑墨水斑进行清洗。
科研人员用宣纸制作了蓝黑墨水污斑模拟样品纸张,将污斑部位浸入40mL、一定浓度(体积百分比浓
度)的84消毒液中,一段时间后取出,用40 mL的去离子水清洗2次,于阴凉处晾干。测定污斑样品纸张
清洗前后色差值以确定去除污斑效果。清洗效果与色差值如表1所示:表1 清洗效果与色差值
清洗前 清洗后① 清洗后② 清洗后③ 清洗后④
清洗效果图
色差值 8.58 22.93 40.70 60.00
科研人员完成了一系列实验,用所得数据绘制如下曲线:
84消毒液作为一种氧化性能适中的溶液,即使低浓度溶液同样具有较好的去除污斑效果,且反应速率较快,
作用时间较短。蓝黑墨水斑经低浓度的84消毒液氧化去污后再经2次水洗,基本检测不出氧化剂残留,短
期内对纸张性能的影响较小。过高浓度的84消毒液可能对纸张造成破坏,加速纸张性能的下降。
依据文章内容回答下列问题。
(1)利用氧化法去除蓝黑墨水污斑是_____(填“物理”或“化学”)变化。
(2)84消毒液有效成分为NaClO,NaClO中氯元素质量分数的计算式为_____。
(3)分析表1,可以得到清洗效果与色差值之间的关系为_____。
(4)由图1可知,去除蓝黑墨水污斑效果与84消毒液浓度的关系是_____。
(5)下列说法正确的是_____(填字母序号)。
A 高浓度的84消毒液可能对纸张造成破坏
B 用84消毒液浸泡后,应进行水洗
C 60℃时,用0.5%的84消毒液浸泡5 min后,没有达到好的清洗效果
33. 过氧化钙(CaO)是一种对环境友好的多功能无机化合物,可以由鸡蛋壳(含CaCO 高达90%)为原
2 3
料制得,其制备流程如下:(1)反应1为高温煅烧碳酸钙,其化学方程式为_____。
(2)反应2的化学方程式为:CaO + H O + 7H O CaO·8H O,该反应属于化合反应。CaO·8H O属
2 2 2 2 2 2 2
于_____(填字母序号)。
A 混合物 B 纯净物 C 化合物
(3)反应2制得的CaO·8H O中,可能含有的固体杂质是_____(填化学式)。
2 2
34. NaClO 是一种重要的杀菌消毒剂,也常用来漂白织物等,其生产工艺流程如下:
2
(1)NaClO 中Cl的化合价为_____。
2
(2)补全化学方程式:2NaClO+_____+_____=2ClO +2NaHSO 。
3 2 4
(3)精制食盐水时,用NaOH溶液将杂质MgCl 转化为沉淀除去,该复分解反应的化学方程式为_____。
2
(4)该工艺流程中体现环保意识的环节是_____(填写一条即可)。
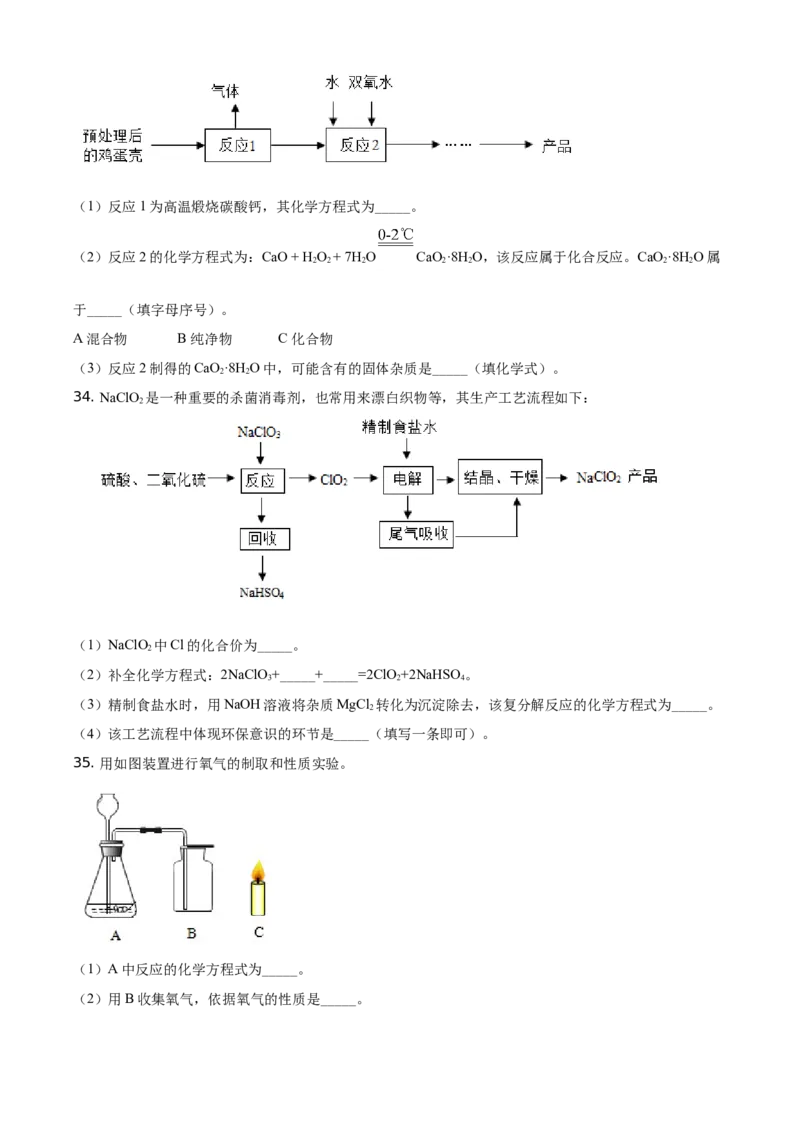
35. 用如图装置进行氧气的制取和性质实验。
(1)A中反应的化学方程式为_____。
(2)用B收集氧气,依据氧气的性质是_____。(3)收集满氧气后,将蜡烛C放入B中,观察到的现象是_____。
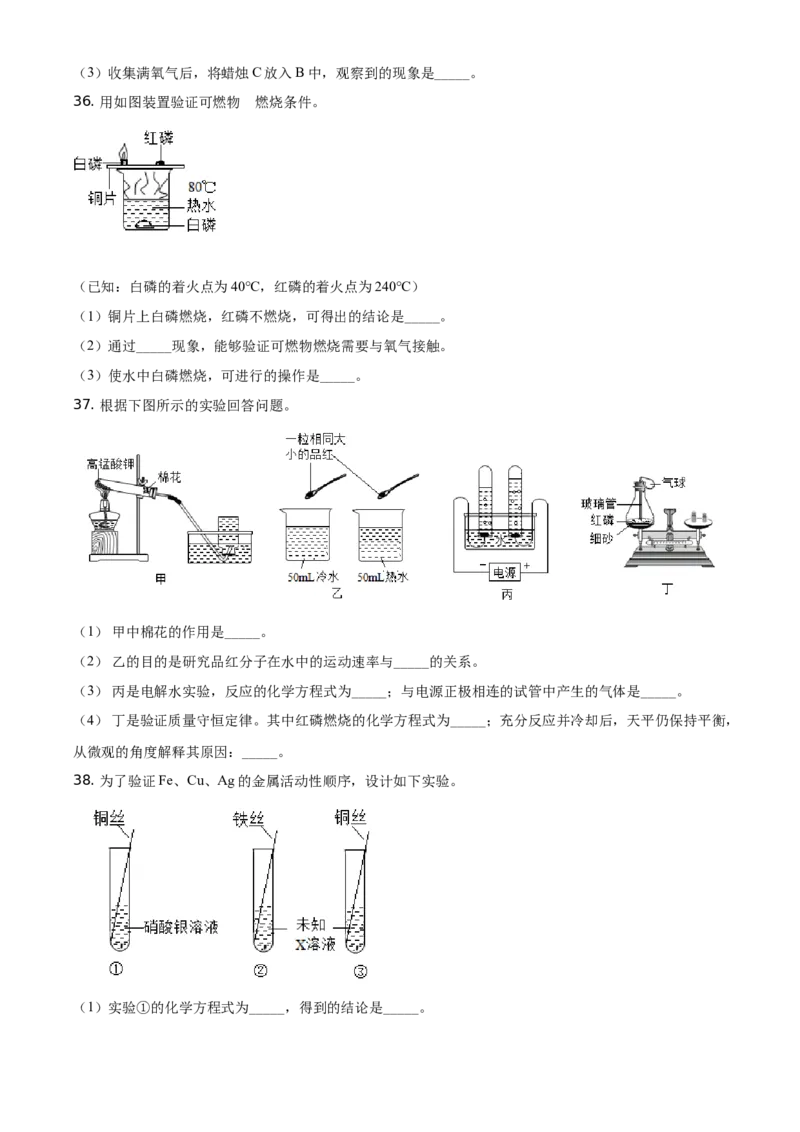
36. 用如图装置验证可燃物 的燃烧条件。
(已知:白磷的着火点为40℃,红磷的着火点为240℃)
(1)铜片上白磷燃烧,红磷不燃烧,可得出的结论是_____。
(2)通过_____现象,能够验证可燃物燃烧需要与氧气接触。
(3)使水中白磷燃烧,可进行的操作是_____。
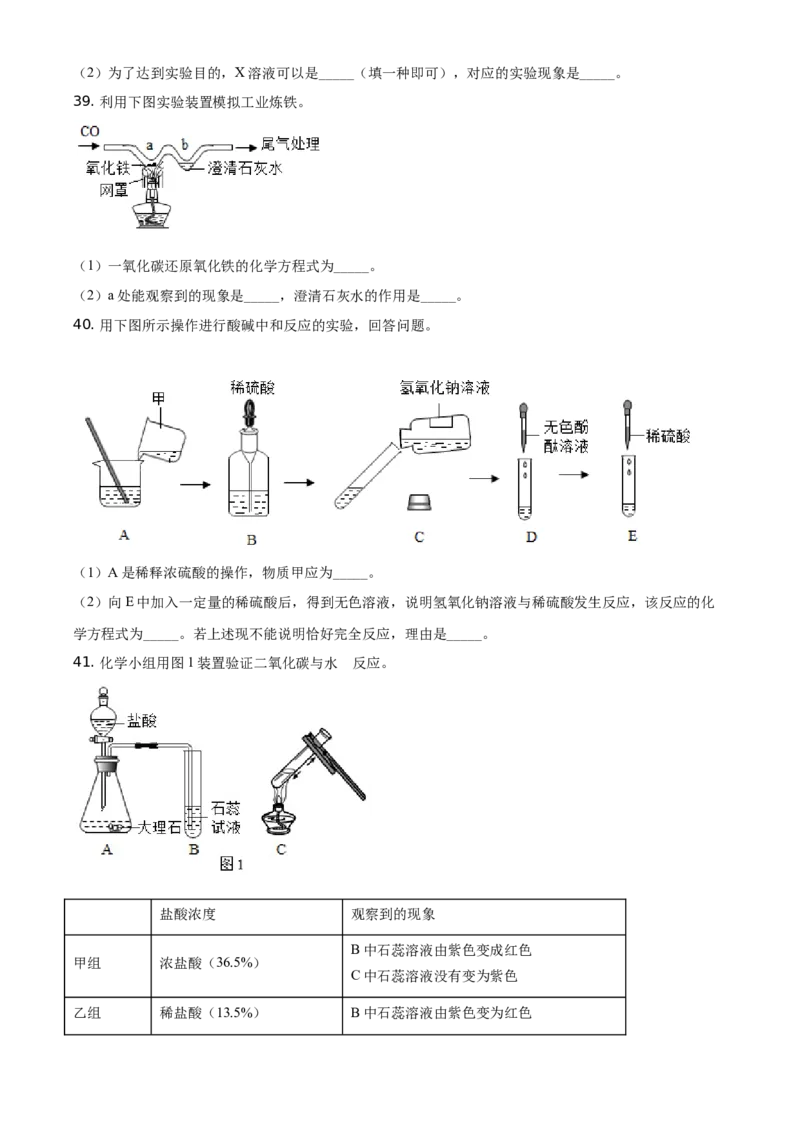
37. 根据下图所示的实验回答问题。
(1) 甲中棉花的作用是_____。
(2) 乙的目的是研究品红分子在水中的运动速率与_____的关系。
(3) 丙是电解水实验,反应的化学方程式为_____;与电源正极相连的试管中产生的气体是_____。
(4) 丁是验证质量守恒定律。其中红磷燃烧的化学方程式为_____;充分反应并冷却后,天平仍保持平衡,
从微观的角度解释其原因:_____。
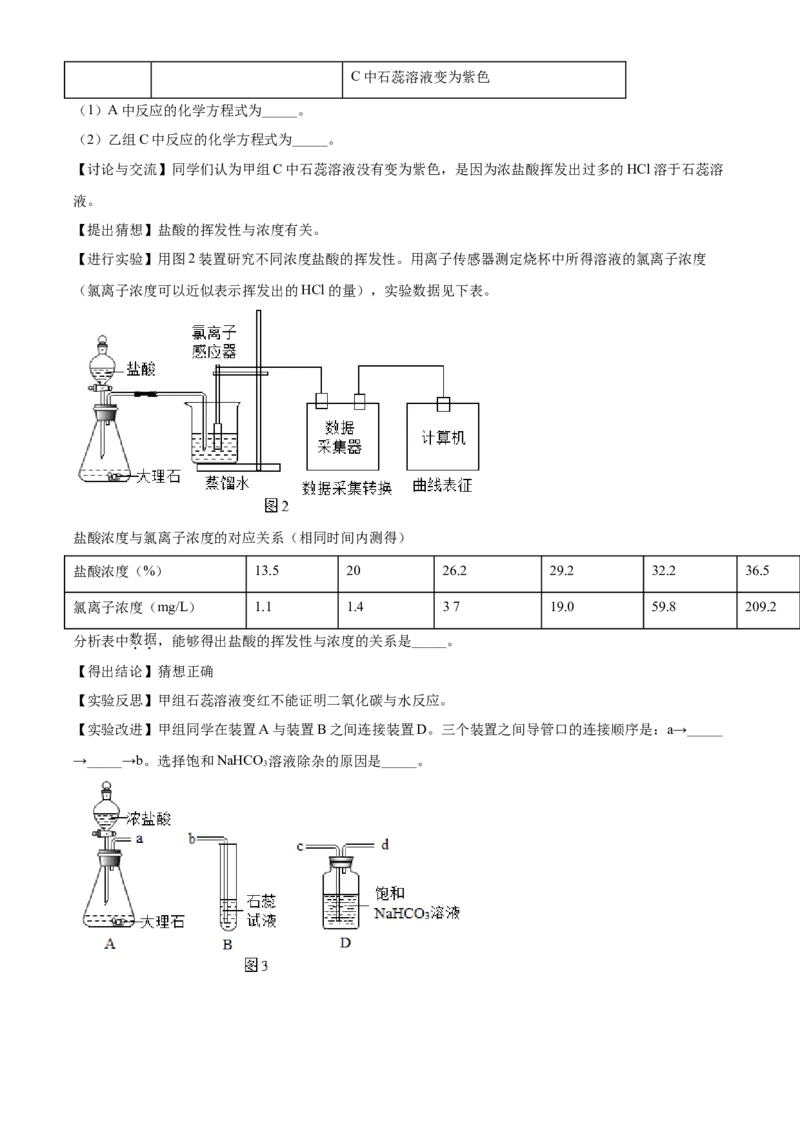
38. 为了验证Fe、Cu、Ag的金属活动性顺序,设计如下实验。
(1)实验①的化学方程式为_____,得到的结论是_____。(2)为了达到实验目的,X溶液可以是_____(填一种即可),对应的实验现象是_____。
39. 利用下图实验装置模拟工业炼铁。
(1)一氧化碳还原氧化铁的化学方程式为_____。
(2)a处能观察到的现象是_____,澄清石灰水的作用是_____。
40. 用下图所示操作进行酸碱中和反应的实验,回答问题。
(1)A是稀释浓硫酸的操作,物质甲应为_____。
(2)向E中加入一定量的稀硫酸后,得到无色溶液,说明氢氧化钠溶液与稀硫酸发生反应,该反应的化
学方程式为_____。若上述现不能说明恰好完全反应,理由是_____。
41. 化学小组用图1装置验证二氧化碳与水 的反应。
盐酸浓度 观察到的现象
B中石蕊溶液由紫色变成红色
甲组 浓盐酸(36.5%)
C中石蕊溶液没有变为紫色
乙组 稀盐酸(13.5%) B中石蕊溶液由紫色变为红色C中石蕊溶液变为紫色
(1)A中反应的化学方程式为_____。
(2)乙组C中反应的化学方程式为_____。
【讨论与交流】同学们认为甲组C中石蕊溶液没有变为紫色,是因为浓盐酸挥发出过多的HCl溶于石蕊溶
液。
【提出猜想】盐酸的挥发性与浓度有关。
【进行实验】用图2装置研究不同浓度盐酸的挥发性。用离子传感器测定烧杯中所得溶液的氯离子浓度
(氯离子浓度可以近似表示挥发出的HCl的量),实验数据见下表。
盐酸浓度与氯离子浓度的对应关系(相同时间内测得)
盐酸浓度(%) 13.5 20 26.2 29.2 32.2 36.5
.
氯离子浓度(mg/L) 1.1 1.4 37 19.0 59.8 209.2
分析表中数据,能够得出盐酸的挥发性与浓度的关系是_____。
【得出结论】猜想正确
【实验反思】甲组石蕊溶液变红不能证明二氧化碳与水反应。
【实验改进】甲组同学在装置A与装置B之间连接装置D。三个装置之间导管口的连接顺序是:a→_____
→_____→b。选择饱和NaHCO 溶液除杂的原因是_____。
3本试卷的题干、答案和解析均由组卷网(http://zujuan.xkw.com)专业教师团队编校出品。
登录组卷网可对本试卷进行单题组卷、细目表分析、布置作业、举一反三等操作。
试卷地址:在组卷网浏览本卷
组卷网是学科网旗下的在线题库平台,覆盖小初高全学段全学科、超过900万精品解析试题。
关注组卷网服务号,可使用移动教学助手功能(布置作业、线上考试、加入错题本、错题训练)。
学科网长期征集全国最新统考试卷、名校试卷、原创题,赢取丰厚稿酬,欢迎合作。
钱老师 QQ:537008204 曹老师 QQ:713000635