文档内容
专题二 氧化还原反应规律在配平及在定量测定中的应用
【考情说明】
氧化还原反应规律及应用是课标卷每年的必考内容,但一般不单独命题,而是分
散在选择题的某个选项或非选择题的某些设问中,选择题往往与阿伏加德罗常数
或化学计算相结合,非选择题则可能与基本理论、元素化合物、化学实验及工艺流
程题相结合,分值一般占4~6分;从考查的内容上看。侧重氧化还原反应的规律
及氧化还原反应方程式的书写、配平及相关计算的考查,尤其是陌生反应方程式
的书写,近几年来更是常考不衰,随着新课标对考生学科素养的提高,这种趋势将
会有增无减。
1.氧化还原反应规律
(1)价态规律
升降规律:氧化还原反应中,化合价有升必有降,升降总值相等。
价态归中规律
含不同价态的同种元素的物质间发生氧化还原反应时,该元素价态的变化一定遵
循“高价+低价―→中间价”。而不会出现交叉现象。简记为“两相靠,不相交”。
歧化反应规律
“中间价―→高价+低价”。
具有多种价态的元素(如氯、硫、氮和磷元素等)均可发生歧化反应,如:Cl +
2
2NaOH===NaCl+NaClO+H O。
2
(2)强弱规律
自发进行的氧化还原反应,一般遵循强氧化剂制弱氧化剂,强还原剂制弱还原剂,
即“由强制弱”。
(3)电子守恒规律
氧化还原反应中,氧化剂得电子总数等于还原剂失电子总数。
2.氧化还原反应配平原则(1)“一般”配平原则
(2)“缺项”配平原则
对于化学反应方程式,所缺物质往往是酸、碱或水、补项的两原则
条件 补项原则
酸性条件下 缺H(氢)或多O(氧)补H+,少O(氧)补H O(水)
2
碱性条件下 缺H(氢)或多O(氧)补H O(水),少O(氧)补OH-
2
3.氧化还原反应定量测定
(1)滴定
①氧化还原滴定法是 以氧化还原反 应为基础的滴定分析方法。利用氧化还原滴定
法可以直接或间接测定许多具有氧化性或还原性的物质,也可以用氧化还原滴定
法间接测定。因此,它的应用非常广泛。
②在氧化还原滴定中,要使分析反应定量地进行完全,常常用强氧化剂和较强的
还原剂作为标准溶液。根据所用标准溶液的不同,氧化还原滴定法可分为高锰酸
钾法、重铬酸钾法等。
(2)计算
对于氧化还原反应的计算,要根据氧化还原反应的实质——反应中氧化剂得到的
电子总数与还原剂失去的电子总数相等,即得失电子守恒。利用守恒思想,可以抛
开繁琐的反应过程,可不写化学方程式,不追究中间反应过程,只要把物质分为始
态和终态,从得电子与失电子两个方面进行整体思维,便可迅速获得正确结果。
考点指导1 信息型方程式的书写
[指导] 新情景下氧化还原方程式书写步骤【典例1】 [2016·课标全国Ⅰ,27(4)]+6价铬的化合物毒性较大,常用NaHSO 将
3
废 液 中 的 Cr O 还 原 成 Cr3 + , 该 反 应 的 离 子 方 程 式 为
2
_____________________________________________________________________
_____________________________________________________________________
。
[师生互动]【对点训练】
1.[2018·课标全国Ⅱ,26(1)(3)]我国是世界上最早制得和使用金属锌的国家。一种
以闪锌矿(ZnS,含有SiO 和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如
2
图所示:
相关金属离子[c (Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
0
金属离子 Fe3+ Fe2+ Zn2+ Cd2+开始沉淀的
1.5 6.3 6.2 7.4
pH
沉淀完全的
2.8 8.3 8.2 9.4
pH
回答下列问题:
(1) 焙 烧 过 程 中 主 要 反 应 的 化 学 方 程 式 为
_____________________________________________________________________
_____________________________________________________________________
。
(2)溶液中的 Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为
_____________________________________________________________________。
答案 (1)2ZnS+3O =====2ZnO+2SO
2 2
(2)Zn+Cd2+===Zn2++Cd
2.[2016·课标全国Ⅱ,26(2)]实验室中可用次氯酸钠溶液与氨反应制备联氨,反应
的化学方程式为_____________________________________________________
__________________________________________________________________。
答案 NaClO+2NH ===N H +NaCl+H O
3 2 4 2
考点指导2 氧化还原反应计算
[指导] 计算流程
【典例2】 [2017·北京理综,27(2)]NSR(NO 储存还原)工作原理:
x
NO 的储存和还原在不同时段交替进行,如图a所示。
x(1)通过BaO和Ba(NO ) 的相互转化实现NO 的储存和还原。储存NO 的物质是
3 2 x x
________。
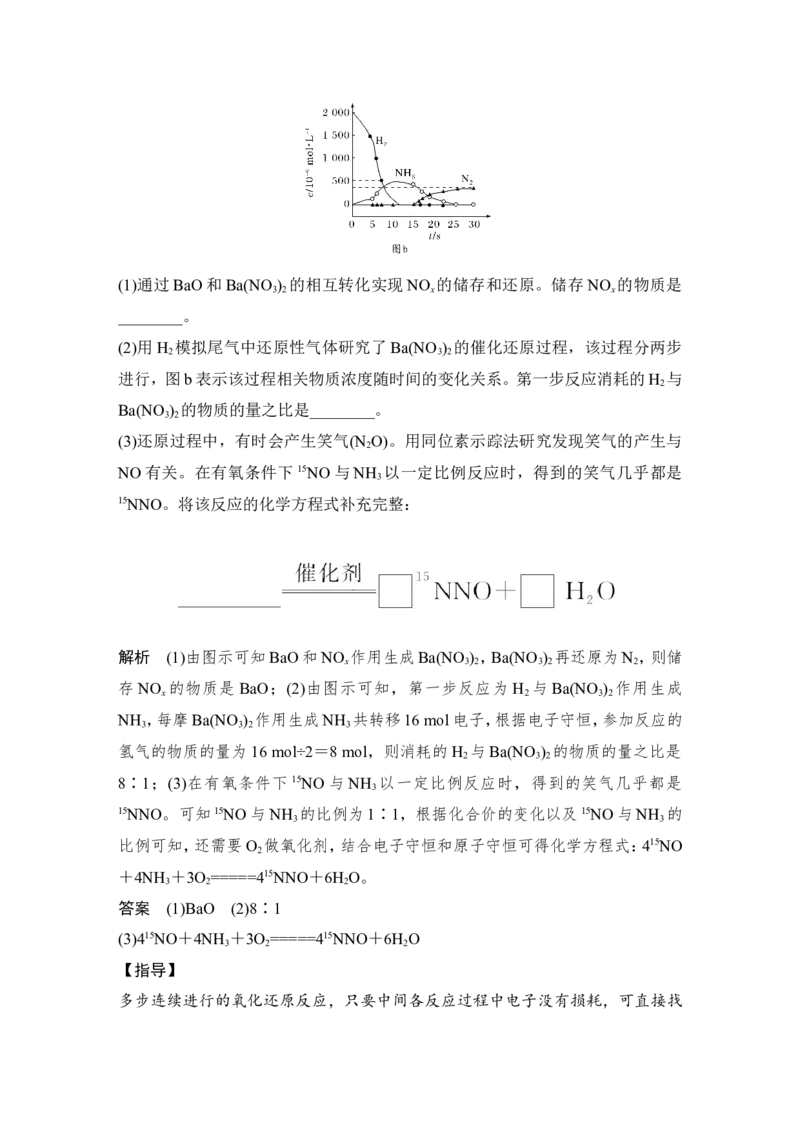
(2)用H 模拟尾气中还原性气体研究了Ba(NO ) 的催化还原过程,该过程分两步
2 3 2
进行,图b表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的H 与
2
Ba(NO ) 的物质的量之比是________。
3 2
(3)还原过程中,有时会产生笑气(N O)。用同位素示踪法研究发现笑气的产生与
2
NO有关。在有氧条件下15NO与NH 以一定比例反应时,得到的笑气几乎都是
3
15NNO。将该反应的化学方程式补充完整:
解析 (1)由图示可知BaO和NO 作用生成Ba(NO ) ,Ba(NO ) 再还原为N ,则储
x 3 2 3 2 2
存NO 的物质是 BaO;(2)由图示可知,第一步反应为 H 与Ba(NO ) 作用生成
x 2 3 2
NH ,每摩Ba(NO ) 作用生成NH 共转移16 mol电子,根据电子守恒,参加反应的
3 3 2 3
氢气的物质的量为16 mol÷2=8 mol,则消耗的H 与Ba(NO ) 的物质的量之比是
2 3 2
8∶1;(3)在有氧条件下 15NO与NH 以一定比例反应时,得到的笑气几乎都是
3
15NNO。可知15NO与NH 的比例为1∶1,根据化合价的变化以及15NO与NH 的
3 3
比例可知,还需要O 做氧化剂,结合电子守恒和原子守恒可得化学方程式:415NO
2
+4NH +3O =====415NNO+6H O。
3 2 2
答案 (1)BaO (2)8∶1
(3)415NO+4NH +3O =====415NNO+6H O
3 2 2
【指导】
多步连续进行的氧化还原反应,只要中间各反应过程中电子没有损耗,可直接找出起始物和最终产物,删去中间产物,建立二者之间的电子守恒关系,快速求解。
【对点训练】
3.[2018·江苏化学,16(4)]Fe O 与 FeS 混合后在缺氧条件下焙烧生成 Fe O 和
2 3 2 3 4
SO ,理论上完全反应消耗的n(FeS )∶n(Fe O )=________。
2 2 2 3
解析 Fe O 与FeS 混合后在缺氧条件下焙烧生成Fe O 和SO ,反应的化学方程
2 3 2 3 4 2
式 为 FeS + 16Fe O =====11Fe O + 2SO ↑ , 理 论 上 完 全 反 应 消 耗 的
2 2 3 3 4 2
n(FeS )∶n(Fe O )=1∶16。
2 2 3
答案 1∶16
考点指导3 氧化还原滴定
【典例3】 (2015·课标全国Ⅱ,28)二氧化氯(ClO ,黄绿色易溶于水的气体)是高效、
2
低毒的消毒剂。回答下列问题:
(1)工业上可用KClO 与Na SO 在H SO 存在下制得ClO ,该反应氧化剂与还原
3 2 3 2 4 2
剂物质的量之比为________。
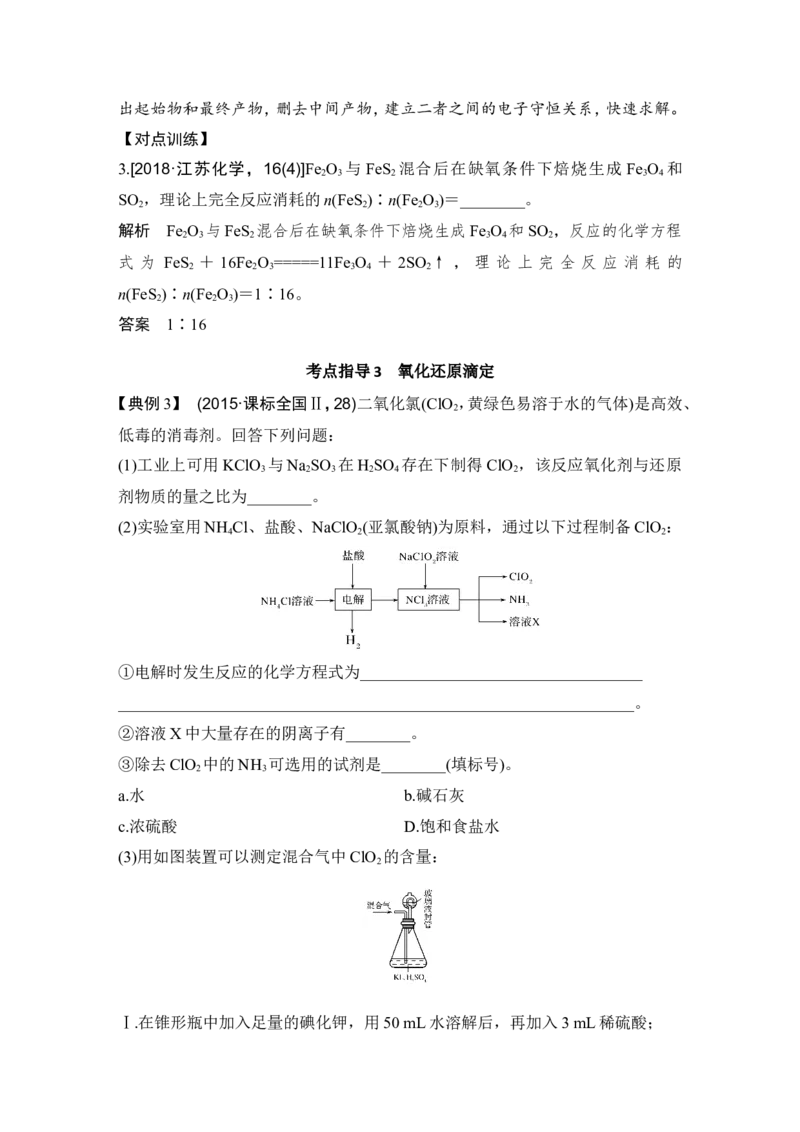
(2)实验室用NH Cl、盐酸、NaClO (亚氯酸钠)为原料,通过以下过程制备ClO :
4 2 2
①电解时发生反应的化学方程式为___________________________________
________________________________________________________________。
②溶液X中大量存在的阴离子有________。
③除去ClO 中的NH 可选用的试剂是________(填标号)。
2 3
a.水 b.碱石灰
c.浓硫酸 D.饱和食盐水
(3)用如图装置可以测定混合气中ClO 的含量:
2
Ⅰ.在锥形瓶中加入足量的碘化钾,用50 mL水溶解后,再加入3 mL稀硫酸;Ⅱ.在玻璃液封装置中加入水,使液面没过玻璃液封管的管口;
Ⅲ.将一定量的混合气体通入锥形瓶中吸收;
Ⅳ.将玻璃液封装置中的水倒入锥形瓶中;
Ⅴ.用0.100 0 mol·L-1硫代硫酸钠标准溶液滴定锥形瓶中的溶液(I +2S O===2I-
2 2
+S O),指示剂显示终点时共用去20.00 mL硫代硫酸钠溶液。在此过程中:
4
① 锥 形 瓶 内 ClO 与 碘 化 钾 反 应 的 离 子 方 程 式 为
2
______________________________________________________________________
_____________________________________________________________________
。
②玻璃液封装置的作用是________________。
③Ⅴ中加入的指示剂通常为________,滴定至终点的现象是________。
④测得混合气中ClO 的质量为________g。
2
解析 (1)由KClO 与Na SO 在H SO 存在下制取ClO 的反应中,KCl
3 2 3 2 4 2
, 则 Na SO 作 还 原 剂 , 根 据 电 子 守 恒 ,
2 3
n(KClO )∶n(Na SO )=2∶1。(2)①由制备ClO 的流程图可知, 电解NH Cl溶液
3 2 3 2 4
和盐酸的混合物得到NCl 溶液和H ,根据电子守恒和质量守恒可写出该反应的
3 2
化学方程式。②由制备ClO 的流程图可知,NaClO 和NCl 两溶液反应生成NH ,
2 2 3 3
说明溶液呈碱性; , ,因此溶液X中大量存在
的阴离子有OH-和Cl-。③ClO 和NH 均是易溶于水的气体,a项错误,d项错误;
2 3
b项,碱石灰与NH 不反应,错误;c项,浓硫酸易吸收NH ,而与ClO 不反应,正
3 3 2
确。
(3)①ClO 与KI溶液反应时, ,反应环境为
2
酸性,从而可写出该反应的离子方程式。②玻璃液封装置的作用是防止残余的
ClO 气体挥发到空气中,污染空气。③步骤V反应中,I →2I-,I 使淀粉溶液显蓝
2 2 2
色,故可选用淀粉溶液作指示剂,滴定至终点时溶液由蓝色变为无色。④由反应2ClO +10I-+8H+===2Cl-+5I +4H O、I +2S O===2I-+S O 可得关系式:
2 2 2 2 2 4
2ClO ~5I ~10S O,n(S O)=0.100 0 mol·L-1×20.00 mL×10-3 L/mL=2×10-3
2 2 2 2
mol,则n(ClO )=2×10-3 mol×2/10=4×10-4 mol,m(ClO )=4×10-4 mol×67.5
2 2
g·mol-1=0.027 00 g。
答案 (1) 2∶1
(2)①NH Cl+2HCl=====3H ↑+NCl ②Cl-、OH- ③c
4 2 3
(3)①2ClO +10I-+8H+===2Cl-+5I +4H O
2 2 2
②吸收残余的二氧化氯气体(其他合理答案也可)
③淀粉溶液 溶液由蓝色变为无色且30 s内不恢复原色
④0.027 00
【指导】 氧化还原反应滴定指示剂的选择
1.自身指示剂:有些标准溶液或被滴定物质本身有颜色,而滴定产物为无色,则滴
定时就无需另加指示剂,自身颜色变化可以起指示剂的作用,此类指示剂称为自
身指示剂。如MnO本身在溶液中显紫红色,还原后的产物Mn2+为无色,所以用高
锰酸钾溶液滴定时,不需要另加指示剂。
2.显色指示剂:有些物质本身并没有颜色,但它能与滴定剂或被测物质反应产生特
殊的颜色,或开始有特殊颜色,滴定后变为无色,因而可指示滴定终点。如滴定前
溶液中有单质碘,滴定后单质碘消失等,可用淀粉等作为指示剂。
【对点训练】
4.甲、乙、丙三位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案:
方案①铜与浓硫酸加热直接反应,即Cu→CuSO
4
方案②由Cu→CuO→CuSO
4
方案③铜放入稀硫酸中,然后不断投入空气
请回答下列问题:
(1)“方案①”中铜和浓硫酸反应的化学方程式是________,该反应体现了浓硫酸
的________性和________性。
(2) 这 两 种 方 案 , 你 认 为 哪 一 种 方 案 更 合 理 ?
__________________________________________________________________
(答编号),理由是__________________________________________________。
(3) 写 出 方 案 ③ 的 发 生 反 应 的 化 学 方 程 式_____________________________________________________________________,
如果用此反应设计一个原电池,试写出电池的电极反应方程式,负极________,正
极________。
解析 (1)铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫与水,反应方程式
为:Cu+2H SO (浓)=====CuSO +SO ↑+2H O,反应中硫元素的化合价部分降
2 4 4 2 2
低生成二氧化硫,部分不变存在与硫酸铜中,浓硫酸表现强氧化性与酸性。
(2)方案①生成二氧化硫,污染空气,硫元素不能完全利用,方案②与方案①相比,
没有污染产生且原料,故方案②更合理。
(3)2Cu+2H SO +O ===2CuSO +2H O,负极Cu-2e-===Cu2+
2 4 2 4 2
正极O +4H++4e-===2H O
2 2
答案 (1)Cu+2H SO (浓)=====CuSO +SO ↑+2H O 强氧化 酸
2 4 4 2 2
(2)② 方案②无污染产生,原料利用率高。
(3)2Cu+2H SO +O ===2CuSO +2H O,负极Cu-2e-===Cu2+
2 4 2 4 2
正极O +4H++4e-===2H O
2 2