文档内容
专题四 阿伏伽德罗常数 基础过关检测
考试时间:70分钟 卷面分值:100分
学校:___________姓名:___________班级:___________考号:___________
注意事项:
1.答题前,务必将自己的姓名、考号填写在答题卡规定的位置上。
2.答选择题时,必须使用2B铅笔将答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦擦干净后,再选涂其它答案标号。
3.答非选择题时,必须将答案书写在专设答题页规定的位置上。
4.所有题目必须在答题卡上作答。在试题卷上答题无效。
5.考试结束后,只交试卷答题页。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32 Cl-35.5
一、选择题(本题含16小题,每题3分,共48分。每题只有一个选项符合题意)
1.(2022·陕西汉中·统考模拟预测) 是阿伏加德罗常数的值。下列说法正确的是
A. 固体中含阴、阳离子的总数为
B.标准状况下, 和足量 反应,生成的 分子数目为
C.常温常压下, 乙烯与丙烯的混合物所含的原子数目为
D. 苯中含有碳碳双键的数目为
【答案】C
【详解】A.过氧化钠由2个钠离子和1个过氧根离子构成, 的物质的量为
0.05mol,含阴、阳离子的总数为 ,故A错误;
B.二氧化硫与氧气的反应是可逆反应,不可能完全转化,因此生成的 分子数目小
于 ,故B错误;
C.乙烯与丙烯的最简式均为CH,则 乙烯与丙烯的混合物所含的原子数目为
2
,故C正确;D.苯分子中不含碳碳双键,故D错误;
故答案选C。
2.(2022·浙江杭州·杭州高级中学校考模拟预测)设 为阿伏加德罗常数的值,下列
说法不正确的是
A.标准状况下, 氦气含有的原子数为
B. 金刚石中的共价键数目为
C. 溶液与足量氯气完全反应时转移电子数为
D. 时, 的稀硫酸中含有 的数目为
【答案】D
【详解】A.氦气为单原子分子, 氦气含有的原子数为 ,A正确;
B.金刚石为正四面体结构,碳碳键的数目为: , 金刚石中的共价键数目
为 ,B正确;
C. 含有 , ,与足量的 反应, ,
转移1mol电子, ,转移2mol电子,转移电子数为 ,C正确;
D.缺少溶液体积,无法计算 的稀硫酸中含有 的数目,D错误;
故选D。
3.(2022·四川成都·统考模拟预测)设N 是阿伏加德罗常数的值,下列说法正确的是
A
A.22.4L环丙烷和丙烯的混合气体中所含共用电子对数为9N
A
B.常温常压下,78g苯中含C=C的数目为3N
A
C.电解精炼铜时,若阴极质量增加64g,则阳极失去的电子数为2N
A
D.1L 2mol/LNaClO溶液中,ClO-数目为2N
A
【答案】C
【详解】A.没有标况不能计算其物质的量,故A错误;
B.苯中不含碳碳双键,故B 错误;
C.电解精炼铜时,阴极上铜离子放电生成铜单质,若阴极质量增加64g,生成铜
试卷第2页,共17页1mol,根据电子守恒可知,阳极失去的电子数为2N ,故C正确;
A
D.次氯酸根离子水解导致次氯酸根离子小于2mol,数目小于2N ,故D错误;
A
故选C。
4.(2022·湖北黄冈·校联考模拟预测)酒驾检验原理:
2KCr O+3CH CHOH+8H SO =3CH COOH+2Cr (SO )+11H O+2KSO 。设N 为阿伏
2 2 7 3 2 2 4 3 2 4 3 2 2 4 A
伽德罗常数的值,下列说法正确的是
A.lmol[2K Cr O+3CH CHOH]完全反应转移电子数为6N
2 2 7 3 2 A
B.25℃时,1LpH=1的HSO 溶液中含SO 数目为0.1N
2 4 A
C.等物质的量的CHCHOH和CHCOOH充分反应生成的HO中含氢键数为2N
3 2 3 2 A
D.1molCH COOH中含sp2—sp3σ键的数目为2N
3 A
【答案】D
【详解】A.反应中铬元素化合价从+6降低到+3,降低3价,故该反应中转移电子数
为12个,则1mol[2K Cr O+3CH CHOH]完全反应转移电子数为12N ,A项错误;
2 2 7 3 2 A
B.25°C时,1LpH=1的HSO 溶液中含H+数目为0.1N ,SO 2-数目0.05N ,B项错误;
2 4 A 4 A
C.等物质的量并不特指1mol,C项错误;
D. CHCOOH中甲基上的碳原子为sp3杂化,羧基上的碳原子为sp2杂化,故可以从
3
羧基上碳原子分析,1molCH COOH共含sp2-sp3σ键的数目为2N ,D项正确。
3 A
故选D。
5.(2022·北京海淀·人大附中校考模拟预测)工业上常用组合试剂对尾气进行处理。
如: 。用 表示阿伏伽德罗常数的值,下列说法
不正确的是
A. 中所含离子总数为
B.标准状况下, 中所含电子总数约为
C.25℃时, 的HCl溶液中含有 的数目约为
D.生成 沉淀时,吸收 的体积在标准状况下约为0.224 L
【答案】C
【详解】A. 中含有 和 ,离子总数为 ,A正确;
B. 物质的量为0.5mol,所含的电子数为 ,B正确;C. 的盐酸溶液,没有告诉溶液体积,无法计算 的数目,C错误;
D. 为0.1mol,根据元素守恒,吸收 0.1mol,在标准状况下约为0.224
L ,D正确;
故选C。
6.(2022·浙江·模拟预测)设 为阿伏加德罗常数的值,下列有关叙述不正确的是
A.0.1mol的 中含有 个中子
B.标准状况下, 和CO混合气体在足量 中充分燃烧,消耗 分子数为
C. 含有 键的数目为
D.常温下, 溶液与 溶液所含 的物质
的量,后者小
【答案】C
【详解】A.元素符号的左上角为质量数,质量数=质子数+中子数,硼元素质子数为
5,1个 中含有6个中子,则 中含有 个中子,A正确;
B.标准状况下, 和CO混合气体的总物质的量为 ,
、CO燃烧反应分别为: 、 ,等物质的量
的 、CO消耗 的量相同,0.2mol的混合气体消耗 的物质的量为0.1mol,即分
子数为 ,B正确;
C. 和 与 形成的配位键为 键,一个 分子中含有3个 键,
所以 含 键的物质的量为 ,C错误;
试卷第4页,共17页D.不考虑 水解和 电离时, 溶液与
溶液中均含有0.5mol氯化铵,由于 水解,溶液中 数目
都减少,且 浓度越大,水解程度越小,所以两溶液中含有的 物质的量不同,
且前者大于后者,D正确;
故选C。
7.(2023·广东广州·一模)科学家进行如图所示的 制备及应用的研究,下列说
法不正确的是
A. 中C原子的杂化类型为
B. 含有约 个电子
C. 和 合成甲醇符合原子利用率100%
D.图中涉及反应包含非极性键的断裂和生成
【答案】C
【详解】A. 中C原子形成4个共价键,杂化类型为 ,A正确;
B.1分子二氧化碳含有22个电子,则 含有电子22mol,数目约
个电子,B正确;
C. 中碳氧原子个数为1:2,甲醇中碳氧原子个数为1:1,故 和 合成甲醇原
子利用率不会是100%,C错误;
D.图中H 参与反应,涉及非极性键的断裂,氯碱工业生成H 和Cl 涉及非极性键的
2 2 2
形成,D正确;故选C。
8.(2022·浙江·模拟预测)设 为阿伏加德罗常数的值,下列说法正确的是
A.11g氚水(超重水)所含中子数为
B.46g 和 混合气体中所含的原子总数为
C.一定条件下,1molFe与1mol 充分反应,Fe失去的电子数目为
D.某温度下,1LpH=6的纯水中所含 的数目为
【答案】B
【详解】A.11g氚水(超重水)的物质的量为 ,1个 分子中含有
12个中子,则11g氚水(超重水)含中子数为 ,故A错误;
B. 和 的最简式均为 ,故46g混合气体中含有的“ ”的物质的量为
1mol,该混合气体中含 个原子,故B正确;
C.根据反应: ,1molFe与1mol 充分反应,Fe过量,氯气全
部反应,则Fe失去的电子数目为 ,故C错误;
D.纯水中 ,又 ,则 ,
,则 的数目为 ,故D错误;
故选B。
9.(2022·浙江·模拟预测)设阿伏加德罗常数的值为 。下列说法正确的是
A.1mol 中含有的 键数为
B.2.8gCO和 的混合物中含有的质子数为
C.1mol苯乙烯中碳碳双键的数目为
试卷第6页,共17页D.0.5mol乙酸乙酯在酸性条件下水解,生成乙醇的分子数为
【答案】B
【详解】A.1个 中 和N原子之间共形成2个配位键,1个 中存
在3个N—H键,1个 中含有8个σ键,则1mol 中含有的σ
键数为 ,A错误;
B.CO与 分子中含有的质子数都是14,二者的相对分子质量都是28,2.8gCO或
的物质的量都是0.1mol,2.8g二者混合物中含有的质子总数为 ,B正确;
C.苯乙烯的结构简式为 ,苯环中不含碳碳双键,故1mol苯乙烯中
含有的碳碳双键数目为 ,C错误;
D.乙酸乙酯在酸性条件下的水解为可逆反应,则0.5mol乙酸乙酯在酸性条件下水解
生成乙醇的分子数小于 ,D错误。
故答案选B。
10.(2023·浙江杭州·学军中学校考模拟预测)设N 代表阿伏加德罗常数的值,下列
A
说法正确的是
A.1mol D18O+(其中D代表 )中含有的中子数为10 N
3 A
B.2N 个HCl分子与44.8 L H 和Cl 的混合气体所含的原子数目均为4N
A 2 2 A
C.物质的量浓度均为1mol/L的NaCl和MgCl 混合溶液中,含有Cl-的数目为3N
2 A
D.32gCu将足量浓、稀硝酸分别还原为NO 和NO,浓、稀硝酸得到的电子数均为N
2 A
【答案】D
【详解】A.一个D原子有1个中子,一个18O有10个中子,故1mol D18O+中含有的
3
中子数为13 N ,A错误;
A
B.未指明标准状况下,H 和Cl 的混合气体的物质的量无法计算,B错误;
2 2
C.未指明溶液体积,无法计算Cl-的数目,C错误;
D.浓、稀硝酸足量,说明Cu完全转化为Cu2+,32gCu转移电子1mol,Cu失电子数与浓、稀硝酸得电子数相等,故浓、稀硝酸得到的电子数均为N ,D正确;
A
故答案选D。
11.(2022·浙江·模拟预测) 为阿伏加德罗常数的值,下列说法正确的是
A. 金刚烷 中含有 键数为
B. 中含有质子数为
C.标准状况下 二氯甲烷中含有氯原子数为
D. 碘蒸气与足量氢气加热,得到 的分子数为
【答案】B
【详解】A.金刚烷中除了C-C键外还含有C—H键,如 ,含有16个C—
H键和12个C—C键,故1mol金刚烷中含有 键的数目为 ,A错误;
B. 的摩尔质量为 ,故 的物质的量为
,每个 分子中含有质子数为70,故 中含有质
子数为 ,B正确:
C.二氯甲烷标准状况下为液体,故不能用标况下的气体摩尔体积计算其物质的量,C
错误;
D.碘与氢气反应生成碘化氢为可逆反应,故得到 的分子数小于 ,D错误;
故选B。
12.(2022·浙江·模拟预测)在特定催化剂条件下, 可除去废气中的氮氧化物,
总反应为 ,设 为阿伏加德罗常数的值,下列说
试卷第8页,共17页法错误的是
A. 所含中子数为
B.生成标准状况下 ,转移的电子数为
C.该反应中消耗 还原剂,生成的 键的个数为
D.装有 的集气瓶中含有的分子数小于
【答案】C
【详解】A.1个 分子含有17个中子,则 所含中子数为 ,A正
确;
B.该反应中 、 、 中 的化合价变化分别为-3→0、+2→0、+4→0,所
以生成标准状况下 (即 ) 时,转移的电子数为 ,B正确;
C.由反应的各物质中元素化合价变化情况可知, 作还原剂,该反应中消耗
还原剂,生成 氮气、 水, 键个数为 ,C错误;
D. ,则装有 (即 ) 的集气瓶中含有的分子数小于 ,
D正确;
故选C。
13.(2022·全国·校联考模拟预测) 表示阿伏伽德罗常数的值。下列说法正确的是
A. 个 和 (标准状况)在光照下充分反应后的气体体积在标准状况下
为56L
B.8.7g MnO 和40mL 的浓盐酸共热可生成 的分子数为0.1
2
C.将浓度均为 的 溶液与KI溶液等体积混合,转移电子数为0.1
D.1g的 和 的混合物所含中子数、电子数均为0.5
【答案】D【详解】A. 个 和 (标准状况) ,即0.5molCH 和2mol氯气在光照
4
下充分反应,由于反应生成一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳和氯化氢等混
合物、且只有一氯甲烷和氯化氢呈气态,则难以计算反应后生成的气体的物质的量、
难以计算气体在标准状况下的体积,A错误;
B.8.7g MnO 和40mL 的浓盐酸共热,即0.1mol MnO 和含0.4molHCl的浓
2 2
盐酸共热,随着反应进行,盐酸浓度降低反应停止,故可生成 的物质的量小于
0.1mol、氯气分子数小于0.1 ,B错误;
C.将浓度均为 的 溶液与KI溶液等体积混合,铁离子和碘离子反应生
成亚铁离子和碘分子,由于该反应可逆,则转移电子数小于0.1 ,C错误;
D. 和 的摩尔质量均为20g/mol,每个 和 分子所含中子、电子
数均为10,则1g的 和 的混合物物质的量为0.05mol,所含中子数、电子数
均为0.5 ,D正确;
答案选D。
14.(2022·重庆·西南大学附中校联考模拟预测)用 表示阿伏加德罗常数的值。下
列说法正确的是
A.1mol 与 溶液完全反应,溶液中存在
B.1mol重水比1mol水多 个质子
C.电解精炼铜时,电路中每通过 个电子时阳极溶解32g
D.常温常压下,1.4g乙烯和丙烯混合气体含有的原子数为
【答案】D
【详解】A. 与 反应生成NaCl和NaClO,ClO-会发生水解生成HClO,所以
试卷第10页,共17页反应后后溶液中含氯粒子有Cl-、ClO-、HClO,根据氯原子守恒,
,A错误;
B.DO和HO质子数相同,中子数不同,B错误;
2 2
C.电解精炼铜时,阳极铜失电子,比铜金属性强的其它杂质金属也会失电子,电路中
每通过 个电子时阳极溶解 小于32g,C错误;
D.乙烯和丙烯混合物最简式为CH,1.4g乙烯和丙烯混合气体含有的原子数为
2
,D正确;
故答案选D。
15.(2022·北京·模拟预测)下列关于“100 mL 0.1 mol·L-1 BaCl 溶液”的说法正确的
2
是
A.该溶液中含有的微粒主要有:BaCl 、Ba2+、Cl-、HO
2 2
B.若取该溶液10 mL,其中c(Ba2+)=0.01 mol·L-1
C.若取该溶液10 mL,恰好能与10 mL 0.1 mol·L-1 Na SO 溶液完全反应
2 4
D.该溶液与0.1 mol·L-1 NaCl溶液中的c(Cl-)相等
【答案】C
【详解】A.BaCl 是强电解质,在水中完全电离为Ba2+、Cl-,不存在BaCl ,同时该
2 2
溶液中还含有溶剂HO分子,A错误;
2
B.溶液的浓度与溶液体积大小无关,所以从该溶液中取该溶液10 mL,物质的浓度不
变,其中c(Ba2+)=0.1 mol·L-1,B错误;
C.BaCl 、NaSO 发生反应:BaCl +Na SO =BaSO ↓+2NaCl,二者恰好反应时物质的
2 2 4 2 2 4 4
量相等,由于两种溶液浓度相同、体积相等,因此10 mL0.1 mol/L BaCl 溶液恰好能与
2
10 mL 0.1 mol·L-1 Na SO 溶液完全反应,C正确;
2 4
D.该溶液中c(Cl-)=2c(BaCl )=0.2 mol/L,0.1 mol·L-1 NaCl溶液中的c(Cl-)=0.1
2
mol·L-1,可见两种溶液中c(Cl-)不相等,D错误;
故合理选项是C。
16.(2023·重庆·统考模拟预测) 是阿伏加德罗常数的值。下列说法正确的是
A.标准状态下,11.2L 分子中所含的O原子数为1.5
B.32.5g 水解形成的 胶体粒子数为0.2C.10g质量分数为46%的乙醇水溶液中含有的氢原子数为1.2
D.工业上将1mol 和3mol 在一定条件下反应转移的电子数为6
【答案】C
【详解】A. 标准状况下是固体,不能通过气体摩尔体积计算,A错误;
B .1个氢氧化铁胶粒是由若干个氢氧化铁构成的,故32.5g 含Fe3+物质的量为
0.2mol,水解形成的 物质的量小于0.2mol,得到的 胶体粒子数少于
0.2 ,B错误;
C.乙醇水溶液中含有的氢原子数包含乙醇和水的氢原子数,其中n(CHCHOH)
3 2
,根据1个乙醇分子中含有6个H原子,故0.1mol乙醇含有H原
子0.6mol;另外,n(H O) ,根据1个水分子中含有2个H原子,故
2
0.3mol水含有H原子0.6mol,则n(H)=0.6mol+0.6mol=1.2mol,氢原子数为1.2N ,C
A
正确;
D. 1mol 和3mol 完全反应则转移电子数为6 ,合成氨的反应是一个可逆反
应,1mol 和3mol 不能完全反应,则转移的电子数小于6 ,D错误;
故选C。
二、非选择题 (本题共5小题,1-3题每题10分,4-5题每题11分,共52分)
17.(2022·浙江杭州·统考二模)以下方法常用于对废水中的苯酚进行定量测定:取
含苯酚废水,加过量溴水使苯酚完全反应,煮沸,再加入过量 溶液生成
三溴苯酚,再用 标准溶液滴定至终点,消耗 溶液
试卷第12页,共17页.已知 (三
溴苯酚) . 和 溶液颜色均为
无色.
(1)消耗 的物质的量为________.
(2)废水中苯酚的物质的量浓度为_______(写出简要计算过程).
【答案】(1)
(2)
【解析】(1)滴定至终点时消耗 溶液 , 的浓度为
,则消耗 的物质的量为
;
(2)根据反应的方程式可知: ,则 ,即苯酚
的物质的量为 ,其体积为 ,则其浓度为
。
18.(2022·浙江宁波·统考二模)单质硫在热的NaOH溶液中发生如下反应:
3S+6NaOH 2NaS+Na SO +3H O。若硫过量,会进一步生成NaS 和NaSO:
2 2 3 2 2 x 2 2 3
(x-1)S+Na S NaS,S+Na SO NaSO。现有3.84 g硫与含0.06 mol NaOH的
2 2 x 2 3 2 2 3
热溶液完全反应,生成a mol Na S 和b mol Na SO,在混合溶液中加入NaClO碱性溶
2 x 2 2 3
液300 mL,恰好将硫元素全部转化为SO 。
请计算:(1)a mol Na S 和b mol Na SO 中a∶b=____。
2 x 2 2 3
(2)NaClO溶液的物质的量浓度为____mol·L-1 (写出计算过程)。
【答案】(1)2:1
(2)1.2
【分析】(1)根据反应过程中S元素得失电子守恒计算NaS 和NaSO 中a∶b的大小;
2 x 2 2 3
(2)硫元素最终全部转化为NaSO ,转移电子总数为硫单质转化为硫酸根离子失去的电
2 4
子数,根据电子守恒计算NaClO的物质的量,然后根据物质的量浓度定义式计算。
(1)3.84 g硫单质的物质的量为n(S)= ,其与含有0.06 mol NaOH溶液
反应,产生a mol Na S 和b mol Na SO,根据电子得失电子数目相等可知:a×x×
2 x 2 2 3
=b×2×2,解得a=2b,所以a:b=2:1;
(2)3.84 g硫单质的物质的量为n(S)= ,其反应产生的a mol Na S 和b
2 x
mol Na SO,在混合溶液中加入NaClO碱性溶液300 mL,S完全转化为NaSO ,
2 2 3 2 4
NaClO得到电子被还原为NaCl,根据氧化还原反应中电子守恒可得0.12 mol×(6-
0)=n(NaClO) ×[1-(-1)],解得n(NaClO)=0.36 mol。由于NaClO碱性溶液体积是300
mL,则该溶液的物质的量浓度c(NaClO)= 。
19.(2022·福建三明·统考三模)为了探究市售Fe O 能否与常见的酸(盐酸、稀硫酸)
3 4
发生反应,实验小组做了以下工作。
Ⅰ.Fe O 的制备
3 4
(1)将可溶性亚铁盐和铁盐按一定配比混合后,加入NaOH溶液,在一定条件下反应可
制行Fe O,反应的离子方程式为_______。
3 4
Ⅱ.Fe O 与酸反应的热力学论证
3 4
(2)理论上完全溶解1.16gFe O 至少需要3 mol/LH SO 溶液的体积约为_______mL(保留
3 4 2 4
1位小数)。
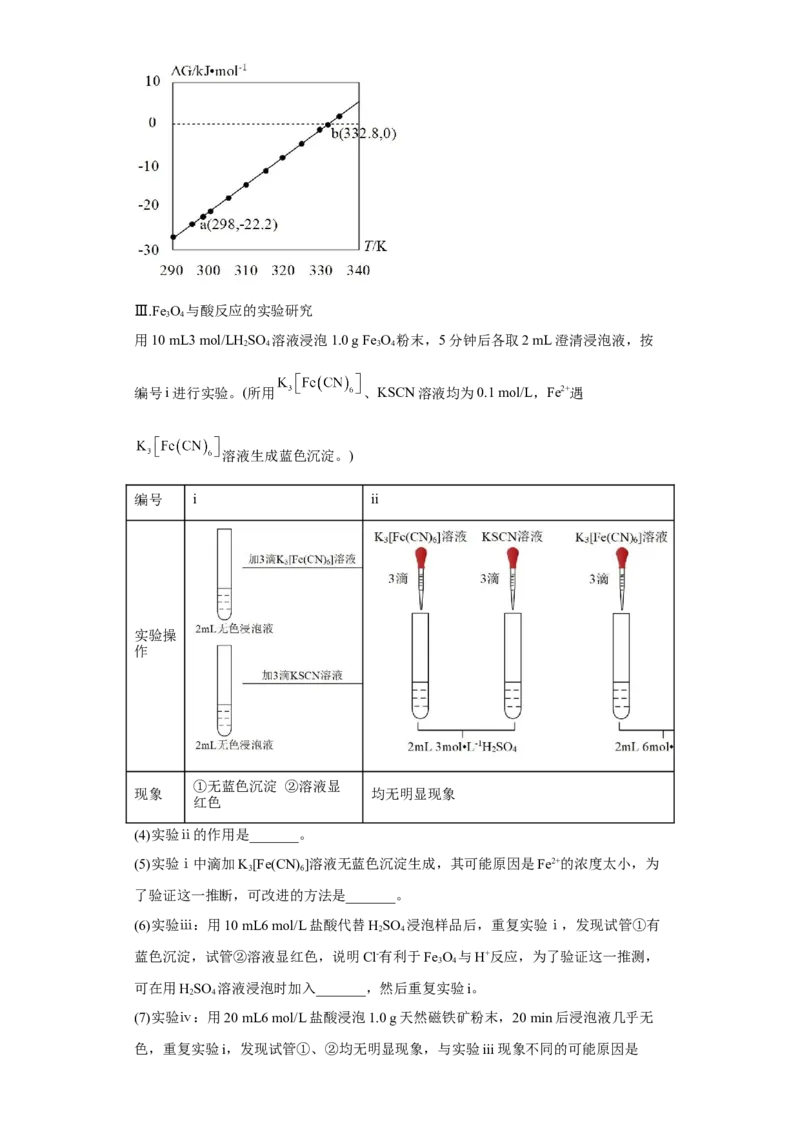
(3)查阅文献:吉布斯自由能 ,在100 kPa下,Fe O 与酸反应的△G与
3 4
温度T的关系如图所示。Fe O 与酸自发反应的温度条件是_______。
3 4
试卷第14页,共17页Ⅲ.Fe O 与酸反应的实验研究
3 4
用10 mL3 mol/LH SO 溶液浸泡1.0 g Fe O 粉末,5分钟后各取2 mL澄清浸泡液,按
2 4 3 4
编号i进行实验。(所用 、KSCN溶液均为0.1 mol/L,Fe2+遇
溶液生成蓝色沉淀。)
编号 i ii
实验操
作
①无蓝色沉淀 ②溶液显
现象 均无明显现象
红色
(4)实验ⅱ的作用是_______。
(5)实验ⅰ中滴加K[Fe(CN) ]溶液无蓝色沉淀生成,其可能原因是Fe2+的浓度太小,为
3 6
了验证这一推断,可改进的方法是_______。
(6)实验ⅲ:用10 mL6 mol/L盐酸代替HSO 浸泡样品后,重复实验ⅰ,发现试管①有
2 4
蓝色沉淀,试管②溶液显红色,说明Cl-有利于Fe O 与H+反应,为了验证这一推测,
3 4
可在用HSO 溶液浸泡时加入_______,然后重复实验i。
2 4
(7)实验ⅳ:用20 mL6 mol/L盐酸浸泡1.0 g天然磁铁矿粉末,20 min后浸泡液几乎无
色,重复实验i,发现试管①、②均无明显现象,与实验iii现象不同的可能原因是_______。
【答案】(1)
(2)6.7
(3)
(4)作对照实验,排出HSO 、HCl对实验现象的干扰。
2 4
(5)在试管中加入植物油隔绝空气,并延长浸泡Fe O 的时间、或者适当升高反应温度、
3 4
搅拌等。
(6)NaCl固体
(7)天然磁铁矿粉末中杂质较多,Fe O 的含量较低
3 4
【解析】(1)将可溶性亚铁盐和铁盐按一定配比混合后,加入NaOH溶液,在一定条件
下反应可制行Fe O,反应的离子方程式为 。
3 4
(2)Fe O 与HSO 溶液反应的化学方程式为 ,
3 4 2 4
1.16gFe O 的物质的量为0.005mol,则需要HSO 的物质的量为0.02mol,则至少需要
3 4 2 4
3 mol/LH SO 溶液的体积约为 。
2 4
(3)反应的 时,反应能自发进行,由图可知,当温度低于332.8K时,该反应的
,故Fe O 与酸自发反应的温度条件是 。
3 4
(4)实验ⅱ的作用是作对照实验,排除HSO 、HCl对实验现象的干扰。
2 4
(5)实验ⅰ中滴加K[Fe(CN) ]溶液无蓝色沉淀生成,其可能原因是Fe2+的浓度太小,也
3 6
可能是Fe2+被空气中的氧气氧化为Fe3+,为了验证这一推断,可改进的方法是在试管中
加入植物油隔绝空气,并延长浸泡Fe O 的时间、或者适当升高反应温度、搅拌等。
3 4
(6)用10 mL6 mol/L盐酸代替HSO 浸泡样品后,重复实验ⅰ,发现试管①有蓝色沉淀,
2 4
试管②溶液显红色,说明Cl-有利于Fe O 与H+反应,为了验证这一推测,可在用
3 4
HSO 溶液浸泡时加入NaCl固体,然后重复实验i。
2 4
(7)
实验ⅳ:用20 mL6 mol/L盐酸浸泡1.0 g天然磁铁矿粉末,20 min后浸泡液几乎无色,
重复实验i,发现试管①、②均无明显现象,与实验iii现象不同的可能原因是天然磁
铁矿粉末中杂质较多,Fe O 的含量较低。
3 4
20.(2022·吉林延边·统考一模)硫酸肼(N H·H SO )又名硫酸联氨,在医药、染料、
2 4 2 4
农业上用途广泛。
已知:①Cl 与NaOH溶液的反应为放热反应,Cl 与热的NaOH溶液反应会生成
2 2
试卷第16页,共17页NaClO
3
②利用尿素法生产水合肼的原理:CO(NH)+2NaOH+NaClO=N H·H O+Na CO+NaCl
2 2 2 4 2 2 3
③硫酸肼的制备原理:NH·H O+HSO =N H·H SO +H O
2 4 2 2 4 2 4 2 4 2
回答下列问题:
Ⅰ.制备NaClO溶液
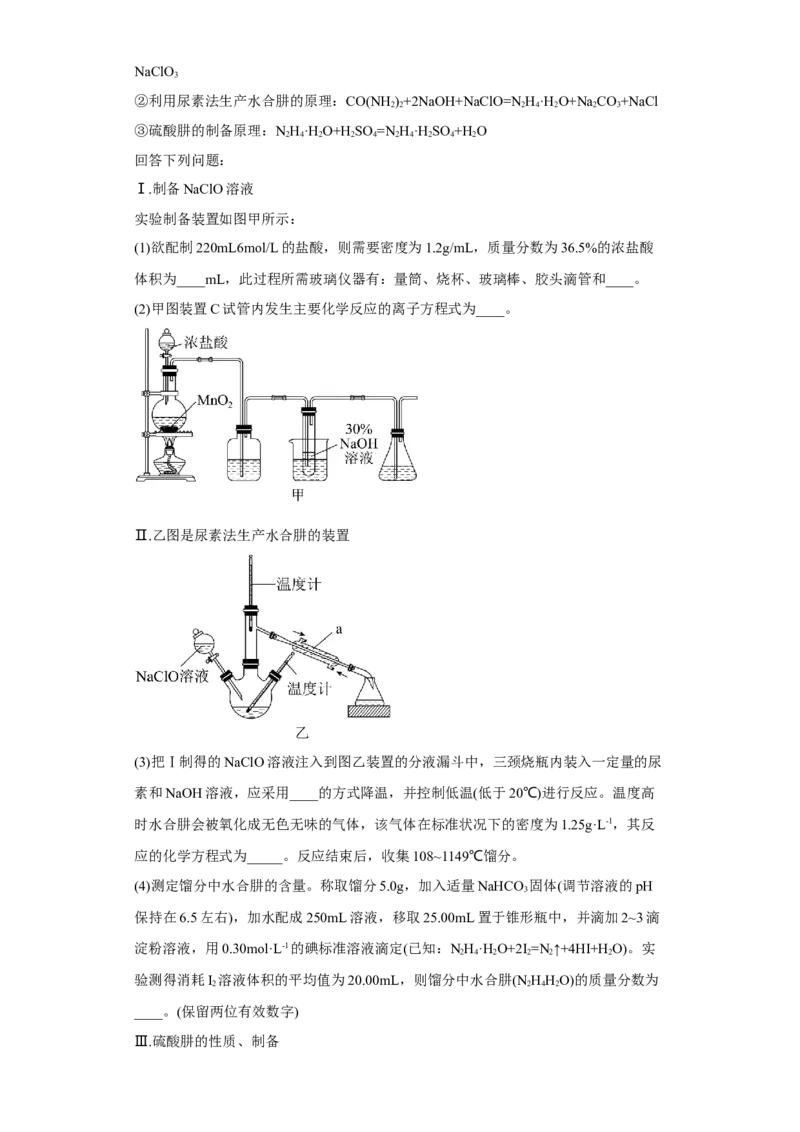
实验制备装置如图甲所示:
(1)欲配制220mL6mol/L的盐酸,则需要密度为1.2g/mL,质量分数为36.5%的浓盐酸
体积为____mL,此过程所需玻璃仪器有:量筒、烧杯、玻璃棒、胶头滴管和____。
(2)甲图装置C试管内发生主要化学反应的离子方程式为____。
Ⅱ.乙图是尿素法生产水合肼的装置
(3)把Ⅰ制得的NaClO溶液注入到图乙装置的分液漏斗中,三颈烧瓶内装入一定量的尿
素和NaOH溶液,应采用____的方式降温,并控制低温(低于20℃)进行反应。温度高
时水合肼会被氧化成无色无味的气体,该气体在标准状况下的密度为1.25g·L-1,其反
应的化学方程式为_____。反应结束后,收集108~1149℃馏分。
(4)测定馏分中水合肼的含量。称取馏分5.0g,加入适量NaHCO 固体(调节溶液的pH
3
保持在6.5左右),加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴
淀粉溶液,用0.30mol·L-1的碘标准溶液滴定(已知:NH·H O+2I =N ↑+4HI+H O)。实
2 4 2 2 2 2
验测得消耗I 溶液体积的平均值为20.00mL,则馏分中水合肼(N HHO)的质量分数为
2 2 4 2
____。(保留两位有效数字)
Ⅲ.硫酸肼的性质、制备已知:硫酸肼(又可以表示为:NHSO )是一种重要的化工原料,硫酸肼属于离子化合
2 6 4
物,易溶于水,溶液呈酸性,水解原理与(NH )SO 类似。
4 2 4
(5)将水合肼转移到烧杯中,滴加一定量浓硫酸,控制温度,得硫酸肼沉淀。洗涤硫酸
肼时用无水乙醇而不用水洗涤的原因是____。
(6)①写出硫酸肼第二步水解反应的离子方程式:____。
②硫酸肼水溶液中离子浓度关系表达正确的是____(填英文字母)。
A.c(SO )=c(N H )+c(N H )+c(N H·H O)
2 2 2 4 2
B.c(SO )>c([N H·H O]+)>c(H+)>c(OH-)
2 5 2
C.2c(NH )+c([N H·H O]+)=c(H+)+c(OH-)
2 2 5 2
D.c(SO )>c(N H )>c(H+)>c(OH-)
2
【答案】(1) 125或125.0 250mL容量瓶
(2)Cl +2OH-=Cl-+ClO-+H O
2 2
(3) 冷(冰)水浴 NH•H O+2NaClO=N ↑+3H O+2NaCl
2 4 2 2 2
(4)30%
(5)乙醇洗涤可降低硫酸肼的溶解,且乙醇易挥发可快速得到干燥固体等
(6) [N H·H O]++H O [N H·2H O]+H+或NH NH+H+ AD
2 5 2 2 2 4 2 2 2 4
【解析】(1)欲配制220mL6mol/L的盐酸,此过程所需玻璃仪器有:量筒、烧杯、玻璃
棒、胶头滴管、250 mL的容量瓶;
,则需要密度为1.2g/mL,质量
分数为36.5%的浓盐酸体积为125mL;
(2)氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,反应方程式为:Cl+2OH-=Cl-
2
+ClO-+H O;
2
(3)使用水浴容易控制温度,采用低温反应,降温的方式可采用冷水水浴;该气体在标
准状况下的密度为1.25g·L-1,M=1.25g·L-1×22.4L/mol=28g/mol,则气体为氮气,反应的
化学方程式为:NH•H O+2NaClO=N ↑+3H O+2NaCl;
2 4 2 2 2
(4)N H·H O+2I =N ↑+4HI+H O,n(N H·H O):n(I)=1:2,
2 4 2 2 2 2 2 4 2 2
试卷第18页,共17页,则馏分中水合肼(N HHO)的质量分数为:
2 4 2
;
(5)洗涤硫酸肼时用无水乙醇而不用水洗涤的原因是:乙醇洗涤可降低硫酸肼的溶解,
且乙醇易挥发可快速得到干燥固体等;
(6)①写出硫酸肼第二步水解反应的离子方程式:[N H·H O]++H O [N H·2H O]
2 5 2 2 2 4 2
+H+或NH NH+H+;
2 2 4
②硫酸肼水溶液中离子浓度关系表达正确的是
A.根据物料守恒c(SO )=c(N H )+c(N H )+c(N H·H O),A正确
2 2 2 4 2
B.水溶液中存在水的电离,c(SO )>c(H+)>c([N H·H O]+) >c(OH-),B错误;
2 5 2
C.根据电荷守恒2c(NH )+c([N H·H O]+)+c(H+)=c(OH-)+2 c(SO ),C错误;
2 2 5 2
D.硫酸肼中NH 水解呈酸性,故c(SO )>c(N H )>c(H+)>c(OH-),D正确;
2 2
故选AD。试卷第20页,共17页