文档内容
大题突破 4 物质结构与性质大题研究(选考)
1.(2022·吉林延边一模)铜是人类广泛使用的一种金属,含铜物质在生产、生活中有着广泛
应用。回答下列问题:
(1)铜锰氧化物(CuMn O)能在常温下催化氧化一氧化碳和甲醛(HCHO)。
2 4
①基态Cu原子的M层电子排布式为______________________________。
②CO和N 互为等电子体。标准状况下V L CO分子中π键数目为__________。
2
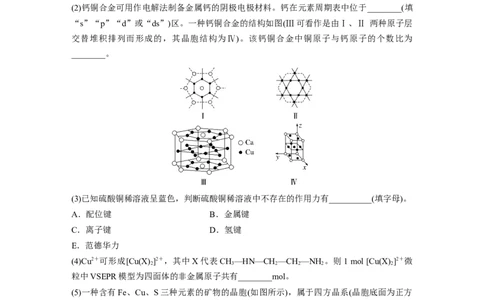
(2)钙铜合金可用作电解法制备金属钙的阴极电极材料。钙在元素周期表中位于________(填
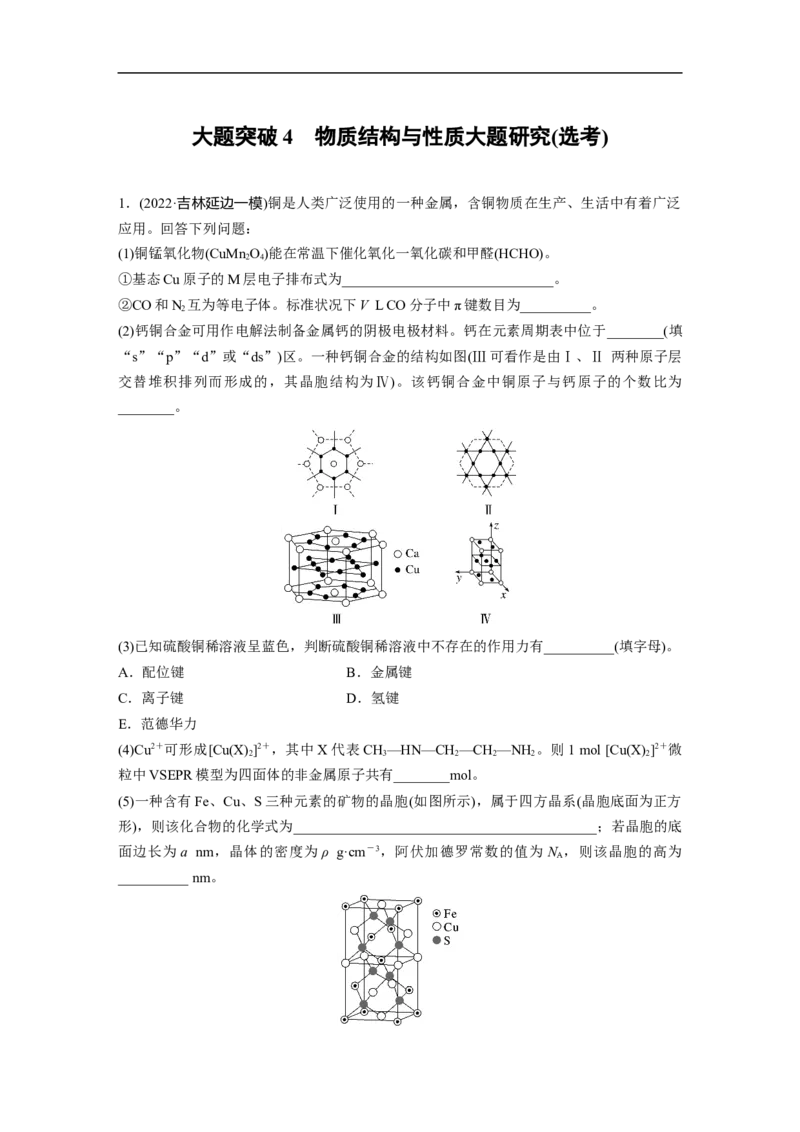
“s”“p”“d”或“ds”)区。一种钙铜合金的结构如图(Ⅲ可看作是由Ⅰ、Ⅱ 两种原子层
交替堆积排列而形成的,其晶胞结构为Ⅳ)。该钙铜合金中铜原子与钙原子的个数比为
________。
(3)已知硫酸铜稀溶液呈蓝色,判断硫酸铜稀溶液中不存在的作用力有__________(填字母)。
A.配位键 B.金属键
C.离子键 D.氢键
E.范德华力
(4)Cu2+可形成[Cu(X) ]2+,其中X代表CH—HN—CH —CH—NH 。则1 mol [Cu(X) ]2+微
2 3 2 2 2 2
粒中VSEPR模型为四面体的非金属原子共有________mol。
(5)一种含有Fe、Cu、S三种元素的矿物的晶胞(如图所示),属于四方晶系(晶胞底面为正方
形),则该化合物的化学式为___________________________________________;若晶胞的底
面边长为a nm,晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为 N ,则该晶胞的高为
A
__________ nm。2.(2022·江西上饶模拟预测)磷酸亚铁锂(LiFePO )电池是新能源汽车动力电池之一。
4
(1)写出基态Fe2+的核外电子排布式:________________________,请从原子结构角度解释
Fe能呈+2价的原因:_____________________________________________________。
(2)PO的立体构型为______________,由两种短周期同主族元素构成且与磷酸根离子互为等
电子体的粒子为______________,P的杂化轨道与O的2p轨道形成____________。
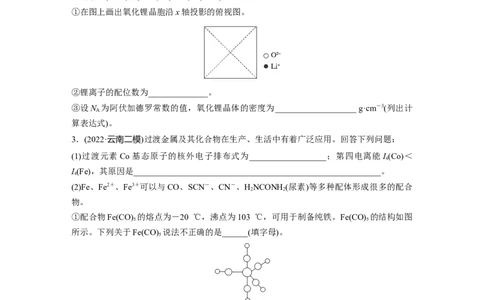
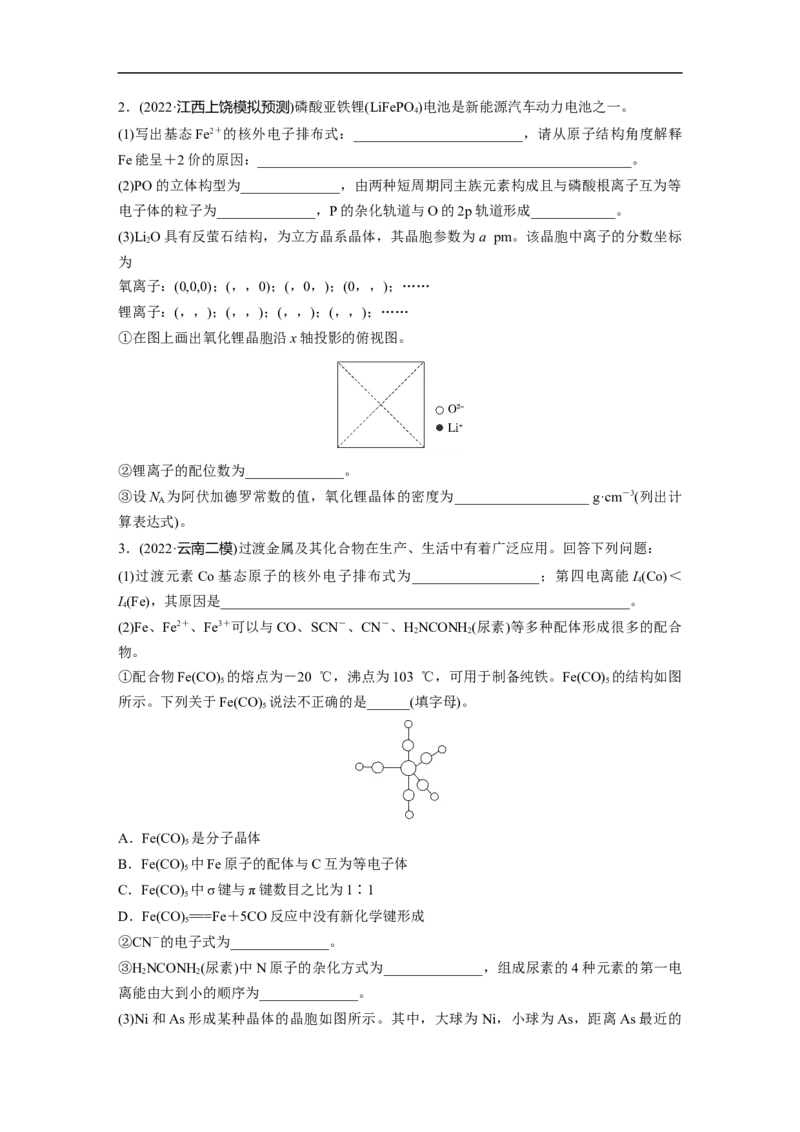
(3)LiO具有反萤石结构,为立方晶系晶体,其晶胞参数为 a pm。该晶胞中离子的分数坐标
2
为
氧离子:(0,0,0);(,,0);(,0,);(0,,);……
锂离子:(,,);(,,);(,,);(,,);……
①在图上画出氧化锂晶胞沿x轴投影的俯视图。
②锂离子的配位数为______________。
③设N 为阿伏加德罗常数的值,氧化锂晶体的密度为___________________ g·cm-3(列出计
A
算表达式)。
3.(2022·云南二模)过渡金属及其化合物在生产、生活中有着广泛应用。回答下列问题:
(1)过渡元素Co基态原子的核外电子排布式为__________________;第四电离能I(Co)<
4
I(Fe),其原因是__________________________________________________________。
4
(2)Fe、Fe2+、Fe3+可以与CO、SCN-、CN-、HNCONH(尿素)等多种配体形成很多的配合
2 2
物。
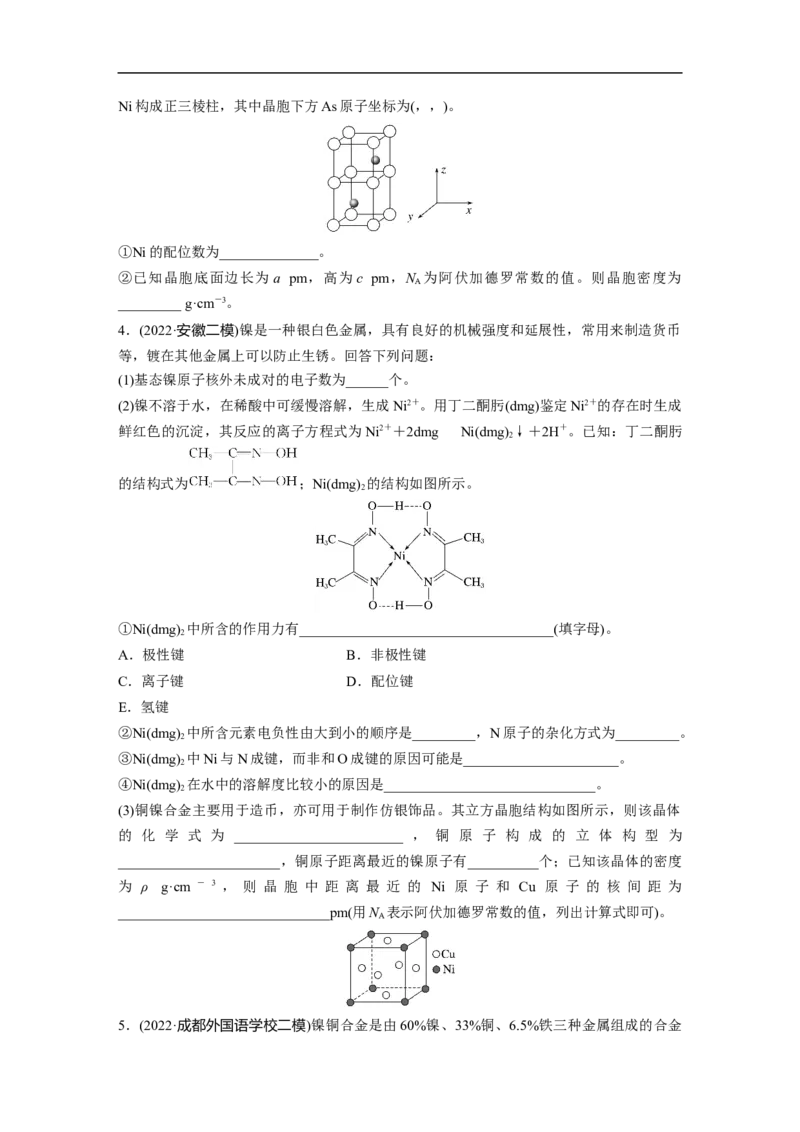
①配合物Fe(CO) 的熔点为-20 ℃,沸点为103 ℃,可用于制备纯铁。Fe(CO) 的结构如图
5 5
所示。下列关于Fe(CO) 说法不正确的是______(填字母)。
5
A.Fe(CO) 是分子晶体
5
B.Fe(CO) 中Fe原子的配体与C互为等电子体
5
C.Fe(CO) 中σ键与π键数目之比为1∶1
5
D.Fe(CO) ===Fe+5CO反应中没有新化学键形成
5
②CN-的电子式为______________。
③HNCONH(尿素)中N原子的杂化方式为______________,组成尿素的4种元素的第一电
2 2
离能由大到小的顺序为______________。
(3)Ni和As形成某种晶体的晶胞如图所示。其中,大球为 Ni,小球为As,距离As最近的Ni构成正三棱柱,其中晶胞下方As原子坐标为(,,)。
①Ni的配位数为______________。
②已知晶胞底面边长为 a pm,高为 c pm,N 为阿伏加德罗常数的值。则晶胞密度为
A
_________ g·cm-3。
4.(2022·安徽二模)镍是一种银白色金属,具有良好的机械强度和延展性,常用来制造货币
等,镀在其他金属上可以防止生锈。回答下列问题:
(1)基态镍原子核外未成对的电子数为______个。
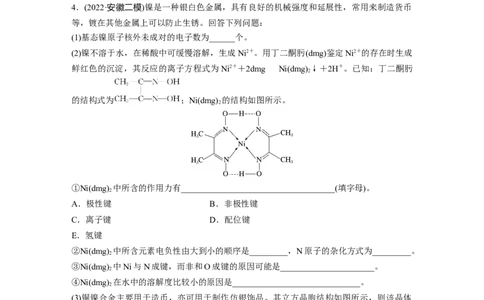
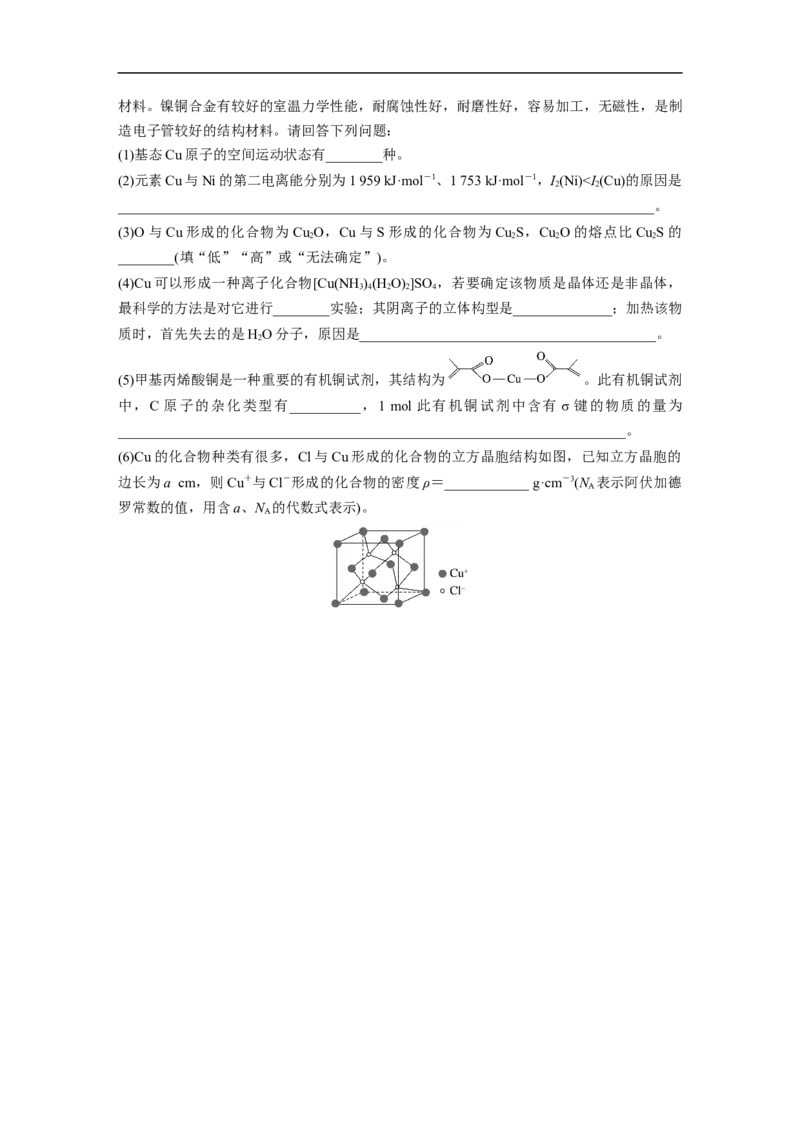
(2)镍不溶于水,在稀酸中可缓慢溶解,生成Ni2+。用丁二酮肟(dmg)鉴定Ni2+的存在时生成
鲜红色的沉淀,其反应的离子方程式为Ni2++2dmgNi(dmg) ↓+2H+。已知:丁二酮肟
2
的结构式为 ;Ni(dmg) 的结构如图所示。
2
①Ni(dmg) 中所含的作用力有____________________________________(填字母)。
2
A.极性键 B.非极性键
C.离子键 D.配位键
E.氢键
②Ni(dmg) 中所含元素电负性由大到小的顺序是_________,N原子的杂化方式为_________。
2
③Ni(dmg) 中Ni与N成键,而非和O成键的原因可能是______________________。
2
④Ni(dmg) 在水中的溶解度比较小的原因是______________________________。
2
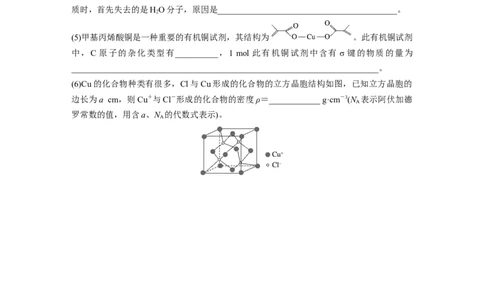
(3)铜镍合金主要用于造币,亦可用于制作仿银饰品。其立方晶胞结构如图所示,则该晶体
的 化 学 式 为 ________________________ , 铜 原 子 构 成 的 立 体 构 型 为
_______________________,铜原子距离最近的镍原子有__________个;已知该晶体的密度
为 ρ g·cm - 3 , 则 晶 胞 中 距 离 最 近 的 Ni 原 子 和 Cu 原 子 的 核 间 距 为
______________________________pm(用N 表示阿伏加德罗常数的值,列出计算式即可)。
A
5.(2022·成都外国语学校二模)镍铜合金是由60%镍、33%铜、6.5%铁三种金属组成的合金材料。镍铜合金有较好的室温力学性能,耐腐蚀性好,耐磨性好,容易加工,无磁性,是制
造电子管较好的结构材料。请回答下列问题:
(1)基态Cu原子的空间运动状态有________种。
(2)元素Cu与Ni的第二电离能分别为1 959 kJ·mol-1、1 753 kJ·mol-1,I(Ni)