文档内容
第 02 讲 物质的量浓度与溶液的配制
(模拟精练+真题演练)
1.(2021·广东·模拟预测)配制500mL的0.100mol·L-1NaCl溶液,需要用到的仪器是
A. B. C. D.
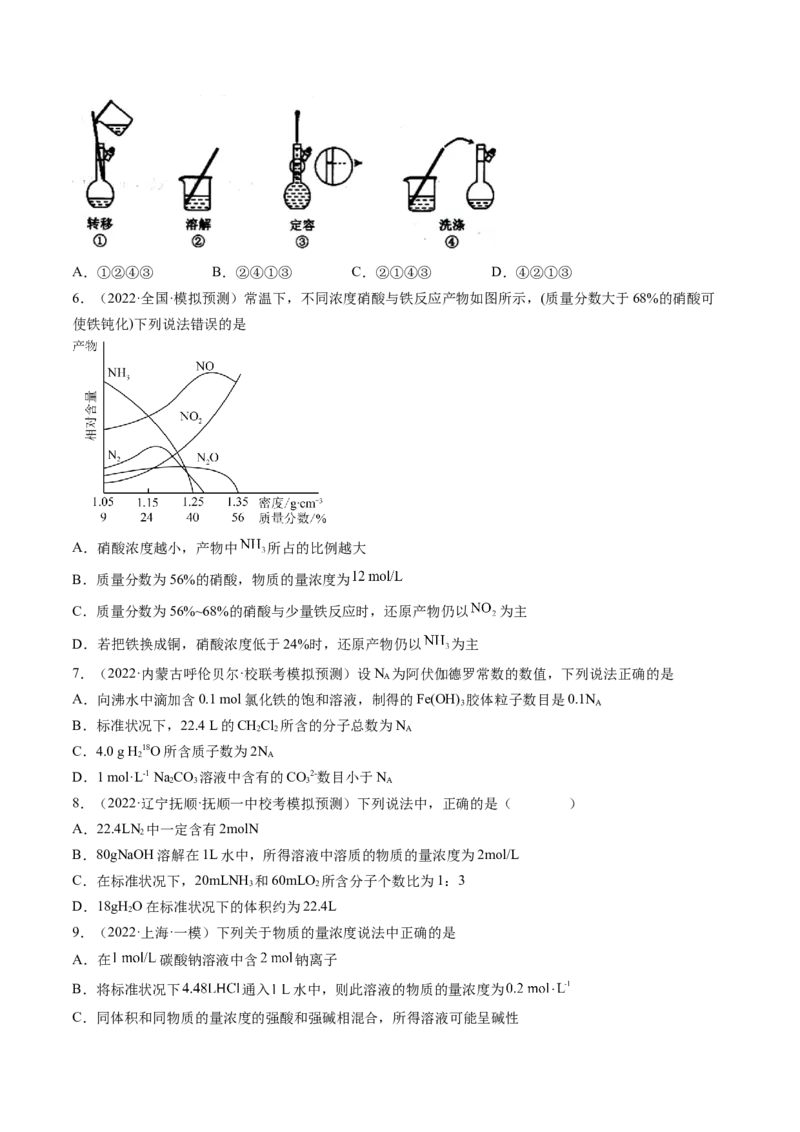
2.(2021·广东·模拟预测)配制450mL0.100mol•L-1的NaCl溶液,部分实验操作示意图如图:
下列说法正确的是
A.容量瓶需用蒸馏水洗涤、干燥后才可使用
B.定容时,仰视容量瓶的刻度线,使配得的NaCl溶液浓度偏低
C.上述实验操作步骤的正确顺序为①②④①③
D.实验中需用到的仪器有:天平、450mL容量瓶、烧杯、玻璃棒、胶头滴管等
3.(2022·上海·模拟预测)将V L浓度为0.3mol/L的盐酸浓度扩大一倍,采取的措施合理的是
A.将溶液加热浓缩至原来体积的一半
B.通入标准状况下的HCl气体6.72L
C.加入3mol/L的盐酸0.2V L,再稀释至1.5V L
D.加入等体积0.9mol/L的盐酸,混合均匀
4.(2021·浙江绍兴·校考模拟预测)配制一定物质的量浓度的溶液的实验中可不选用的仪器是(
)
A. B. C. D.
5.(2021·河北石家庄·石家庄二中校考模拟预测)下图是配制100mL0.5 NaCl溶液的部分实验操
作,在配制过程中的正确实验顺序是A.①②④③ B.②④①③ C.②①④③ D.④②①③
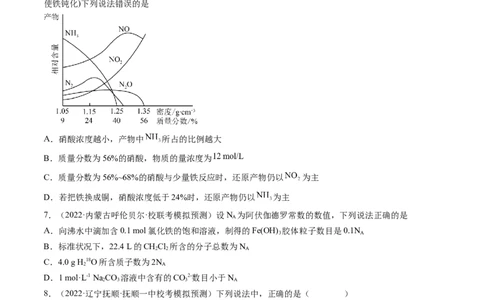
6.(2022·全国·模拟预测)常温下,不同浓度硝酸与铁反应产物如图所示,(质量分数大于68%的硝酸可
使铁钝化)下列说法错误的是
A.硝酸浓度越小,产物中 所占的比例越大
B.质量分数为56%的硝酸,物质的量浓度为
C.质量分数为56%~68%的硝酸与少量铁反应时,还原产物仍以 为主
D.若把铁换成铜,硝酸浓度低于24%时,还原产物仍以 为主
7.(2022·内蒙古呼伦贝尔·校联考模拟预测)设N 为阿伏伽德罗常数的数值,下列说法正确的是
A
A.向沸水中滴加含0.1 mol氯化铁的饱和溶液,制得的Fe(OH) 胶体粒子数目是0.1N
3 A
B.标准状况下,22.4 L的CHCl 所含的分子总数为N
2 2 A
C.4.0 g H 18O所含质子数为2N
2 A
D.1 mol·L-1 NaCO 溶液中含有的CO2-数目小于N
2 3 3 A
8.(2022·辽宁抚顺·抚顺一中校考模拟预测)下列说法中,正确的是( )
A.22.4LN 中一定含有2molN
2
B.80gNaOH溶解在1L水中,所得溶液中溶质的物质的量浓度为2mol/L
C.在标准状况下,20mLNH 和60mLO 所含分子个数比为1:3
3 2
D.18gHO在标准状况下的体积约为22.4L
2
9.(2022·上海·一模)下列关于物质的量浓度说法中正确的是
A.在 碳酸钠溶液中含 钠离子
B.将标准状况下 通入 水中,则此溶液的物质的量浓度为
C.同体积和同物质的量浓度的强酸和强碱相混合,所得溶液可能呈碱性D.饱和溶液的物质的量浓度一定大于不饱和溶液的物质的量浓度
10.(2020·浙江·统考模拟预测)用密度为1.84g•mL-1、质量分数为 98% 的浓硫酸配制 180mL 2mol•L-1稀
硫酸。下列各步骤中操作正确的是
A.计算、量取:用 20 mL 量筒量取 19.6 mL 浓硫酸
B.溶解、稀释:将浓硫酸倒入烧杯 ,再加入 80 mL 左右的蒸馏水 ,搅拌
C.转移、洗涤:将溶液转移到容量瓶中,用蒸馏水洗涤烧杯和玻璃棒,洗涤液转入容量瓶重复2~3次
D.定容、摇匀:加水至凹液面最低处与刻度线相切,摇匀,最后在容量瓶上贴上标签
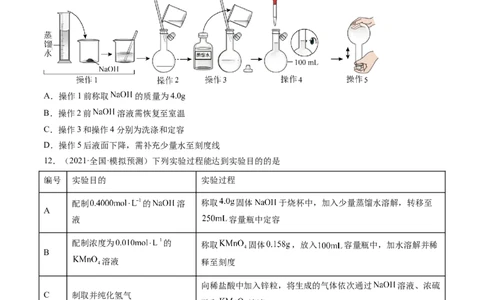
11.(2021·北京东城·统考二模)配制 溶液的操作如下所示。下列说法不正确的是
A.操作1前称取 的质量为4.0g
B.操作2前 溶液需恢复至室温
C.操作3和操作4分别为洗涤和定容
D.操作5后液面下降,需补充少量水至刻度线
12.(2021·全国·模拟预测)下列实验过程能达到实验目的的是
编号 实验目的 实验过程
配制 的 溶 称取 固体 于烧杯中,加入少量蒸馏水溶解,转移至
A
液 容量瓶中定容
配制浓度为 的 称取 固体 ,放入 容量瓶中,加水溶解并稀
B
溶液 释至刻度
向稀盐酸中加入锌粒,将生成的气体依次通过 溶液、浓硫
C 制取并纯化氢气
酸和 溶液
将浓硫酸慢慢加入水中,并不断搅拌使产生的热量迅速扩散,以
D 配制稀硫酸
防液体溅出
13.(2023·上海杨浦·统考二模)室温下,甲同学配制5%的 溶液100g,乙同学配制 的
溶液100mL( 的溶解度为 水),下列说法正确的是
A.所需溶质的质量相同 B.所需仪器均包括100mL容量瓶
C.所配溶液均为不饱和溶液 D.所配溶液质量相同
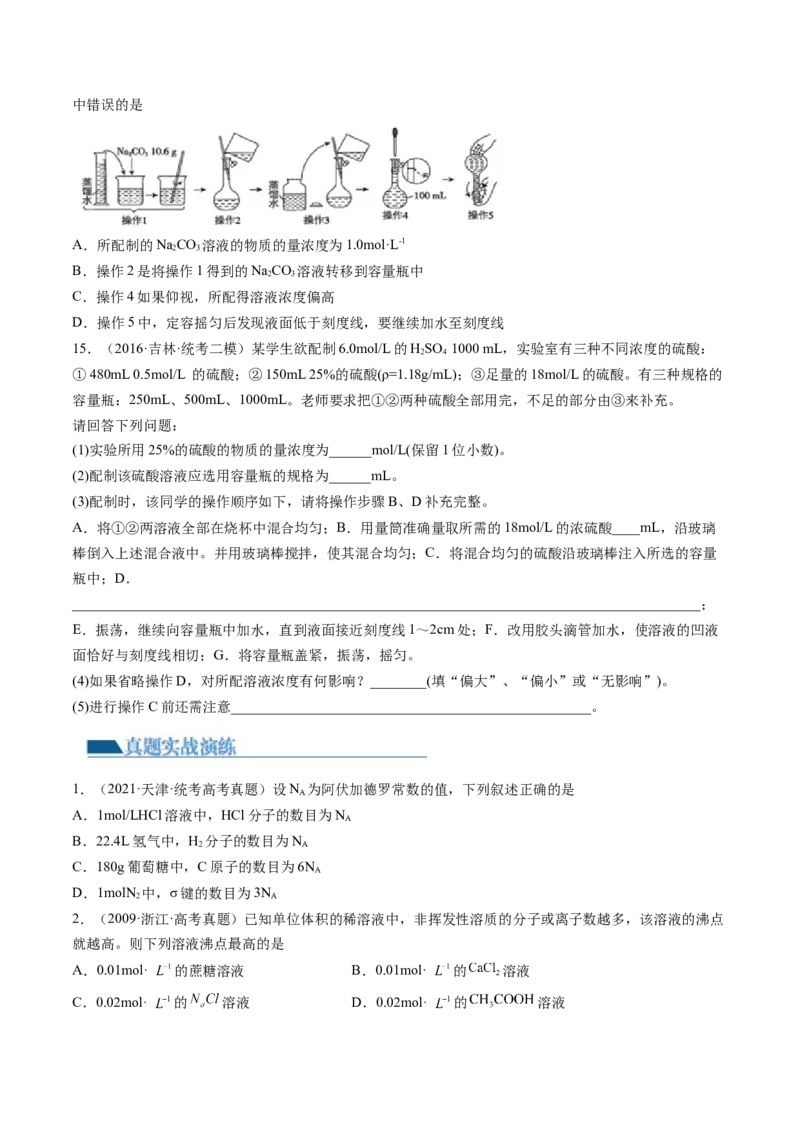
14.(2022·山东威海·校考模拟预测)(双选)如图所示是配制一定物质的量浓度溶液的过程。下列说法中错误的是
A.所配制的NaCO 溶液的物质的量浓度为1.0mol·L-1
2 3
B.操作2是将操作1得到的NaCO 溶液转移到容量瓶中
2 3
C.操作4如果仰视,所配得溶液浓度偏高
D.操作5中,定容摇匀后发现液面低于刻度线,要继续加水至刻度线
15.(2016·吉林·统考二模)某学生欲配制6.0mol/L的HSO 1000 mL,实验室有三种不同浓度的硫酸:
2 4
①480mL 0.5mol/L 的硫酸;②150mL 25%的硫酸(ρ=1.18g/mL);③足量的18mol/L的硫酸。有三种规格的
容量瓶:250mL、500mL、1000mL。老师要求把①②两种硫酸全部用完,不足的部分由③来补充。
请回答下列问题:
(1)实验所用25%的硫酸的物质的量浓度为______mol/L(保留1位小数)。
(2)配制该硫酸溶液应选用容量瓶的规格为______mL。
(3)配制时,该同学的操作顺序如下,请将操作步骤B、D补充完整。
A.将①②两溶液全部在烧杯中混合均匀;B.用量筒准确量取所需的18mol/L的浓硫酸____mL,沿玻璃
棒倒入上述混合液中。并用玻璃棒搅拌,使其混合均匀;C.将混合均匀的硫酸沿玻璃棒注入所选的容量
瓶中;D.
_________________________________________________________________________________________;
E.振荡,继续向容量瓶中加水,直到液面接近刻度线1~2cm处;F.改用胶头滴管加水,使溶液的凹液
面恰好与刻度线相切;G.将容量瓶盖紧,振荡,摇匀。
(4)如果省略操作D,对所配溶液浓度有何影响?________(填“偏大”、“偏小”或“无影响”)。
(5)进行操作C前还需注意___________________________________________________。
1.(2021·天津·统考高考真题)设N 为阿伏加德罗常数的值,下列叙述正确的是
A
A.1mol/LHCl溶液中,HCl分子的数目为N
A
B.22.4L氢气中,H 分子的数目为N
2 A
C.180g葡萄糖中,C原子的数目为6N
A
D.1molN 中,σ键的数目为3N
2 A
2.(2009·浙江·高考真题)已知单位体积的稀溶液中,非挥发性溶质的分子或离子数越多,该溶液的沸点
就越高。则下列溶液沸点最高的是
A.0.01mol· 的蔗糖溶液 B.0.01mol· 的 溶液
C.0.02mol· 的 溶液 D.0.02mol· 的 溶液3.(2020·天津·高考真题)为测定CuSO 溶液的浓度,甲、乙两同学设计了两个方案。回答下列问题:
4
Ⅰ.甲方案
实验原理:
实验步骤:
(1)判断 沉淀完全的操作为____________。
(2)步骤②判断沉淀是否洗净所选用的试剂为_____________。
(3)步骤③灼烧时盛装样品的仪器名称为__________。
(4)固体质量为wg,则c(CuSO )=________mol‧L-1。
4
(5)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得c(CuSO )_________(填“偏高”、“偏低”或“无影
4
响”)。
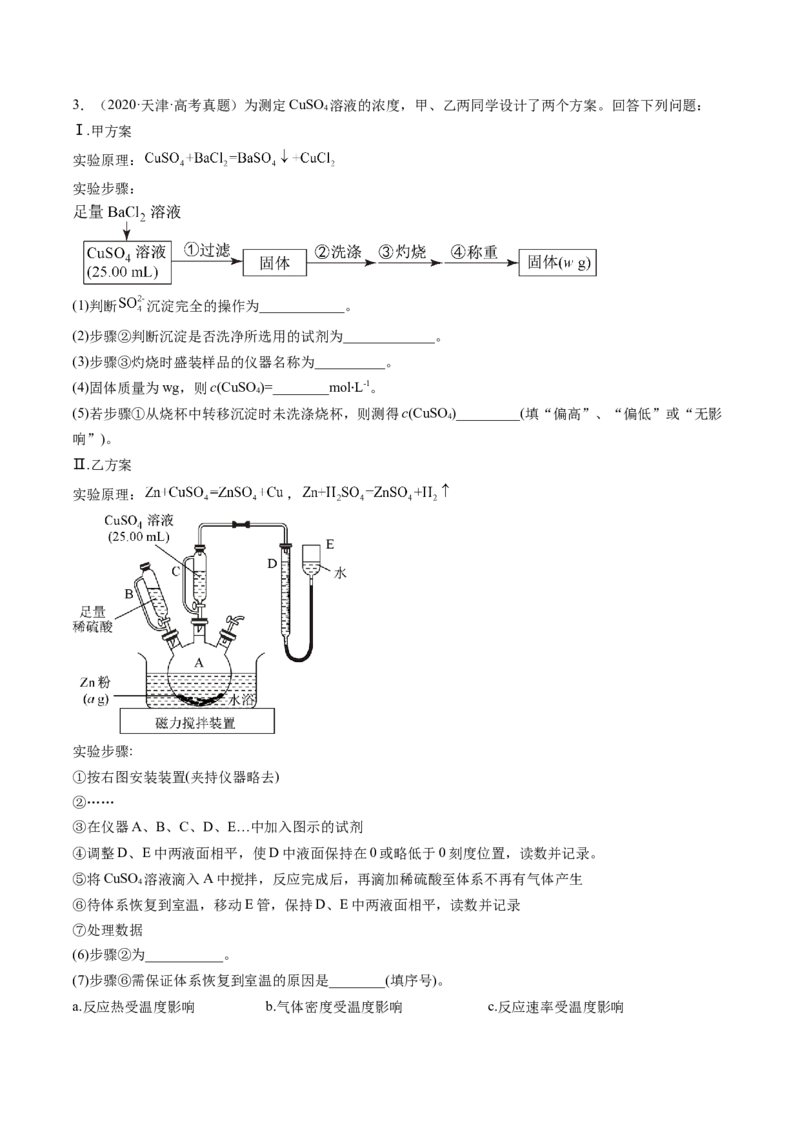
Ⅱ.乙方案
实验原理: ,
实验步骤:
①按右图安装装置(夹持仪器略去)
②……
③在仪器A、B、C、D、E…中加入图示的试剂
④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录。
⑤将CuSO 溶液滴入A中搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生
4
⑥待体系恢复到室温,移动E管,保持D、E中两液面相平,读数并记录
⑦处理数据
(6)步骤②为___________。
(7)步骤⑥需保证体系恢复到室温的原因是________(填序号)。
a.反应热受温度影响 b.气体密度受温度影响 c.反应速率受温度影响(8)Zn粉质量为ag,若测得H 体积为bmL,已知实验条件下 ,则c(CuSO )______mol‧L-1(列
2 4
出计算表达式)。
(9)若步骤⑥E管液面高于D管,未调液面即读数,则测得c(CuSO )________(填“偏高”、“偏低”或
4
“无影响”)。
(10)是否能用同样的装置和方法测定MgSO 溶液的浓度:_________(填“是”或“否”)。
4
4.(2017·上海·统考高考真题)6克冰醋酸完全溶于水配成500毫升溶液,用此醋酸溶液滴定20毫升某一
未知浓度的氢氧化钠溶液,共消耗这种醋酸溶液30毫升。求:
(1)醋酸溶液的物质的量的浓度_________。
(2)未知氢氧化钠溶液的物质的量的浓度________________。
5.(2007·上海·高考真题)一定量的氢气在氯气中燃烧,所得混合物用100mL 3.00mol/L的NaOH溶液
(密度为1.12g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol。
(1)原NaOH溶液的质量分数为___________
(2)所得溶液中Cl-的物质的量为_______mol
(3)所用氯气和参加反应的氢气的物质的量之比n(Cl ):n(H )=_____________。
2 2