文档内容
第 10 讲 铁及其重要化合物
目录
考情分析
考点二 铁及其化合物的转化及应用
网络构建
【夯基·必备基础知识梳理】
考点一 铁及其氧化物 知识点1 亚铁盐的性质及应用
【夯基·必备基础知识梳理】 知识点2 铁盐的性质及应用
知识点1 铁 知识点3 Fe2+和Fe3+的检验
知识点2 铁的重要化合物 知识点4 “铁三角”的转化关系及其应用
【提升·必考题型归纳】 【提升·必考题型归纳】
考向1 考查铁及其化合物的性质与应用 考向1 考查Fe2+、Fe3+ 的性质及其检验
考向2 考查氢氧化亚铁的制备 考向2 考查“铁三角”的转化及应用
考向3 考查铁及其化合物的有关计算 考向3 实验探究铁及其重要化合物的转化关
系
真题感悟
考点要求 考题统计 考情分析
2023浙江1月卷4题,2分 分析近三年高考试题,从分值来看,铁所占的比重最
铁及其化合物的 2022广东卷6题,3分 大,除铁是重要的金属元素外,还取决于铁元素与生产
性质及应用 2021河北卷1题,3分 生活的紧密联系,Fe、Fe2+、Fe3+之间的转化,以及所
2023湖南卷7题,3分 承载的氧化还原反应等重要知识点。考查内容主要集中
Fe2+、Fe3+的检
在“铁三角”,Fe与酸的反应,铁的变价、Fe(OH) 和
2022广东卷11题,3分 2
验
Fe(OH) 的性质等。考查内容能在多种题型中出现,选
2021湖南卷3题,3分 3
择、简答、实验、推断、计算都有。
2023浙江1月卷16题,2
铁及其化合物的 预测新的一年高考可能会在选择题中考查铁及其化合物
分
转化 的性质和应用与转化,在化工流程题或综合实验题中考
2021广东卷10题,2分
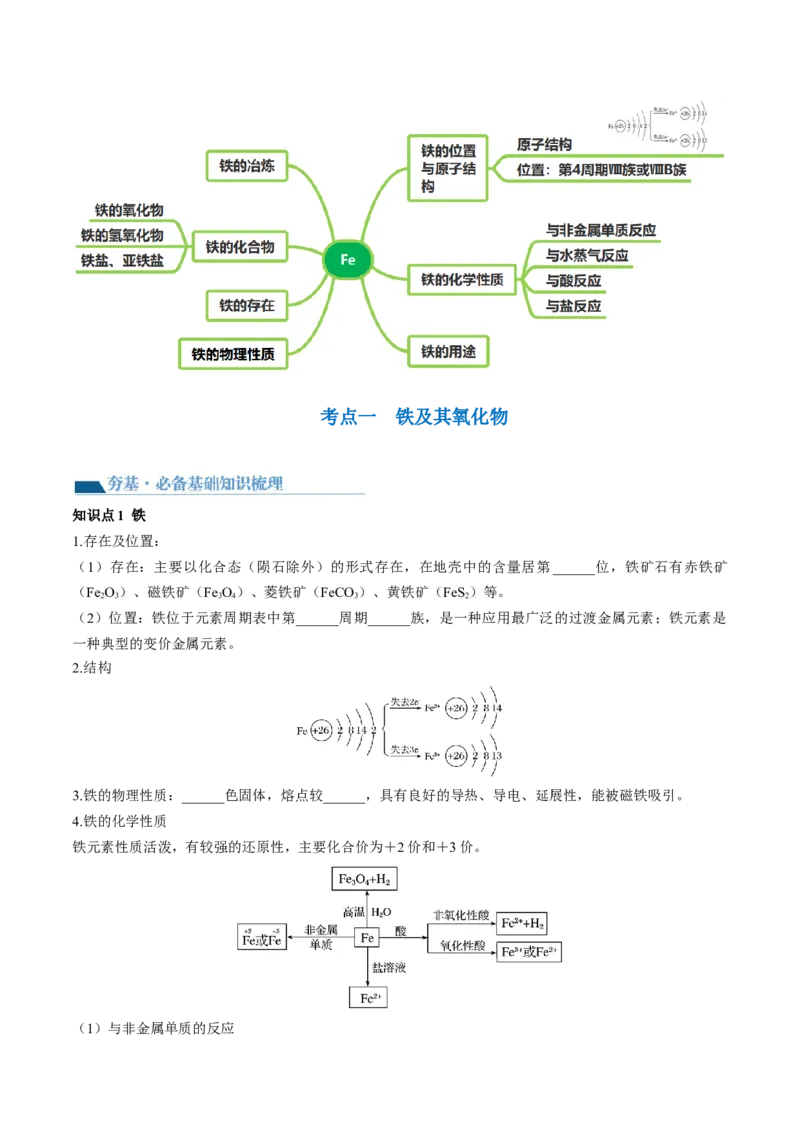
查铁及其化合物的转化。考点一 铁及其氧化物
知识点1 铁
1.存在及位置:
(1)存在:主要以化合态(陨石除外)的形式存在,在地壳中的含量居第______位,铁矿石有赤铁矿
(Fe O)、磁铁矿(Fe O)、菱铁矿(FeCO)、黄铁矿(FeS)等。
2 3 3 4 3 2
(2)位置:铁位于元素周期表中第______周期______族,是一种应用最广泛的过渡金属元素;铁元素是
一种典型的变价金属元素。
2.结构
3.铁的物理性质:______色固体,熔点较______,具有良好的导热、导电、延展性,能被磁铁吸引。
4.铁的化学性质
铁元素性质活泼,有较强的还原性,主要化合价为+2价和+3价。
(1)与非金属单质的反应①与O 的反应:
2
常温:铁在______的空气中被腐蚀生成铁锈,其主要成分为______。
点燃:3Fe+2O=====Fe O。
2 3 4
②与Cl 的反应:2Fe+3Cl=====2FeCl 。
2 2 3
③与S的反应:Fe+S FeS。
④与I 的反应:Fe+I FeI
2 2 2
(2)与水的反应
常温下铁与水不反应,在高温条件下与水蒸气反应:3Fe+4HO(g)=====Fe O+4H。
2 3 4 2
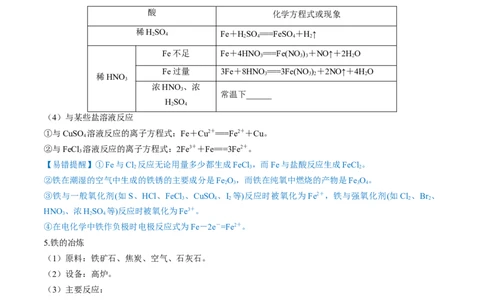
(3)与酸的反应
酸 化学方程式或现象
稀H 2 SO 4 Fe+H 2 SO 4 ===FeSO 4 +H 2 ↑
Fe不足 Fe+4HNO===Fe(NO)+NO↑+2HO
3 3 3 2
Fe过量 3Fe+8HNO===3Fe(NO)+2NO↑+4HO
稀HNO 3 3 2 2
3
浓HNO、浓
3
常温下______
HSO
2 4
(4)与某些盐溶液反应
①与CuSO 溶液反应的离子方程式:Fe+Cu2+===Fe2++Cu。
4
②与FeCl 溶液反应的离子方程式:2Fe3++Fe===3Fe2+。
3
【易错提醒】①Fe与Cl 反应无论用量多少都生成FeCl ,而Fe与盐酸反应生成FeCl 。
2 3 2
②铁在潮湿的空气中生成的铁锈的主要成分是Fe O,而铁在纯氧中燃烧的产物是Fe O。
2 3 3 4
③铁与一般氧化剂(如S、HCl、FeCl 、CuSO 、I 等)反应时被氧化为Fe2+,铁与强氧化剂(如Cl 、Br 、
3 4 2 2 2
HNO、浓HSO 等)反应时被氧化为Fe3+。
3 2 4
④在电化学中铁作负极时电极反应式为Fe-2e-=Fe2+。
5.铁的冶炼
(1)原料:铁矿石、焦炭、空气、石灰石。
(2)设备:高炉。
(3)主要反应:
①还原剂的生成:C+O=====CO,CO+C=====2CO;
2 2 2
②铁的生成:Fe O+3CO=====2Fe+3CO。
2 3 2
知识点2 铁的重要化合物
1.铁的氧化物
1)铁的氧化物物理性质
化学式 FeO Fe O Fe O
2 3 3 4
俗称 ______ ____________
色态 黑色粉末 红棕色粉末 黑色晶体溶解性 难溶于水 难溶于水 难溶于水
铁的价态 ______价 ______价 +2价,+3价
2)铁的氧化物化学性质
①FeO、Fe O、Fe O 分别与盐酸反应的离子方程式为
2 3 3 4
FeO+2H+= Fe2++HO,
2
Fe O+6H+= 2Fe3++3HO,
2 3 2
Fe O+8H+= 2Fe3++Fe2++4HO。
3 4 2
②Fe O 分别与HNO 和HI反应的离子方程式为
3 4 3
3Fe O+28H++NO -=9Fe3++NO↑+14HO;
3 4 3 2
Fe O+8H++2I-=3Fe2++I+4HO。
3 4 2 2
③FeO与HNO 反应时,除考虑与H+的反应外,还要考虑Fe2+被HNO 氧化成Fe3+。
3 3
3FeO+6H++NO -=3Fe3++NO↑+3HO;
3 2
④Fe O 与HI反应时,除考虑与H+的反应外,还要考虑Fe3+被I-还原成Fe2+
2 3
Fe O+6H++2I-=2Fe2++I+3HO。
2 3 2 2
⑤高温时,都能被C、CO、Al等还原剂还原,生成单质铁
2.铁的氢氧化物
1)Fe(OH) 是______色______状物,易被空气中的氧气氧化生成Fe(OH) ,颜色由白色变为______色,最后
2 3
变为______色,方程式为4Fe(OH) +O+2HO===4Fe(OH) 。
2 2 2 3
2)Fe(OH) 是______色、难溶于水的固体,在空气中久置会部分失水生成铁锈(Fe O·xHO),受热易分解,
3 2 3 2
方程式为 2Fe(OH) Fe O +3HO;制取Fe(OH) 用可溶性铁盐与碱反应,离子方程式:Fe3++3OH-
3 2 3 2 3
===Fe(OH) ↓。
3
3)二者之间的关系:在空气中,Fe(OH) 能够非常迅速地被氧气氧化成Fe(OH) ,现象是白色絮状沉淀迅速
2 3
变成灰绿色,最后变成红褐色,化学方程式为4Fe(OH) +O+2HO===4Fe(OH) 。
2 2 2 3
【易错提醒】①Fe(OH) 与硝酸反应不是发生中和反应生成盐和水,而是发生氧化还原反应3Fe(OH) +
2 2
10HNO=3Fe(NO)+NO↑+8HO。
3 3 3 2
②Fe(OH) 与氢碘酸(HI)反应不是发生中和反应生成盐和水,而是发生氧化还原反应2Fe(OH) +6HI=2FeI
3 3 2
+I+6HO。
2 2
4)制法
(1)可溶性亚铁盐与强碱或氨水反应:Fe2++2OH-===Fe(OH) ↓或Fe2++2NH ·HO===Fe(OH) ↓+2NH+。
2 3 2 2 4
注意:空气中,Fe(OH) 能够非常迅速地被氧气氧化成Fe(OH) ,防止Fe(OH) 氧化的方法:
2 3 2
A.将配制溶液的蒸馏水煮沸,驱除溶液中的氧气。
B.将盛有NaOH溶液的胶头滴管尖端插入盛有亚铁盐溶液的试管底部,并慢慢挤出NaOH溶液。
C.在亚铁盐溶液上面充入保护气,如H、N、稀有气体等。
2 2
D.在亚铁盐溶液上面加保护层,如苯、植物油等。
E.常见的制备Fe(OH) 的装置:
2说明:①②原理一样,都是先用氢气将装置中的空气排尽,并使生成的 Fe(OH) 处在氢气的保护中;③中
2
液面加苯阻止了空气进入;④中阳极为铁,阴极为石墨,利用电解实验可以制得纯净的Fe(OH) 白色沉淀。
2
(2)可溶性铁盐与强碱或氨水反应:Fe3++3OH-===Fe(OH) ↓或Fe3++3NH ·HO===Fe(OH) ↓+3NH+。
3 3 2 3 4
考向1 考查铁及其重要化合物的性质与应用
例1.(2023·江苏徐州·统考三模)下列有关铁及其化合物的性质与用途具有对应关系的是
A. 能与盐酸反应,可用于制作红色颜料
B. 具有氧化性,可用于除去水中悬浮杂质
C.铁粉具有还原性,可用于食品袋中的抗氧化剂
D.FeS难溶于水,可用于除去废水中的
【变式训练1】(2023·广东汕头·统考二模)铁及其化合物在生活中应用广泛,下列有关离子方程式书写正
确的是
A.将铁片投入到稀硝酸中:
B.向 溶液中通入少量 :
C.用铁氰化钾溶液检验 :
D.往 溶液中加入过量 粉:
【变式训练2】(2023·上海黄浦·统考二模)把铁条放入盛有过量稀硫酸的试管中,下列改变不能加快氢气
产生速率的是
A.改铁条为镁条 B.滴加少量CuSO 溶液
4
C.改稀硫酸为98%的硫酸 D.升高溶液的温度
考向2 考查氢氧化亚铁的制备
例2.(2022秋·湖南邵阳·高三湖南省邵东市第一中学校考)某化学兴趣小组利用药品:铁粉、稀硫酸、
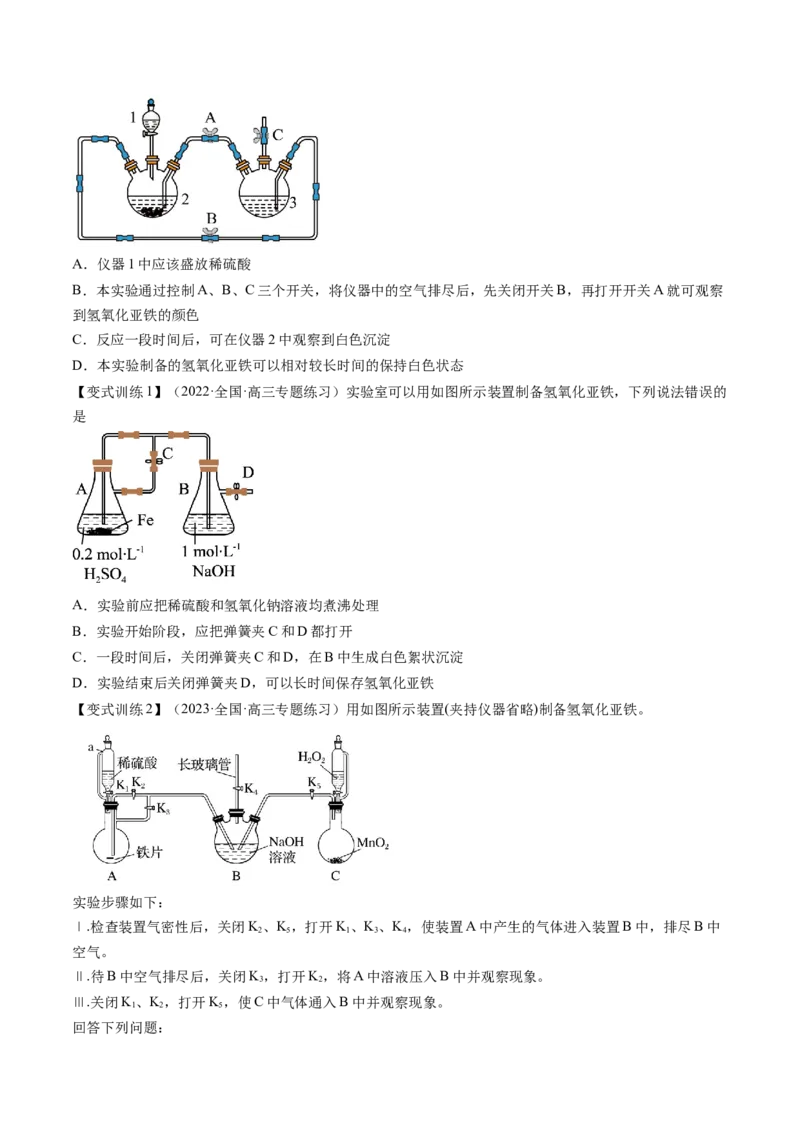
氢氧化钠溶液,用下图装置制备氢氧化亚铁并观察其颜色。下列有关说法不正确的是。A.仪器1中应该盛放稀硫酸
B.本实验通过控制A、B、C三个开关,将仪器中的空气排尽后,先关闭开关B,再打开开关A就可观察
到氢氧化亚铁的颜色
C.反应一段时间后,可在仪器2中观察到白色沉淀
D.本实验制备的氢氧化亚铁可以相对较长时间的保持白色状态
【变式训练1】(2022·全国·高三专题练习)实验室可以用如图所示装置制备氢氧化亚铁,下列说法错误的
是
A.实验前应把稀硫酸和氢氧化钠溶液均煮沸处理
B.实验开始阶段,应把弹簧夹C和D都打开
C.一段时间后,关闭弹簧夹C和D,在B中生成白色絮状沉淀
D.实验结束后关闭弹簧夹D,可以长时间保存氢氧化亚铁
【变式训练2】(2023·全国·高三专题练习)用如图所示装置(夹持仪器省略)制备氢氧化亚铁。
实验步骤如下:
Ⅰ.检查装置气密性后,关闭K、K,打开K、K、K,使装置A中产生的气体进入装置B中,排尽B中
2 5 1 3 4
空气。
Ⅱ.待B中空气排尽后,关闭K,打开K,将A中溶液压入B中并观察现象。
3 2
Ⅲ.关闭K、K,打开K,使C中气体通入B中并观察现象。
1 2 5
回答下列问题:(1)仪器a的名称是_______,B中长玻璃管的作用是_______。
(2)装置A中金属离子的检验方法是_______。
(3)步骤 Ⅲ 装置B中的现象是_______,其发生反应的化学方程式为_______。
考向3 考查铁及其化合物的有关计算
例3.(2023·山东烟台·校联考模拟预测)实验室对某铁的氧化物(Fe O)进行如下实验。下列说法错误的是
x
A.
B.溶液A为 和 混合溶液
C.反应②生成标准状况下1.12 L
D.Zn至少参加了3个氧化还原反应
【变式训练1】(2023·全国·模拟预测)盐X由三种常见元素组成,某科学兴小组称取 盐X进行实验,
数据和现象如下:
已知:①气体B为两种气体的混合物,能被水完全吸收。
②取D溶液 ,用 的 溶液滴定,消耗 溶液 。
下列说法错误的是
A.试剂Y可能为 溶液
B.盐X的化学式为
C.用 的 溶液滴定溶液D时可用酚酞作指示剂
D.若在X的稀溶液中通入足量 气体,发生反应的离子方程式为:
【变式训练2】(2022·浙江舟山·浙江省普陀中学校考模拟预测)取48.0gFe O,一定温度下加热,残留固
2 3
体47.36g。将该剩余固体溶于足量盐酸,此过程没有气体产生;所得溶液中再加入足量KI溶液。请计算:
(1)生成I 的物质的量_____。
2
(2)若分解产物为Fe O,求Fe O 的分解率_____。
3 4 2 3考点二 铁及其化合物的转化及应用
知识点1 亚铁盐的性质及应用
1.Fe2+的氧化性和还原性
①含有Fe2+的溶液呈______色,Fe2+处于铁的中间价态,既有氧化性,又有还原性,其中以还原性为主,
如:遇Br 、Cl、HO、NO(H+)等均表现为还原性。
2 2 2 2
②Fe2+的酸性溶液与HO 反应的离子方程式:2Fe2++HO+2H+===2Fe3++2HO。
2 2 2 2 2
③向FeSO 溶液中滴加酸性KMnO 溶液,溶液褪色。反应的离子方程式:MnO+5Fe2++8H+===5Fe3++
4 4
Mn2++4HO。
2
2.可水解
Fe(OH) 是弱碱,含Fe2+的盐(如硫酸亚铁)溶液呈______性。配制硫酸亚铁溶液时常加少量硫酸抑制Fe2+的
2
______,加少量______防止Fe2+被氧化。
知识点2 铁盐的性质及应用
1.氧化性:含有Fe3+的溶液呈棕黄色,Fe3+处于铁的高价态,遇Fe、Cu、HI、HS、SO等均表现为氧化性。
2
①Fe3+与S2-、I-、HS-、SO等具有较强还原性的离子不能大量共存。
②Fe3+可腐蚀印刷电路板上的铜箔,反应的离子方程式为2Fe3++Cu===Cu2++2Fe2+。
2.易水解:Fe(OH) 是很弱的碱,且溶度积很小,因而Fe3+极易水解,只能存在于酸性较强的溶液中。
3
①利用Fe3+易水解的性质,实验室可用FeCl 滴入沸水中制取氢氧化铁胶体,反应的化学方程式:FeCl +
3 3
3HO Fe(OH) (胶体)+3HCl。
2 3
②利用Fe3+易水解的性质,工业上常用调节pH方法除去溶液中的铁离子。
③利用Fe3+易水解的性质,实验室配制氯化铁溶液,通常将氯化铁固体先溶于较浓的盐酸中,然后再稀释
至所需浓度。
④Fe3+与HCO、[Al(OH) ]-、CO、ClO-等水解呈碱性的离子不能大量共存。
4
3.特性:含有Fe3+的盐溶液遇到KSCN时变成血红色,含有Fe3+的盐溶液遇到酚类物质时变成紫色。
知识点3 Fe2+和Fe3+的检验
1.Fe2+的检验
方法1 ―――――――→无现象―――――――→溶液变______色,证明含有Fe2+
――――――――→产生白色絮状沉淀,迅速变成灰绿色,最终变为红褐色,证明含
方法2
有Fe2+
方法3 ―――――――――→生成______色沉淀,证明含有Fe2+
2.Fe3+的检验
方法1 ――――――――→溶液变______色,证明含有Fe3+
方法2 ―――――――→产生______色沉淀,证明含有Fe3+
方法3 ―――――――――→生成______色沉淀,证明含有Fe3+
3.混合溶液中Fe3+、Fe2+的检验
①Fe3+的检验a.――→溶液变血红色,说明含有Fe3+
b.――→试纸变蓝色,说明含有Fe3+
②Fe2+的检验
a.――→KMnO 溶液褪色,说明含有Fe2+
4
b.――→溴水褪色,说明含有Fe2+
c.――→生成蓝色沉淀,说明含有Fe2+
【易错提醒】检验Fe2+和Fe3+时的注意事项
(1)检验Fe2+时不能先加氯水后加KSCN溶液,也不能将加KSCN后的混合溶液加入足量的新制氯水中(新
制氯水能氧化SCN-),检验Fe2+最好用K[Fe(CN) ]溶液。
3 6
(2)Fe3+、Fe2+、Cl-同时存在时不能用酸性KMnO 溶液检验Fe2+(Cl-能还原酸性KMnO ,有干扰)。
4 4
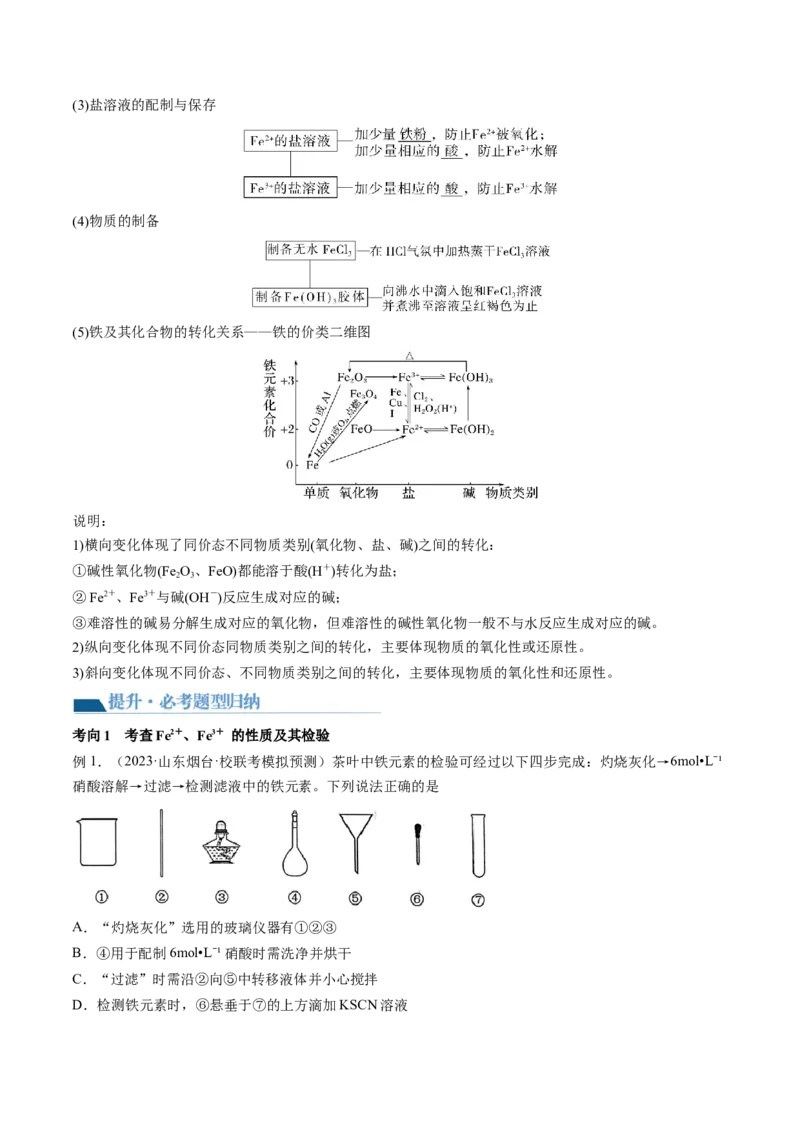
知识点4 “铁三角”的转化关系及其应用
1.“铁三角”的转化
用离子方程式表现转化
①2Fe3++HS===2Fe2++S↓+2H+
2
②2Fe3++SO +2HO===2Fe2++4H++SO
2 2
③3Fe2++4H++NO===3Fe3++2HO+NO↑
2
④5Fe2++MnO+8H+===5Fe3++Mn2++4HO
2
⑤2Fe2++HO+2H+===2Fe3++2HO
2 2 2
2.应用
(1)判断离子共存
①Fe2+与NO(H+)、ClO-、MnO(H+)发生氧化还原反应,不能大量共存;
②Fe3+与S2-、I-、SO发生氧化还原反应,不能大量共存;
③Fe2+、Fe3+与HCO、CO等水解相互促进生成沉淀,不能大量共存。
(2)除杂
溶液 杂质 除杂方法
FeCl FeCl 加过量铁粉后过滤
2 3
FeCl FeCl 加氯水或HO
3 2 2 2
FeCl CuCl 加过量铁粉后过滤
2 2(3)盐溶液的配制与保存
(4)物质的制备
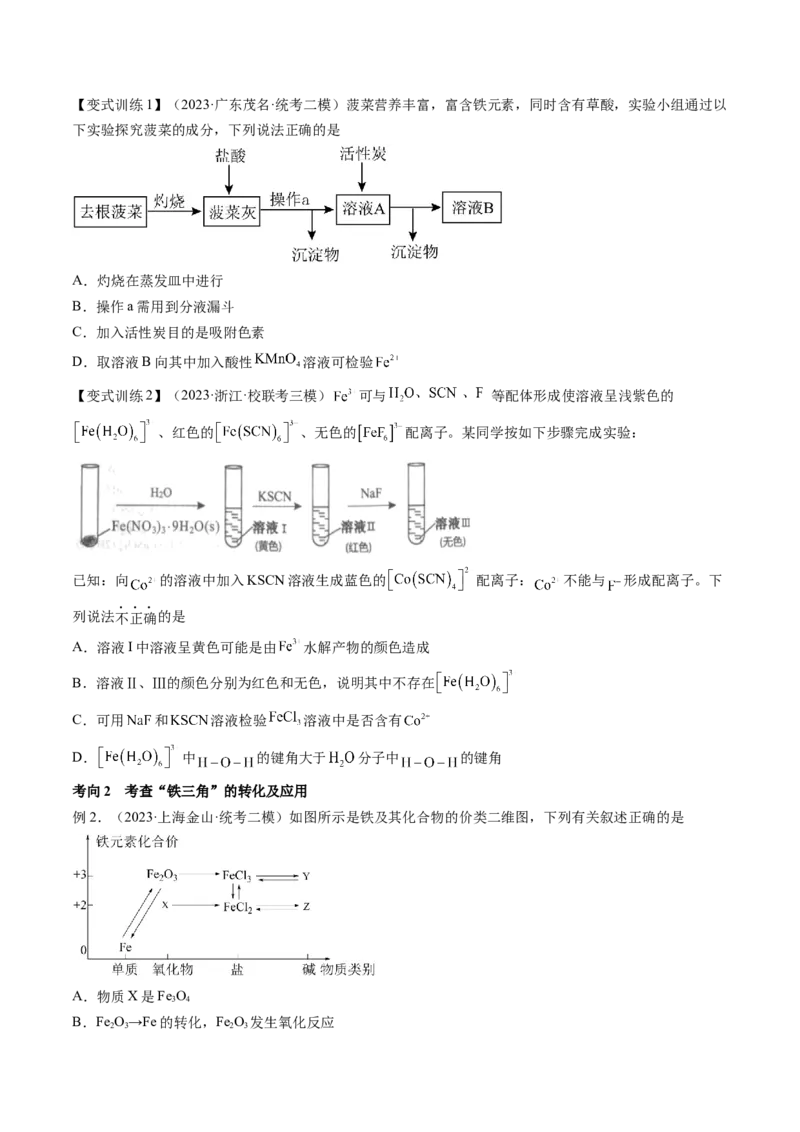
(5)铁及其化合物的转化关系——铁的价类二维图
说明:
1)横向变化体现了同价态不同物质类别(氧化物、盐、碱)之间的转化:
①碱性氧化物(Fe O、FeO)都能溶于酸(H+)转化为盐;
2 3
②Fe2+、Fe3+与碱(OH-)反应生成对应的碱;
③难溶性的碱易分解生成对应的氧化物,但难溶性的碱性氧化物一般不与水反应生成对应的碱。
2)纵向变化体现不同价态同物质类别之间的转化,主要体现物质的氧化性或还原性。
3)斜向变化体现不同价态、不同物质类别之间的转化,主要体现物质的氧化性和还原性。
考向1 考查Fe2+、Fe3+ 的性质及其检验
例1.(2023·山东烟台·校联考模拟预测)茶叶中铁元素的检验可经过以下四步完成:灼烧灰化→6mol•L⁻¹
硝酸溶解→过滤→检测滤液中的铁元素。下列说法正确的是
A.“灼烧灰化”选用的玻璃仪器有①②③
B.④用于配制6mol•L⁻¹硝酸时需洗净并烘干
C.“过滤”时需沿②向⑤中转移液体并小心搅拌
D.检测铁元素时,⑥悬垂于⑦的上方滴加KSCN溶液【变式训练1】(2023·广东茂名·统考二模)菠菜营养丰富,富含铁元素,同时含有草酸,实验小组通过以
下实验探究菠菜的成分,下列说法正确的是
A.灼烧在蒸发皿中进行
B.操作a需用到分液漏斗
C.加入活性炭目的是吸附色素
D.取溶液B向其中加入酸性 溶液可检验
【变式训练2】(2023·浙江·校联考三模) 可与 等配体形成使溶液呈浅紫色的
、红色的 、无色的 配离子。某同学按如下步骤完成实验:
已知:向 的溶液中加入KSCN溶液生成蓝色的 配离子: 不能与 形成配离子。下
列说法不正确的是
A.溶液I中溶液呈黄色可能是由 水解产物的颜色造成
B.溶液Ⅱ、Ⅲ的颜色分别为红色和无色,说明其中不存在
C.可用 和 溶液检验 溶液中是否含有
D. 中 的键角大于 分子中 的键角
考向2 考查“铁三角”的转化及应用
例2.(2023·上海金山·统考二模)如图所示是铁及其化合物的价类二维图,下列有关叙述正确的是
A.物质X是Fe O
3 4
B.Fe O→Fe的转化,Fe O 发生氧化反应
2 3 2 3C.在空气中Z→Y的现象是白色沉淀迅速变成灰绿色,最终变成红褐色
D.可通过复分解反应实现FeCl 和FeCl 的相互转化
2 3
【变式训练1】(2023·广东广州·统考二模)下列关于铁及其化合物之间转化反应的方程式书写正确的是
A. (g)通过灼热铁粉:
B.过量铁粉加入稀硝酸中:
C.氢氧化铁中加入氢碘酸:
D. 溶液中加入酸性 溶液:
【变式训练2】(2023·河北石家庄·校联考模拟预测)废料利用是节能减排的重要方式,以硫铁矿烧渣(主
要成分为Fe O、FeO、 等)为原料来制备铁红(Fe O)的生产流程如图。下列说法错误的是
2 3 2 3
A.将硫铁矿烧渣粉碎,有利于提高浸出率
B.加入过量铁粉的目的是将 全部还原为
C.步骤Ⅳ的反应温度越高,越有利于提高反应速率和产率
D.“煅烧”步骤的化学方程式为
考向3 实验探究铁及其重要化合物的转化关系
例3.(2023·河南安阳·统考三模)某化学实验小组设计如下实验探究Zn与溶液中Fe3+发生反应的原理。
实验 试剂 现象
2 mL0.1 mol· L-1FeCl 溶液、过 黄色溶液很快变浅,接着有无色气泡产生,固体中未检出铁单
3
I
量锌粉 质
2 mL1 mol· L-1FeCl 溶液 很快有大量气体产生,出现红褐色浑浊,30 min左右产生红褐
3
Ⅱ
(pH≈0.70)、过量锌粉 色沉淀,溶液颜色变浅,产生少量铁单质
下列说法错误的是
A.实验I说明Fe3+被还原为Fe2+
B.可用酸性高锰酸钾溶液检验实验I得到的溶液中含有Fe2+
C.实验Ⅱ发生了置换反应和复分解反应
D.实验说明Fe3+、H+与Zn的反应与离子浓度有关【变式训练】(2023·北京西城·统考二模)探究Cu与 溶液的反应,进行如下实验。
实验①:向10mL0.2mol/L 溶液(pH≈1)中加入0.1gCu粉,振荡后静置,取上层清液,滴加
溶液,有蓝色沉淀产生。6h后,溶液由棕黄色变为蓝绿色。实验过程中未见有气泡产生,溶
液的pH几乎不变。
实验②:在密闭容器中向10mL0.6mol/L 溶液中加入0.1gCu粉,10h后溶液变为淡蓝色。
实验③:在密闭容器中向10mL0.6mol/L 溶液中分别加入0.1gCu粉和0.1g 固体,0.5h溶液变黄,
3h溶液变为黄绿色。下列说法不正确的是
A.实验①中发生了反应:
B.推测实验②的离子方程式是:
C.对比实验①和②,①中溶解Cu的主是
D.对比实验②和③, 与 反应的速率大于 与Cu反应的速率
1.(2023·浙江·高考真题)物质的性质决定用途,下列两者对应关系不正确的是
A. 能使某些色素褪色,可用作漂白剂 B.金属钠导热性好,可用作传热介质
C. 溶液呈碱性,可用作消毒剂 D. 呈红色,可用作颜料
2.(2023·上海·统考高考真题)下列物质中,能通过化学氧化法去除石油开采过程中伴生的 的是
A.氨水 B.双氧水 C. 溶液 D.NaOH溶液
3.(2023·上海·统考高考真题)月球土壤中富含铁元素,主要以铁单质和亚铁离子的形式存在,但嫦娥五
号取回的微陨石撞击处的月壤样品中存在大量的三价铁,有可能是以下哪个原因造成的
A. B.
C. D.
4.(2022·海南·统考高考真题)依据下列实验,预测的实验现象正确的是
选项 实验内容 预测的实验现象
A 溶液中滴加NaOH溶液至过量 产生白色沉淀后沉淀消失
B 溶液中滴加KSCN溶液 溶液变血红色
C AgI悬浊液中滴加NaCl溶液至过量 黄色沉淀全部转化为白色沉淀
D 酸性 溶液中滴加乙醇至过量 溶液紫红色褪去
5.(2022·广东·高考真题)为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌铁片放入酸化的 溶液中。一段时间后,取溶液分别实验,能说明铁片没有被腐蚀的是
A.加入 溶液产生沉淀 B.加入淀粉碘化钾溶液无蓝色出现
C.加入 溶液无红色出现 D.加入 溶液无蓝色沉淀生成