文档内容
INCLUDEPICTURE "F:\\方正文件\\2019 文
件\\课件\\2020 版 创新设计 高考总复习
化学 人教版\\第二章.tif" \*
MERGEFORMATINET
第1讲 物质的组成、性质及分类
【2020·备考】
最新考纲:1.了解分子、原子、离子等概念的含义;了解原子团的定义。2.理解物理
变化与化学变化的区别与联系。3.理解混合物和纯净物、单质和化合物、金属和非
金属的概念。4.理解酸、碱、盐、氧化物的概念及其相互联系。5.了解胶体是一种常
见的分散系,了解溶液和胶体的区别。
核心素养:1.宏观辨识与微观探析:能从不同层次、不同角度认识物质的多样性,
能够对物质进行分类,能够运用物质分类的方法理解物质的性质。2.科学精神与社
会责任:要注意胶体的知识与生产生活实际的联系,赞赏化学对社会发展的重大
贡献,能对与化学有关的社会热点问题做出正确的价值判断。考点一 物质的组成与分类
(频数:★☆☆ 难度:★☆☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 物
质的组成与分类属于初中与高中的衔接知识,要求较低,重点掌握物质分类特点,
抓住有关反例进行反驳,另外随着对传统文化考查力度的加大,古诗词中有关物
质的组成与分类的题目在考题中逐渐增多,复习时应加以关注。
1.辨析:物质组成的相关概念
(1)元素与核素
元素:具有相同核电荷数的一类原子的总称。
核素:具有一定数目质子和一定数目中子的一种原子,如H元素有1H、2H、3H 3种
原子,即3种核素。
(2)单质与化合物
(3)游离态与化合态
(4)纯净物与混合物
纯净物:由同种单质或化合物组成的物质。
混合物:由几种不同的单质或化合物组成的物质。
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
由同种元素组成的物质不一定是纯净物,如O 和O 组成的物质为混合物。
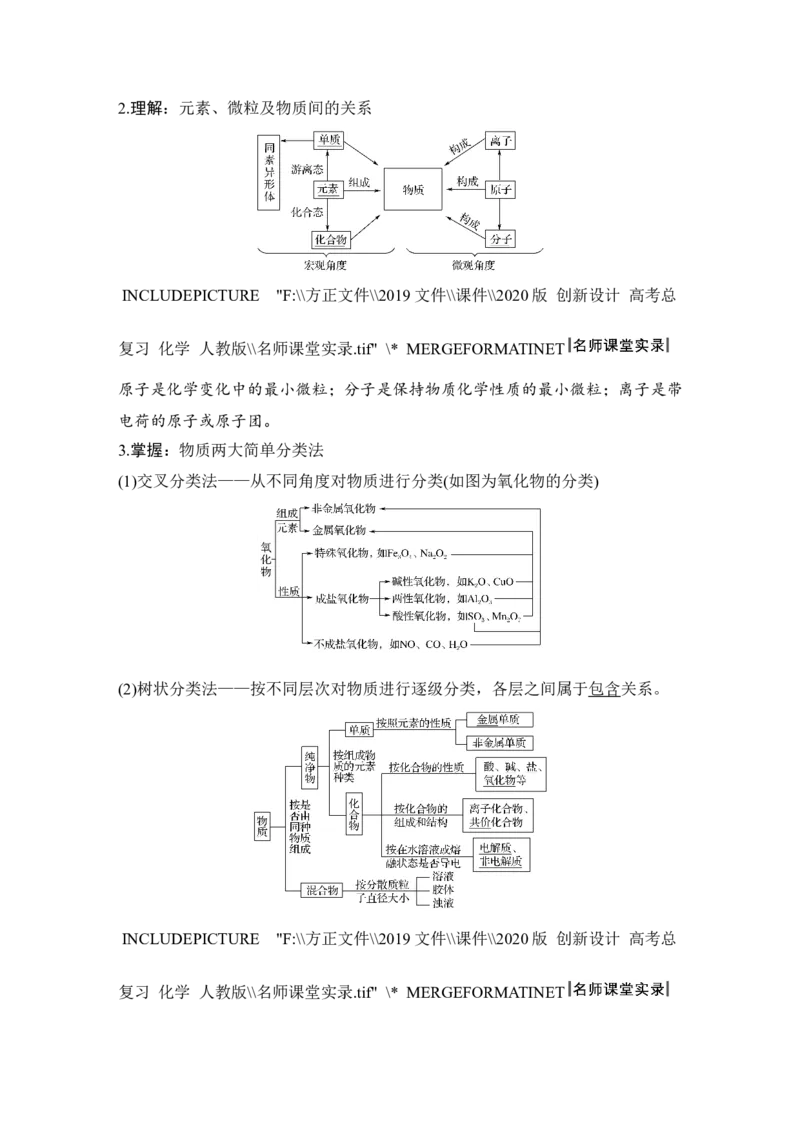
2 32.理解:元素、微粒及物质间的关系
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
原子是化学变化中的最小微粒;分子是保持物质化学性质的最小微粒;离子是带
电荷的原子或原子团。
3.掌握:物质两大简单分类法
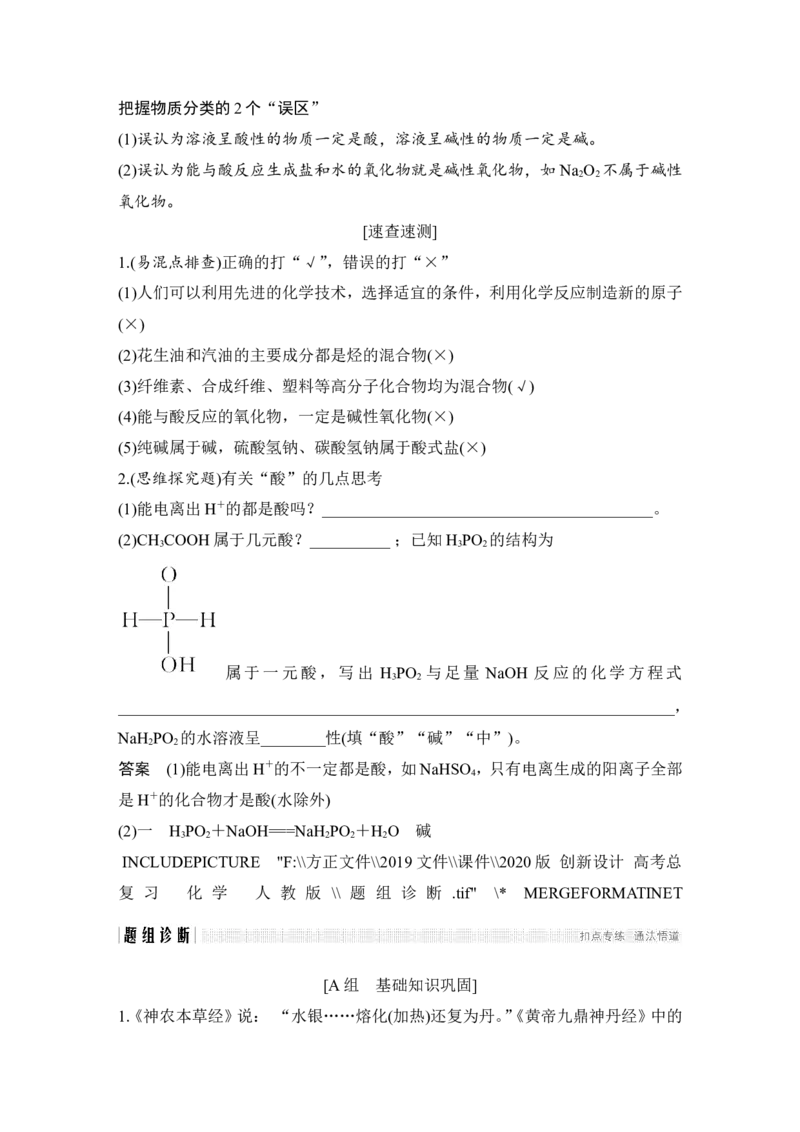
(1)交叉分类法——从不同角度对物质进行分类(如图为氧化物的分类)
(2)树状分类法——按不同层次对物质进行逐级分类,各层之间属于包含关系。
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET把握物质分类的2个“误区”
(1)误认为溶液呈酸性的物质一定是酸,溶液呈碱性的物质一定是碱。
(2)误认为能与酸反应生成盐和水的氧化物就是碱性氧化物,如 Na O 不属于碱性
2 2
氧化物。
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)人们可以利用先进的化学技术,选择适宜的条件,利用化学反应制造新的原子
(×)
(2)花生油和汽油的主要成分都是烃的混合物(×)
(3)纤维素、合成纤维、塑料等高分子化合物均为混合物(√)
(4)能与酸反应的氧化物,一定是碱性氧化物(×)
(5)纯碱属于碱,硫酸氢钠、碳酸氢钠属于酸式盐(×)
2.(思维探究题)有关“酸”的几点思考
(1)能电离出H+的都是酸吗?_________________________________________。
(2)CH COOH属于几元酸?__________ ;已知H PO 的结构为
3 3 2
属于一元酸,写出 H PO 与足量 NaOH 反应的化学方程式
3 2
_____________________________________________________________________,
NaH PO 的水溶液呈________性(填“酸”“碱”“中”)。
2 2
答案 (1)能电离出H+的不一定都是酸,如NaHSO ,只有电离生成的阳离子全部
4
是H+的化合物才是酸(水除外)
(2)一 H PO +NaOH===NaH PO +H O 碱
3 2 2 2 2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.《神农本草经》说: “水银……熔化(加热)还复为丹。”《黄帝九鼎神丹经》中的“柔丹”、“伏丹”都是在土釜中加热Hg制得的。这里的“丹”是指( )
A.氯化物 B.合金
C.硫化物 D.氧化物
解析 在土釜中加热Hg,金属汞可以和氧气发生反应得到氧化汞,氧化汞属于物
质分类中的氧化物。
答案 D
2.下列与化学有关的文献,理解错误的是( )
A.《咏石灰》(明·于谦)中“……烈火焚烧若等闲……要留清白在人间”其中“清
白”是指氢氧化钙
B.《咏煤炭》(明·于谦)中“凿开混沌得乌金……不辞辛苦出山林”其中“乌金”
的主要成分是煤炭
C.《天工开物》中记载: “以硝石、硫磺为主。草木灰为辅。……魂散惊而魄齑
粉”文中提到的是火药
D.《天工开物》中有如下描述: “世间丝、麻、裘、褐皆具素质……”文中的
“裘”主要成分是蛋白质
解析 A.《咏石灰》(明·于谦)中“……烈火焚烧若等闲……要留清白在人间”,描
述的是碳酸钙的受热分解生成CaO与水反应生成Ca(OH) ,Ca(OH) 与CO 反应
2 2 2
生成CaCO 的过程,其中“清白”是指碳酸钙,故A错误;B.《咏煤炭》(明·于谦)
3
中“凿开混沌得乌金……不辞辛苦出山林”描述的是煤炭的开采,其中“乌金”
的主要成分是煤炭,故B正确;C《. 天工开物》中记载: “以硝石、硫磺为主。草木
灰为辅。……魂散惊而魄齑粉” ,消石、硫磺是制造火药的主要原料,故C正确;
D.《天工开物》中有如下描述: “世间丝、麻、裘、褐皆具素质……”文中的
“裘”指的是动物的毛皮,主要成分是蛋白质,故D正确。
答案 A
3.(2019·大连重点中学考试)下列物质中一定属于纯净物的一组是( )
①冰水混合物 ②爆鸣气 ③铝热剂 ④普通玻璃
⑤水玻璃 ⑥漂白粉 ⑦二甲苯 ⑧TNT ⑨溴苯
⑩C H ⑪含氧40%的氧化镁 ⑫花生油 ⑬福尔马林
5 12
⑭密封保存的NO 气体
2A.①⑧⑨⑪ B.②③④⑥
C.⑦⑩⑫⑬⑭ D.①④⑧⑨⑪⑫
解析 ①冰水混合物的成分为水,为纯净物;②爆鸣气是氢气和氧气的混合物;③
铝热剂是铝和金属氧化物的混合物;④普通玻璃是硅酸钠、硅酸钙、二氧化硅的混
合物;⑤水玻璃是硅酸钠的水溶液,属于混合物;⑥漂白粉是氯化钙、次氯酸钙的
混合物;⑦二甲苯不一定是纯净物,可能是邻二甲苯、对二甲苯、间二甲苯的混合
物;⑧TNT 是三硝基甲苯的俗称,属于纯净物;⑨溴苯是纯净物;⑩C H 不一定
5 12
表示纯净物,可能是正戊烷、异戊烷、新戊烷的混合物;⑪氧化镁中氧的含量为
40%,故含氧40%的氧化镁是纯净物;⑫花生油有多种成分,是混合物;⑬福尔马
林是甲醛的水溶液,属于混合物;⑭密封保存的NO 气体,存在2NO N O
2 2 2 4
平衡体系,为混合物。综上所述,①⑧⑨⑪一定属于纯净物,A项正确。
答案 A
4.(2018·湖南省浏阳市期中联考)对物质进行分类是一种简单、有效的科学方法。
下列各组物质的分类都正确的是( )
A.空气(混合物)、C H OH(醇)、H SO (离子化合物)、CO (非电解质)
2 5 2 4 2
B.NO (酸性氧化物)、CH CHO(有机物)、CO(无机物)、CH COOCH (酯)
2 3 3 3
C.HCl(共价化合物)、CH COOH(羧酸)、Na O (碱性氧化物)、CH I(卤代烃)
3 2 2 3
D.液氨(氢化物)、NH Cl(铵盐)、HNO (含氧酸)、NaOH(强电解质)
4 3
解析 A.硫酸中的化学键属于共价键,属于共价化合物,故A错误;B.NO 不属于
2
酸性氧化物,故B错误;C.过氧化钠和盐酸反应生成氯化钠、水以及氧气,属于过
氧化物,不属于碱性氧化物,故C错误;D.液氨属于氢化物、NH Cl属于铵盐、
4
HNO 属于含氧酸、NaOH属于强电解质,故D正确。
3
答案 D
【归纳总结】
1.纯净物和混合物的区别纯净物 混合物
有固定的组成和结构 无固定的组成和结构
有固定的熔、沸点 无固定的熔、沸点
保持一种物质的性质 保持原有物质各自的性质
2.常见混合物
①分散系(如溶液、胶体、浊液等);②高分子(如蛋白质、纤维素、聚合物、淀粉等);
③常见特殊名称的混合物:石油、石油的各种馏分、煤、漂白粉、碱石灰、福尔马林、
油脂、天然气、水煤气、铝热剂、氨水、氯水、王水等。
3.易错辨析点
确定分子式的有机物可能是纯净物也可能是混合物,如C H 的结构有正丁烷和
4 10
异丁烷,二者组成混合物。
[B组 考试能力过关]
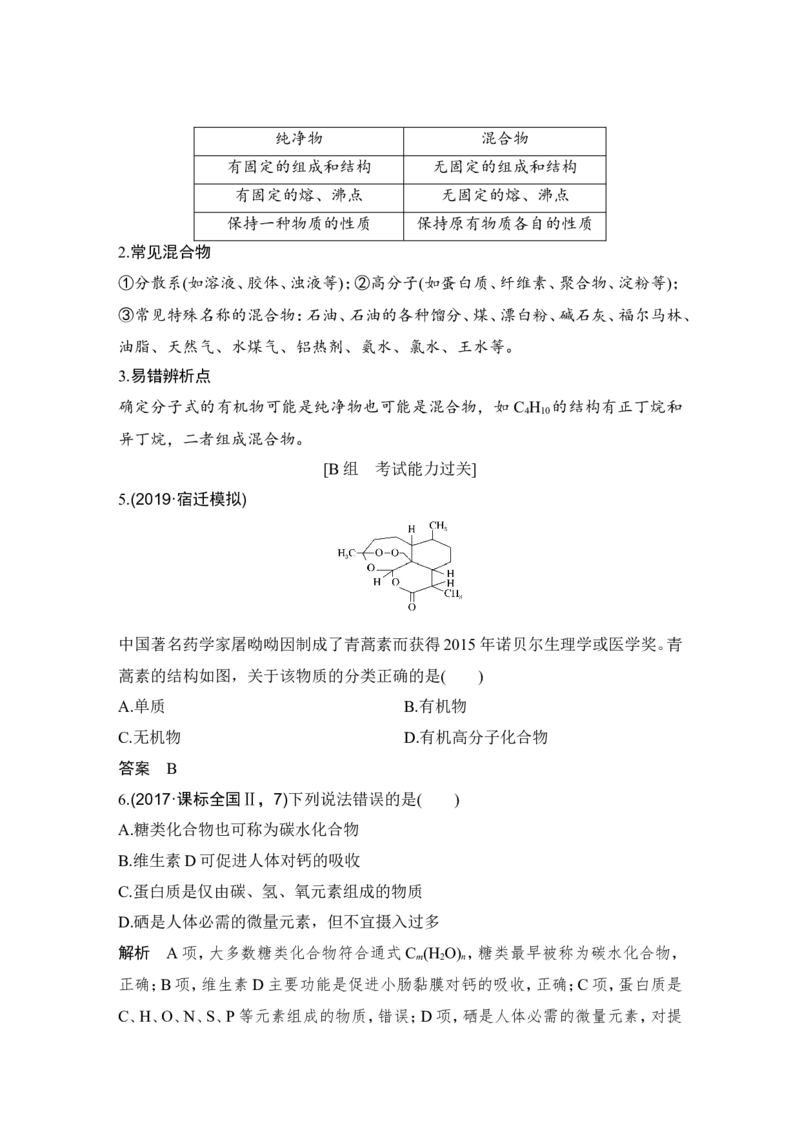
5.(2019·宿迁模拟)
中国著名药学家屠呦呦因制成了青蒿素而获得2015年诺贝尔生理学或医学奖。青
蒿素的结构如图,关于该物质的分类正确的是( )
A.单质 B.有机物
C.无机物 D.有机高分子化合物
答案 B
6.(2017·课标全国Ⅱ,7)下列说法错误的是( )
A.糖类化合物也可称为碳水化合物
B.维生素D可促进人体对钙的吸收
C.蛋白质是仅由碳、氢、氧元素组成的物质
D.硒是人体必需的微量元素,但不宜摄入过多
解析 A项,大多数糖类化合物符合通式C (H O) ,糖类最早被称为碳水化合物,
m 2 n
正确;B项,维生素D主要功能是促进小肠黏膜对钙的吸收,正确;C项,蛋白质是
C、H、O、N、S、P等元素组成的物质,错误;D项,硒是人体必需的微量元素,对提高免疫力和预防癌症非常重要,但摄入过多对人体产生危害,正确。
答案 C
考点二 物质的性质与变化
(频数:★★☆ 难度:★☆☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 物
质的性质、用途和转化应属于元素化合物的知识体系,主要考查常见代表物的性
质特点,体现学以致用的原则;物理变化和化学变化的判断是初中延伸出来的知
识点,复习时注意古典文献中的一些变化过程判断。
1.物理变化与化学变化
(1)宏观角度
物理变化没有新物质生成,化学变化有新物质生成。
(2)微观角度
化学变化过程中同时伴随着旧化学键的断裂和新化学键的形成。只有化学键断裂
而没有新化学键形成的过程不是化学变化,如NaCl晶体的熔化。
(3)二者关系
化学变化中一定伴随着物理变化,但物理变化过程中一般没有化学变化。
(4)物质变化与性质的关系
①图示②应用下列用途体现物质物理性质的是ae;体现物质化学性质的是bcd。
a.用铝箔包装物品 b.NaHCO 作为食品工业的膨松剂
3
c.浓氨水检验输送氯气的管道是否泄漏 d.SO 漂白纸浆 e.液态丙烷作制冷剂
2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
原子是化学变化中的最小微粒,原子核遭到破坏的过程不属于化学变化,核裂变、
核聚变虽有新物质生成,均不属于化学变化。
2.化学反应的分类
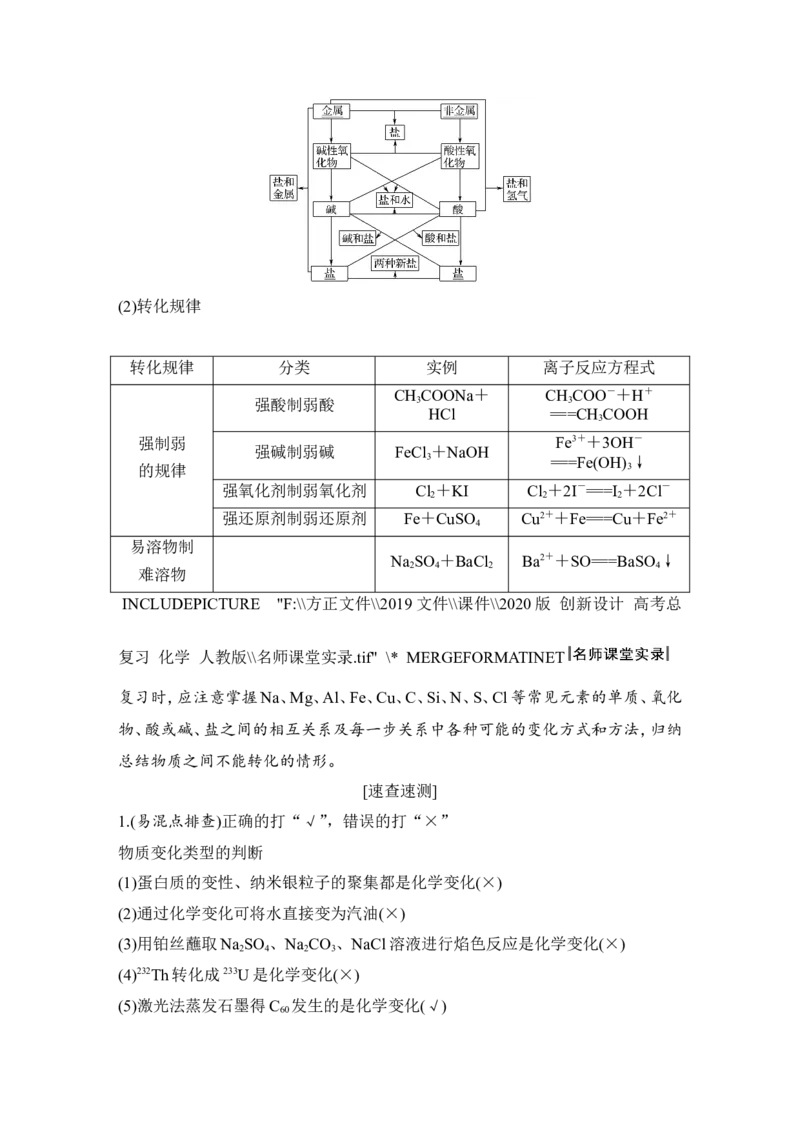
3.单质、氧化物、酸、碱和盐的转化
(1)转换关系(2)转化规律
转化规律 分类 实例 离子反应方程式
CH COONa+ CH COO-+H+
强酸制弱酸 3 3
HCl ===CH COOH
3
强制弱 Fe3++3OH-
强碱制弱碱 FeCl +NaOH
3 ===Fe(OH) ↓
的规律 3
强氧化剂制弱氧化剂 Cl +KI Cl +2I-===I +2Cl-
2 2 2
强还原剂制弱还原剂 Fe+CuSO Cu2++Fe===Cu+Fe2+
4
易溶物制
Na SO +BaCl Ba2++SO===BaSO ↓
2 4 2 4
难溶物
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
复习时,应注意掌握Na、Mg、Al、Fe、Cu、C、Si、N、S、Cl等常见元素的单质、氧化
物、酸或碱、盐之间的相互关系及每一步关系中各种可能的变化方式和方法,归纳
总结物质之间不能转化的情形。
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
物质变化类型的判断
(1)蛋白质的变性、纳米银粒子的聚集都是化学变化(×)
(2)通过化学变化可将水直接变为汽油(×)
(3)用铂丝蘸取Na SO 、Na CO 、NaCl溶液进行焰色反应是化学变化(×)
2 4 2 3
(4)232Th转化成233U是化学变化(×)
(5)激光法蒸发石墨得C 发生的是化学变化(√)
60(6)NH Cl溶液除铁锈是化学变化、食盐水导电是物理变化(×)
4
2.(思维探究题)《天工开物》是世界第一部记录农业和手工业生产技术的百科全书
以大量生动细节留存了丰富的古代科技史料,被誉为“百科全书之祖”,对书中描
述作出正确解释
描述 解释
凡火药,硫为纯阳,硝为纯阴,此乾坤幻出神物
“硝”指的是____
也
凡墨烧烟凝质而为之 “烟”指的是________
凡虚伪方士以炉火惑人者,唯朱砂银愚人易惑 “朱砂银”指的是________
这句话描述的对象为
五金之长,熔化成形之后,住世永无变更
________
答案 硝酸钾 炭黑 硫化汞 黄金
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.下列生活中的做法没有利用物质化学性质的是( )
A.葡萄酒中添加二氧化硫
B.鲜花店的老板用浸泡了高锰酸钾的硅土延长鲜花的保存期
C.用双氧水漂洗衣服上的污渍
D.夏天超市用干冰给物质降温
解析 葡萄酒中添加二氧化硫的作用是抗氧化、防腐、杀菌,利用了它的化学性质,
A项不符合题意;成熟的植物会产生乙烯气体,高锰酸钾会和乙烯发生氧化反应,
所以可以起到鲜花保鲜的作用,B项不符合题意;双氧水具有氧化性,可以漂白衣
物,C项不符合题意;干冰为固体二氧化碳,受热后直接汽化,吸收周围的热量达
到降低温度的效果,所以这种做法利用了物质的物理性质,D项符合题意。答案 D
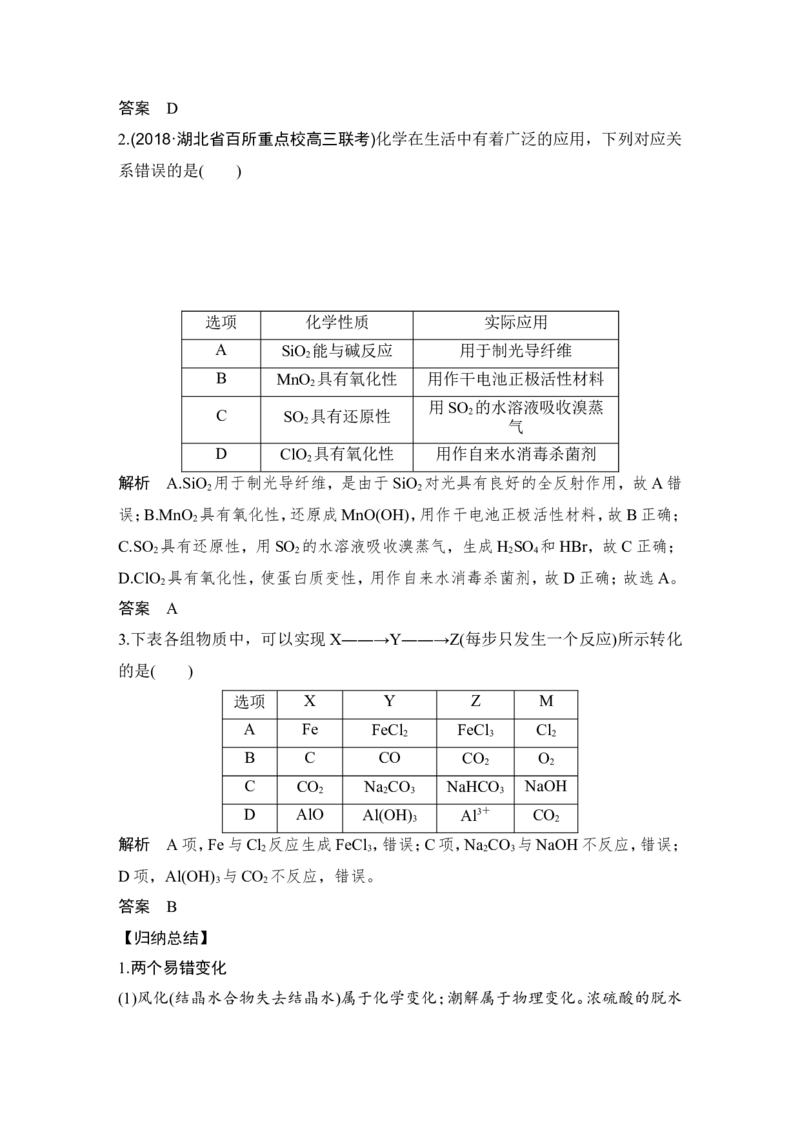
2.(2018·湖北省百所重点校高三联考)化学在生活中有着广泛的应用,下列对应关
系错误的是( )
选项 化学性质 实际应用
A SiO 能与碱反应 用于制光导纤维
2
B MnO 具有氧化性 用作干电池正极活性材料
2
用SO 的水溶液吸收溴蒸
C SO 具有还原性 2
2 气
D ClO 具有氧化性 用作自来水消毒杀菌剂
2
解析 A.SiO 用于制光导纤维,是由于SiO 对光具有良好的全反射作用,故A错
2 2
误;B.MnO 具有氧化性,还原成MnO(OH),用作干电池正极活性材料,故B正确;
2
C.SO 具有还原性,用SO 的水溶液吸收溴蒸气,生成H SO 和HBr,故C正确;
2 2 2 4
D.ClO 具有氧化性,使蛋白质变性,用作自来水消毒杀菌剂,故D正确;故选A。
2
答案 A
3.下表各组物质中,可以实现X――→Y――→Z(每步只发生一个反应)所示转化
的是( )
选项 X Y Z M
A Fe FeCl FeCl Cl
2 3 2
B C CO CO O
2 2
C CO Na CO NaHCO NaOH
2 2 3 3
D AlO Al(OH) Al3+ CO
3 2
解析 A项,Fe与Cl 反应生成FeCl ,错误;C项,Na CO 与NaOH不反应,错误;
2 3 2 3
D项,Al(OH) 与CO 不反应,错误。
3 2
答案 B
【归纳总结】
1.两个易错变化
(1)风化(结晶水合物失去结晶水)属于化学变化;潮解属于物理变化。浓硫酸的脱水性属于化学性质。
(2) 煤的干馏、煤的气化以及煤的液化都属于化学变化,石油的分馏属于物理变化
石油的裂化和裂解都属于化学变化。
2.三个易错转化
(1)S燃烧不能直接生成SO 而是生成SO 。
3 2
(2)N 与O 反应,一步反应只生成NO,不能直接生成NO 。
2 2 2
(3)Fe与Cl 反应,只生成FeCl ,不能直接生成FeCl 。
2 3 2
[B组 考试能力过关]
4.(2018·北京理综,7)下列我国科技成果所涉及物质的应用中,发生的不是化学变
化的是( )
B.氘、氚用作“人 C.偏二甲肼用作发
A.甲醇低温所制氢 D.开采可燃冰,将
造太阳”核聚变燃 射“天宫二号”的
气用于新能源汽车 其作为能源使用
料 火箭燃料
解析 由甲醇制备氢气的过程中有新物质生成,显然属于化学变化,A项不符合
题意;原子是化学变化中的最小粒子,核聚变过程中原子发生了变化,所以核聚变
属于核反应,而不是化学反应,B项符合题意;偏二甲肼用作发射火箭的燃料,是
利用其还原性,与氧化剂(常见的是四氧化二氮)发生氧化还原反应,反应时放出大
量的热,把火箭送入太空,C项不符合题意;可燃冰作为能源是由于其主要成分(甲
烷)燃烧时放出大量的热,燃烧属于化学变化,D项不符合题意。
答案 B
5.(2018·海南化学,5)化学与生产生活密切相关,下列说法错误的是( )
A.Na O 可与CO 反应放出氧气,可用于制作呼吸面具
2 2 2
B.SiO 具有导电性,可用于制作光导纤维和光电池
2
C.聚四氟乙烯耐酸碱腐蚀,可用作化工反应器的内壁涂层
D.氯水具有较强的氧化性,可用于漂白纸张、织物等
答案 B
6.(2018·江苏化学,9)在给定条件下,下列选项所示的物质间转化均能实现的是()
A.NaHCO (s)――→Na CO (s)――→NaOH(aq)
3 2 3
B.Al(s)――→NaAlO (aq)――→Al(OH) (s)
2 3
C.AgNO (aq)――→[Ag(NH ) ]+(aq)――→Ag(s)
3 3 2
D.Fe O (s)――→Fe(s)――→FeCl (aq)
2 3 3
解析 2NaHCO =====Na CO +CO ↑+H O,Na CO +Ca(OH) ===CaCO ↓+
3 2 3 2 2 2 3 2 3
2NaOH,A项正确;2Al+2NaOH+2H O===2NaAlO +3H ↑,NaAlO 与过量HCl
2 2 2 2
反应生成Al3+,即AlO+4H+===Al3++2H O,B项错误;蔗糖分子中不含醛基,无
2
还原性,不能发生银镜反应,C项错误;Fe O +2Al=====Al O +2Fe,而Fe与HCl
2 3 2 3
反应只能生成FeCl :Fe+2HCl===FeCl +H ↑,D项错误。
2 2 2
答案 A
考点三 分散系 胶体
(频数:★★☆ 难度:★★☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 分
散系和胶体考查力度不大,低频地出现在“化学、社会、生活”题目的某个选项中,
复习时抓住胶体的性质进行落实,另外注意一些与胶体有关的生产、生活现象。
1.分散系
(1)概念: 把一种 ( 或几种 ) 物质 ( 分散质 ) 分散在另一种 ( 或几种 ) 物质 ( 分散剂 ) 中 所得
到的体系。
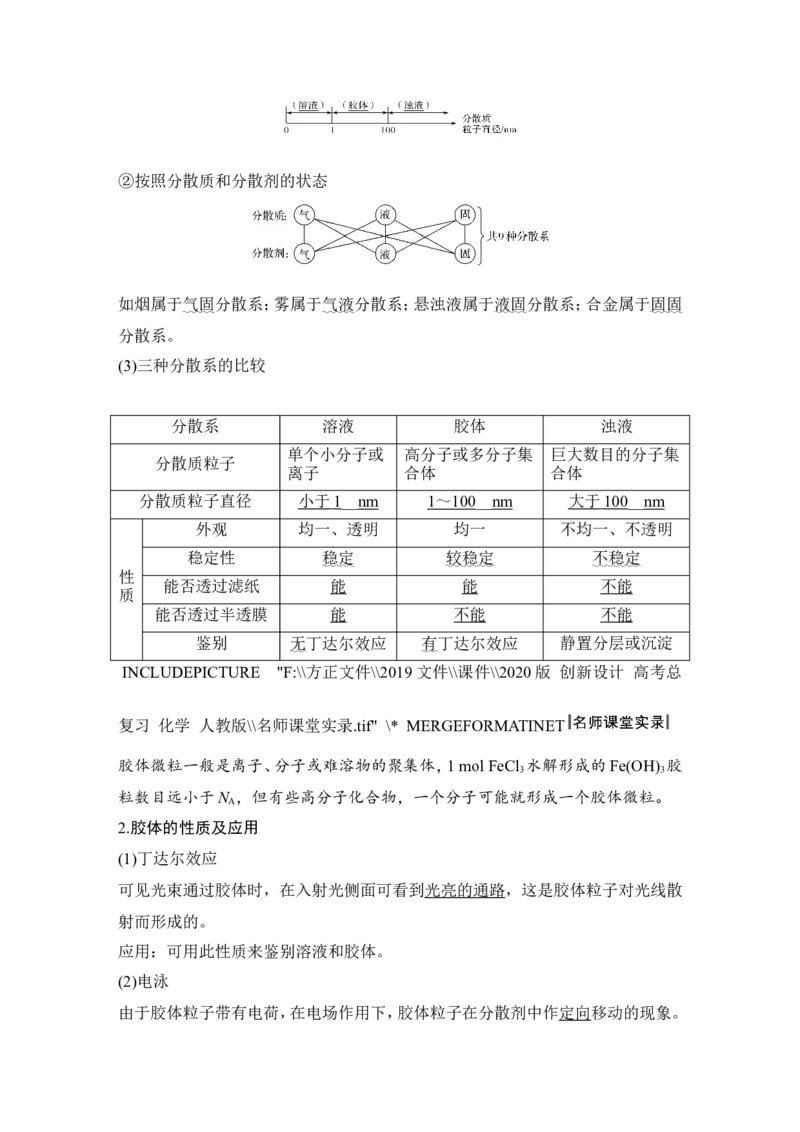
(2)分类
①按照分散质粒子的大小②按照分散质和分散剂的状态
如烟属于气固分散系;雾属于气液分散系;悬浊液属于液固分散系;合金属于固固
分散系。
(3)三种分散系的比较
分散系 溶液 胶体 浊液
单个小分子或 高分子或多分子集 巨大数目的分子集
分散质粒子
离子 合体 合体
分散质粒子直径 小于 1__nm 1 ~ 100 __nm 大于 10 0__nm
外观 均一、透明 均一 不均一、不透明
稳定性 稳定 较稳定 不稳定
性
能否透过滤纸 能 能 不能
质
能否透过半透膜 能 不能 不能
鉴别 无丁达尔效应 有丁达尔效应 静置分层或沉淀
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
胶体微粒一般是离子、分子或难溶物的聚集体,1 mol FeCl 水解形成的Fe(OH) 胶
3 3
粒数目远小于N ,但有些高分子化合物,一个分子可能就形成一个胶体微粒。
A
2.胶体的性质及应用
(1)丁达尔效应
可见光束通过胶体时,在入射光侧面可看到光亮的通路,这是胶体粒子对光线散
射而形成的。
应用:可用此性质来鉴别溶液和胶体。
(2)电泳
由于胶体粒子带有电荷,在电场作用下,胶体粒子在分散剂中作定向移动的现象。应用:此性质可用于工业上的静电除尘。
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
电泳可证明胶体粒子带电,但胶体不带电,整个分散系仍呈电中性,胶粒带电的原
因是因为吸附了体系中的带电离子造成的。
(3)聚沉
①概念:使胶体凝聚形成沉淀析出的现象。
②方法:加热或搅拌、加入电解质溶液、加入带相反电荷的胶体粒子的胶体。
③应用:如制作豆腐、明矾净水等。
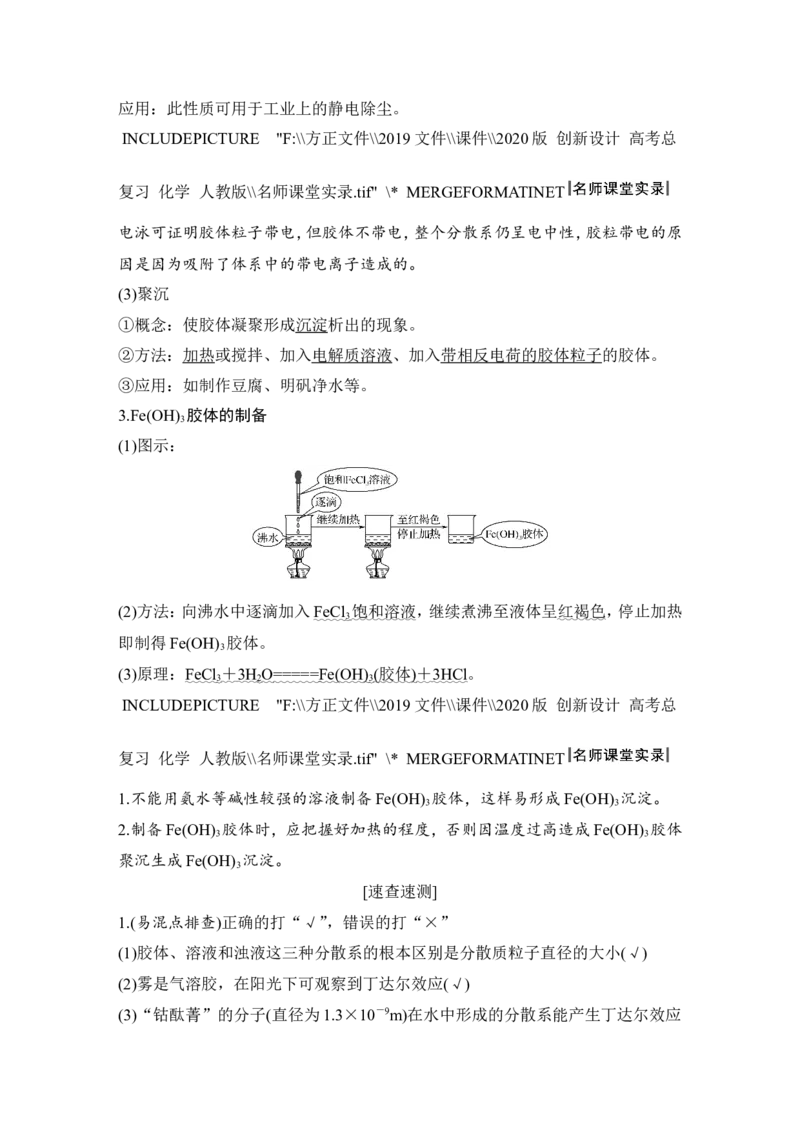
3.Fe(OH) 胶体的制备
3
(1)图示:
(2)方法:向沸水中逐滴加入FeCl 饱和溶液,继续煮沸至液体呈红褐色,停止加热
3
即制得Fe(OH) 胶体。
3
(3)原理:FeCl + 3H O ===== Fe(OH) ( 胶体 ) + 3HCl 。
3 2 3
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
1.不能用氨水等碱性较强的溶液制备Fe(OH) 胶体,这样易形成Fe(OH) 沉淀。
3 3
2.制备Fe(OH) 胶体时,应把握好加热的程度,否则因温度过高造成Fe(OH) 胶体
3 3
聚沉生成Fe(OH) 沉淀。
3
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)胶体、溶液和浊液这三种分散系的根本区别是分散质粒子直径的大小(√)
(2)雾是气溶胶,在阳光下可观察到丁达尔效应(√)
(3)“钴酞菁”的分子(直径为1.3×10-9m)在水中形成的分散系能产生丁达尔效应(√)
(4)胶体与溶液都可以通过滤纸、半透膜和分子筛(×)
(5)明矾与水反应生成的Al(OH) 胶体能吸附水中悬浮物,可用于水的净化(√)
3
2.(教材改编题)[RJ必修1·P 5改编]当光束通过下列分散系:①有尘埃的空气
42
②稀硫酸 ③蒸馏水
④Fe(OH) 胶体,能观察到丁达尔效应的是( )
3
A.①② B.②③
C.①④ D.②④
答案 C
3.(思维探究题)某同学在实验室进行了如图所示的实验,回答下列问题:
(1)利用____________方法(填分离方法),可将Z中固体与液体分离。
(2) 如 何 确 定 X 、 Z 烧 杯 中 的 液 体 属 于 何 种 分 散 质 :
_____________________________________________________________________。
(3)Y中反应的离子方程式为____________________________________________。
答案 (1)过滤
(2)通过丁达尔效应进行确定,能发生丁达尔效应的分散系是胶体,不能发生丁达
尔效应的分散系是溶液
(3)3CaCO + 2Fe3 + + 3H O===2Fe(OH) ( 胶 体 ) + 3CO ↑ + 3Ca2 +
3 2 3 2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.(2019·吉林省实验中学期中)FeCl 溶液、Fe(OH) 胶体、Fe(OH) 浊液是三种重要
3 3 3
的分散系,下列叙述中错误的是( )
A.Fe(OH) 胶体区别于其他分散系的本质特征是分散质粒子的直径在10-9~
3
10-7 mB.分别用一束光透过三种分散系,只有Fe(OH) 胶体具有丁达尔效应
3
C.三种分散系的颜色都相同,且均能与盐酸反应,具有吸附性
D.三种分散系均属于混合物
解析 A项,胶体区别于溶液或浊液的本质特征是胶体粒子的直径在10-9~10-
7m,正确;B项,胶体能产生丁达尔效应,溶液和浊液不会产生丁达尔效应,正确;
C项,只有胶体具有吸附性,FeCl 溶液和Fe(OH) 浊液没有吸附性,FeCl 溶液为
3 3 3
棕黄色,而Fe(OH) 胶体和Fe(OH) 浊液都为红褐色,错误;D项,溶液、胶体、浊液
3 3
均属于混合物,正确。
答案 C
2.(2018·广西南宁第二中学月考)向含有c(FeCl )=0.2 mol/L、c(FeCl )=0.1 mol/L
3 2
的混合溶液中滴加稀NaOH溶液,可得到一种黑色分散系,其中分散质粒子是直
径约为9.3 nm的金属氧化物,下列有关说法中正确的是( )
A.该分散系的分散质为Fe O
2 3
B.可用过滤的方法将黑色金属氧化物与Na+分离开
C.向沸水中逐滴滴加0.1 mol/L FeCl 溶液也可得到Fe(OH) 胶体
3 3
D.加入NaOH时发生的反应可能为Fe2++2Fe3++8OH-===Fe O +4H O
3 4 2
解析 Fe O 为红棕色,由题意知得到一种黑色分散系,A错误;该黑色金属氧化
2 3
物的粒子直径约为9.3 nm,属于胶体,胶体、溶液都可以透过滤纸,不能用过滤方
法分离,B错误;向沸水中滴加饱和FeCl 溶液可得到Fe(OH) 胶体,C错误;
3 3
FeCl 、FeCl 与NaOH反应生成Fe O 、H O和NaCl,离子方程式为Fe2++2Fe3++
2 3 3 4 2
8OH-===Fe O +4H O,D正确。
3 4 2
答案 D
3.下列事实与胶体性质无关的是( )
A.水泥厂和冶金厂常用高压直流电除去排放气体中的大量烟尘,减少对空气的污
染
B.将植物油倒入水中用力搅拌形成油水混合物
C.一束光通过长时间保存的Na SiO 溶液时出现光亮的“通路”
2 3
D.FeCl 溶液能使血液聚沉
3
解析 烟尘是气溶胶,其中的胶粒带电,在直流电作用下可产生电泳现象,使烟尘
沉降而除去,A正确;将植物油倒入水中用力搅拌形成的油水混合物是乳浊液,不是胶体,B错误;丁达尔效应是胶体特有的现象,长时间保存的Na SiO 溶液出现
2 3
丁达尔效应,说明长时间保存的Na SiO 溶液中SiO发生水解生成了H SiO 胶体,
2 3 2 3
C正确;血液是胶体,FeCl 是电解质,电解质溶液可以使胶体聚沉,D正确。
3
答案 B
【归纳总结】
净水剂及其作用原理
胶体粒子的直径一般在1~100 nm之间,它决定了胶体粒子具有较大的表面积,
吸附力很强,能在水中吸附悬浮固体或色素形成沉淀,从而达到净化水的目的,这
就是胶体净水的原理。能在水中自然形成胶体,并且对水质无明显副作用的物质
有KAl(SO ) ·12H O、FeCl ·6H O等,这样的物质被称为净水剂,其形成胶体的化
4 2 2 3 2
学原理是Al3+、Fe3+发生水解反应分别生成Al(OH) 胶体、Fe(OH) 胶体。
3 3
[B组 考试能力过关]
4.(2017·浙江卷)下列分散系能产生“丁达尔效应”的是( )
A.稀硫酸 B.硫酸铜溶液
C.氢氧化铁胶体 D.酒精溶液
解析 本题为容易题。“丁达尔效应”是胶体特有的性质,常用于鉴别胶体和其
他分散系。
答案 C
5.下列说法正确的是( )
A.(2016·课标全国Ⅱ)将NaOH浓溶液滴加到饱和FeCl 溶液中制备Fe(OH) 胶体
3 3
B.(2015·安徽理综,9B)Fe(OH) 胶体无色、透明,能产生丁达尔现象
3
C.(2014·重庆理综,3A)浓氨水中滴加FeCl 饱和溶液可制得Fe(OH) 胶体
3 3
D.(2014·福建理综,8D)用可见光束照射以区别溶液和胶体
答案 DINCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\分层课时作业.TIF" \* MERGEFORMATINET
[A级 全员必做题]
1.(2018·福建厦门外国语学校开学考试,7)化学在生活中应用广泛,下列物质性质
与对应用途错误的是( )
A.明矾易水解生成胶体,可用作净水剂
B.晶体硅熔点高硬度大,可用作芯片
C.氮气化学性质稳定,可用作粮食保护气
D.溴化银见光易分解,可用作胶片感光剂
解析 晶体硅为半导体,可用作芯片,B项错误。
答案 B
2.化学与人们的生产、生活密切相关,下列说法正确的是( )
A.人体摄入的糖类、油脂、蛋白质必须先经过水解才能吸收
B.爆竹爆炸产生的SO 、SO 等硫的氧化物对环境造成了严重污染
2 3
C.次氯酸盐、H O 、乙醇等物质可用于杀菌消毒是利用其强氧化性
2 2
D.利用“地沟油”可制备肥皂,变废为宝
解析 人体摄入的葡萄糖是单糖,不能水解,A项错误;爆竹爆炸过程中发生硫与
氧气的反应,但硫与氧气不能直接反应生成SO ,B项错误;乙醇杀菌消毒是因为
3
乙醇能使细菌蛋白脱水而变性,与强氧化性无关,C项错误;“地沟油”的主要成
分是油脂,碱性条件下水解生成高级脂肪酸盐,可制备肥皂,D项正确。
答案 D
3.氧元素是地壳中含量最多的元素。下列说法正确的是( )
A.16O 与18O 互为同位素
2 3
B.氧元素与其他短周期非金属元素均能形成酸性氧化物
C.氧与钠形成的化合物中,阴、阳离子个数比均为1∶2
D.O 变成O 以及16O变成18O的变化均属于化学变化
2 3
解析 同位素是同种元素不同原子之间的关系,16O 与18O 互为同素异形体,A项
2 3
错误;氧元素与氢元素形成的H O、H O 均不是酸性氧化物,B项错误;Na O和
2 2 2 2Na O (其阴离子为O)中,阴、阳离子个数比均为1∶2,C项正确;O 变成O 属于化
2 2 2 3
学变化,16O变成18O不属于化学变化,是核反应,D项错误。
答案 C
4.下列说法正确的是:①Fe(OH) 胶体和CuSO 溶液都是混合物;②BaSO 是一种
3 4 4
难溶于水的强电解质;③冰醋酸、纯碱、小苏打分别属于酸、碱、盐;④太阳能、氢
能和海洋能都属于新能源;⑤置换反应都属于离子反应。
A.①②④ B.①②⑤
C.②③④ D.③④⑤
解析 纯碱是Na CO ,是盐不是碱;不在溶液或熔融状态下发生的置换反应不是
2 3
离子反应,如C与Fe O 的反应。
2 3
答案 A
5.下列过程只发生物理变化的是( )
A.煤经过气化和液化等可得到清洁能源
B.在新购置的房子中放置竹炭,吸收有毒气体
C.用明矾的水溶液浸泡铜器可除去其表现的铜锈
D.用氢氟酸刻蚀玻璃制备工艺美术画
解析 煤的气化和液化均为化学变化,A项错误;竹炭,即用竹子烧制的炭,具有
吸附性,其吸收有毒气体的过程中只发生物理变化,B项正确;Al3+水解使溶液显
酸性,除去铜锈,发生化学变化,C项错误;氢氟酸刻蚀玻璃是HF与玻璃中的SiO
2
反应,是化学变化,D项错误。
答案 B
6.(2019·东北五校联考)下列有关物质、变化的说法中,正确的是( )
A.化学变化不产生新元素,产生新元素的变化不是化学变化
B.向煮沸的1 mol·L-1 NaOH溶液中滴加FeCl 饱和溶液制备Fe(OH) 胶体
3 3
C.有沉淀析出的变化一定是化学变化
D.液氯、乙醇、NH 均属于非电解质
3
解析 化学变化产生新物质,不产生新元素,反应前后元素的种类不变,因此产生
新元素的变化不是化学变化,A项正确;制备Fe(OH) 胶体,是向沸水中滴加饱和
3
FeCl 溶液并继续煮沸至液体呈红褐色,B项错误;有沉淀析出的变化不一定是化
3
学变化,如饱和溶液在外界条件变化时析出溶质,则发生的是物理变化,C项错误液氯属于单质,既不是电解质又不是非电解质,D项错误。
答案 A
7.(2018·福建晋江四校联考,1)现代生活需要人们有一定的科学素养,下列有关化
学的科学常识正确的是( )
A.铝的钝化、煤的气化、漂白粉杀菌消毒过程均有化学反应发生
B.碳酸钠可用于治疗胃酸过多、制备食品发酵剂
C.浓硫酸可刻蚀石英制艺术品
D.氢氧化铁胶体、淀粉溶液、NaCl溶液均具有丁达尔效应
解析 B项,治疗胃酸过多、制备食品发酵剂的是碳酸氢钠;C项,刻蚀石英制艺
术品的是氢氟酸;D项,NaCl溶液没有丁达尔效应。
答案 A
8.下列说法正确的是( )
A.不能发生丁达尔效应的分散系是溶液
B.将1 L 2 mol·L-1的FeCl 溶液制成胶体后,其中含有的氢氧化铁胶粒数为2N
3 A
C.纳米粒子的大小与胶体粒子相当,但纳米粒子的体系不一定是胶体
D.将饱和FeCl 溶液加热至沸腾,制得Fe(OH) 胶体
3 3
解析 不能发生丁达尔效应的分散系不一定是溶液,也可能是浊液,A项错误;由
于氢氧化铁胶粒是多个氢氧化铁的聚集体,故将1 L 2 mol·L-1的FeCl 溶液制成
3
胶体后,其中含有的氢氧化铁胶粒数小于2N ,B项错误;胶体是指分散质粒子直
A
径在1~100 nm之间的分散系,属于混合物,纳米粒子的大小与胶体粒子相当,但
纳米粒子的体系不一定是胶体,C项正确;制备Fe(OH) 胶体的操作是:向沸水中
3
逐滴滴加饱和FeCl 溶液,煮沸至溶液呈红褐色,即停止加热,D项错误。
3
答案 C
9.(2019·福建福州八县(市)协作校联考,4)下列关于胶体的叙述不正确的是( )
A.胶体区别于其他分散系的本质特征是丁达尔现象
B.Fe(OH) 胶体能够使水中悬浮的固体颗粒沉降,达到净水的目的
3
C.往Fe(OH) 胶体中逐滴加入稀硫酸时,开始时会出现沉淀,再继续滴加时,沉淀
3
又会消失
D.用盐卤点豆腐、河海交汇处可沉积成沙洲等都与胶体性质有关
解析 胶体区别于其他分散系的本质特征是胶体粒子直径在 1~100 nm之间,A项错误;Fe(OH) 胶体的表面积较大,能吸附水中悬浮的固体颗粒达到净水的目的,
3
B项正确;电解质溶液能使胶体聚沉,故往Fe(OH) 胶体中逐滴加入稀硫酸时,开
3
始产生氢氧化铁沉淀,继续滴加稀硫酸,氢氧化铁与稀硫酸发生中和反应而溶解,
C项正确;用盐卤点豆腐、河海交汇处可沉积成沙洲等都与胶体的聚沉有关,D项
正确。
答案 A
10.(2018·山东青岛一模,7)华夏文明源远流长,勤劳智慧的中国人民探索认知世界,
创造美好生活的过程贯穿始终。以下说法从化学视角理解,错误的是( )
A 日照澄洲江雾开,淘金女伴满江隈(唐) 诗中包含了丁达尔现象
B 高奴出脂水,颇似淳漆,燃之如麻(宋) 文中提到的“脂水”是指油脂
C 水银乃至阴毒物,因火煅丹砂而出(明) 这段记载中,涉及氧化还原反应
制玻璃的某成分可用于制造光导
D 百宝都从海舶来,玻璃大镜比门排(清)
纤维
解析 A项,雾属于胶体,可见光通过时会出现丁达尔现象,正确;B项,根据描述
可知“脂水”指的是石油,错误;C项,丹砂的主要成分是HgS,由丹砂煅烧制水
银(Hg),涉及氧化还原反应,正确;D项,制玻璃的成分二氧化硅可用于制造光导
纤维,正确。
答案 B
11.宋代《本草图经》中记载: “取此一物,置于铁板上,聚炭封之,囊袋吹令火炽
其矾即沸,流出色赤如融金汁者是真也。看沸定汁尽,去火待冷,取出挼为末,色似
黄丹,收之。”下列说法错误的是( )
A.文中“矾”的化学式是FeSO ·7H O
4 2
B.“色赤”的物质可能是Fe O
2 3
C.“矾”受热分解时硫元素都表现氧化性
D.可通过焰色反应区分“矾”和朴硝(Na SO ·10H O)
2 4 2
解析 “矾”指绿矾,其化学式是FeSO ·7H O,A项正确;“色赤”说明产物为红
4 2
色,FeSO ·7H O中含有铁元素,其分解产物Fe O 为红色,B项正确;根据氧化还
4 2 2 3
原反应原理及产物 Fe O 可知“矾”受热分解反应的化学方程 式为
2 3
2FeSO ·7H O=====Fe O +SO ↑+SO ↑+14H O↑,只有部分S元素表现氧化
4 2 2 3 2 3 2
性,C项错误;由于朴硝中含有钠元素,因此可用焰色反应区分“矾”和朴硝。
答案 C12.A、B、C、X均为中学化学常见的物质,它们之间有如下转化关系(其他产物已略
去):
下列说法不正确的是( )
A.若A是NH ,则C可能是氧化物
3
B.若A是非金属单质,则C与水反应的生成物为强酸
C.若X是金属单质,则B、C中X的化合价可能是B>C
D.若X是强碱,则B可能是两性物质
解析 A、B、C、X可以分别为NH 、NO、NO 、O ,A项正确;A、B、C、X可以分别
3 2 2
为S、SO 、SO 、O ,C与水反应的生成物为强酸,或A、B、C、X可以分别为C、
2 3 2
CO、CO 、O ,C与水反应的生成物为弱酸,B项错误;A、B、C、X可以分别为Cl 、
2 2 2
FeCl 、FeCl 、Fe,则B、C中铁的化合价B>C,C项正确;A、B、C、X可以分别为
3 2
AlCl 、Al(OH) 、NaAlO 、NaOH,Al(OH) 是两性物质,D项正确。
3 3 2 3
答案 B
13.按要求回答下列问题。
(1)下面是某同学对有关物质进行分类的列表:
碱性氧 酸性氧
碱 酸 盐
化物 化物
第一组 Na CO H SO NaHCO CaO CO
2 3 2 4 3 2
第二组 NaOH HCl NaCl Na O CO
2
第三组 KOH CH COOH CaF Al O SO
3 2 2 3 2
每组分类均有错误,其错误的物质分别是________、________、________。(填化学
式)
(2)鉴别胶体和溶液所采用的方法是观察是否能发生________现象。
(3)一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段
时间后,测得有关数据如表所示:
物质 M N Q P反应前质量/g 50 1 3 12
反应后质量/g x 26 3 30
①该变化的基本反应类型是________反应。
②物质Q在反应中起的作用是________。
解析 (1)第一组中的Na CO 是盐;第二组中的CO不是酸性氧化物;第三组中的
2 3
Al O 是两性氧化物。(2)胶体具有丁达尔效应,而溶液不具有。(3)①由质量守恒可
2 3
得,x=7,则N和P的质量增加,二者是生成物,M是反应物,所以该反应是分解
反应。②反应前后Q的质量不变,故Q是催化剂,起催化作用。
答案 (1)Na CO CO Al O (2)丁达尔
2 3 2 3
(3)①分解 ②催化作用
[B级 拔高选做题]
14.分类法是一种行之有效、简单易行的科学方法,某同学用如表所示的形式对所
学知识进行分类,其中甲与乙、丙、丁、戊是包含关系。
选项 甲 乙、丙、丁、戊
① 常见干燥剂 浓硫酸、石灰石、碱石灰、五氧化二磷
② 常见合金 不锈钢、青铜、硬铝、生铁
③ 基本营养物质 油脂、蛋白质、纤维素、无机盐
④ 腐蚀品 盐酸、浓硫酸、烧碱、硝酸
⑤ 碱性氧化物 过氧化钠、氧化镁、氧化铝、氧化铁
⑥ 弱电解质 次氯酸、一水合氨、水、醋酸
正确的组合是( )
A.①② B.④⑤⑥
C.②④⑥ D.①⑤⑥
解析 ①中,石灰石不具备吸水性,不能作干燥剂;③中,纤维素不能被人体吸收,
不属于营养物质;⑤中,过氧化钠不是碱性氧化物,氧化铝是两性氧化物,C项正
确。
答案 C
15.《本草纲目》记载了利尿剂甘汞(Hg Cl )的制法:“用水银一两,白矾
2 2
[KAl(SO ) ·12H O]二两,食盐一两,同研不见星,铺于铁器内,以小乌盆覆之。筛灶
4 2 2
灰,盐水和,封固盆口。以炭打二炷香取开,则粉升于盆上矣。其白如雪,轻盈可爱。
一两汞,可升粉八钱。”下列叙述错误的是(Hg的相对原子质量为201)( )A.上述制法中,使用了升华法分离甘汞
B.甘汞是共价化合物,化学名称为氯化亚汞
C.制备甘汞的反应中,n(氧化剂)∶n(还原剂)=4∶1
D.若题中1两等于10钱,则甘汞的产率约为68%
解析 甘汞加热可以升华,为共价化合物;汞不活泼,KAl(SO ) ·12H O和NaCl无
4 2 2
法氧化汞,则空气中的O 作氧化剂,1 mol O 得到4 mol电子,1 mol Hg被氧化为
2 2
Hg Cl 失去1 mol电子,根据得失电子守恒,n(氧化剂)∶n(还原剂)=1∶4,设10
2 2
钱汞理论上制得甘汞的质量为x,由关系式2Hg~Hg Cl 可知=,解得x≈11.77钱,
2 2
而1两汞实际可得8钱甘汞,甘汞的产率为8钱÷11.77钱×100%≈68%。
答案 C
16.(原创改编)短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素
组成的二元化合物,其中p是天然气的主要成分。n是元素Z的单质,通常为黄绿
色气体,q的水溶液具有漂白性,0.01 mol·L-1r溶液的pH为2,s通常是难溶于水
的混合物。上述物质的转化关系如图所示。
(1)m、p、q、r的分子式分别为________、________、________、________。s的成分
有_____________________________________________________________
(写分子式)。
(2)q的水溶液和明矾均可净水,其原理相同吗?________,明矾的净水原理是
_____________________________________________________________________。
(3)n+m→q+r是置换反应吗?__________________________________________。
为什么?__________________________________________________________。
(4)证明酸性H CO >q的化学方程式为____________________________________
2 3
_____________________________________________________________________
。
(5)非金属氧化物都是酸性氧化物吗?酸性氧化物都能与水反应生成相应的酸吗?
试举例说明。_________________________________________________________________________________________________________________________。
答案 (1)H O CH HClO HCl CH Cl、CH Cl 、CHCl 、CCl
2 4 3 2 2 3 4
(2)不相同 明矾水解生成Al(OH) 胶体,吸附水中悬浮物而净水 (3)不是 产物
3
中无单质生成
(4)NaClO+CO +H O===NaHCO +HClO
2 2 3
(5)非金属氧化物不都是酸性氧化物,例如:CO、NO、NO 等,不是酸性氧化物;酸
2
性氧化物不一定都能与水反应生成相应的酸,例如:SiO 是酸性氧化物,但其不与
2
水反应