文档内容
考点 06 物质的量 气体摩尔体积
目录
................................................................................................................................................1
1.高考真题考点分布......................................................................................................................................1
2.命题规律及备考策略..................................................................................................................................1
................................................................................................................................................2
考法01 物质的量、阿伏加德罗常数.........................................................................................................2
考法02 摩尔质量..........................................................................................................................................3
考法03 气体摩尔体积..................................................................................................................................5
考法04 有关阿伏加德罗常数的正误判断.................................................................................................9
..............................................................................................................................................14
1.高考真题考点分布
考点内容 考点分布
2023辽宁卷5题,3分;2023全国甲卷10题,6分;2023浙江6月7题,3
分;2022福建卷5题,4分;2022重庆卷5题,32分;2022全国甲卷11
题,6分;2022浙江6月12题,2分;2022浙江1月12题,2分;2022海南
阿伏加德罗常数 卷7题,3分;2022辽宁卷3题,3分;2021全国甲卷8题,6分;2021浙江
6月18题,2分;2021湖南卷5题,3分;2021河北卷7题,3分;2021广
东卷11题,4分;2021天津卷7题,4分;2021浙江1月18题,2分;2021
湖北卷6题,3分;2021海南卷7题,3分
阿伏加德罗定律 2021年山东卷6题,3分
2.命题规律及备考策略
【命题规律】
分析近几年高考试题,有关化学计量主要体现在单独考查 N 及化学计算中。选择题常与电离平衡、氧化
A
还原反应、化学反应中的能量变化等考点结合进行考查;填空题保持实验题、反应原理题等融合,涉及物
质的量及阿伏加德罗定律的灵活运用。
【备考策略】
1.了解物质的量及其单位、摩尔质量、气体摩尔体积、物质的量浓度、阿伏伽德罗常数的含义;2.能根据微粒(原子、分子、离子等)物质的量、数目、气体体积(标准状况下)之间的相互关系进行有关计
算;
3.正确判断有关阿伏加德罗常数正误的“三大步骤”
第一步:查看物质的状态及所处状况——正确运用气体摩尔体积的前提;
第二步:分析题干所给物理量与物质的量的关系——正确进行换算的前提;
第三步:准确把握物质的微观结构和物质变化过程中微粒数目的变化——正确判断微粒数目的前提。
【命题预测】
预计2025年依旧关注N 考查的常见角度,如物质结构、氧化还原反应、盐类水解、有机物结构等;填空
A
题中往往渗透于化学平衡计算、物质的组成或含量的计算,充分利用化学计算技法,如守恒法、关系式法
等。
考法01 物质的量、阿伏加德罗常数
1.物质的量(n)
表示含有一定数目粒子的集合体的物理量,单位为_______。
2.物质的量的规范表示方法:
3.阿伏加德罗常数(N )
A
1mol任何粒子的粒子数叫做阿伏加德罗常数,符号为_______,通常用6.02×1023mol-1表示。公式:N =
A
_______。
【易错提醒】
专有化:“物质的量”四个字是一个整体的物理量名词,不能说成“物质量”或“物质的数量”等。
微观化:只用来描述微观粒子,如原子、分子、离子、中子、质子、电子等及这些粒子的特定组合,如
NaCl;不能表示宏观的物质。
具体化:必须指明具体粒子的种类,常用化学式表示,如“1 mol O”“2 mol O ”“1.5 mol O ”;不能说“1
2 3
mol氧”。
集体化:物质的量可以表示多个微粒的特定组合或集合体,如1 mol NaCl、0.5 mol HSO 。
2 4
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)摩尔是物质的量的单位( )
(2)1 mol NaCl和1 mol HCl含有相同的粒子数目( )
(3)1 mol任何物质都含有6.02×1023个分子( )
(4)1 mol水中含有2 mol氢和1 mol氧( )(5)阿伏加德罗常数(N )就是6.02×1023( )
A
(6)0.012 kg 12C中约含有6.02×1023个碳原子( )
考向 考查有关“物质的量”概念理解与辨析
【例】下列对摩尔(mol)的有关说法中错误的是( )
A.摩尔是一个单位而非物理量
B.摩尔既能用来计量纯净物,又能用来计量混合物
C.1mol任何气体所含气体的分子数目都相等
D.0.5mol氦约含有1.204×1024个电子
【名师点睛】
本题考查的是物质中含有的各种粒子或微观结构的问题,一般来说先计算物质基本微粒中含有多少个需要
计算的粒子或微观结构,再乘以该物质的物质的量,就可以计算出相应结果,稀有气体分子都是单原子分
子。
【对点】下列有关叙述正确的是( )
A.1 mol任何物质都含有6.02×1023个分子
B.硫酸的摩尔质量为98 g
C.2 mol H O是1 mol H O摩尔质量的2倍
2 2
D.摩尔是物质的量的单位
考法02 摩尔质量
1.定义:单位物质的量的物质所具有的质量。常用的单位是_______。公式:M=_______。
2.数值:以 g·mol-1为单位时,任何粒子的摩尔质量在数值上都_______该粒子的相对分子(原子)质量。
【易错提醒】
1.摩尔质量只是以 g·mol-1作单位时,在数值上与该粒子的相对分子质量或相对原子质量相等。
2.由于电子的质量非常微小,所以离子的摩尔质量以 g·mol-1 为单位时,其数值近似等于该离子的相对分
子质量或相对原子质量,如Na和Na+的摩尔质量都为23 g·mol-1。
3.对于指定的物质来说,其摩尔质量的值是一个定值,不随物质的物质的量多少而改变。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)硫酸的摩尔质量为98 g( )
(2)2 mol H O是1 mol H O摩尔质量的2倍( )
2 2
(3)NaOH的摩尔质量为40 g( )
(4)1 mol O 的质量与它的相对分子质量相等( )
2
(5)1 mol OH-的质量为17 g·mol-1( )
(6)氖气的摩尔质量(单位g·mol-1)在数值上等于它的相对原子质量( )(7)2 mol H O的摩尔质量是1 mol H O的摩尔质量的2倍( )
2 2
(8)相同质量的CO与N 所含分子数、原子数均相同( )
2
(9)17 g —OH与17 g OH-所含电子数均为10N ( )
A
(10)31 g白磷中所含共价键数目为N ( )
A
(11)30 g SiO 中含有硅氧键个数为N ( )
2 A
(12)32 g甲醇中所含共价键数目为5N ( )
A
考向01 考查摩尔质量
【例1】偏二甲肼(C HN)是一种高能燃料,燃烧产生的巨大能量可为航天运载火箭提供推动力。下列叙述
2 8 2
正确的是( )
A.偏二甲肼的摩尔质量为60 g
B.6.02×1023个偏二甲肼分子的质量约为60 g
C.1 mol偏二甲肼的质量为60 g· mol-1
D.6 g偏二甲肼含有N 个偏二甲肼分子
A
【名师点睛】
1.同种物质的摩尔质量、相对原子(分子)质量、1 mol该物质的质量在数值上是相等的,但含义不同,三者
的单位也不同。摩尔质量的单位为 g· mol-1,相对原子(分子)质量的单位为1,1 mol该物质的质量单位为
g。
2.对于具体的物质,其摩尔质量是确定的,不随物质的量的多少而变化,也不随物质的聚集状态的变化
而变化。
考向02 物质的量、质量、微粒数之间的关系
【例2】下列叙述正确的是( )
A.24 g镁与27 g铝含有相同的质子数
B.等质量的氧气和臭氧,电子数相同
C.1 mol重水与1 mol水中,中子数比为2∶1
D.1 mol乙烷和1 mol乙烯,化学键数目相同
【对点01】某硫原子的质量是a g,12C原子的质量是b g,若N 表示阿伏加德罗常数的值,则下列说法正
A
确的是( )
12b
A.该硫原子的相对原子质量为
a
m
B.m g该硫原子的物质的量为 mol
aN
A
C.该硫原子的摩尔质量是aN g
A
D.a g该硫原子中所含的电子数目为16N
A
【对点02】(1)某氯原子的质量是a g,12C原子的质量是b g,用N 表示阿伏加德罗常数的值。
A①该氯原子的相对原子质量为________;
②该氯原子的摩尔质量是________;
③m g该氯原子的物质的量为________;
④n g该氯原子所含的电子数为________。
(2)12.4 g Na R含Na+ 0.4 mol,则NaR的摩尔质量为________,R的相对原子质量为________。含R的质
2 2
量为1.6 g的NaR,其物质的量为________。
2
【思维建模】
记住特殊物质中1 mol物质所含微粒(分子、原子、电子、质子、中子等)的数目,如Ne、DO、18O 、—
2 2
OH、OH-等)
考法03 气体摩尔体积
1.影响物质体积大小的因素
①粒子的大小(物质的本性);
②粒子间距的大小(由温度与压强共同决定);
③粒子的数目(物质的量的大小)。
2.气体摩尔体积
(1)含义:单位物质的量的气体所占的体积,符号为V ,标准状况下,V 约为______________。
m m
(2)常用单位:L/mol(或L·mol-1)。
(3)数值:在_______下(指温度为0℃,压强为101 kPa)约为22.4 L·mol-1。
(4)基本关系式:n===
(5)影响因素:气体摩尔体积的数值不是固定不变的,它决定于气体所处的_______和_______。
(6)适用对象:单一气体或互不反应的混合气体
【特别提醒】
(1)1个条件:必须为标准状况。非标准状况下,1 mol气体的体积不一定是22.4 L。
(2)1种状态:必须为气态。如水、酒精、SO 、CCl 等物质在标准状况下不是气体。
3 4
(3)2个数据:“1 mol”,“约为22.4 L”。
3.阿伏加德罗定律及其推论
(1)阿伏加德罗定律:在相同的温度和压强下,相同体积的任何气体,含有相同数目的粒子(或气体的物质
的量相同)。
【名师提醒】
可总结为:“三同”定“一同”,即同温、同压下,同体积的任何气体具有相同的分子数。
(2)阿伏加德罗定律的推论(以下用到的符号:ρ为密度,p为压强,n为物质的量,M为摩尔质量,m为质
量,V为体积,T为热力学温度)
条件 推论公式 语言叙述
T、p相同 = 同温、同压下,气体的体积与其物质的量成正比
T、V相同 = 温度、体积相同的气体,其压强与其物质的量成正比T、p相同 = 同温、同压下,气体的密度与其摩尔质量(或相对分子质量)成正比
T、p、m相
= 同温同压下,相同质量的任何气体的体积与它们的摩尔质量成反比
同
T、V、m相
= 同温同体积时,相同质量的任何气体的压强与它们的摩尔质量成反比
同
T、p、V相 同温同压下,同体积的任何气体的质量比等于它们的摩尔质量之比,
==
同 也等于它们的密度之比
【方法技巧】
1.适用于任何气体,包括混合气体,但不适用于非气体。
2.推论可利用pV=nRT和n===推导(其中p为压强,V为气体的体积,R为常数。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)标准状况下,H 和N 的气体摩尔体积均为22.4 L( )
2 2
(2)在标准状况下,1 mol O 与1 mol SO 的体积相同( )
2 3
(3)在同温同压下,22.4 L的任何气体的物质的量都是1 mol( )
(4)在标准状况下,1 mol O 与1 mol SO 的体积相同( )
2 3
(5)在标准状况下,氢气的气体摩尔体积为22.4 L( )
(6)在相同条件下,相同体积的CO、N 的混合气体与O 的分子个数相同,原子个数也相同( )
2 2
(7)温度相同、体积相同的O(g)和N(g)所含的分子数一定相同( )
2 2
(8)等温等压下,SO 气体与CO 气体的密度之比等于16∶11( )
2 2
(9)标准状况下,1 mol氢气所占的体积是0.5 mol氧气所占的2倍( )
(10)温度和容积相同的两容器中分别盛有5 mol O 和2 mol N ,则压强之比为5∶2( )
2 2
(11)标准状况下,0.5 mol氢气和0.5 mol氧气组成的混合气体的体积约为22.4 L( )
(12)标准状况下,1 mol气体的体积约是22.4 L,如果当1 mol气体的体积约是22.4 L时,则该气体所处的状
况一定是标准状况( )
考向1 气体摩尔体积
【例1】CH 与Cl 光照条件下充分反应生成一系列卤代烃,设N 为阿伏加德罗常数的值。下列说法正确
4 2 A
的是( )
A.标准状况下,22.4 L CHCl 含有的氯原子数为3N
3 A
B.标准状况下,22.4 L Cl 完全反应后得到的HCl分子数为2N
2 A
C.16 g CH 与足量Cl 充分反应后得到的卤代烃分子总数为N
4 2 A
D.1 mol CH 和1 mol Cl 充分反应可以得到CHCl的分子数为N
4 2 3 A
【思维建模】
“四看法”突破气体摩尔体积(标准状况下)的有关计算一看物质的状态是否为气态 V 适用于计算气体的物质的量
m
二看温度和压强是否处于标准状况 V =22.4 L·mol-1适用于标准状况(0 ℃、101 kPa),不适用于常
m
温常压
三看气体分子的组成 根据气体分子组成确定原子数、质子数、电子数
四看物质量的关系 根据恒等式“n=N/N =m/M=V/V ”进行简单计算
A m
考向2 阿伏加德罗定律及应用
【例2】(2024•重庆市期中)某密闭刚性容器由可动活塞隔成甲、乙两室,室温下向甲中充入由H 和O 组成
2 2
的混合气体19g,向乙中充入1mol空气,此时活塞的位置如图所示。下列有关说法正确的是( )
A.甲室混合气体的分子总数为3N
A
B.甲室H、O 的物质的量之比为1:3
2 2
C.甲室混合气体的密度是同温同压下H 密度的9.5倍
2
D.若将甲室气体点燃引爆并恢复至室温,忽略生成水的体积,活塞最终停留在刻度2处
【思维建模】
解答阿伏加德罗定律及推论题的思维模板
第一步 分析“条件” 分析题干中的条件(同温同压、同温同容),找出异同
第二步 明确“要求” 析题目要求,明确要求的比例关系,如压强、物质的量、密度等
第三步 利用“规律” 利用阿伏加德罗定律及其推论,根据条件和要求进行分析、判断
考向3 气体摩尔质量计算的常用方法
【例3】按要求解答问题
(1)已知标准状况下,气体A的密度为2.857 g·L-1,则气体A的相对分子质量为_______,可能是_______气
体。
(2)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为_______。
(3)CO和CO 的混合气体18 g,完全燃烧后测得CO 体积为11.2 L(标准状况),则
2 2
①混合气体在标准状况下的密度是_______g·L-1。
②混合气体的平均摩尔质量是_______ g·mol-1。
【思维建模】
1.根据物质的质量(m)和物质的量(n):M=
N ⋅m
M= A
N
2.根据一定质量(m)的物质中微粒数目(N)和阿伏加德罗常数(N ):
A
3.根据一个粒子的质量(m)和阿伏加德罗常数(N ):M=N ·m
A A
4.M在数值上和相对原子(M)相等:M(相对原子质量)=
r r
5.根据标准状况下气体的密度ρ:M=ρ×22.4 L·mol-1
6.根据气体的相对密度(D=ρ/ρ ):=D
1 2【对点01】(2024·黑龙江哈尔滨·三模)设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.等物质的量的C H 和C HO完全燃烧,消耗O 分子数目均为3N
2 4 2 6 2 A
B.NaO 与CO 反应生成标准状况下O44.8L,转移电子数目为4N
2 2 2 2 A
C.25℃,1LpH=12的Ba(OH) 溶液中含有OH-数目为0.02N
2 A
D.标准状况下,22.4 mLCHCl 中含有碳原子数目为10-3N
2 2 A
【对点02】(2024•湖南省长沙市开学考试)同温同压下,质量忽略不计的两气球A和B,分别充入X气体和
Y气体,且充气后两气球的体积相同。若相同条件下,A气球放在CO中下沉,B气球放在O 中上浮。下
2
列叙述或表示正确的是( )
A.X气体的相对分子质量比Y气体的相对分子质量大
B.X可能是CO,Y可能是CH
2 4
C.X气体的密度小于Y气体的密度
D.充气后A气球质量比B气球质量大
【对点03】在一定条件下,m g NHHCO 完全分解生成NH 、CO、HO(g),按要求填空。
4 3 3 2 2
(1)若所得混合气体对H 的相对密度为d,则混合气体的物质的量为 。NH HCO 的摩尔质量为
2 4 3
(用含m、d的代数式表示)。
(2)若所得混合气体的密度折合成标准状况为ρ g·L-1,则混合气体的平均摩尔质量为 (用
含ρ的代数式表示)。
(3)若在该条件下,所得NH 、CO 、HO(g)的体积分数分别为a%、b%、c%,则混合气体的平均相对分子
3 2 2
质量为 (用含a、b、c的代数式表示)。
考法04 有关阿伏加德罗常数的正误判断
一、气体与状况陷阱
二、“组成和结构”陷阱
1.一定混合物中分子、原子数目的判断
(1)等质量的实验式相同的物质含有的原子数相同,如NO 与NO、C H 与C H、O 与O。
2 2 4 2 4 3 6 2 3
(2)等质量的摩尔质量相同的物质含有的分子数相同,如N 与CO、CO 与NO、HSO 与HPO 。
2 2 2 2 4 3 4
(3)等物质的量的CO 与SO 中氧原子数相同。
2 22.有关物质的组成与化学键结构的关注点
(1)物质的构成
有些物质是由分子构成的,分子又是由原子构成的。有的分子是单原子分子,如稀有气体 He、Ne等;有
的分子为双原子分子,如Cl 、N 、O 、H 、Br 、I 等;有的分子为多原子分子,如O 、P 、HO、CH 、
2 2 2 2 2 2 3 4 2 4
CO 等。
2
(2)物质的微观结构
记特殊物质中所含粒子(分子、原子、电子、质子、中子等)的数目,如Ne、DO、18O、—OH、OH-等。
2 2
(3)物质中所含的化学键
理解物质中所含化学键的数目,如一分子HO、C H 中化学键的数目分别为3、3n+1。
2 2 n 2n+2
常考物质中所含共价键数目说明:
CH P Si SiO 石墨 金刚石
4 4 2
几种常考物质
(C—H) (P—P) (Si—Si) (Si—O) (C—C) (C—C)
每摩尔含共价键数目 4N 6N 2N 4N 1.5N 2N
A A A A A A
三、氧化还原反应中电子转移的陷阱
1.关注特殊反应
(1)Na O 与水或CO 反应,产生1 mol O 均转移2 mol电子。
2 2 2 2
(2)铁与硝酸反应时,常温下在浓硝酸中钝化,溶于足量稀硝酸生成Fe(NO ),硝酸不足时生成Fe(NO )。
3 3 3 2
2
(3)NO 与HO反应,当1 mol NO 参加反应时,转移电子 mol。
2 2 2 3
(4)氯气与足量NaOH溶液反应,1 mol Cl 转移1 mol电子;氯气与足量金属反应,1 mol Cl 转移2 mol电
2 2
子。
2.明确反应实质
Na、Mg、Al在化合物中的化合价分别为+1、+2、+3,因此1 mol Na与足量O 反应,无论生成NaO还是
2 2
NaO ,均转移1 mol电子;1 mol Mg与足量O 、N 、盐酸等物质反应,均转移2 mol电子;1 mol Al无论
2 2 2 2
溶于足量盐酸还是足量NaOH溶液,均转移3 mol电子。
3.注意过量问题
如向含1 mol FeBr 的溶液中通少量Cl 和通足量Cl,转移的电子数不一样。
2 2 2
四、突破特殊反应(或隐含反应)设置的陷阱
1.特殊的反应——可逆反应
若反应为可逆反应,则反应物不能完全转化,常考的可逆反应有:
(1)N +3H 2NH
2 2 3
(2)2SO +O 2SO
2 2 3
(3)Cl +H O HCl+HClO
2 2
(4)2NO NO
2 2 4
(5)H +I 2HI
2 2
(6)酯化反应及酯的水解反应2.特殊的变化——浓度因素
(1)足量MnO 与浓盐酸反应,随着反应的进行,浓盐酸变稀盐酸,反应停止。
2
(2)足量Cu与浓HSO 反应,随着反应的进行,浓硫酸变稀硫酸,反应停止。
2 4
(3)足量Cu与浓HNO 反应,随着反应的进行,浓硝酸变稀硝酸,得到NO 和NO的混合气体。
3 2
(4)足量Zn与浓HSO 反应,随着反应的进行,浓硫酸变稀硫酸,得到SO 和H 的混合气体。
2 4 2 2
(5)常温下,铁、铝遇浓硝酸、浓硫酸发生“钝化”。
五、突破电解质溶液中离子变化陷阱
弱电解质的电离 弱电解质不能完全电离,要注意电离产生的离子的浓度
盐类的水解 弱碱阳离子、弱酸根离子发生水解,导致相应离子数目发生变化
溶液的体积 有些题目未告知溶液的体积,不能将溶液体积看作1 L进行计算
(1)注意所给条件是否与电解质的组成有关,如 pH=3的 HSO 溶液中 c(H+)=10-3 mol·L-1,与电解质组成无
2 3
关。
(2)多元弱酸根离子发生水解,溶液中阴离子的数目增加;多元弱碱阳离子发生水解,溶液中阳离子数目增
加。
(3)求溶液中所含氢、氧原子数目时,不要忽略溶剂水中的氢、氧原子数目。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1) 常温常压下,11.2 L SO 含有的氧原子数小于N ( )
2 A
(2)标准状况下,18 g HO所含的氧原子数目为N ( )
2 A
(3)室温下,1 mol CH 中含有5N 原子( )
4 A
(4)常温常压下,1 mol CO 与SO 的混合气体中含氧原子数为2N ( )
2 2 A
(5)2 g石墨晶体中,含有的质子数目为6N ( )
A
(6)2 mol SO 和1 mol O 在一定条件下充分反应后,混合物的分子数为2N ( )
2 2 A
(7)密闭容器中2a mol NO与a mol O 充分反应,产物的分子数为2aN ( )
2 A
(8)标准状况下,0.1 mol Cl 溶于水,转移的电子数目为0.1N ( )
2 A
(9)1 L 0.1 mol·L-1的氨水中有N 个NH( )
A
(10)向含4 mol HCl的浓盐酸中,加入足量的MnO ,加热,充分反应后,生成N 个Cl( )
2 A 2
(11)用含有1 mol FeCl 的溶液充分反应后得的Fe(OH) 胶体中含有N 个Fe(OH) 胶粒( )
3 3 A 3
(12)48 g正丁烷和10 g异丁烷的混合物中共价键的数目为13N ( )
A
(13)10 g质量分数为34%的HO 溶液含有的氢原子数为0.2N ( )
2 2 A
(14)2 mol冰醋酸与4 mol乙醇一定条件下充分反应,生成乙酸乙酯的个数为2N ( )
A
(15)在反应KClO+8HCl=KCl+4Cl ↑+4H O中,每生成4 mol Cl 转移的电子数为8N ( )
4 2 2 2 A
考向1 通过结构特点考查微粒数目
【例1】(2024·河北卷,4)超氧化钾(KO )可用作潜水或宇航装置的CO 吸收剂和供氧剂,反应为
2 24KO +2CO =2K CO+O ,N 为阿伏加德罗常数的值。下列说法正确的是( )
2 2 2 3 2 A
A.44gCO 中 键的数目为2N
2 A
B.1mol KO 晶体中离子的数目为3N
2 A
C.1 L1mol·L-1 KCO 溶液中CO2-的数目为N
2 3 3 A
D.该反应中每转移1mol电子生成O 的数目为1.5N
2 A
【思维建模】
考向2 考查化学键数
【例2】(2024·贵州省部分学校高考信息考试)柴油汽车常用尿素( )溶液处理尾气,发生
反应:4NO+O +2CO(NH )=4N +2CO +4H O。设N 表示阿伏加德罗常数的值,下列说法正确的是( )
2 2 2 2 2 2 A
A.上述反应涉及的元素中,基态原子第一电离能最大的为O
B.常温下,22.4LCO 含有共用电子对数目为4 N
2 A
C.反应4 mol NO时转移的电子数目为8 N
A
D.1个尿素分子中含有7个 键
【名师点睛】
应熟知常考物质的结构式,如苯环中不含有碳碳双键;1 mol Na O 含O是1 mol; 1 mol 白磷(P )中含有
2 2 4
的P—P键的数目为6N 。
A
考向3 结合氧化还原反应考查转移电子
【例3】N 表示阿伏加德罗常数的值。下列说法正确的是( )
A
A.一定条件下,2.3 g Na与O 完全反应生成3.6 g产物时失去的电子数为0.1N
2 A
B.电解精炼铜时,当电路中转移N 个电子时,阳极溶解32 g铜
A
C.用浓盐酸分别和KMnO 、KClO 反应制备1 mol氯气,转移的电子数均为2N
4 3 A
D.5.6 g Fe粉与足量S粉加热充分反应转移的电子数为0.3N
A
【名师点睛】
1.要注意特殊物质,如由过氧化钠、过氧化氢制取1 mol氧气转移2 mol电子;
2.铁与硫、碘、非氧化性酸反应,1 mol铁转移2 mol电子;1 mol铁与足量的氯气、稀硝酸反应,转移3mol电子;
3.要注意反应顺序、反应限度。
考向4 通过隐含过程的可逆性考查粒子数目
【例4】设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.2 mol·L-1的AlCl 溶液中含有Al3+的数目小于2N
3 A
B.常温常压下,2.2 g CO 和NO的混合气体含有的原子数为0.15N
2 2 A
C.300 mL 2 mol·L-1蔗糖溶液中所含分子数为0.6N
A
D.在密闭容器中通入2 mol SO 和1 mol O ,一定条件下充分反应生成SO 的分子数为2N
2 2 3 A
【对点01】N 表示阿伏加德罗常数的值,下列说法正确的是( )
A
A.1 L 0.1 mol·L-1的AlCl 溶液中含有Al3+的数目为0.1N
3 A
B.常温常压下,2.0 g HO和DO中含有的电子数一定为N
2 A
C.常温常压下,31 g白磷燃烧生成PO 时,断裂P—P键的数目为N
4 6 A
D.0.1 mol NaHCO 晶体中阴、阳离子总数为0.3N
3 A
【对点02】(2024•福建省十一所学校高三联考)光催化CO 转化与选择性有机合成耦合到同一反应系统中,
2
具有实现可持续经济和社会发展目标的潜力。其中某种反应如下,设 N 为阿伏加德罗常数的值,下列说
A
法正确的是( )
CO+2n n +nNH +H O+CO+xH
2 3 2 2
A.该反应为缩聚反应
B.1mol CO 含有的 键数为4 N
2 A
C.1mol 含有的碳碳双键数为3 N
A
D.该反应每消耗1mol CO,生成 分子的数目为
2
【对点03】N 表示阿伏加德罗常数的值。下列说法不正确的是( )
A
A.0.1 mol Fe和0.1 mol Cu分别与0.1 mol Cl 完全反应,转移电子数均为0.2N
2 A
B.用NaO 与CO 反应或KMnO 分解制得1 mol O ,转移的电子数均为4N
2 2 2 4 2 A
C.标准状况下,锌与某浓度的HSO 反应生成11.2 L气体,反应中转移的电子数为6.02×1023
2 4
D.在2CuH+2HCl===CuCl +Cu+2H↑反应中,每生成22.4 L(标况)H ,反应转移的电子为1.5N
2 2 2 A
【对点04】N 表示阿伏加德罗常数的值。下列说法正确的是( )
A
A.标准状况下,33.6 mL氯气通入足量水中发生反应,转移电子数为1.5×10-3N
A
B.1 mol N 与3 mol H 充分反应后,生成0.5 mol NH ,转移1.5N 个电子
2 2 3 A
C.常温常压下,0.1 mol·L-1的NaHCO 溶液中含有的HCO的数目一定小于0.5N
3 A
D.含19.6 g H SO 的浓硫酸与足量铜反应,生成SO 的分子数为0.1N
2 4 2 A
【名师提醒】“九防”巧避阿伏加德罗常数正误判断的陷阱
示例 错因分析
1.常温常压下,22.4 L氯气与足量的镁粉充分反应,转移的电子数
非标准状况
为2N
A
2.在pH=13的NaOH溶液中OH-的数目为0.1×6.02×1023 溶液的体积未知
3.密闭容器中2 mol NO与1 mol O 充分反应,产物的分子数为
2
NO 部分转化为NO
2 2 4
2N
A
4.含2 mol硫酸的浓硫酸与足量铜共热,转移的电子数为2N 浓度变化,导致反应停止
A
5.2 L 1 mol·L-1 FeCl 溶液中所含Fe3+的数目为2N 盐类水解
3 A
总结:一防“标准状况非气体”,二防“只有浓度缺体积”,三防“溶剂粒子被忽视”,四防
“胶体微粒、聚合物”,五防“阴阳离子能水解”,六防“弱电解质部分电离”,七防“可逆
反应未到底”, 八防“浓度变化、反应停止(或反应改变)”, 九防“特殊物质特殊结构”。
题型一 物质的量
1.下列关于“物质的量”“摩尔”和“摩尔质量”的叙述中正确的是
A.物质的摩尔质量等于其相对分子(原子)质量
B.“物质的量”是国际单位制中的一个基本单位
C.“摩尔”是“物质的量”的单位
D.1mol任何物质都含有约6.02×1023个原子
2.火箭燃料为偏二甲肼(C HN),它是一种高能燃料,燃烧产生的巨大能量可作为航天运载火箭的推动
2 8 2
力。下列叙述正确的是( )
A.偏二甲肼(C HN)的摩尔质量为60
2 8 2
B.6.02×1023个偏二甲肼(C HN)分子的质量约为60g
2 8 2
C.1 mol 偏二甲肼(C HN)的质量为60 g·mol-1
2 8 2
D.60g偏二甲肼(C HN)中含有N 个氮原子
2 8 2 A
3.(2024•浙江师大附中质检)我国宇航员已经在太空泡茶了。茶装在特制包装袋中,注水后用加热器进行
加热就可以喝了。下列说法正确的是( )
A.宇航员太空泡茶用水的 HO的摩尔质量是18g
2
B.18g太空泡茶用水中含有原子的物质的量为3mol
C.在标准状况下,1mol水的体积约是22.4L
D.18g太空泡茶用水中含有6.02×1023个H原子4.(2024•北京省顺义区期中)Ⅰ.工业上常用电解 溶液制备 ,反应方程式如下:2NaCl+2HO
2
2NaOH+H↑+Cl↑。回答下列问题:
2 2
(1)用 的NaCl溶液进行电解制备 。
①该NaCl溶液中Na+的物质的量是 mol;
②标准状况下,理论上最多能产生Cl L;
2
③该反应中两种气体产物的质量比是 ;
④当 恰好完全反应时,停止电解,把所得溶液稀释到 ,则所得 溶液的物质的量浓度为
。
(2)写出该反应的离子方程式 。
Ⅱ.我国科学家用CO 人工合成淀粉时,第一步需要将CO 转化为甲醇,反应的化学方程式为:CO+3H
2 2 2 2
CHOH+H O。
3 2
(3)做还原剂的物质是 ;
(4)反应中每生成1 mol CH OH,消耗CO 的物质的量是 mol,转移电子的物质的量是 mol。
3 2
(5)对于反应:5CO+ Ba(NO ) N+ BaO+5CO 。
3 2 2 2
①发生还原反应的物质为 ;
②若有 参与反应,则反应中转移的电子的物质的量为 mol。
题型二 气体摩尔体积 阿伏加德罗定律
5.(2024•云南省大理市开学考试)常温常压下,用氢气、氦气分别吹出体积相同的两个气球,下列说法错
误的是( )
A.两个气球内的压强相同 B.氢气球和氦气球的质量不同
C.气球内两种气体的分子数相同 D.气球内两种气体的原子数相同
6.下列选项中的物质所含指定原子数目一定相等的是( )
A.等温等压下,相同体积的O 和O 两种气体中的氧原子数
2 3
B.等温等压下,相同体积的C H 和C H、C H 的混合气体的总原子数
2 4 2 2 2 6
C.温度和压强不同,相同质量的NO和CO 两种气体的总原子数
2 2
D.温度和压强不同时,相同质量的NH 和CH 两种气体中的氢原子数
3 4
7.(2024•重庆市期中)常温常压下,分别向三个气球(同一规格,忽略气球自身的重量)中充入两种按体积比
1:1混合的气体,得到体积相等的①、②、③三个气球(如图)。下列判断不正确的是( )
A.三个气球中所含气体的分子数相等
B.三个气球中所含气体的物质的量相等
C.三个气球中气体分子间的平均距离相等
D.将三个气球放在空气中,只有一个往下沉8.(2024•海南省农垦中学期末)在两个密闭容器中,分别充有质量相等的甲、乙两种气体,它们的温度和
密度均相同。试根据甲、乙的摩尔质量(M)的关系,判断下列说法中正确的是( )
A.若M(甲)>M(乙),则分子数:甲>乙
B.若M(甲)乙
C.若M(甲)乙
D.若M(甲)>M(乙),则气体体积:甲<乙
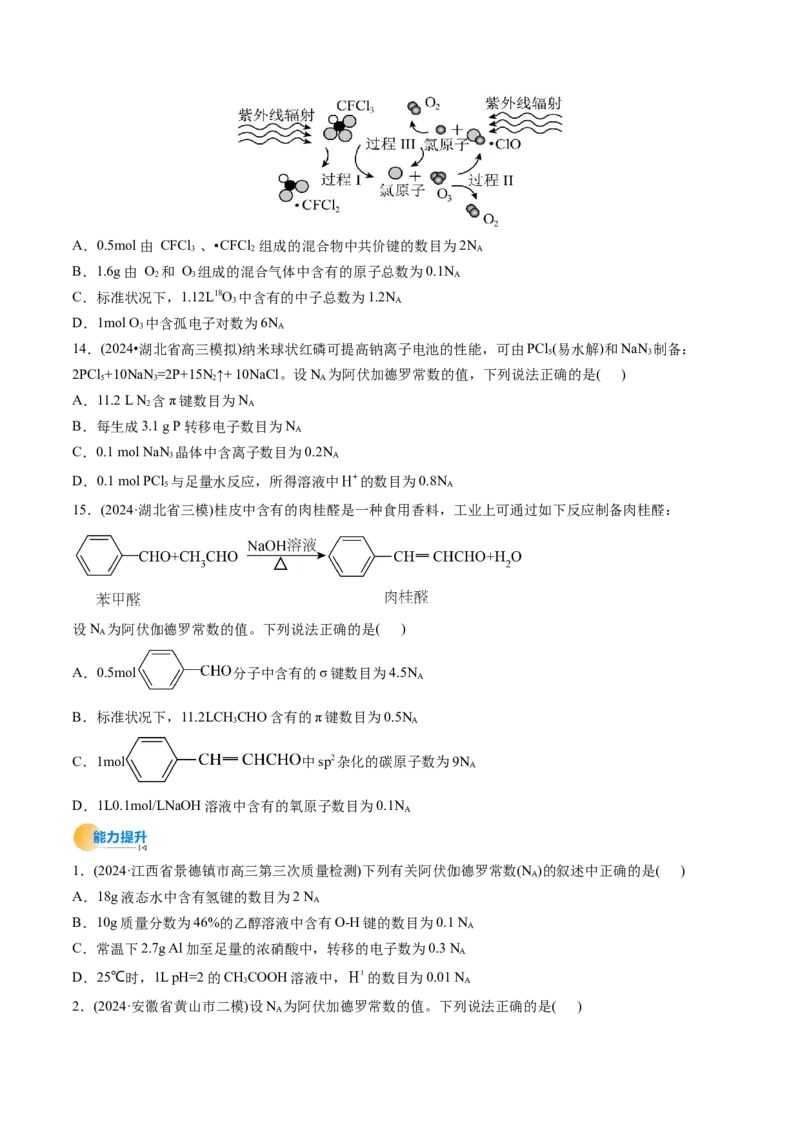
9.(2024•河北省开学考试)在一密闭刚性容器中由可滑动隔板将容器分为甲乙两部分。现向甲室通入O,
2
乙室通入1molN ,隔板位置如图所示,则下列说法不正确的是
2
A.甲乙的分子数之比2:1
B.甲乙的密度比为8:7
C.甲乙的质量比为8:7
D.若向甲室通入H 充分反应后,恢复至室温,隔板停留在2处,则通入的H 物质的量可能为
2 2
题型三 阿伏加德罗常数(N )
A
10.(2024·广东省汕头市二模)设N 为阿伏加德罗常数的值,下列说法中正确的是V
A
A.标准状况下,22.4L正丙醇(C HO)分子中含有 的数目为8 N
3 8 A
B.24g质量分数为25%的甲醛水溶液中含有氢原子数目为2.4 N
A
C.pH=1的HSO 溶液与足量的Zn反应产生的氢气分子数目为0.05 N
2 4 A
D.0.1mol FeI 与0.1molCl 反应时,转移电子的数目为0.3 N
2 2 A
11.(2024•四川省成都市第七中学高三模拟)N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.1mol化学式为C H O 的单糖分子中含-CHO的数目为N
6 12 6 A
B.标准状况下,2.24LSO 溶于水,溶液中HSO -、SO 2-和SO 的微粒数之和小于0.1 N
2 3 3 2 A
C.过量酸性KMnO 溶液与1molH O 完全反应,转移电子数为N
4 2 2 A
D.常温下,已知 ,则该温度下CaSO 饱和溶液中含有 个
4
12.(2024·吉林省通化市二模)新制氢氧化铜和葡萄糖的反应可用来检验血糖,其反应为:
CHOH(CHOH) CHO+2Cu(OH) +NaOH CHOH(CHOH) COONa+Cu O↓+3HO,设N 为阿伏加德罗常数
2 4 2 2 4 2 2 A
的值,下列说法正确的是( )
A.18gCHOH(CHOH) CHO中含有羟基的数目为0.6 N
2 4 A
B.每消耗1mol Cu(OH) ,转移电子的数目为2 N
2 A
C.1L1mol·L-1CHOH(CHOH) COONa溶液中含有的离子数目为2 N
2 4 A
D.标准状况下,112mLH O(l)中含有的分子数目约为6.2 N
2 A
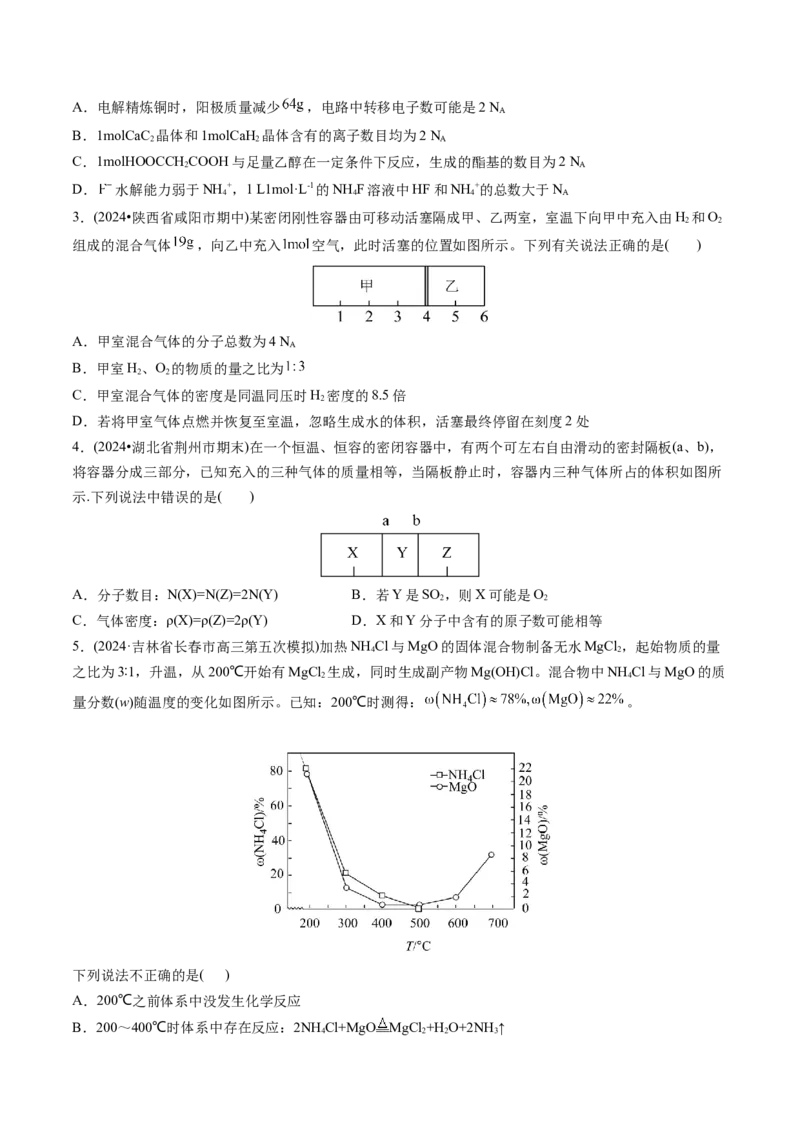
13.(2024·福建省泉州市一模)氟利昂—11(CFCl )破坏臭氧层的反应过程如图所示。设 N 为阿伏加德罗常
3 A
数的值,下列说法正确的是( )A.0.5mol由 CFCl 、•CFCl 组成的混合物中共价键的数目为2N
3 2 A
B.1.6g由 O 和 O 组成的混合气体中含有的原子总数为0.1N
2 3 A
C.标准状况下,1.12L18O 中含有的中子总数为1.2N
3 A
D.1mol O 中含孤电子对数为6N
3 A
14.(2024•湖北省高三模拟)纳米球状红磷可提高钠离子电池的性能,可由PCl (易水解)和NaN 制备:
5 3
2PCl +10NaN=2P+15N ↑+ 10NaCl。设N 为阿伏加德罗常数的值,下列说法正确的是( )
5 3 2 A
A.11.2 L N 含π键数目为N
2 A
B.每生成3.1 g P转移电子数目为N
A
C.0.1 mol NaN 晶体中含离子数目为0.2N
3 A
D.0.1 mol PCl 与足量水反应,所得溶液中 的数目为0.8N
5 A
15.(2024·湖北省三模)桂皮中含有的肉桂醛是一种食用香料,工业上可通过如下反应制备肉桂醛:
设N 为阿伏伽德罗常数的值。下列说法正确的是( )
A
A.0.5mol 分子中含有的σ键数目为4.5N
A
B.标准状况下,11.2LCHCHO含有的π键数目为0.5N
3 A
C.1mol 中sp2杂化的碳原子数为9N
A
D.1L0.1mol/LNaOH溶液中含有的氧原子数目为0.1N
A
1.(2024·江西省景德镇市高三第三次质量检测)下列有关阿伏伽德罗常数(N )的叙述中正确的是( )
A
A.18g液态水中含有氢键的数目为2 N
A
B.10g质量分数为46%的乙醇溶液中含有O-H键的数目为0.1 N
A
C.常温下2.7g Al加至足量的浓硝酸中,转移的电子数为0.3 N
A
D.25℃时,1L pH=2的CHCOOH溶液中, 的数目为0.01 N
3 A
2.(2024·安徽省黄山市二模)设N 为阿伏加德罗常数的值。下列说法正确的是( )
AA.电解精炼铜时,阳极质量减少 ,电路中转移电子数可能是2 N
A
B.1molCaC 晶体和1molCaH 晶体含有的离子数目均为2 N
2 2 A
C.1molHOOCCH COOH与足量乙醇在一定条件下反应,生成的酯基的数目为2 N
2 A
D. 水解能力弱于NH +,1 L1mol·L-1的NH F溶液中HF和NH +的总数大于N
4 4 4 A
3.(2024•陕西省咸阳市期中)某密闭刚性容器由可移动活塞隔成甲、乙两室,室温下向甲中充入由H 和O
2 2
组成的混合气体 ,向乙中充入 空气,此时活塞的位置如图所示。下列有关说法正确的是( )
A.甲室混合气体的分子总数为4 N
A
B.甲室H、O 的物质的量之比为
2 2
C.甲室混合气体的密度是同温同压时H 密度的8.5倍
2
D.若将甲室气体点燃并恢复至室温,忽略生成水的体积,活塞最终停留在刻度2处
4.(2024•湖北省荆州市期末)在一个恒温、恒容的密闭容器中,有两个可左右自由滑动的密封隔板(a、b),
将容器分成三部分,已知充入的三种气体的质量相等,当隔板静止时,容器内三种气体所占的体积如图所
示.下列说法中错误的是( )
A.分子数目:N(X)=N(Z)=2N(Y) B.若Y是SO ,则X可能是O
2 2
C.气体密度:ρ(X)=ρ(Z)=2ρ(Y) D.X和Y分子中含有的原子数可能相等
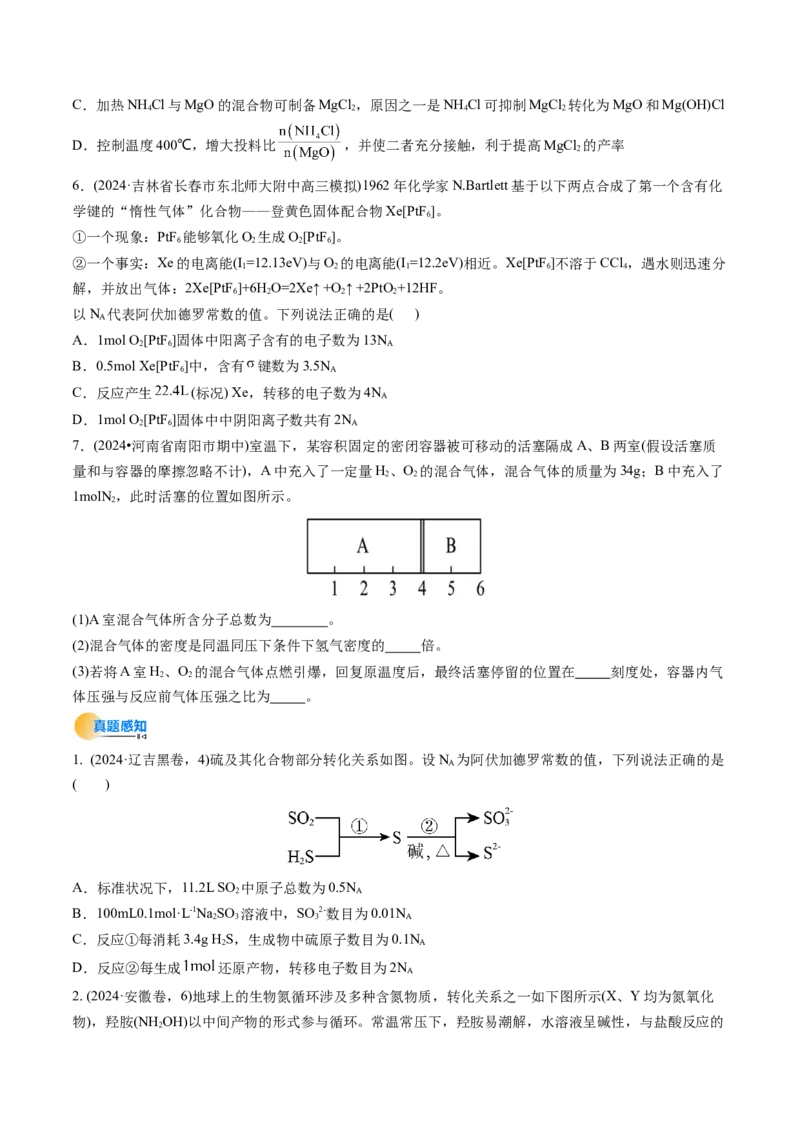
5.(2024·吉林省长春市高三第五次模拟)加热NH Cl与MgO的固体混合物制备无水MgCl ,起始物质的量
4 2
之比为3∶1,升温,从200℃开始有MgCl 生成,同时生成副产物Mg(OH)Cl。混合物中NH Cl与MgO的质
2 4
量分数(w)随温度的变化如图所示。已知:200℃时测得: 。
下列说法不正确的是( )
A.200℃之前体系中没发生化学反应
B.200~400℃时体系中存在反应:2NH Cl+MgO MgCl +H O+2NH ↑
4 2 2 3C.加热NH Cl与MgO的混合物可制备MgCl ,原因之一是NH Cl可抑制MgCl 转化为MgO和Mg(OH)Cl
4 2 4 2
D.控制温度400℃,增大投料比 ,并使二者充分接触,利于提高MgCl 的产率
2
6.(2024·吉林省长春市东北师大附中高三模拟)1962年化学家N.Bartlett基于以下两点合成了第一个含有化
学键的“惰性气体”化合物——登黄色固体配合物Xe[PtF ]。
6
①一个现象:PtF 能够氧化O 生成O[PtF]。
6 2 2 6
②一个事实:Xe的电离能(I=12.13eV)与O 的电离能(I=12.2eV)相近。Xe[PtF ]不溶于CCl ,遇水则迅速分
1 2 1 6 4
解,并放出气体:2Xe[PtF ]+6H O=2Xe↑ +O ↑ +2PtO+12HF。
6 2 2 2
以N 代表阿伏加德罗常数的值。下列说法正确的是( )
A
A.1mol O[PtF]固体中阳离子含有的电子数为13N
2 6 A
B.0.5mol Xe[PtF ]中,含有 键数为3.5N
6 A
C.反应产生 (标况) Xe,转移的电子数为4N
A
D.1mol O[PtF]固体中中阴阳离子数共有2N
2 6 A
7.(2024•河南省南阳市期中)室温下,某容积固定的密闭容器被可移动的活塞隔成A、B两室(假设活塞质
量和与容器的摩擦忽略不计),A中充入了一定量H、O 的混合气体,混合气体的质量为34g;B中充入了
2 2
1molN ,此时活塞的位置如图所示。
2
(1)A室混合气体所含分子总数为 。
(2)混合气体的密度是同温同压下条件下氢气密度的 倍。
(3)若将A室H、O 的混合气体点燃引爆,回复原温度后,最终活塞停留的位置在 刻度处,容器内气
2 2
体压强与反应前气体压强之比为 。
1. (2024·辽吉黑卷,4)硫及其化合物部分转化关系如图。设N 为阿伏加德罗常数的值,下列说法正确的是
A
( )
A.标准状况下,11.2L SO 中原子总数为0.5N
2 A
B.100mL0.1mol·L-1NaSO 溶液中,SO 2-数目为0.01N
2 3 3 A
C.反应①每消耗3.4g HS,生成物中硫原子数目为0.1N
2 A
D.反应②每生成 还原产物,转移电子数目为2N
A
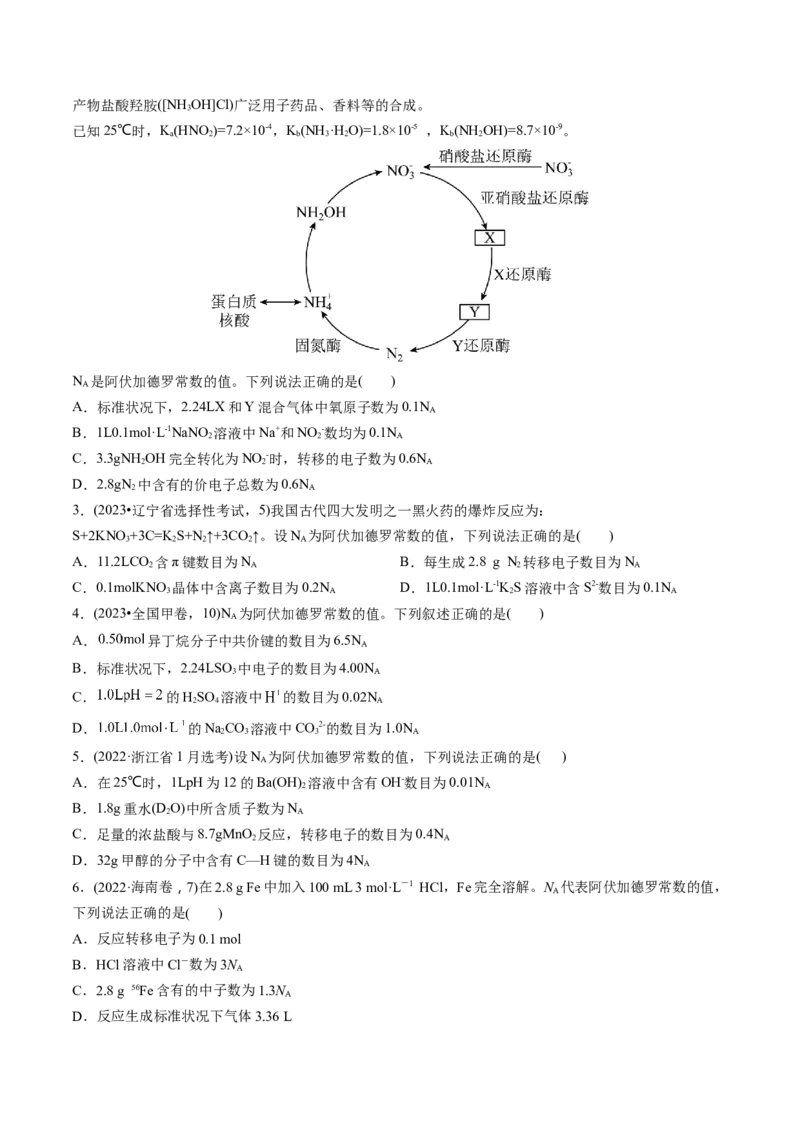
2. (2024·安徽卷,6)地球上的生物氮循环涉及多种含氮物质,转化关系之一如下图所示(X、Y均为氮氧化
物),羟胺(NH OH)以中间产物的形式参与循环。常温常压下,羟胺易潮解,水溶液呈碱性,与盐酸反应的
2产物盐酸羟胺([NH OH]Cl)广泛用子药品、香料等的合成。
3
已知25℃时,K(HNO)=7.2×10-4,K(NH ·H O)=1.8×10-5 ,K(NH OH)=8.7×10-9。
a 2 b 3 2 b 2
N 是阿伏加德罗常数的值。下列说法正确的是( )
A
A.标准状况下,2.24LX和Y混合气体中氧原子数为0.1N
A
B.1L0.1mol·L-1NaNO 溶液中Na+和NO -数均为0.1N
2 2 A
C.3.3gNH OH完全转化为NO -时,转移的电子数为0.6N
2 2 A
D.2.8gN 中含有的价电子总数为0.6N
2 A
3.(2023•辽宁省选择性考试,5)我国古代四大发明之一黑火药的爆炸反应为:
S+2KNO +3C=K S+N↑+3CO ↑。设N 为阿伏加德罗常数的值,下列说法正确的是( )
3 2 2 2 A
A.11.2LCO 含π键数目为N B.每生成2.8 g N 转移电子数目为N
2 A 2 A
C.0.1molKNO 晶体中含离子数目为0.2N D.1L0.1mol·L-1KS溶液中含S2-数目为0.1N
3 A 2 A
4.(2023•全国甲卷,10)N 为阿伏加德罗常数的值。下列叙述正确的是( )
A
A. 异丁烷分子中共价键的数目为6.5N
A
B.标准状况下,2.24LSO 中电子的数目为4.00N
3 A
C. 的HSO 溶液中 的数目为0.02N
2 4 A
D. 的NaCO 溶液中CO2-的数目为1.0N
2 3 3 A
5.(2022·浙江省1月选考)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
B.1.8g重水(D O)中所含质子数为N
2 A
C.足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 A
D.32g甲醇的分子中含有C—H键的数目为4N
A
6.(2022·海南卷,7)在2.8 g Fe中加入100 mL 3 mol·L-1 HCl,Fe完全溶解。N 代表阿伏加德罗常数的值,
A
下列说法正确的是( )
A.反应转移电子为0.1 mol
B.HCl溶液中Cl-数为3N
A
C.2.8 g 56Fe含有的中子数为1.3N
A
D.反应生成标准状况下气体3.36 L7.(2021•全国甲卷)N 为阿伏加德罗常数的值。下列叙述正确的是( )
A
A. 重水(D O)中含有的质子数为10 N
2 A
B.3mol的NO 与HO完全反应时转移的电子数为4N
2 2 A
C.32g环状 ( )分子中含有的S-S键数为1N
A
D.1L pH=4的0.1mol·L-1 KCr O 溶液中Cr O2-离子数为0.1 N
2 2 7 2 7 A
8.(2021•浙江6月选考)设N 为阿伏加德罗常数的值,下列说法不正确的是( )
A
A.标准状况下,1.12L18O 中含有中子数为N
2 A
B.31gP (分子结构: )中的共价键数目为1.5N
4 A
C.100mL 0.1mol·Lˉ1的NaOH水溶液中含有氧原子数为0.01N
A
D.18.9g三肽C H NO (相对分子质量:189)中的肽键数目为0.2N
6 33 3 4 A
9.(2021•湖南选择性考试)N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.18g H 18O含有的中子数为10N
2 A
B.0.1mol•L﹣1HClO 溶液中含有的H+数为0.1N
4 A
C.2mol NO与1mol O 在密闭容器中充分反应后的分子数为2N
2 A
D.11.2L CH 和22.4L Cl (均为标准状况)在光照下充分反应后的分子数为1.5N
4 2 A
10.(2021•河北选择性考试)N 是阿伏加德罗常数的值,下列说法错误的是( )
A
A.22.4L(标准状况)氟气所含的质子数为18N
A
B.1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2N
A
C.电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为N
A
D.1L1mol•L-1溴化铵水溶液中NH +与H+离子数之和大于N
4 A
11.(2021•湖北选择性考试) N 为阿伏加德罗常数的值。下列说法错误的是( )
A
A.23 g C HOH中sp3杂化的原子数为N
2 5 A
B.0.5 mol XeF 中氙的价层电子对数为3N
4 A
C.1 mol [Cu(H O) ]2+中配位键的个数为4N
2 4 A
D.标准状况下,11.2 L CO和H 的混合气体中分子数为0.5N
2 A
12.(2021•海南选择性考试) N 代表阿伏加德罗常数的值。下列说法正确的是( )
A
A.0.1mol27Al3+中含有的电子数为1.3N
A
B.3.9 g Na O 中含有的共价键的数目为0.1N
2 2 A
C.0.1mol肼(H N-NH)含有的孤电子对数为0.2N
2 2 A
D.CH=CH +H →CH-CH,生成1mol乙烷时断裂的共价键总数为N
2 2 2 3 3 A
13.(2021•山东卷) X、Y均为短周期金属元素,同温同压下,0.1molX的单质与足量稀盐酸反应,生成H
2
体积为VL;0.1molY的单质与足量稀硫酸反应,生成H 体积为VL。下列说法错误的是( )
1 2 2A.X、Y生成H 的物质的量之比一定为
2
B.X、Y消耗酸的物质的量之比一定为
C.产物中X、Y化合价之比一定为
D.由 一定能确定产物中X、Y的化合价