文档内容
【基础知识】氧化还原反应
考点二 氧化还原反应的强弱规律及价态规律
【必备知识】
一、价态原则
1、最高价态——只有氧化性,如HSO 、KMnO 等;
2 4 4
最低价态——只有还原性,如金属单质、Cl-、S2-等;
中间价态——既有氧化性,又有还原性,如Fe2+、S、Cl 等。
2
2、归中反应:“两相靠,不相交”
例、6HCl+NaClO===NaCl+3Cl↑+3HO中,氧化剂为NaClO ,还原剂为HCl,氧化产物和还原产物都
3 2 2 3
为Cl。
2
3、歧化反应
例、Cl+2NaOH===NaCl+NaClO+HO
2 2
二、强弱规律
1、氧化性、还原性强弱的比较方法
①根据化学方程式判断
同一个反应中,氧化性最强的是氧化剂,还原性最强的是还原剂。
②根据相同条件下产物的价态高低判断
如2Fe+3Cl=====2FeCl ;Fe+S=====FeS,则氧化性:Cl>S。
2 3 2
(3)根据反应条件、浓度大小、酸碱性及反应的剧烈程度判断
反应条件要求越低,浓度越大,反应越剧烈,对应物质的氧化性或还原性越强。
2、常见强弱比较
氧化性:Ag+ ﹥ Hg2+ ﹥Cu2+ ﹥Pb2+ ﹥Sn2+﹥Fe2+
MnO(H+)>Cl >Br >Fe3+>I >稀HSO >S
2 2 2 2 4
还原性:S2- ﹥ SO (SO 2-) ﹥ I- ﹥ Fe2+ ﹥ Br- ﹥ Cl-
2 3
注意:氧化性、还原性的强弱取决于得、失电子的难易程度,与得、失电子数目的多少无关。
三、先后规律及应用(强者优先)
往FeBr 通少量氯气,先反应的是Fe2+;往FeI 通少量氯气,先反应的是I-。
2 2
例、实验室制备高铁酸钾(K FeO)并探究其性质。
2 4
(1)制备 KFeO 的反应为 3Cl +2Fe(OH) +10KOH===2K FeO +6KCl+8HO,由此得出氧化性:
2 4 2 3 2 4 2
Cl________(填“>”或“<”)FeO。
2
(2)K FeO 的性质探究:用KOH溶液将紫色KFeO 固体溶出,得到紫色KFeO 溶液。取少量该溶液,滴
2 4 2 4 2 4
加盐酸,有Cl 产生。
2
该实验表明Cl 和FeO的氧化性强弱关系与(1)相反,原因是__________________________。
2
【答案】 (1)> (2)溶液的酸碱性不同
【解析】 (1)同一反应中,氧化性:氧化剂>氧化产物。(2)对比两个反应的异同,制备反应在碱性条件下,
性质探究实验是在酸性条件下,氧化性强弱关系不同说明酸碱性的不同影响氧化性的强弱。
例、MnO +4HCl(浓)=====MnCl +Cl↑+2HO,2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO,可
2 2 2 2 4 2 2 2
判断氧化性:KMnO MnO 。为了提高KMnO 的氧化性,需酸化处理,所加入的酸为 。
4 2 4
【答案】> 硫酸
例、下列各组物质:①Cu与HNO 溶液 ②Cu与FeCl 溶液 ③Zn与HSO 溶液 ④Fe与FeCl 溶液
3 3 2 4 3
⑤Cl 与NaOH溶液 ⑥Fe与HNO 溶液
2 3
⑦Fe与HSO 溶液 ⑧Na与O
2 4 2(1)由于浓度不同而发生不同氧化还原反应的是__________________________(填序号,下同)。
(2)由于温度不同而发生不同氧化还原反应的是________________________________。
(3)氧化还原反应不受浓度、温度影响的是__________________。
【答案】 (1)①③⑥⑦ (2)⑤⑥⑦⑧ (3)②④
【解析】 ⑥Fe和浓HNO 常温下钝化,加热继续反应,Fe和稀HNO 反应,HNO 被还原成NO。⑦Fe
3 3 3
和浓HSO 常温下钝化,加热继续反应,Fe和稀HSO 反应生成FeSO 和H。
2 4 2 4 4 2
例、根据反应事实判断性质的强弱。
①向Co O 固体中滴加浓盐酸,有黄绿色气体生成
2 3
②将氯气通入碘水中,溶液褪色生成两种酸(HCl和HIO )
3
则Cl、HIO 、Co O 的氧化性由强到弱的顺序:_____________________;HCl、CoCl 、I 的还原性由强到
2 3 2 3 2 2
弱的顺序:_____________________________________________。
【答案】 Co O>Cl>HIO I>HCl>CoCl
2 3 2 3 2 2
【概念辨析】
1、金属原子失电子数越多,金属的还原性越强( )
2、元素的非金属性越强,其氧化性越强,相应单质越活泼( )
3、强氧化剂与强还原剂混合不一定能发生氧化还原反应( )
4、向浓HSO 中通入HS气体,1 mol浓HSO 转移电子数可能是6N ,也可能是2N ( )
2 4 2 2 4 A A
5、1 mol KClO 与足量的浓盐酸反应,转移电子数为6N ( )
3 A
6、SO 的还原性较强,而浓硫酸具有很强的氧化性,所以浓硫酸不能干燥SO 气体( )
2 2
【答案】 1.× 2.× 3.√ 4.√ 5.× 6.×
【跟踪练习】
1、(2019浙江4月)反应8NH +3Cl N+6NH Cl,被氧化的NH 与被还原的Cl 的物质的量之比为(
3 2 2 4 3 2
)
A.2∶3 B.8∶3 C.6∶3 D.3∶2
【答案】A
【解析】该氧化还原反应用双线桥表示为 ,可知实际升价的N原子为2个,所以2
个NH 被氧化,同时Cl 全部被还原,观察计量数,Cl 为3个,因而被氧化的NH 与被还原的Cl 的物质
3 2 2 3 2
的量之比为2:3。故答案选A。
2、铊(Tl)盐与氰化钾(KCN)被列为A级危险品。已知下列反应在一定条件下能够发生:①Tl3++2Ag===Tl+
+2Ag+,②Ag++Fe2+===Ag+Fe3+,③Fe+2Fe3+===3Fe2+,下列离子氧化性比较顺序正确的是( )
A.Tl3+>Fe3+>Ag+ B.Fe3+>Ag+>Tl3+
C.Tl+>Ag+>Fe2+ D.Tl3+>Ag+>Fe3+
【答案】 D
3、已知I-、Fe2+、SO 、Cl-和HO 均有还原性,它们在酸性溶液中还原性的强弱顺序为
2 2 2
Cl-<Fe2+<HO<I-<SO ,则下列反应不能发生的是( )
2 2 2
A.2Fe3++SO +2HO===2Fe2++SO+4H+ B.I+SO +2HO===HSO +2HI
2 2 2 2 2 2 4
C.HO+HSO ===SO ↑+O↑+2HO D.2Fe2++Cl===2Fe3++2Cl-
2 2 2 4 2 2 2 2
【答案】 C
【解析】 A项,还原性:SO >Fe2+,反应能发生;B项,还原性:SO >I-,反应能发生;C项,还原
2 2
性:HO<SO ,反应不能发生。
2 2 2
4、为防止废弃的硒单质(Se)造成环境污染,通常用浓硫酸将其转化成二氧化硒(SeO ),再用KI溶液处理后
2
回收Se。发生的反应为①Se+2HSO (浓)===2SO ↑+SeO+2HO;②SeO+4KI+4HNO===4KNO+Se
2 4 2 2 2 2 3 3
+2I+2HO,下列说法错误的是( )
2 2
A.①中SO 是还原产物,SeO 是氧化产物 B.②中KI是还原剂,SeO 是氧化剂
2 2 2C.每生成0.4 mol I 共转移1.2 mol电子 D.氧化性由强到弱的顺序是HSO (浓)>SeO >HNO
2 2 4 2 3
【答案】 C
【解析】 反应②中,生成2 mol碘单质,转移4 mol电子,则每生成0.4 mol I 共转移0.8 mol电子,故C
2
错误;在同一反应中氧化剂的氧化性大于氧化产物的氧化性,反应①中氧化性:HSO (浓)>SeO ,反应②
2 4 2
中硝酸既不是氧化剂也不是还原剂,说明氧化性:SeO >HNO ,故D正确。
2 3
5、(2021·浙江卷)关于反应KHIO +9HI===2KI+4I+6HO,下列说法正确的是( )
2 3 6 2 2
A. K HIO 发生氧化反应 B.KI是还原产物
2 3 6
C.生成12.7 g I 时,转移0.1 mol电子 D.还原剂与氧化剂的物质的量之比为7∶1
2
【答案】 D
【解析】 反应中KHIO 中I元素的化合价降低,发生得电子的还原反应,A错误;KI中的I-由HI变
2 3 6
化而来,化合价没有发生变化,KI既不是氧化产物也不是还原产物,B错误;12.7 g I 的物质的量为0.05
2
mol,根据反应方程式,每生成4 mol I 转移7 mol电子,则生成0.05 mol I 时转移电子的物质的量为0.087
2 2
5 mol,C错误;反应中HI为还原剂,KHIO 为氧化剂,在反应中每消耗1 mol K HIO 就有7 mol HI失
2 3 6 2 3 6
电子,则还原剂与氧化剂的物质的量之比为7∶1,D正确。
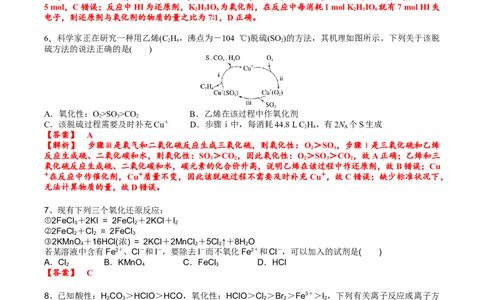
6、科学家正在研究一种用乙烯(C H,沸点为-104 ℃)脱硫(SO )的方法,其机理如图所示。下列关于该脱
2 4 2
硫方法的说法正确的是( )
A.氧化性:O>SO>CO B.乙烯在该过程中作氧化剂
2 3 2
C.该脱硫过程需要及时补充Cu+ D.步骤ⅰ中,每消耗44.8 L C H,有2N 个S生成
2 4 A
【答案】 A
【解析】 步骤ⅲ是氧气和二氧化硫反应生成三氧化硫,则氧化性:O >SO ,步骤ⅰ是三氧化硫和乙烯
2 3
反应生成硫、二氧化碳和水,则氧化性:SO >CO ,因此氧化性:O >SO >CO ,故A正确;乙烯和三
3 2 2 3 2
氧化硫反应生成硫、二氧化碳和水,碳元素的化合价升高,说明乙烯在该过程中作还原剂,故B错误;Cu
+在反应中作催化剂,Cu+质量不变,因此该脱硫过程不需要及时补充 Cu+,故C错误;缺少标准状况下,
无法计算物质的量,故D错误。
7、现有下列三个氧化还原反应:
①2FeCl +2KI = 2FeCl +2KCl+I
3 2 2
②2FeCl +Cl = 2FeCl
2 2 3
③2KMnO +16HCl(浓) = 2KCl+2MnCl +5Cl ↑+8H O
4 2 2 2
若某溶液中含有Fe2+、Cl-和I-,要除去I-而不氧化Fe2+和Cl-,可以加入的试剂是( )
A.Cl B.KMnO C.FeCl D.HCl
2 4 3
【答案】 C
8、已知酸性:H CO >HClO>HCO,氧化性:HClO>Cl >Br >Fe3+>I ,下列有关离子反应或离子方
2 3 2 2 2
程式的叙述中,正确的是( )
A.能使pH试纸显深红色的溶液中,Fe3+、Cl-、Ba2+、I-能大量共存
B.向溴水中加入足量氯化亚铁溶液能使溶液变成无色
C.向NaClO溶液中通入少量二氧化碳的离子方程式:ClO-+CO +H O = HClO+HCO
2 2
D.向FeI 溶液中滴加少量氯水,反应的离子方程式为:2Fe2++Cl = 2Fe3++2Cl-
2 2
【答案】 C