文档内容
解密 05 物质结构元素周期律
一、选择题
1.(2021·湖南株洲市高三一模)2020 年12月17日1时59分,嫦娥五号返回器携带“月球土特产”在
内蒙古四子王旗预定区域安全着陆,探月工程嫦娥五号任务取得圆满成功。经探测,月壤中含有大量3He
,这是一种未来可能进行热核聚变发电的清洁能源,而地球上主要是 4He。下列有关说法中正确的是
( )
A.1 个 3 He 原子中有 3 个中子 B.3 He 与 4 He 互为同位素
C.3 He 与 4 He 互为同素异形体 D.3 He 与 4 He 的性质完全相同
2.(2021·广东佛山市高三一模)2020年11月6日,长征六号运载火箭成功将New Sat9-18卫星送入预
定轨道,提供动力的化学反应为:C HN+2N O=3N +2CO +4H O.下列说法错误的是( )
2 8 2 2 4 2 2 2
A.N 的电子式: B.CO 的结构式:
2 2
C.N 既是氧化产物又是还原产物 D.氧化性:NO<CO
2 2 4 2
3.(2021·湖南长沙市长郡中学高三月考)2019年,我国青年化学家雷晓光被遴选为“青年化学家元素
周期表”氮元素的代言人。下列与氮元素有关的说法正确的是( )
A.14N与14C互为同位素 B.Si N 中N为+3价
3 4
C.NH 的热稳定性比HF的强 D.N 的电子式为
3 2
4.(2021·广东中山市·高一期末)中国科学院院士张青莲教授曾主持测定了铟( In)等9种元素相对原子
49
质量的新值,被采用为国际新标准.铟与铷( Rb)同周期.下列说法不正确的是( )
37
A.In是第五周期IIIA族元素 B. 的中子数与电子数的差值为17
C.原子半径:In<Rb D.碱性:In(OH) >RbOH
3
5.(2021·吉林长春市东北师大附中月考)下列说法错误的是( )
A.X和Y两种元素为同一周期第IIA族和第IIIA族元素,若X的原子序数为x,则Y的原子序数可
能为x+1,x+11, x+25
B.短周期元素Z和W组成化合物ZW,若W的原子序数为x,Z的原子序数不可能是x+14
3
C.短周期元素Q和M组成化合物QM,Q和M所在的族序数可能为VA和第VIA
2
D.利用元素周期表中氟、氯、硫、磷附近的元素研制新型农药
6.(2021·广东佛山市期末)下列各组物质,所含化学键类型完全相同的是( )
A.MgCl 和KCl B.NaOH和NaCl
2C.HO 和NaO D.NH 和NH Cl
2 2 2 2 3 4
7.(2020·南昌市新建区第二中学期末)下列说法中正确的是( )
A.氯化氢溶于水能电离出H+、Cl-,所以氯化氢是离子化合物
B.碘晶体受热转变成碘蒸气,吸收的热量用于克服碘原子间的作用力
C.HO分子比HS分子稳定,是因为HO分子间有氢键
2 2 2
D.质子数和电子数均相等的微粒,可以是不同的分子或不同的原子或不同的离子
8.(2021·江苏盐城市期末)下列关于元素周期表的认识中,其中不正确的是( )
A.历史上,门捷列夫是发现元素周期表第一人
B.元素性质特别是化学性质主要是由原子最外层电子数决定的
C.元素原子的电子层数等于所在周期的周期序数
D.主族元素原子的最外层电子数等于其所在族的族序数
9.(2021·山东济宁市期末)2019年是国际化学元素周期表150周年。下列关于元素周期表的说法正确
的是( )
A.ⅠA、IIA族的元素全部是金属元素,均能与酸发生反应生成氢气
B.元素周期表包含7个周期、7个主族、7个副族、1个Ⅷ族、1个零族
C.现代元素周期表是按照相对原子量的大小顺序进行对元素进行排列
D.零族元素中所有原子的最外层电子数都是8个,化学性质稳定
10.(2021·山东济宁市·高一期末)根据原子结构及元素周期律的知识,下列推断正确的是( )
A. Cl和 Cl的得电子能力相同
B.Cl- 的离子结构示意图:
C.Cl、S、O元素的非金属性逐渐增强
D.同周期元素含氧酸的酸性随核电荷数的增加而增强
11.(2020·安徽省太和第一中学高三月考)SCl 在工业生产中有着广泛的用途。已知:
2
12SCl +16H O=S+24HCl+4H SO ,下列叙述正确的是( )
2 2 8 2 4
A.S2﹣和Cl﹣的结构示意图都可以表示为
B.SCl 的电子式是
2C.水的比例模型是
D.S 中硫原子最外层均满足8电子稳定结构,其结构式可表示为S﹣S﹣S﹣S﹣S﹣S﹣S﹣S
8
12.(2021·浙江宁波市期末)下列说法正确的是( )
A.短周期共有18种核素
B.可以在周期表中金属与非金属的分界处寻找半导体材料
C.原子核外电子排布,先排满K层再排L层、先排满M层再排N层
D.Cl 和CH 分子中每个原子的最外电子层都形成了具有8个电子的稳定结构
2 4
13.(2020·江西宜春市高安中学月考)两种短周期元素X和Y形成的单质分别能和氢气反应放出能量
Q 和Q。已知Q>Q ,下列判断一定正确的是( )
1 2 2 1
A.沸点:HX>HY B.还原性:HY>HX
C.酸性:HXO>HYO D.稳定性HY>HX
4 4
14.(2021·北京朝阳区高三期末)由下列实验及相应事实推理所得的结论,不能用元素周期律解释的是(
)
实验 事实 结论
将体积相同的Na和K
A K与HO反应更剧烈 金属性:K>Na
2
分别投入冷水中
B 将足量硫酸与NaPO 溶液混合 生成HPO 非金属性:S>P
3 4 3 4
C 分别加热HCl气体和HI气体 HI气体更易分解 稳定性:HCl>HI
D 分别加热NaCO 固体和NaHCO 固体 NaHCO 固体更易分解 热稳定性:NaCO>NaHCO
2 3 3 3 2 3 3
15.(2021·四川省广汉中学高三月考)U、V、W、X、Y是原子序数依次增大的五种短周期元素,质子
数之和39,V、W同周期,U、X同主族,U、W能形成两种液态化合物UW和UW。Y元素的周期序数
2 2 2
与主族序数相等。下列说法中正确的是( )
A.简单离子半径:X>Y>W
B.XYU 中有离子键,其YU 原子团的空间构型是正四面体,在潮湿的空气中会变质而产生H
4 4 2
C.U、V、W、X形成的一种离子化合物,与W、X、Y组成的盐溶液相遇时,会产生大量的气泡
D.1 mol X的淡黄色化合物,投入到1 L 2mol / L的氯化亚铁溶液中,产生的气体在标准状况下的体
积为5.6 L
16.(2021·山东聊城市高三月考)短周期主族元素R、X、Y、Z的原子序数依次增大,R元素最高正价
和最低负价的代数和为2,在短周期主族元素中X原子半径最大,Y的单质可与某些金属氧化物反应用于焊接钢轨,Z元素形成的单质可使湿润的有色布条褪色。下列说法错误的是( )
A.最高价氧化物对应水化物的碱性:X>Y
B.R元素的氢化物可用作制冷剂
C.Z元素分别与X、Y元素形成的化合物一定是离子化合物
D.工业上常用电解法冶炼X和Y的单质
17.(2021·河北石家庄市辛集中学期末)已知W、X、Y、Z为短周期元素,原子序数依次增大。W、Z
同主族,X、Y、Z同周期,其中只有X为金属元素。下列说法一定正确的是( )
A.原子半径: ,同周期元素的简单离子中,X离子半径可能最小
B.W的含氧酸的酸性比Z的含氧酸的酸性强
C.W的气态氢化物的稳定性低于Y的气态氢化物
D.若W与X原子序数差为5,则形成化合物的化学式为XW
3 2
18.(2021·广东揭阳市期末)短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单氢化物可
用作制冷剂,且W形成的单质在空气中占比最大,Y的原子半径是所有短周期主族元素中最大的。由X、
Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气体产生。下列说
法不正确的是( )
A.X的简单氢化物的热稳定性比W的强
B.Z与X属于同一主族,与Y属于同一周期
C.Y的简单离子与X的简单离子具有相同的电子层结构
D.W的简单氢化物溶于水形成的水溶液可使蓝色石蕊试纸变红
19.(2021·山东枣庄市高三期末)LDFCB是电池的一种电解质,该电解质阴离子由同周期元素原子
W、X、Y、Z构成(如图),Y的最外层电子数等于X的核外电子总数,四种原子最外层电子数之和为20,
下列说法正确的是( )
A.四种元素的单质中,有分子晶体、共价晶体和金属晶体三种情况
B.原子半径:
C.W、Z形成的化合物分子中各原子均满足8电子稳定结构D.四种元素形成的简单氢化物中Z的沸点最高
20.(2021·沙坪坝区重庆八中高三月考)已知R、X、Y、Z是四种原子序数依次增大的主族元素,其中
R是短周期元素中原子半径最小的。Z最外层电子数是次外层电子数的3倍。四种元素组成某种离子的结
构如图所示。下列说法不正确的是( )
A.原子半径:X>Y>Z
B.简单氢化物的沸点:Z>Y>X
C.R与Y形成的化合物不可能含离子键
D.四种元素可共同形成多种既能与酸反应又能与碱反应的化合物
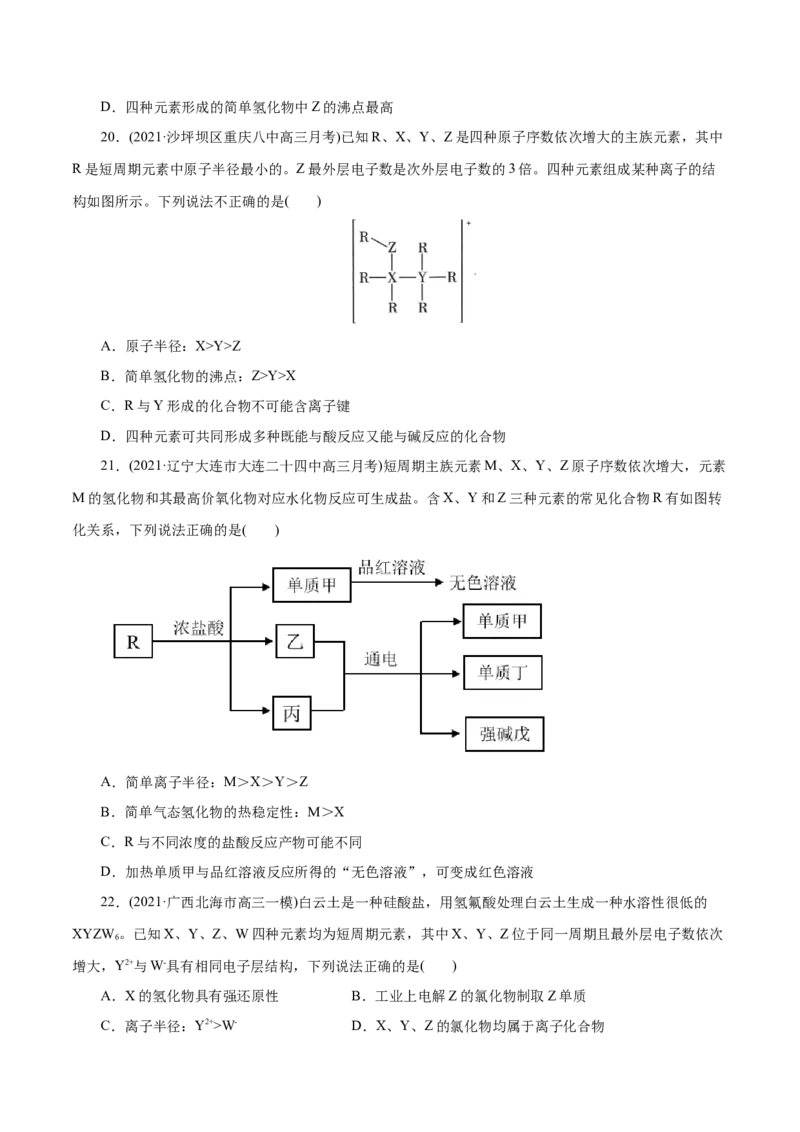
21.(2021·辽宁大连市大连二十四中高三月考)短周期主族元素M、X、Y、Z原子序数依次增大,元素
M的氢化物和其最高价氧化物对应水化物反应可生成盐。含X、Y和Z三种元素的常见化合物R有如图转
化关系,下列说法正确的是( )
A.简单离子半径:M>X>Y>Z
B.简单气态氢化物的热稳定性:M>X
C.R与不同浓度的盐酸反应产物可能不同
D.加热单质甲与品红溶液反应所得的“无色溶液”,可变成红色溶液
22.(2021·广西北海市高三一模)白云土是一种硅酸盐,用氢氟酸处理白云土生成一种水溶性很低的
XYZW 。已知X、Y、Z、W四种元素均为短周期元素,其中X、Y、Z位于同一周期且最外层电子数依次
6
增大,Y2+与W-具有相同电子层结构,下列说法正确的是( )
A.X的氢化物具有强还原性 B.工业上电解Z的氯化物制取Z单质
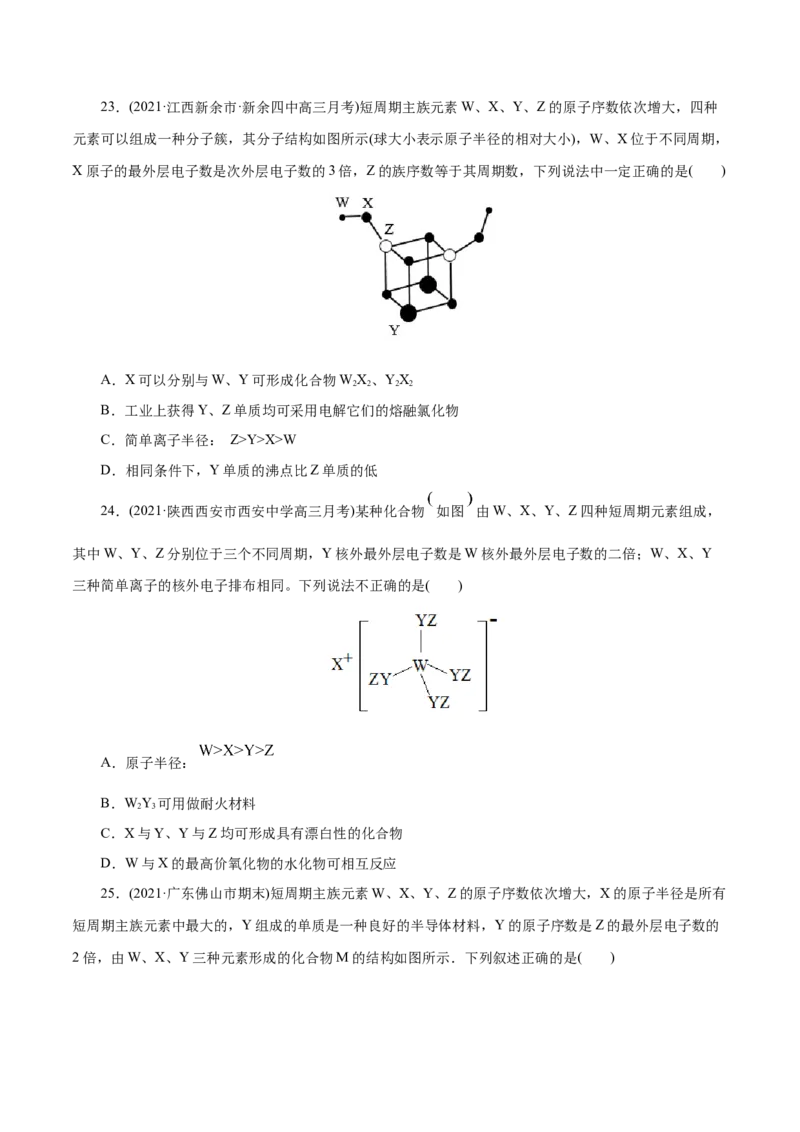
C.离子半径:Y2+>W- D.X、Y、Z的氯化物均属于离子化合物23.(2021·江西新余市·新余四中高三月考)短周期主族元素W、X、Y、Z的原子序数依次增大,四种
元素可以组成一种分子簇,其分子结构如图所示(球大小表示原子半径的相对大小),W、X位于不同周期,
X原子的最外层电子数是次外层电子数的3倍,Z的族序数等于其周期数,下列说法中一定正确的是( )
A.X可以分别与W、Y可形成化合物WX、YX
2 2 2 2
B.工业上获得Y、Z单质均可采用电解它们的熔融氯化物
C.简单离子半径: Z>Y>X>W
D.相同条件下,Y单质的沸点比Z单质的低
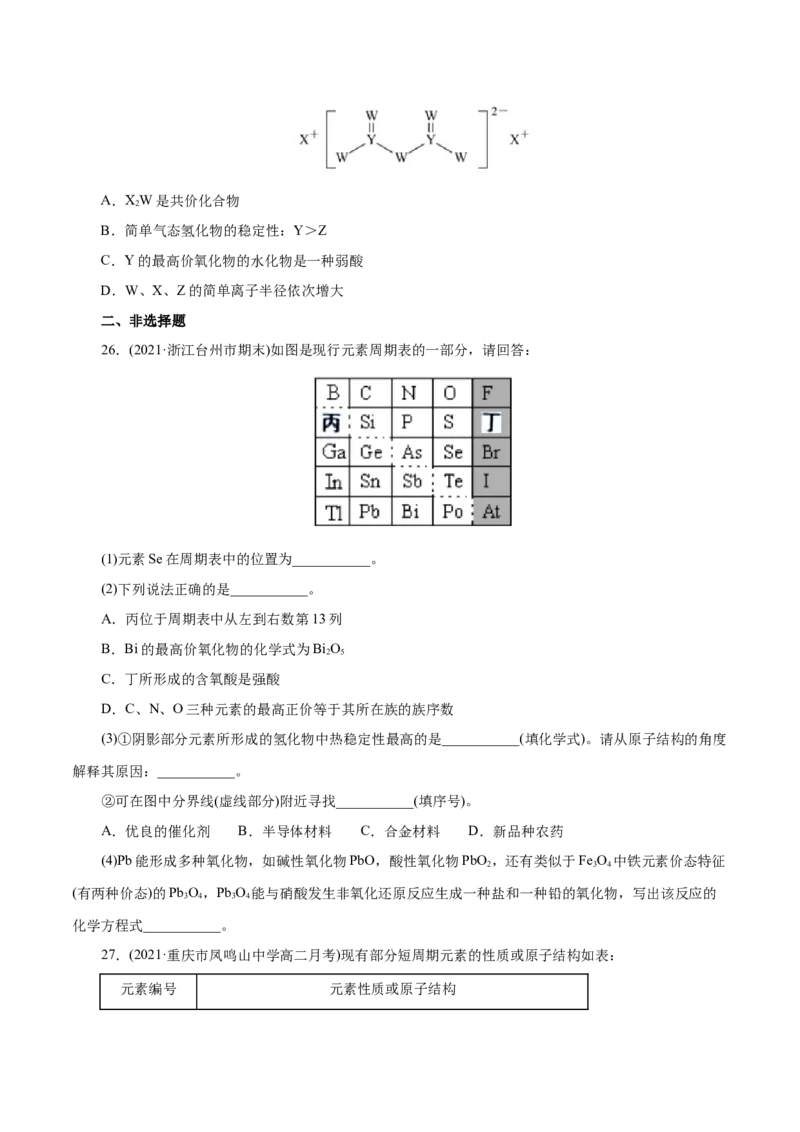
24.(2021·陕西西安市西安中学高三月考)某种化合物 如图 由W、X、Y、Z四种短周期元素组成,
其中W、Y、Z分别位于三个不同周期,Y核外最外层电子数是W核外最外层电子数的二倍;W、X、Y
三种简单离子的核外电子排布相同。下列说法不正确的是( )
A.原子半径:
B.WY 可用做耐火材料
2 3
C.X与Y、Y与Z均可形成具有漂白性的化合物
D.W与X的最高价氧化物的水化物可相互反应
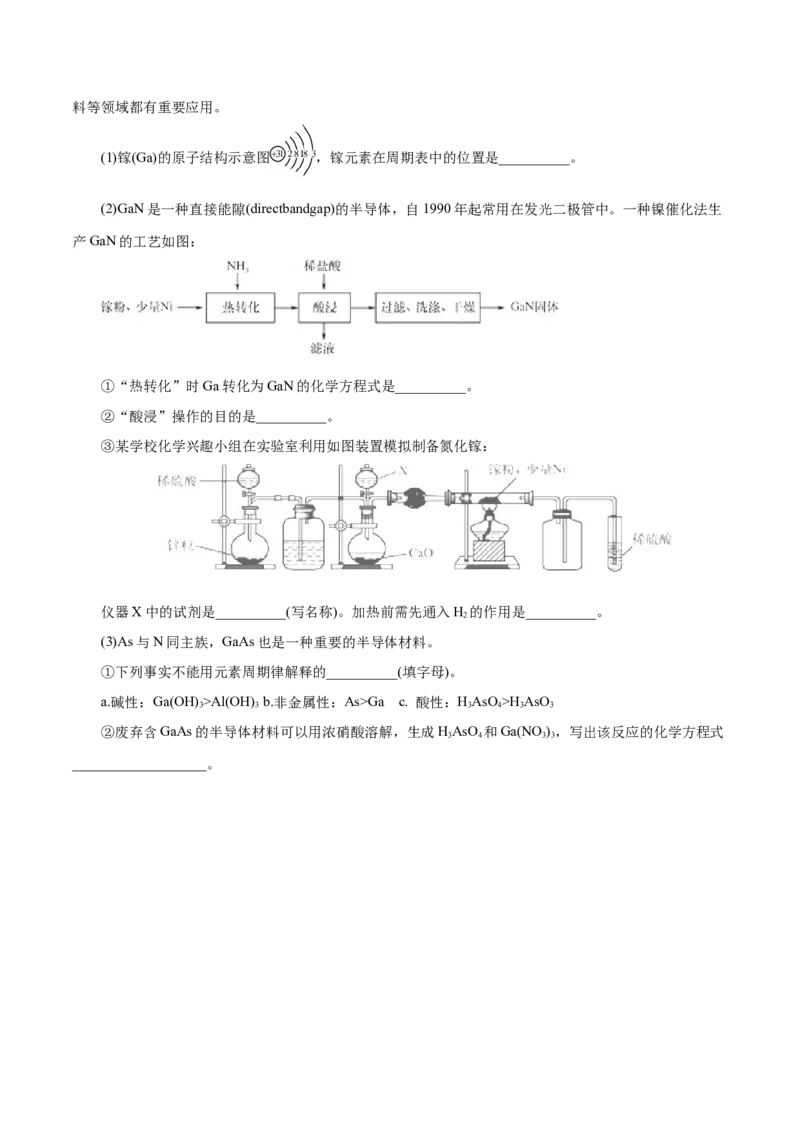
25.(2021·广东佛山市期末)短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是所有
短周期主族元素中最大的,Y组成的单质是一种良好的半导体材料,Y的原子序数是Z的最外层电子数的
2倍,由W、X、Y三种元素形成的化合物M的结构如图所示.下列叙述正确的是( )A.XW是共价化合物
2
B.简单气态氢化物的稳定性:Y>Z
C.Y的最高价氧化物的水化物是一种弱酸
D.W、X、Z的简单离子半径依次增大
二、非选择题
26.(2021·浙江台州市期末)如图是现行元素周期表的一部分,请回答:
(1)元素Se在周期表中的位置为___________。
(2)下列说法正确的是___________。
A.丙位于周期表中从左到右数第13列
B.Bi的最高价氧化物的化学式为BiO
2 5
C.丁所形成的含氧酸是强酸
D.C、N、O三种元素的最高正价等于其所在族的族序数
(3)①阴影部分元素所形成的氢化物中热稳定性最高的是___________(填化学式)。请从原子结构的角度
解释其原因:___________。
②可在图中分界线(虚线部分)附近寻找___________(填序号)。
A.优良的催化剂 B.半导体材料 C.合金材料 D.新品种农药
(4)Pb能形成多种氧化物,如碱性氧化物PbO,酸性氧化物PbO ,还有类似于Fe O 中铁元素价态特征
2 3 4
(有两种价态)的Pb O,Pb O 能与硝酸发生非氧化还原反应生成一种盐和一种铅的氧化物,写出该反应的
3 4 3 4
化学方程式___________。
27.(2021·重庆市凤鸣山中学高二月考)现有部分短周期元素的性质或原子结构如表:
元素编号 元素性质或原子结构X 最外层电子数是次外层电子数的2倍
Y 常温下单质为双原子分子,其氢化物水溶液呈碱性
Z 第三周期元素的简单离子中半径最小
(1)元素X在元素周期表中的位置为____,X的一种同位元素可测定文物年代,这种同位素的符号是
______(用元素符号表示)。
(2)元素Z的离子结构示意图为________,元素Y与氢元素形成离子YH 的电子式为________。
(3)元素X 、Y 、Z的原子半径从大到小的顺序为________(用元素符号表示)。
(4)元素X与元素Y相比,非金属性较强的是________(用元素符号表示)。下列表述中能证明这一事实
的是________。
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物对应水化物的酸性比X的最高价氧化物对应水化物的酸性强
c.X与Y形成的化合物中X元素呈正价状态
(5)Y的最高价氧化物的水化物与气态氢化物合成的化合物含的化学键类型是_________。
(6) )写出Z元素最高价氧化物对应的水化物与NaOH溶液反应的离子方程式:________。
28.(2021·宁夏长庆高级中学高三月考)A、B、C、D、E、F是原子序数依次增大的短周期主族元素,
A、E在元素周期表中的相对位置如图,A与氧元素能形成两种无色气体,C是地壳中含量最多的元素,D
是地壳中含量最多的金属元素。
A
E
(1)C在元素周期表中的位置为______,其离子的结构示意图为______。
(2)AE 的电子式为______。
2
(3)元素B与氢元素能形成含有18个电子的分子,其中含有的化学键有______、______。
(4)A、B、C最简单氢化物的稳定性由强到弱的顺序是______(填分子式)。
(5)实验室制取F 气体的离子方程式为______。
2
(6)在微电子工业中,B的最简单气态氢化物的水溶液可作刻蚀剂HO 的清除剂,所发生反应的产物不
2 2
污染环境,其化学方程式为______。
(7)DF 的水溶液可作净水剂,写出有关的离子方程式______。
3
29.(2021·安徽黄山市屯溪一中高三月考)金属镓(Ga)应用广泛,在半导体和光电材料、合金、磁性材料等领域都有重要应用。
(1)镓(Ga)的原子结构示意图 ,镓元素在周期表中的位置是__________。
(2)GaN是一种直接能隙(directbandgap)的半导体,自1990年起常用在发光二极管中。一种镍催化法生
产GaN的工艺如图:
①“热转化”时Ga转化为GaN的化学方程式是__________。
②“酸浸”操作的目的是__________。
③某学校化学兴趣小组在实验室利用如图装置模拟制备氮化镓:
仪器X中的试剂是__________(写名称)。加热前需先通入H 的作用是__________。
2
(3)As与N同主族,GaAs也是一种重要的半导体材料。
①下列事实不能用元素周期律解释的__________(填字母)。
a.碱性:Ga(OH) >Al(OH) b.非金属性:As>Ga c. 酸性:HAsO >H AsO
3 3 3 4 3 3
②废弃含GaAs的半导体材料可以用浓硝酸溶解,生成HAsO 和Ga(NO ),写出该反应的化学方程式
3 4 3 3
___________________。