文档内容
高频考点 32 盐类水解的原理及应用
1.(双选)(2022 ·海南卷)NaClO溶液具有漂白能力,已知25℃时,K (HClO)=4.0×10-8。下列关于NaClO
a
溶液说法正确的是( )
A.0.01mol/L NaClO溶液中,c(ClO—)<0.01mol/L
B.长期露置在空气中,释放Cl ,漂白能力减弱
2
C.通入过量SO ,反应的离子方程式为SO +ClO—+H O=HSO +HClO
2 2 2
D.25℃,pH=7.0的NaClO和HClO的混合溶液中,c(HClO)>c(ClO—)=c(Na+)
1.AD A.由题意可知,次氯酸是弱酸,次氯酸根离子会在溶液中发生水解反应使溶液呈碱性,则
0.01mol/L次氯酸钠溶液中次氯酸根离子浓度0.01mol/L,故A正确;B.次氯酸钠是强碱弱酸盐,次氯酸钠
在溶液中发生水解反应生成次氯酸和氢氧化钠,溶液中次氯酸长期露置在空气中遇光会发生分解反应生成
盐酸和氧气,不可能释放出氯气,故B错误;C.过量的二氧化硫与次氯酸钠溶液发生氧化还原反应生成
硫酸和氯化钠,反应的离子方程式为SO +ClO−+H O=Cl—+ +2H+,故C错误;D.25℃,pH=7.0的次氯酸
2 2
钠和次氯酸的混合溶液呈中性,溶液中存在电荷守恒关系c(ClO—)+c(OH—)=c(H+)+c(Na+),则溶液中c(ClO
—)=c(Na+),由次氯酸的电离常数可知,次氯酸根离子在溶液中水解常数为K = = =
h
>K ,则等浓度的次氯酸钠和次氯酸的混合溶液中,次氯酸根离子的水解程度大于次氯酸的电离
a
程度,溶液呈碱性,所以中性溶液中次氯酸的浓度大于次氯酸根离子,溶液中微粒浓度的大小关系为
c(HClO)>c(ClO-)=c(Na+),故D正确;故选AD。
FeCl FeCl Na SO 0.1molL-1
2.(2022·湖南卷)为探究 3的性质,进行了如下实验( 3和 2 3溶液浓度均为 )。
实
操作与现象
验
① 在5mL水中滴加2滴 FeCl 3溶液,呈棕黄色;煮沸,溶液变红褐色。
5mL FeCl Na SO
在 3溶液中滴加2滴 2 3溶液,变红褐色;
②
K Fe(CN)
再滴加 3 6 溶液,产生蓝色沉淀。5mL Na SO FeCl
在 2 3溶液中滴加2滴 3溶液,变红褐色;
③ K Fe(CN)
将上述混合液分成两份,一份滴加 3 6 溶液,无蓝色沉淀生;
另一份煮沸,产生红褐色沉淀。
依据上述实验现象,结论不合理的是( )
Fe3+
A.实验①说明加热促进 水解反应
Fe3+
B.实验②说明 既发生了水解反应,又发生了还原反应
Fe3+
C.实验③说明 发生了水解反应,但没有发生还原反应
SO2- Fe3+
D.整个实验说明 3 对 的水解反应无影响,但对还原反应有影响
2.D A.铁离子的水解反应为吸热反应,加热煮沸可促进水解平衡正向移动,使水解程度加深,生成较
多的氢氧化铁,从而使溶液显红褐色,故A正确;B.在5mLFeCl 溶液中滴加2滴同浓度的Na SO 溶液,
3 2 3
根据现象和分析可知,Fe3+既发生了水解反应,生成红褐色的氢氧化铁,又被亚硫酸根离子还原,得到亚
铁离子,加入铁氰化钾溶液后,出现特征蓝色沉淀,故B正确;C.实验③中在5mL Na SO 溶液中滴加2
2 3
滴同浓度少量FeCl 溶液,根据现象和分析可知,仍发生铁离子的水解反应,但未来得及发生铁离子的还原
3
反应,即水解反应比氧化还原反应速率快,故C正确;D.结合三组实验,说明铁离子与亚硫酸根离子混
合时,铁离子的水解反应占主导作用,比氧化还原反应的速率快,因证据不足,不能说明亚硫酸离子对铁
离子的水解作用无影响,事实上,亚硫酸根离子水解显碱性,可促进铁离子的水解反应,故D错误。综上
所述,答案为D。
3.(2021·北京卷)下列实验中,均产生白色沉淀。
下列分析不正确的是( )
A.Na CO 与NaHCO 溶液中所含微粒种类相同
2 3 3
B.CaCl 能促进Na CO 、NaHCO 水解
2 2 3 3
C.Al (SO ) 能促进Na CO 、NaHCO 水解
2 4 3 2 3 3
D.4个实验中,溶液滴入后,试管中溶液pH均降低3.B A.Na CO 溶液、NaHCO 溶液均存在Na+、 、 、H CO 、H+、OH-、H O,故含有的微粒种类
2 3 3 2 3 2
相同,A正确;B. H++ ,加入Ca2+后,Ca2+和 反应生成沉淀,促进 的电离,B
错误;C.Al3+与 、 都能发生互相促进的水解反应,C正确;D.由题干信息可知形成沉淀时会消
耗碳酸根和碳酸氢根,则它们浓度减小,水解产生的氢氧根的浓度会减小,pH减小,D正确;故选B。
4.(2021·山东·高密三中高三期中)下列说法中正确的是( )
A.AlCl 溶液和Al (SO ) 溶液分别加热、蒸发、浓缩结晶、灼烧,所得固体的成分相同
3 2 4 3
B.实验室配制FeCl 溶液时,先将FeCl 溶于水,再加入少量的盐酸
3 3
C.向CuCl 溶液中加入CuO调节pH,可除去溶液中混有的Fe3+
2
D.用Na CO 和Al (SO ) 两种溶液作泡沫灭火剂效果更好
2 3 2 4 3
4.C A.AlCl 溶液水解生成氢氧化铝和氯化氢,氯化氢易挥发,加热、蒸发、浓缩结晶,氯化氢挥发得到
3
水解产物氢氧化铝,灼烧得到氧化铝;Al (SO ) 溶液水解生成氢氧化铝和硫酸,硫酸是难挥发性酸,加热、
2 4 3
蒸发、浓缩结晶、灼烧,水挥发得到硫酸铝固体,所得固体的成分不相同,故A错误;B.配制FeCl 溶液
3
时,应将FeCl 固体溶解在盐酸中抑制铁离子水解,再加水稀释到所需浓度,故B错误;C.Fe3++3H O
3 2
Fe(OH) +3H+,向CuCl 溶液中加入CuO,消耗H+,使上述平衡正向移动生成氢氧化铁沉淀,达到通过调节
3 2
pH除去溶液中混有的Fe3+的目的,故C正确;D.泡沫灭火器中常使用的原料是NaHCO 和Al (SO ) ,故D
3 2 4 3
错误;
答案选C。
5.化学与生产、生活密切相关。下列说法错误的是( )
A.用Na S除去工业废水中的Cu2+和Hg2+
2
B.用广泛pH试纸测得氯水的pH为2
C.用纯碱溶液除油污,加热可提高去污能力
D.用明矾除去水中的悬浮物
5.B A.向工业废水中加入Na S,可以使Cu2+和Hg2+转化为CuS和HgS沉淀,从而除去,故A正确;B.氯
2
水溶液具有强氧化性,可以将广泛pH试纸漂白,不能用广泛pH试纸测氯水溶液的pH,故B错误;C.纯
碱即碳酸钠,水解呈碱性,加热可以促进水解,增强碱性,提高去污能力,故C正确;D.明矾溶于水电
离出的铝离子水解生成氢氧化铝胶体,胶体具有吸附性,因此可用明矾除去水中的悬浮物,故D正确;故
选B。6.新型冠状病毒灭活疫苗的辅料中含有 、 等。已知 为三元酸,室温时,
、 、 。室温时,向 溶液中逐滴加入等浓度的 溶液至过
量。下列叙述正确的是( )
A.该过程中发生反应的离子方程式有
B.反应 的平衡常数的数量级为
C.当所得溶液中溶质只有 时,溶液显碱性
D.当所得溶液的 时,溶液中:
6.D A.已知H PO 为三元酸,0.1mol·L−1H PO 溶液中逐滴加入等浓度的NaOH溶液至过量, 首先发生,
3 4 3 4
H PO +OH−=H PO +H O,其次发生H PO +OH−=HPO +H O,最后发生HPO +OH−=PO +H O,A错误;B.
3 4 2 2 2 2 2
反应PO +H O HPO +OH−的平衡表达式为K= = = =
2
⇌
=10-1.3,平衡常数的数量级为10-2,B错误;C. H PO HPO +H+,K =10-7.2,H PO +H O H PO +OH−的
2 a2 2 2 3 4
⇌ ⇌
K= = = = =10-11.8<10-7.2,H PO 电离大于H PO 水解显酸性,C
2 2
错误;D.由反应 H PO HPO +H+,K =10-7.2,H PO H PO +H+,K =10-2.2,可得K ×K =10-2.2×10-7.2=
2 a2 3 4 2 a1 a1 a2
⇌ ⇌
× = ,当所得溶液的pH=6时, =10-9.4,中:
c(HPO )=10-9.4+12c(H PO )=102.6c(H PO )>200 c(H PO ),D正确;故选D。
3 4 3 4 3 47.(双选)(2022·河北·模拟预测)室温下,通过下列实验探究 的性质:
实
实验操作和现象
验
1 用pH试纸测定 溶液的pH,测得pH约为10
2 向浓度为 溶液中加入足量NaOH,有刺激性气味气体产生
3 浓度均为 溶液和NaCl溶液等体积混合,有晶体析出,过滤
下列说法正确的是A. 溶液中存在:
B.由实验1可得:
C.实验2中发生反应的离子方程式:
D.实验3中所得滤液中存在:
7.AB A.根据质子守恒 溶液中存在:
,A项正确;B.由实验1溶液呈碱性可知,水解程度:
< ,故可得: ,B项正确;
C.实验2中发生反应的离子方程式为: , ,C项错误;
D.析出晶体为NaHCO ,根据物料守恒,实验3中所得滤液中存在: ,
3
, ,故:
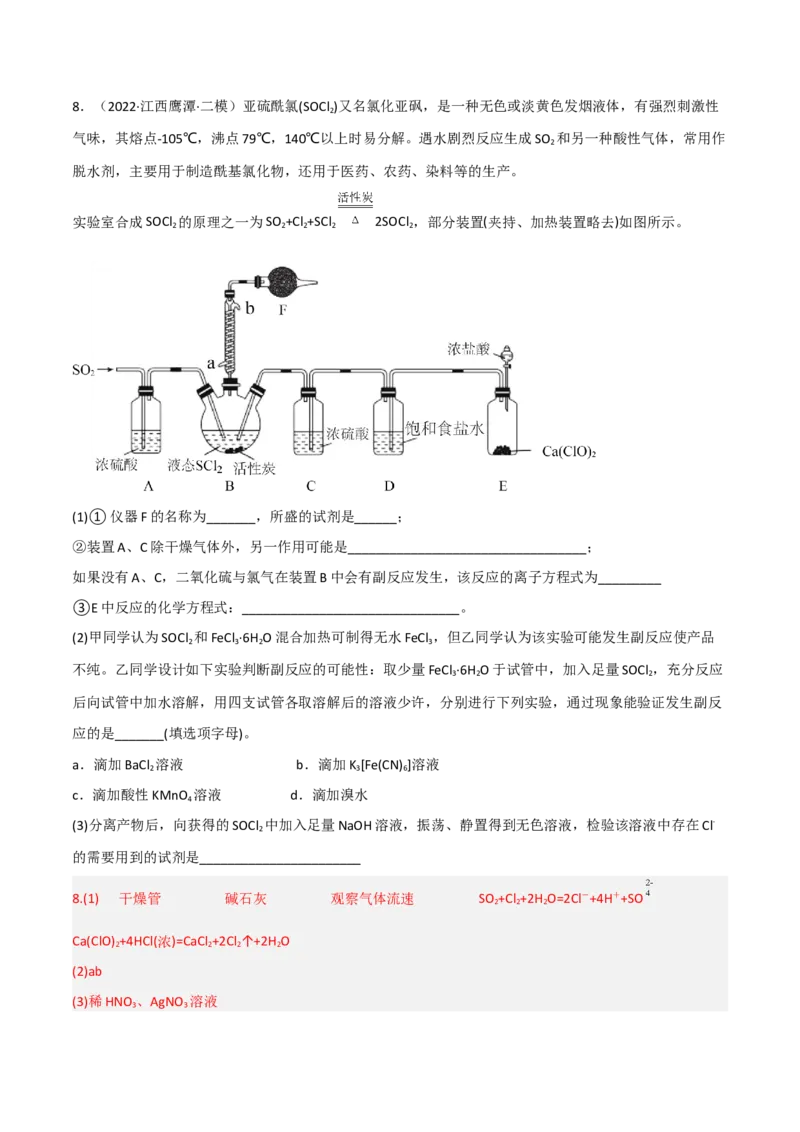
,D项错误;答案选AB。8.(2022·江西鹰潭·二模)亚硫酰氯(SOCl )又名氯化亚砜,是一种无色或淡黄色发烟液体,有强烈刺激性
2
气味,其熔点-105℃,沸点79℃,140℃以上时易分解。遇水剧烈反应生成SO 和另一种酸性气体,常用作
2
脱水剂,主要用于制造酰基氯化物,还用于医药、农药、染料等的生产。
实验室合成SOCl 的原理之一为SO +Cl +SCl 2SOCl ,部分装置(夹持、加热装置略去)如图所示。
2 2 2 2 2
(1)①仪器F的名称为_______,所盛的试剂是______;
②装置A、C除干燥气体外,另一作用可能是__________________________________;
如果没有A、C,二氧化硫与氯气在装置B中会有副反应发生,该反应的离子方程式为_________
③E中反应的化学方程式:_______________________________。
(2)甲同学认为SOCl 和FeCl ·6H O混合加热可制得无水FeCl ,但乙同学认为该实验可能发生副反应使产品
2 3 2 3
不纯。乙同学设计如下实验判断副反应的可能性:取少量FeCl ·6H O于试管中,加入足量SOCl ,充分反应
3 2 2
后向试管中加水溶解,用四支试管各取溶解后的溶液少许,分别进行下列实验,通过现象能验证发生副反
应的是_______(填选项字母)。
a.滴加BaCl 溶液 b.滴加K [Fe(CN) ]溶液
2 3 6
c.滴加酸性KMnO 溶液 d.滴加溴水
4
(3)分离产物后,向获得的SOCl 中加入足量NaOH溶液,振荡、静置得到无色溶液,检验该溶液中存在Cl-
2
的需要用到的试剂是_______________________
8.(1) 干燥管 碱石灰 观察气体流速 SO +Cl +2H O=2Cl-+4H++SO
2 2 2
Ca(ClO) +4HCl(浓)=CaCl +2Cl ↑+2H O
2 2 2 2
(2)ab
(3)稀HNO 、AgNO 溶液
3 3解析:(1)①仪器F的名称为干燥管,中的试剂的作用是除去未反应的SO 和Cl ,同时可以防止空气中的
2 2
水蒸气进入三颈烧瓶,因为亚硫酰氯遇水剧烈反应,所以仪器F中可以装有碱石灰;故答案为:干燥管;
碱石灰;
②根据反应方程式:SO +Cl +SCl 2SOCl ,SO 和Cl 的物质的量最好相等,所以装置A、C除干燥气体
2 2 2 2 2 2
外,另一作用是观察气体流速,控制SO 和Cl 的物质的量之比;如果没有A、C,二氧化硫与氯气和水发生
2 2
氧化还原反应生成盐酸和硫酸,该反应的离子方程式为SO +Cl +2H O=2Cl-+4H++SO ,故答案为:观察气
2 2 2
体流速;SO +Cl +2H O=2Cl-+4H++SO ;
2 2 2
③装置 E中次氯酸钙和浓盐酸反应制取氯气,发生反应的化学方程式为:
Ca(ClO) +4HCl(浓)=CaCl +2Cl ↑+2H O,故答案为:Ca(ClO) +4HCl(浓)=CaCl +2Cl ↑+2H O;
2 2 2 2 2 2 2 2
(2)FeCl 具有强氧化性,会和SOCl 发生氧化还原反应,可能发生的副反应
3 2
SOCl +2FeCl •6H O=FeSO +6HCl+FeCl +9H O,
2 3 2 4 2 2
a.滴加BaCl 溶液与硫酸根反应生成硫酸钡沉淀,可检验硫酸根存在,进而说明产物有FeSO ,能验证发生
2 4
副反应,a选;
b.滴加K [Fe(CN) ]溶液与Fe2+形成蓝色沉淀,可检验Fe2+存在,能验证发生副反应,b选;
3 6
c.由于溶液中存在氯离子,加入酸性KMnO 溶液必然会褪色,无法证明发生副反应,c不选;
4
d.滴加溴水会和SOCl 发生氧化还原反应,无法证明发生副反应,d不选;故答案为:ab;
2
(3)检验Cl-的存在,方法是取少量溶液于洁净的试管,滴入稀HNO 酸化,再加入AgNO 溶液,产生白色沉
3 3
淀,则说明溶液中有Cl-的存在;所以检验溶液中存在Cl-的试剂有:稀HNO 、AgNO 溶液。
3 3