文档内容
2020年天津市普通高中学业水平等级性考试
化 学
相对原子质量:H1 O16 S32 Co 59 Cu 64 Zn 65 Ba 137
第I卷
1.在全国人民众志成城抗击新冠病毒期间,使用的“84消毒液”的主要有效成分是
A. NaOH B. NaCl C. NaClO D. Na CO
2 3
【答案】C
【解析】
【详解】工业上用Cl 与NaOH溶液反应制取“84消毒液”,反应原理为Cl +2NaOH=NaCl+NaCl
2 2
O+H O,NaClO具有强氧化性,能用于杀菌消毒,故“84消毒液”的主要有效成分是NaClO,
2
答案选C。
2.晋朝葛洪的《肘后备急方》中记载:“青蒿一握,以水二升渍,绞取汁,尽服之……”,受
此启发为人类做出巨大贡献的科学家是
A. 屠呦呦 B. 钟南山 C. 侯德榜 D. 张青莲
【答案】A
【解析】
【详解】A.屠呦呦的主要贡献是发现了治疗疟疾的青蒿素,测定了青蒿素的组成、结构,成
功合成双氢青蒿素等;
B.钟南山是中国工程院院士,著名呼吸病学专家,长期从事呼吸内科的医疗、教学、科研工
作,重点开展哮喘,慢阻肺疾病,呼吸衰竭和呼吸系统常见疾病的规范化诊疗、疑难病、少
见病和呼吸危重症监护与救治等方面的研究;
C.侯德榜的主要贡献是:揭开了索尔维制碱法的秘密、创立了侯氏制碱法等;
D.张青莲的主要贡献:主持测定了铟、铱、锑、铕、铈、锗、锌、镝几种元素的相对原子质
量新值,被国际原子量委员会采用为国际新标准;
“青蒿一握,以水二升渍,绞取汁,尽服之……”描述的是从青蒿中提取青蒿素治疗疟疾的
过程,受此启发为人类做出巨大贡献的科学家是屠呦呦;答案选A。
3.下列说法错误的是
第- 1 -页 | 共21页A. 淀粉和纤维素均可水解产生葡萄糖
B. 油脂的水解反应可用于生产甘油
C. 氨基酸是组成蛋白质的基本结构单元
D. 淀粉、纤维素和油脂均是天然高分子
【答案】D
【解析】
【详解】A.淀粉和纤维素都属于多糖,两者水解的最终产物都为葡萄糖,A正确;
B.油脂在酸性条件下水解成高级脂肪酸和甘油,在碱性条件下水解成高级脂肪酸盐和甘油,
则油脂的水解反应可用于生产甘油,B正确;
C.氨基酸中含有氨基和羧基,氨基酸可以通过缩聚反应形成蛋白质,蛋白质水解最终生成氨
基酸,故氨基酸是组成蛋白质的基本结构单元,C正确;
D.天然高分子的相对分子质量是上万,淀粉和纤维素都是天然高分子,而油脂的相对分子质
量还不到1000,故油脂不属于高分子,D错误;
答案选D。
4.下列离子方程式书写正确的是
A. CaCO 与稀硝酸反应:CO2-+2H+=H O+CO
3 3 2 2
B. FeSO 溶液与溴水反应:2Fe2++Br =2Fe3++2Br-
4 2
C. NaOH溶液与过量H C O 溶液反应:H C O +2OH-=C O2-+2H O
2 2 4 2 2 4 2 4 2
D. C H ONa溶液中通入少量CO : 2C H O-+CO +H O=2C H OH+CO2-
6 5 2 6 5 2 2 6 5 3
【答案】B
【解析】
【详解】A.CaCO 与稀硝酸反应生成硝酸钙和水和二氧化碳,碳酸钙是固体难溶物,写离
3
子方程式时不能拆成离子形式,正确的离子方程式为:
CaCO +2H+ =Ca2++H O+CO ,故A错误;
3 2 2
B.FeSO 溶液与溴水反应时,溴单质氧化了亚铁离子,将亚铁离子氧化成铁离子,正确的离
4
子方程式为:2Fe2+ +Br =2Fe3+ +2Br-,故B正确;
2
C.氢氧化钠与过量的草酸反应,说明氢氧化钠的量不足,生成草酸氢钠,正确的离子方程
第- 2 -页 | 共21页式为H C O +OH-=HC O-+H O,故C错误;
2 2 4 2 4 2
D.苯酚钠中通入少量或过量二氧化碳都生成苯酚和碳酸氢钠,苯酚的酸性弱于碳酸强于碳
酸氢根,故正确的离子方程式为:C H O-+CO +H O=C H OH+HCO-,故D错误;
6 5 2 2 6 5 3
答案选B。
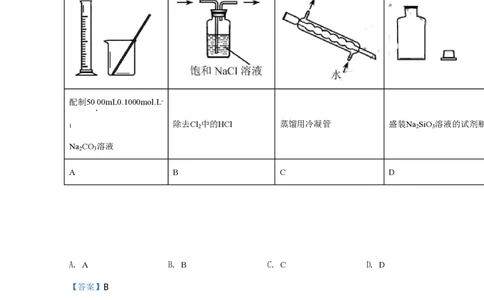
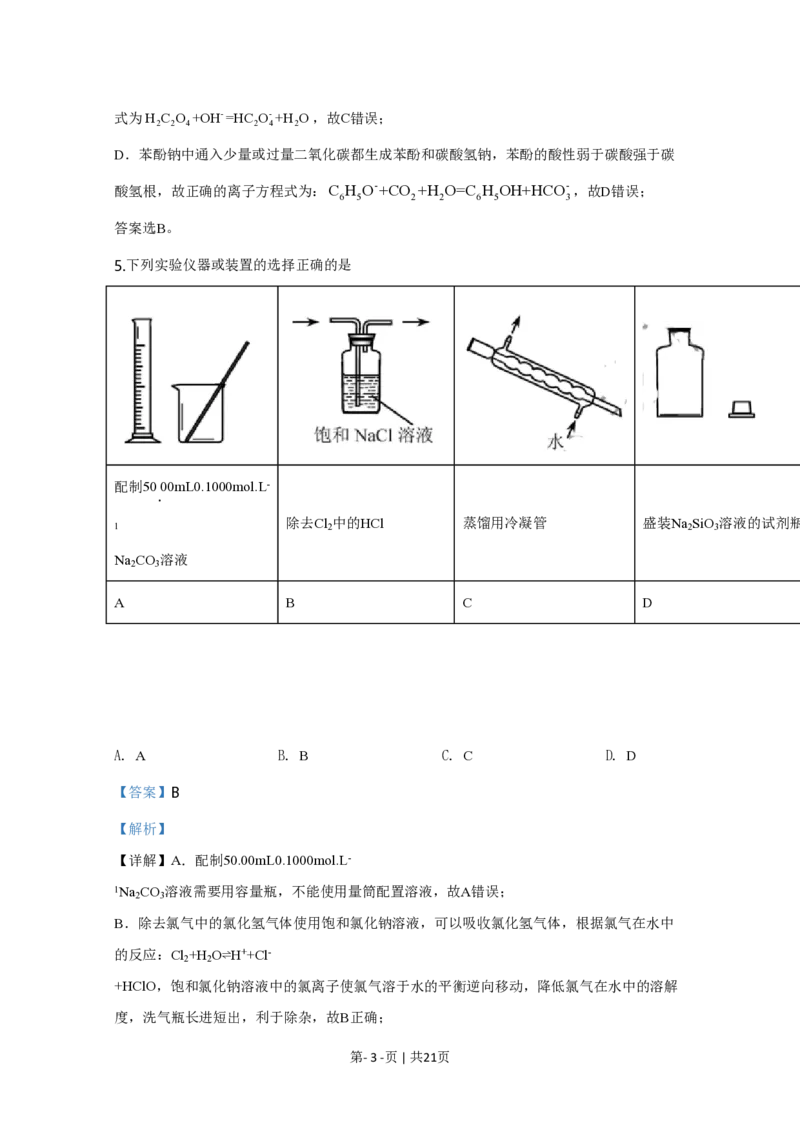
5.下列实验仪器或装置的选择正确的是
配制5000mL0.1000mol.L-
.
除去Cl 中的HCl 蒸馏用冷凝管 盛装Na SiO 溶液的试剂瓶
1 2 2 3
Na CO 溶液
2 3
A B C D
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A.配制50.00mL0.1000mol.L-
1Na CO 溶液需要用容量瓶,不能使用量筒配置溶液,故A错误;
2 3
B.除去氯气中的氯化氢气体使用饱和氯化钠溶液,可以吸收氯化氢气体,根据氯气在水中
的反应:Cl +H O⇌H++Cl-
2 2
+HClO,饱和氯化钠溶液中的氯离子使氯气溶于水的平衡逆向移动,降低氯气在水中的溶解
度,洗气瓶长进短出,利于除杂,故B正确;
第- 3 -页 | 共21页C.蒸馏要使用直形冷凝管,不能使用球形冷凝管,故C错误;
D.硅酸钠溶液呈碱性,硅酸钠溶液是一种矿物胶,能将玻璃塞与试剂瓶的瓶口粘在一起,
盛装Na SiO 溶液的试剂瓶不能使用玻璃塞,应使用橡胶塞,故D错误。
2 3
答案选B。
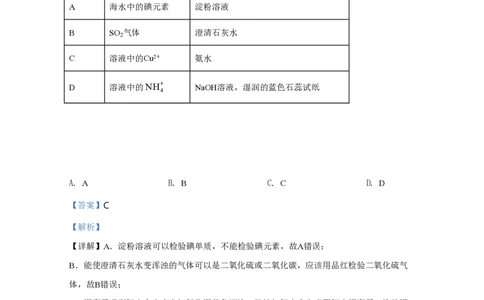
6.检验下列物所选用的试剂正确的是
待检验物质 所用试剂
A 海水中的碘元素 淀粉溶液
B SO 气体 澄清石灰水
2
C 溶液中的Cu2+ 氨水
D 溶液中的NH+ NaOH溶液,湿润的蓝色石蕊试纸
4
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.淀粉溶液可以检验碘单质,不能检验碘元素,故A错误;
B.能使澄清石灰水变浑浊的气体可以是二氧化硫或二氧化碳,应该用品红检验二氧化硫气
体,故B错误;
C.铜离子遇到氨水会先产生氢氧化铜蓝色沉淀,继续加氨水会生成四氨合铜离子,检验铜
离子可以用氨水,故C正确;
D.铵根离子遇氢氧化钠溶液(加热)生成氨气,氨气能使湿润的红色石蕊试纸变蓝,不能
使用湿润的蓝色石蕊试纸检验氨气,故D错误;
答案选C。
7.常温下,下列有关电解质溶液的说法错误的是
第- 4 -页 | 共21页A. 相同浓度的 HCOONa和NaF两溶液,前者的pH较大,则 K (HCOOH)>K (HF)
a a
B. 相同浓度的CH COOH和CH COONa两溶液等体积混合后pH约为4.7,则溶液中
3 3
c
CH
COO-
>c
Na+
>c
H+
>c
OH-
3
C. FeS溶于稀硫酸,而CuS不溶于稀硫酸,则K (FeS)>K (CuS)
sp sp
D. 在1mol L-1Na S溶液中,c S2- +c HS- +cH S=1mol L-1
g 2 2 g
【答案】A
【解析】
【详解】A.HCOONa和NaF的浓度相同,HCOONa溶液的pH较大,说明HCOO-的水解程度
较大,根据越弱越水解,因此甲酸的电离平衡常数较小,即K (HCOOH)<K (HF),故A错误
a a
;
B.相同浓度的CH COOH和CH COONa两溶液等体积混合后pH约为4.7,此时溶液呈酸性,
3 3
氢离子浓度大于氢氧根浓度,说明溶液中醋酸电离程度大于水解程度,则醋酸根浓度大于钠
离子浓度,则溶液中c(CH COO-)>c(Na+)>c(H+)>c(OH-),故B正确;
3
C.CuS的溶解度较小,将CuS投入到稀硫酸溶液中,CuS溶解平衡电离出的S2−不足以与H+发
生反应,而将FeS投入到稀硫酸后可以得到H S气体,说明K (FeS)>K (CuS),故C正确;
2 sp sp
D.根据溶液中的物料守恒定律,1 mol∙L−1
Na S溶液中所有含S元素的粒子的总物质的量的浓度为1 mol∙L−1,即c(S2−)+c(HS-)+c(H S)=1
2 2
mol∙L−1,故D正确;
综上所述,答案为A。
8.短周期元素X、Y、Z、W的原子序数依次增大。用表中信息判断下列说法正确的是
元素
X Y Z W
最高价氧化物的水化物 H ZO
3 4
0.1mol×L-1溶液对应的pH(25℃) 1.00 13.00 1.57 0.70
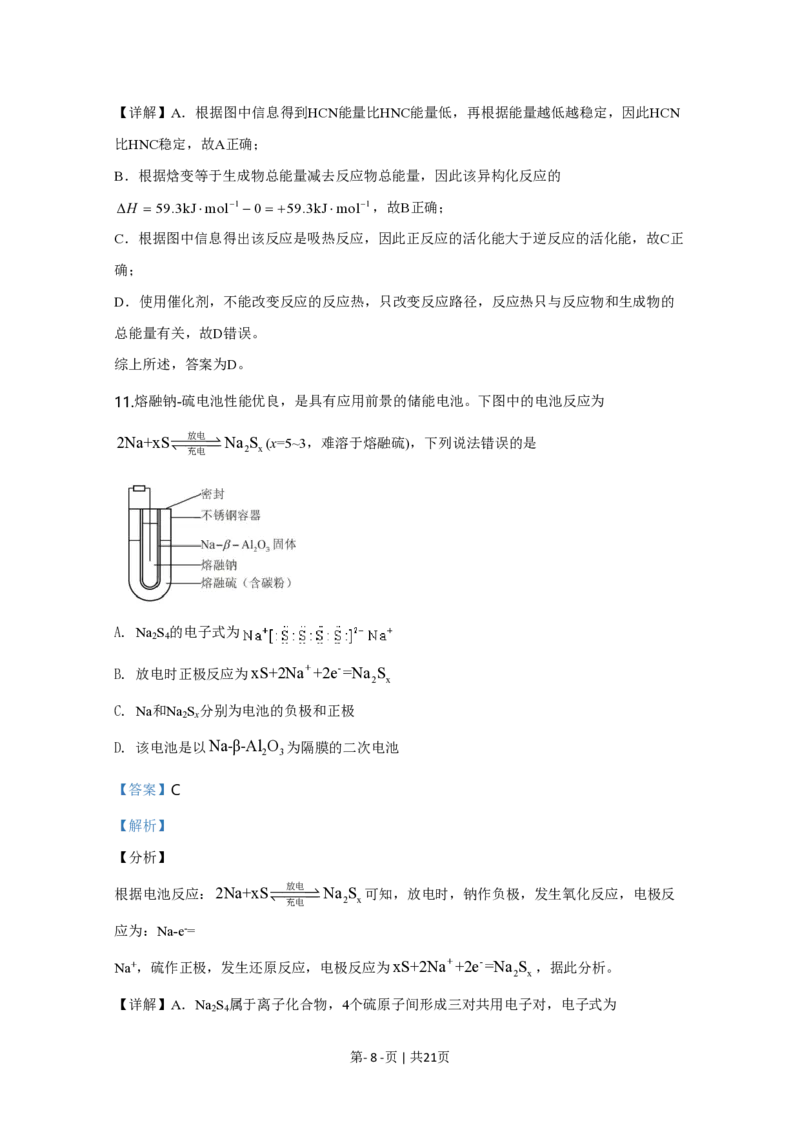
A. 元素电负性:ZCoCl 2-
4 4
【答案】D
【解析】
【详解】A.1个[Co(H O) ]2+中含有18个σ键,1个[CoCl ]2-
2 6 4
中含有4个σ键,等物质的量的[Co(H O) ]2+和[CoCl ]2-所含σ键数之比为18:4=9:2,A错误;
2 6 4
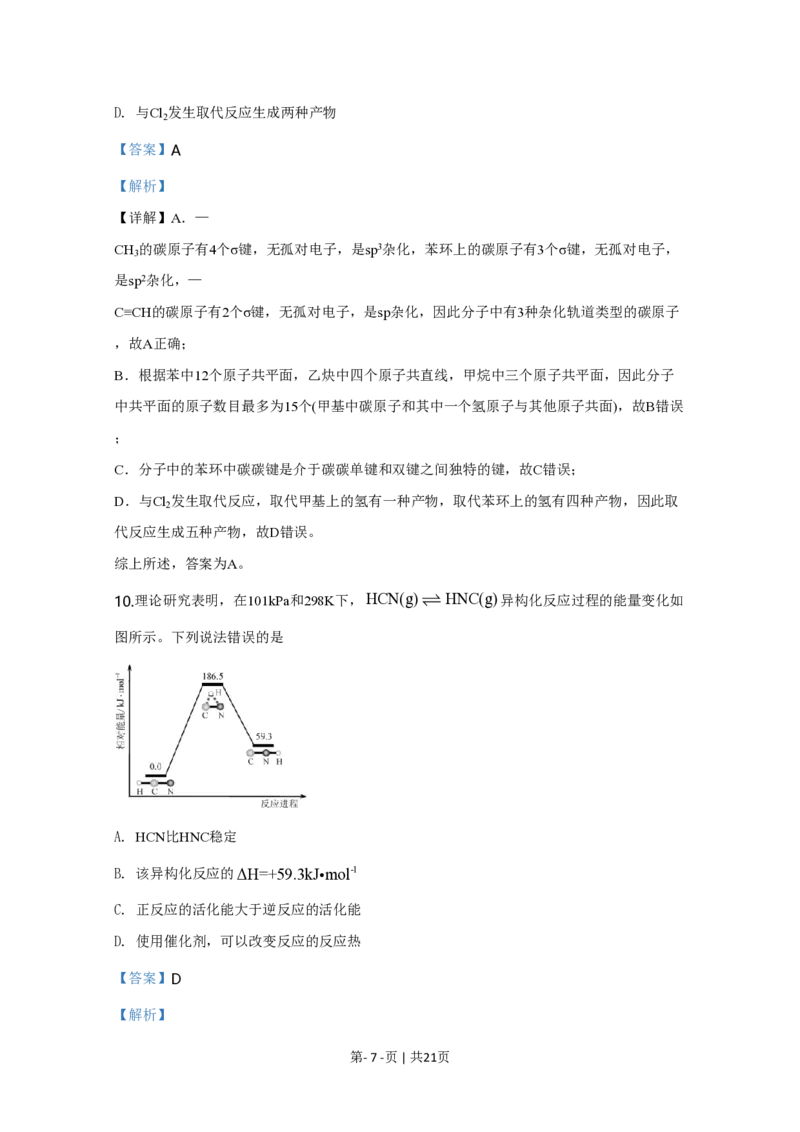
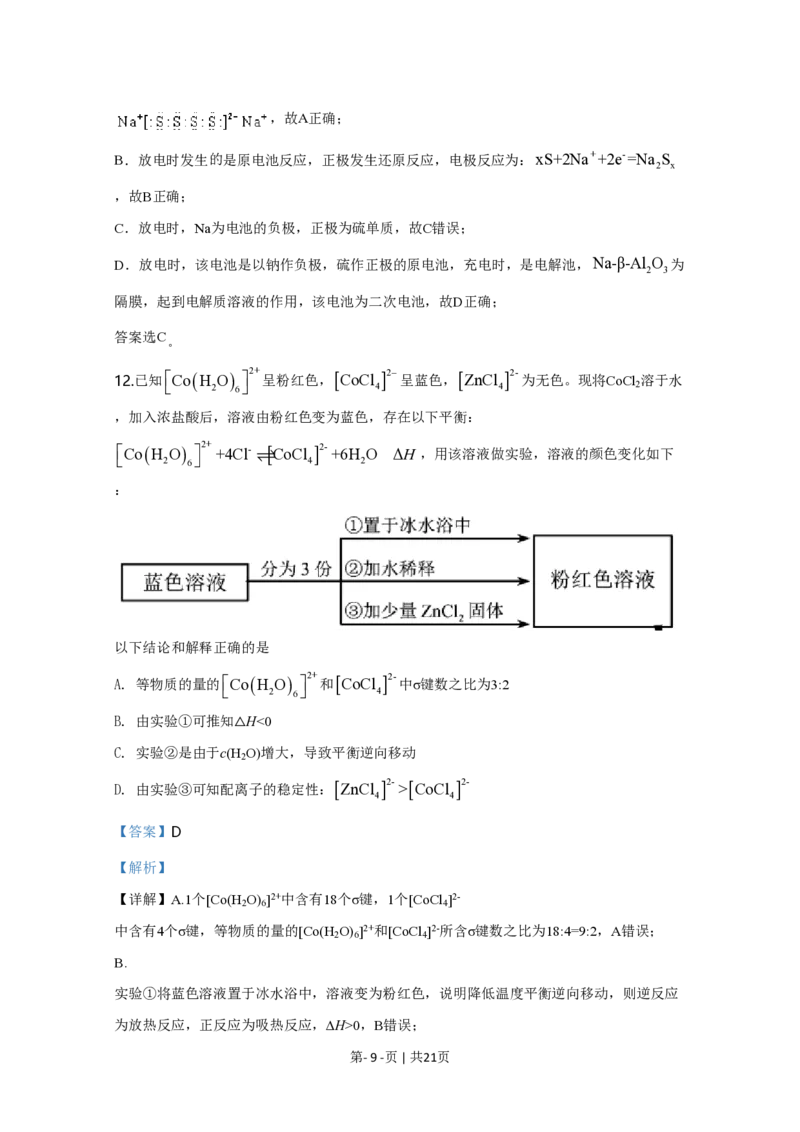
B.
实验①将蓝色溶液置于冰水浴中,溶液变为粉红色,说明降低温度平衡逆向移动,则逆反应
为放热反应,正反应为吸热反应,∆H>0,B错误;
第- 9 -页 | 共21页C. 实验②加水稀释,溶液变为粉红色,加水稀释,溶液的体积增大,[Co(H O) ]2+、[CoCl ]2-
2 6 4
、Cl-浓度都减小,[Co(H O) ]2+、Cl-的化学计量数之和大于[CoCl ]2-
2 6 4
的化学计量数,则瞬时浓度商>化学平衡常数,平衡逆向移动,C错误;
D. 实验③加入少量ZnCl 固体,溶液变为粉红色,说明Zn2+与Cl-结合成更稳定的[ZnCl ]2-
2 4
,导致溶液中c(Cl-)减小,平衡逆向移动,则由此说明稳定性:[ZnCl ]2->[CoCl ]2-
4 4
,D正确;
答案选D。
【点睛】本题有两个易错点:A项中[Co(H O) ]2+中不仅有Co2+与H O分子间的配位键,而且
2 6 2
每个H O分子中还有两个O—
2
Hσ键;C项中H O为溶剂,视为纯液体,加水稀释,溶液体积增大,相当于利用“对气体参与
2
的反应,增大体积、减小压强,平衡向气体系数之和增大的方向移动”来理解。
第Ⅱ卷
13.Fe、Co、Ni是三种重要的金属元素。回答下列问题:
(1)Fe、Co、Ni在周期表中的位置为_________,基态Fe原子的电子排布式为__________。
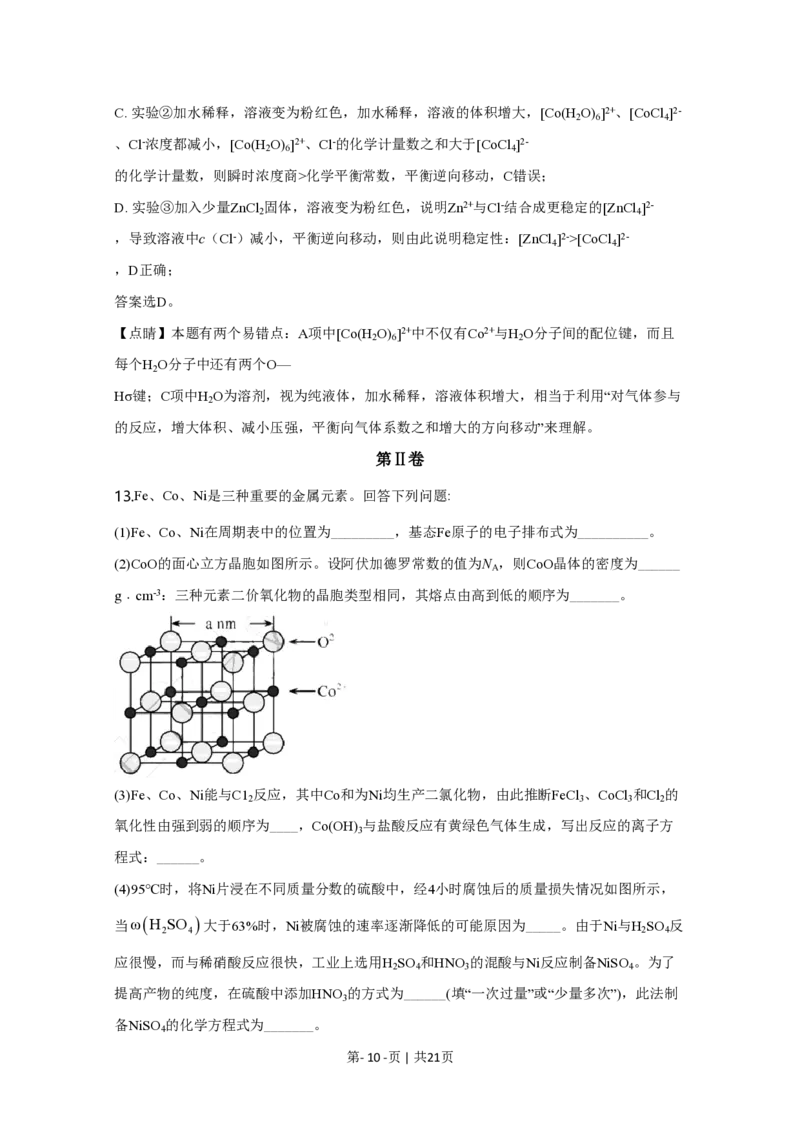
(2)CoO的面心立方晶胞如图所示。设阿伏加德罗常数的值为N ,则CoO晶体的密度为______
A
g﹒cm-3:三种元素二价氧化物的晶胞类型相同,其熔点由高到低的顺序为_______。
(3)Fe、Co、Ni能与C1 反应,其中Co和为Ni均生产二氯化物,由此推断FeCl 、CoCl 和Cl 的
2 3 3 2
氧化性由强到弱的顺序为____,Co(OH) 与盐酸反应有黄绿色气体生成,写出反应的离子方
3
程式:______。
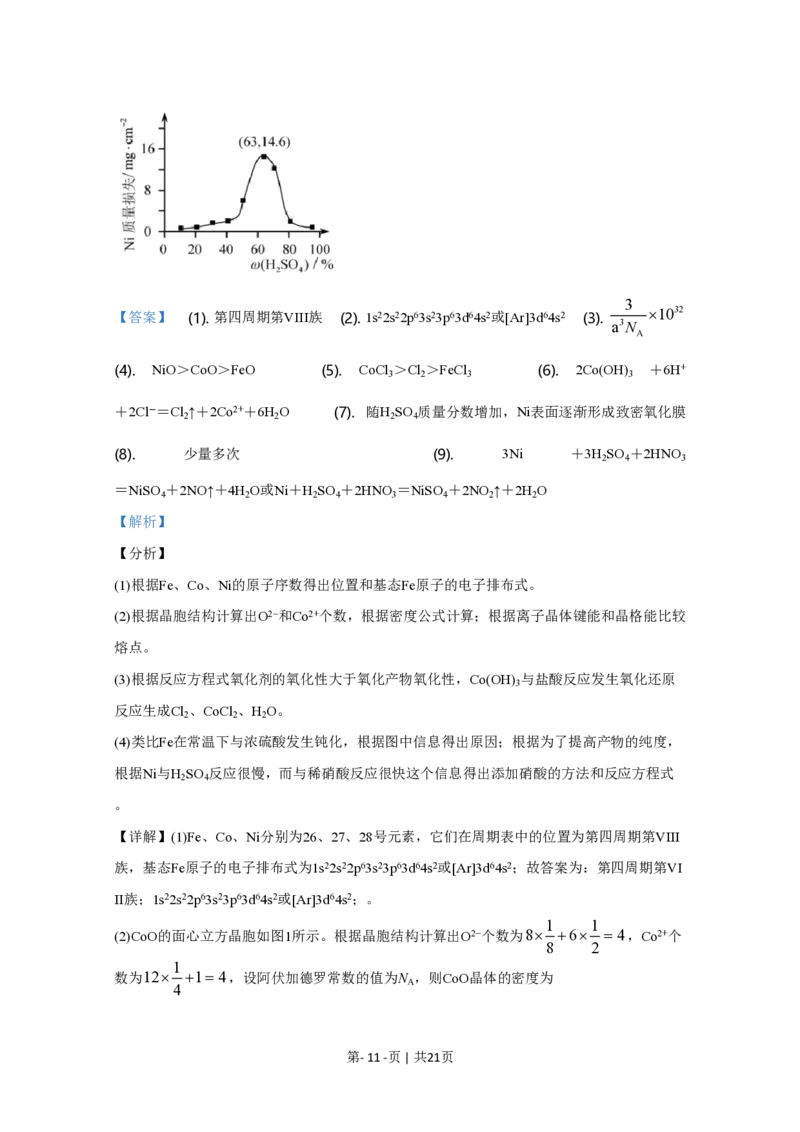
(4)95℃时,将Ni片浸在不同质量分数的硫酸中,经4小时腐蚀后的质量损失情况如图所示,
当ωH SO 大于63%时,Ni被腐蚀的速率逐渐降低的可能原因为_____。由于Ni与H SO 反
2 4 2 4
应很慢,而与稀硝酸反应很快,工业上选用H SO 和HNO 的混酸与Ni反应制备NiSO 。为了
2 4 3 4
提高产物的纯度,在硫酸中添加HNO 的方式为______(填“一次过量”或“少量多次”),此法制
3
备NiSO 的化学方程式为_______。
4
第- 10 -页 | 共21页3
【答案】 (1). 第四周期第VIII族 (2). 1s22s22p63s23p63d64s2或[Ar]3d64s2 (3).
´1032
a3N
A
(4). NiO>CoO>FeO (5). CoCl >Cl >FeCl (6). 2Co(OH) +6H+
3 2 3 3
+2Cl-=Cl ↑+2Co2++6H O (7). 随H SO 质量分数增加,Ni表面逐渐形成致密氧化膜
2 2 2 4
(8). 少量多次 (9). 3Ni +3H SO +2HNO
2 4 3
=NiSO +2NO↑+4H O或Ni+H SO +2HNO =NiSO +2NO ↑+2H O
4 2 2 4 3 4 2 2
【解析】
【分析】
(1)根据Fe、Co、Ni的原子序数得出位置和基态Fe原子的电子排布式。
(2)根据晶胞结构计算出O2−和Co2+个数,根据密度公式计算;根据离子晶体键能和晶格能比较
熔点。
(3)根据反应方程式氧化剂的氧化性大于氧化产物氧化性,Co(OH) 与盐酸反应发生氧化还原
3
反应生成Cl 、CoCl 、H O。
2 2 2
(4)类比Fe在常温下与浓硫酸发生钝化,根据图中信息得出原因;根据为了提高产物的纯度,
根据Ni与H SO 反应很慢,而与稀硝酸反应很快这个信息得出添加硝酸的方法和反应方程式
2 4
。
【详解】(1)Fe、Co、Ni分别为26、27、28号元素,它们在周期表中的位置为第四周期第VIII
族,基态Fe原子的电子排布式为1s22s22p63s23p63d64s2或[Ar]3d64s2;故答案为:第四周期第VI
II族;1s22s22p63s23p63d64s2或[Ar]3d64s2;。
1 1
(2)CoO的面心立方晶胞如图1所示。根据晶胞结构计算出O2−个数为8´ +6´ =4,Co2+个
8 2
1
数为12´ +1=4,设阿伏加德罗常数的值为N ,则CoO晶体的密度为
A
4
第- 11 -页 | 共21页75g×mol-1
´4
m N mol-1 3 ;三种元素二价氧化物的晶胞类型相同,离子
ρ= = A = ´1032g×cm-3
V (a´10-10cm)3 a3N
A
半径Fe2+>Co2+>Ni2+,NiO、CoO、FeO,离子键键长越来越长,键能越来越小,晶格能按N
iO、CoO、FeO依次减小,因此其熔点由高到低的顺序为NiO>CoO>FeO;故答案为:
3
´1032
;NiO>CoO>FeO。
a3N
A
(3)Fe、Co、Ni能与Cl 反应,其中Co和为Ni均生产二氯化物,根据铁和氯气反应生成FeCl ,
2 3
氧化剂的氧化性大于氧化产物氧化性,因此氧化性:Cl >FeCl ,氯气与Co和为Ni均生产二
2 3
氯化物,说明氯气的氧化性比CoCl 弱,由此推断FeCl 、CoCl 和Cl 的氧化性由强到弱的顺序
3 3 3 2
为CoCl >Cl >FeCl ,Co(OH) 与盐酸反应有黄绿色气体生成,发生氧化还原反应生成Cl 、
3 2 3 3 2
CoCl 、H O,其离子方程式:2Co(OH) +6H++2Cl-=Cl ↑+2Co2++6H O;故答案为:CoCl
2 2 3 2 2
>Cl >FeCl ;2Co(OH) +6H+ +2Cl-=Cl ↑+2Co2++6H O。
3 2 3 3 2 2
(4)类比Fe在常温下与浓硫酸发生钝化,根据图中信息,当wH SO 大于63%时,Ni被腐蚀
2 4
的速率逐渐降低的可能原因为随H SO 质量分数增加,Ni表面逐渐形成致密氧化膜。工业上
2 4
选用H SO 和HNO 的混酸与Ni反应制备NiSO 。为了提高产物的纯度,根据Ni与H SO 反应很
2 4 3 4 2 4
慢,而与稀硝酸反应很快,因此在硫酸中少量多次添加HNO 的方式来提高反应速率,反应
3
生成NiSO 、H O,根据硝酸浓度不同得到NO或NO ,此法制备NiSO 的化学方程式为3Ni+3
4 2 2 4
H SO +2HNO =NiSO +2NO↑+4H O或Ni+H SO +2HNO
2 4 3 4 2 2 4 3
=NiSO +2NO ↑+2H O;故答案为:随H SO 质量分数增加,Ni表面逐渐形成致密氧化膜;
4 2 2 2 4
少量多次;3Ni +3H SO +2HNO
2 4 3
=NiSO +2NO↑+4H O或Ni+H SO +2HNO =NiSO +2NO ↑+2H O。
4 2 2 4 3 4 2 2
【点睛】物质结构是常考题型,主要考查电子排布式、晶胞计算、氧化还原反应、学生学习
知识的能力的考查。
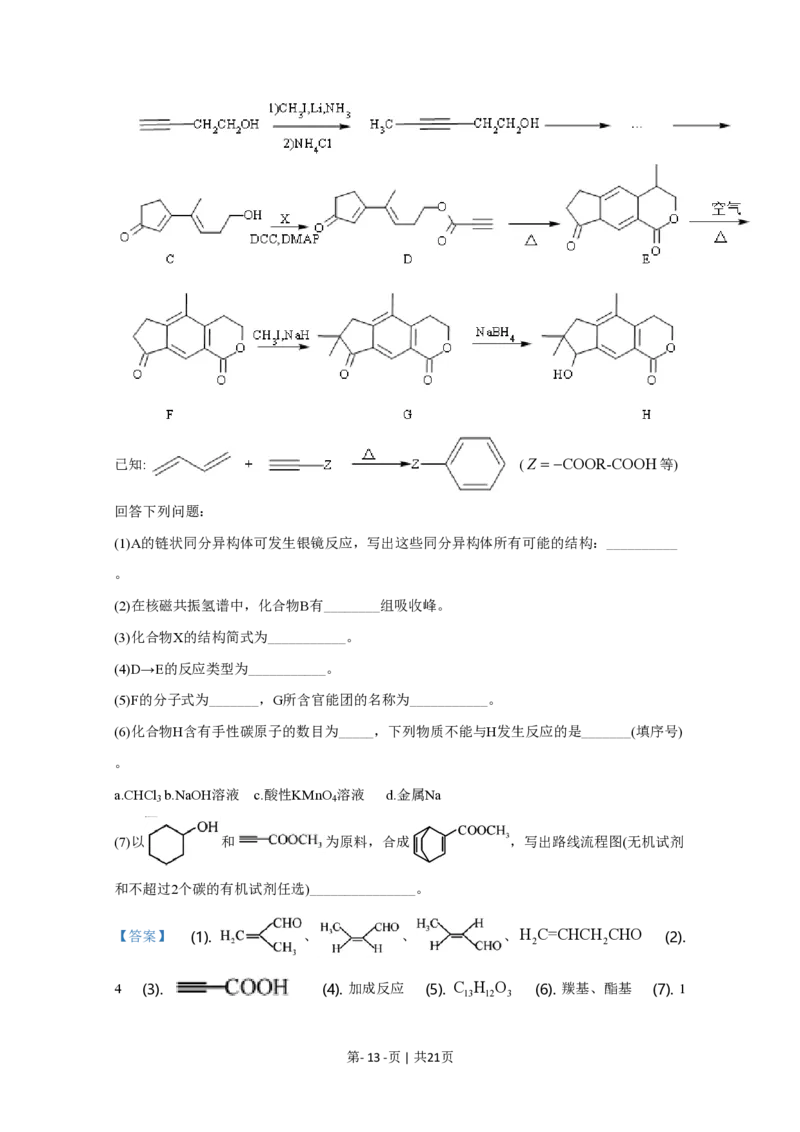
14.天然产物H具有抗肿瘤、镇痉等生物活性,可通过以下路线合成。
第- 12 -页 | 共21页已知: (Z =-COOR-COOH等)
回答下列问题:
(1)A的链状同分异构体可发生银镜反应,写出这些同分异构体所有可能的结构:__________
。
(2)在核磁共振氢谱中,化合物B有________组吸收峰。
(3)化合物X的结构简式为___________。
(4)D→E的反应类型为___________。
(5)F的分子式为_______,G所含官能团的名称为___________。
(6)化合物H含有手性碳原子的数目为_____,下列物质不能与H发生反应的是_______(填序号)
。
a.CHCl b.NaOH溶液 c.酸性KMnO 溶液 d.金属Na
3 4
(7)以 和 为原料,合成 ,写出路线流程图(无机试剂
和不超过2个碳的有机试剂任选)_______________。
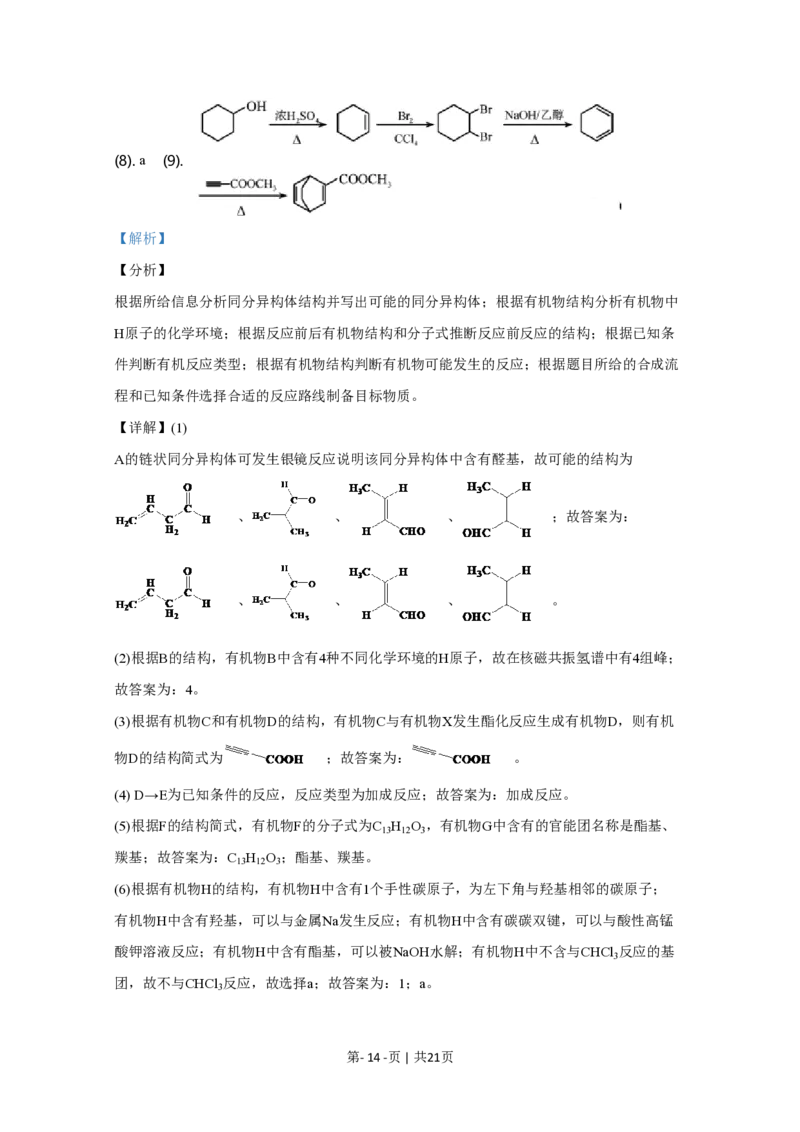
【答案】 (1). 、 、 、H C=CHCH CHO (2).
2 2
4 (3). (4). 加成反应 (5). C H O (6). 羰基、酯基 (7). 1
13 12 3
第- 13 -页 | 共21页(8). a (9).
【解析】
【分析】
根据所给信息分析同分异构体结构并写出可能的同分异构体;根据有机物结构分析有机物中
H原子的化学环境;根据反应前后有机物结构和分子式推断反应前反应的结构;根据已知条
件判断有机反应类型;根据有机物结构判断有机物可能发生的反应;根据题目所给的合成流
程和已知条件选择合适的反应路线制备目标物质。
【详解】(1)
A的链状同分异构体可发生银镜反应说明该同分异构体中含有醛基,故可能的结构为
、 、 、 ;故答案为:
、 、 、 。
(2)根据B的结构,有机物B中含有4种不同化学环境的H原子,故在核磁共振氢谱中有4组峰;
故答案为:4。
(3)根据有机物C和有机物D的结构,有机物C与有机物X发生酯化反应生成有机物D,则有机
物D的结构简式为 ;故答案为: 。
(4) D→E为已知条件的反应,反应类型为加成反应;故答案为:加成反应。
(5)根据F的结构简式,有机物F的分子式为C H O ,有机物G中含有的官能团名称是酯基、
13 12 3
羰基;故答案为:C H O ;酯基、羰基。
13 12 3
(6)根据有机物H的结构,有机物H中含有1个手性碳原子,为左下角与羟基相邻的碳原子;
有机物H中含有羟基,可以与金属Na发生反应;有机物H中含有碳碳双键,可以与酸性高锰
酸钾溶液反应;有机物H中含有酯基,可以被NaOH水解;有机物H中不含与CHCl 反应的基
3
团,故不与CHCl 反应,故选择a;故答案为:1;a。
3
第- 14 -页 | 共21页(7)利用 和 反应制得 ,可先将环己醇脱水得
环己烯,将环己烯( )与溴发生加成反应再发生消去反应制得1,3-
环己二烯( ),将1,3-环己二烯与 发生已知条件的反应制得
浓H SO
,反应的具体流程为: ¾¾¾2 ¾4®
D
¾¾Br 2¾® ¾N¾aOH¾/乙¾醇®
CCl 4 Δ
;故答案为: ¾ 浓 ¾ H ¾2 SO ¾4® ¾¾Br 2¾®
D CCl 4
¾N¾aOH¾/乙¾醇® 。
Δ
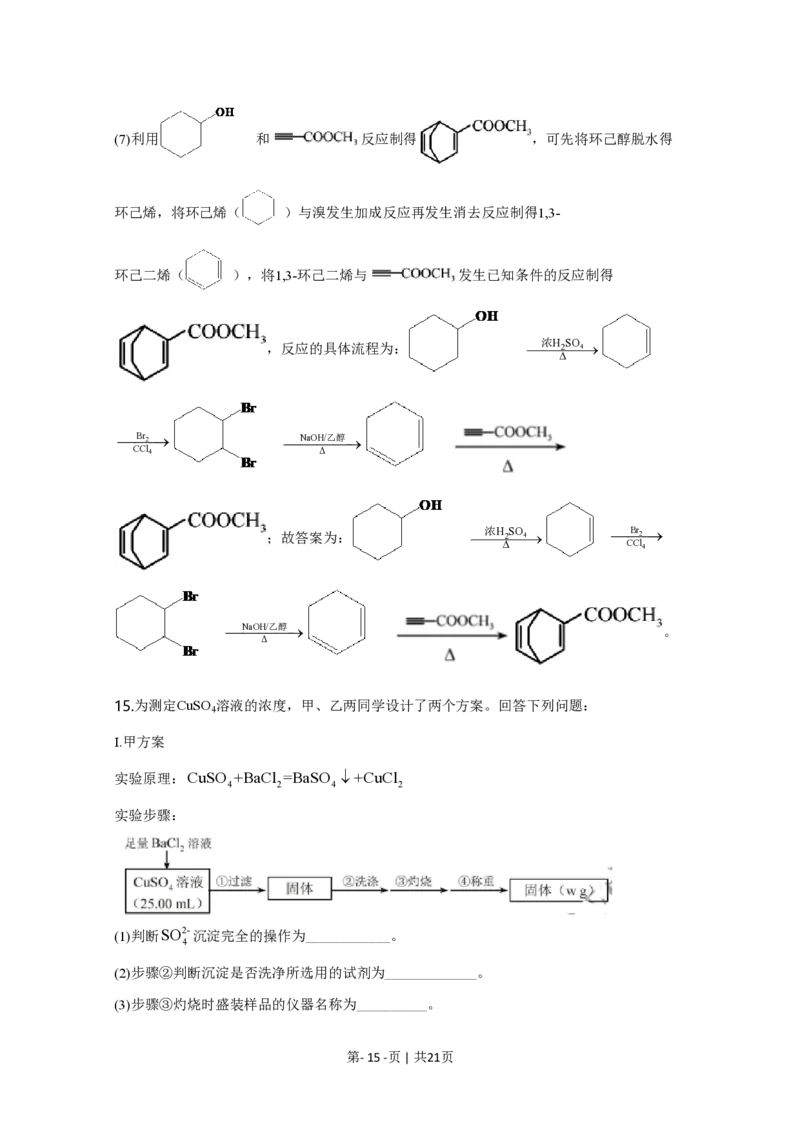
15.为测定CuSO 溶液的浓度,甲、乙两同学设计了两个方案。回答下列问题:
4
Ⅰ.甲方案
实验原理:CuSO +BaCl =BaSO ¯+CuCl
4 2 4 2
实验步骤:
(1)判断SO2-沉淀完全的操作为____________。
4
(2)步骤②判断沉淀是否洗净所选用的试剂为_____________。
(3)步骤③灼烧时盛装样品的仪器名称为__________。
第- 15 -页 | 共21页(4)固体质量为wg,则c(CuSO )=________mol‧L-1。
4
(5)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得c(CuSO )_________(填“偏高”、“偏低”
4
或“无影响”)。
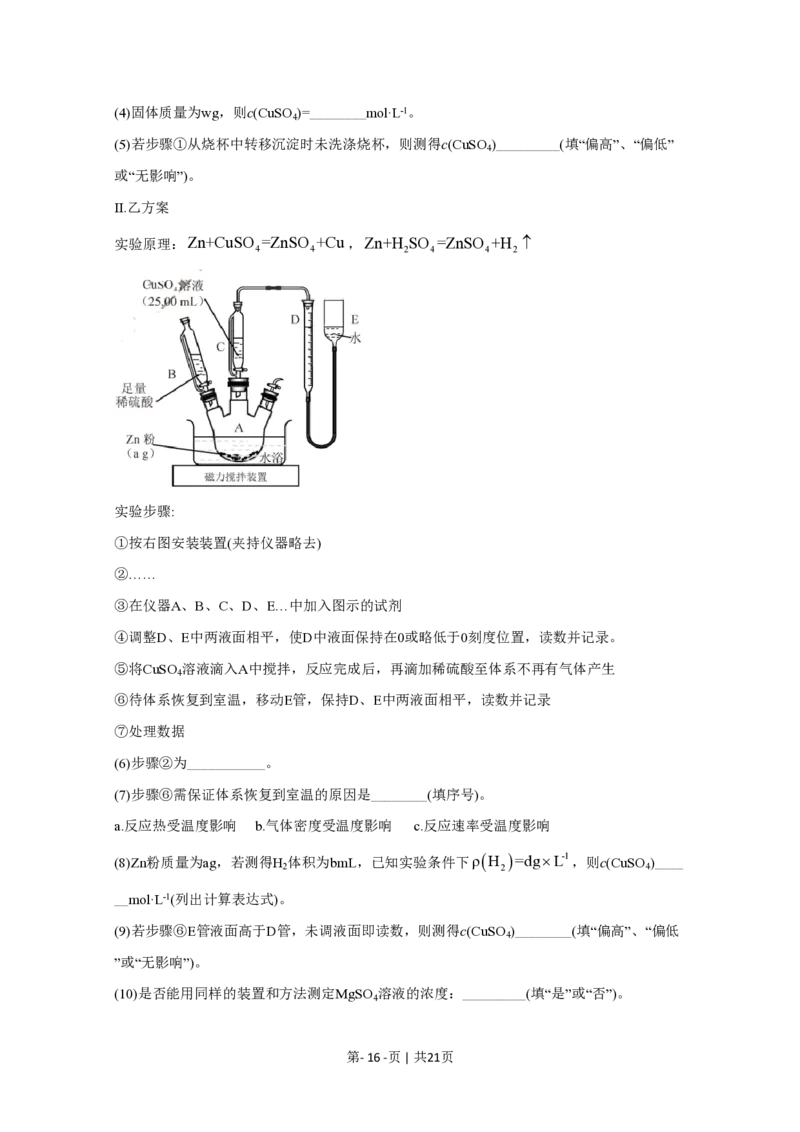
Ⅱ.乙方案
实验原理:Zn+CuSO =ZnSO +Cu,Zn+H SO =ZnSO +H
4 4 2 4 4 2
实验步骤:
①按右图安装装置(夹持仪器略去)
②……
③在仪器A、B、C、D、E…中加入图示的试剂
④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录。
⑤将CuSO 溶液滴入A中搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生
4
⑥待体系恢复到室温,移动E管,保持D、E中两液面相平,读数并记录
⑦处理数据
(6)步骤②为___________。
(7)步骤⑥需保证体系恢复到室温的原因是________(填序号)。
a.反应热受温度影响 b.气体密度受温度影响 c.反应速率受温度影响
(8)Zn粉质量为ag,若测得H
体积为bmL,已知实验条件下ρH =dg´L-1,则c(CuSO
)____
2 2 4
__mol‧L-1(列出计算表达式)。
(9)若步骤⑥E管液面高于D管,未调液面即读数,则测得c(CuSO )________(填“偏高”、“偏低
4
”或“无影响”)。
(10)是否能用同样的装置和方法测定MgSO 溶液的浓度:_________(填“是”或“否”)。
4
第- 16 -页 | 共21页【答案】 (1). 向上层清液中继续滴加BaCl 溶液,无白色沉淀生成,则沉淀完全 (2).
2
40w
AgNO 溶液 (3). 坩埚 (4). (5). 偏低 (6). 检查装置气密性 (7). b (8).
3
233
a bd´10-3
-
65 2 (9). 偏高 (10). 否
25´10-3
【解析】
【分析】
甲方案是利用溶液中的硫酸铜与氯化钡反应生成硫酸钡沉淀,经灼烧、洗涤、称重后得到的
固体是硫酸钡,利用硫酸根守恒,计算出硫酸铜的物质的量,从而计算出浓度;乙方案是利
用锌与稀硫酸反应释放出氢气的体积,换算成质量,计算出与稀硫酸反应的锌的物质的量,
再利用锌的总的物质的量减去与酸反应的锌的物质的量,得到与硫酸铜反应的锌的物质的量
n
,根据锌和硫酸铜的物质的量关系,计算出硫酸铜的物质的量,根据c= 得到硫酸铜的浓度
V
,据此分析。
【详解】Ⅰ.(1)硫酸根离子的检验是滴加氯化钡溶液,若产生白色沉淀,证明溶液中含有硫
酸根离子,故判断SO2-沉淀完全的操作向上层清液中继续滴加BaCl 溶液,无白色沉淀生成
4 2
,则沉淀完全;
(2)步骤②判断沉淀是否洗净所选用的试剂为AgNO 溶液,硫酸钡沉淀中可能附着有氯化钡,
3
为了证明还有没氯离子,需要加入硝酸银溶液,若产生白色沉淀,证明没有洗净;
(3)步骤③灼烧时盛装样品的仪器为坩埚;
wg
(4)固体质量为wg,为硫酸钡的质量,硫酸钡的物质的量为n= ,根据硫酸根守恒
233g/mol
wg
n 40w
可知,CuSO ~BaSO ,则c(CuSO )= = 233g/mol = mol‧L-1;
4 4 4
V 233
0.025L
(5)若步骤①从烧杯中转移沉淀时未洗涤烧杯,会使固体的质量偏小,物质的量偏小,根据
n
c= 可知,则测得c(CuSO )偏低;
4
V
Ⅱ.(6)加入药品之前需检查装置的气密性;步骤②为检查装置气密性;
(7)气体的体积受温度和压强的影响较大,气体的质量不随温度和压强的变化而改变,密度也
受温度和压强的影响,步骤⑥需保证体系恢复到室温的原因是气体密度受温度影响;反应热
第- 17 -页 | 共21页不受温度的影响,只与反应物和生成物自身的能量有关,不随温度压强而改变;反应速率受
温度影响,温度越高,反应速率越快,步骤⑥需保证体系恢复到室温与反应速率无关;
(8)Zn粉质量为ag,若测得H
体积为bmL,已知实验条件下ρH =dg´L-1,氢气的质量=
2 2
ρH V=db´10-3g,利用氢气的质量得到氢气的物质的量n=
2
d´b´10-3g d´b´10-3
= mol,根据Zn+H SO =ZnSO +H ,与酸反应的锌的物质的
2g/mol 2 2 4 4 2
d´b´10-3 ag
量为 mol,锌的总物质的量为 ,与硫酸铜反应的锌的物质的量为
2 65g/mol
ag d´b´10-3
- mol,根据Zn+CuSO =ZnSO +Cu,则c(CuSO )=
65g/mol 2 4 4 4
ag db´10-3
- mol
65g/mol 2 ;
25´10-3L
(9)若步骤⑥E管液面高于D管,未调液面即读数,得到氢气的体积偏小,与硫酸反应的锌的
质量偏小,与硫酸铜反应的锌的质量偏大,则测得c(CuSO )偏高;
4
(10) 不能用同样的装置和方法测定MgSO 溶液的浓度,硫酸镁不和锌发生置换反应。
4
【点睛】本题甲方案计算时,需要根据硫酸根守恒,是易错点。
16.利用太阳能光解水,制备的H 用于还原CO 合成有机物,可实现资源的再利用。回答下列
2 2
问题:
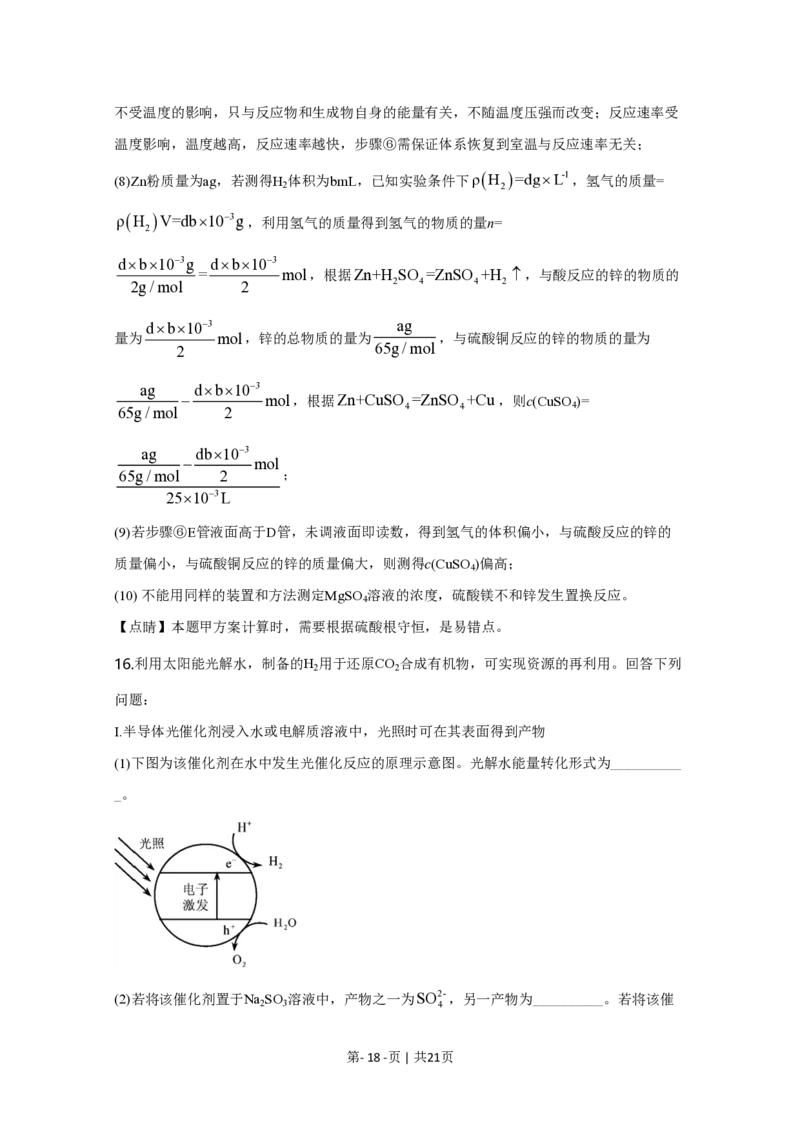
Ⅰ.半导体光催化剂浸入水或电解质溶液中,光照时可在其表面得到产物
(1)下图为该催化剂在水中发生光催化反应的原理示意图。光解水能量转化形式为__________
_。
(2)若将该催化剂置于Na SO 溶液中,产物之一为SO2-,另一产物为__________。若将该催
2 3 4
第- 18 -页 | 共21页化剂置于AgNO 溶液中,产物之一为O ,写出生成另一产物的离子反应式__________。
3 2
Ⅱ.用H 还原CO 可以在一定条下合成CH OH(不考虑副反应):
2 2 3
CO (g)+3H (g) CH OH(g)+H O(g) ΔH<0
2 2 ƒ 3 2
(3)某温度下,恒容密闭容器中,CO 和H 的起始浓度分别为 a mol‧L-1和3 a mol‧L-
2 2
1,反应平衡时,CH OH的产率为b,该温度下反应平衡常数的值为___________。
3
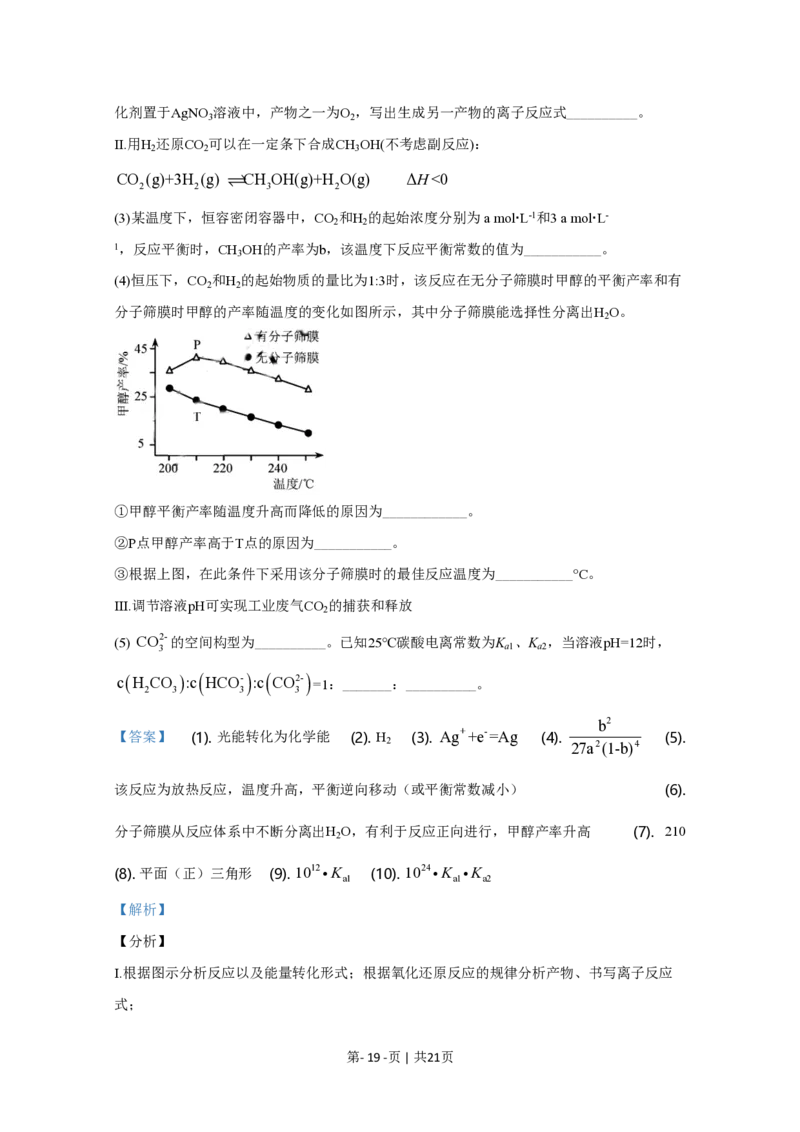
(4)恒压下,CO 和H 的起始物质的量比为1:3时,该反应在无分子筛膜时甲醇的平衡产率和有
2 2
分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出H O。
2
①甲醇平衡产率随温度升高而降低的原因为____________。
②P点甲醇产率高于T点的原因为___________。
③根据上图,在此条件下采用该分子筛膜时的最佳反应温度为___________°C。
Ⅲ.调节溶液pH可实现工业废气CO 的捕获和释放
2
(5) CO2-的空间构型为__________。已知25℃碳酸电离常数为K 、K ,当溶液pH=12时,
3 a1 a2
cH CO :c HCO- :c CO2- =1:_______:__________。
2 3 3 3
b2
【答案】 (1). 光能转化为化学能 (2). H (3). Ag++e-=Ag (4). (5).
2 27a2(1-b)4
该反应为放热反应,温度升高,平衡逆向移动(或平衡常数减小) (6).
分子筛膜从反应体系中不断分离出H O,有利于反应正向进行,甲醇产率升高 (7). 210
2
(8). 平面(正)三角形 (9). 1012 g K a1 (10). 1024 g K a1g K a2
【解析】
【分析】
I.根据图示分析反应以及能量转化形式;根据氧化还原反应的规律分析产物、书写离子反应
式;
第- 19 -页 | 共21页II.用三段式和平衡常数表达式计算平衡常数,依据外界条件对化学平衡的影响分析作答;
III.用价层电子对互斥理论判断CO2-的空间构型,利用电离平衡常数表达式计算粒子浓度的
3
比值。
光照
【详解】I.(1)根据图示,该催化剂在水中发生光催化反应的方程式为2H O 2H ↑+O ↑
2 2 2
催化剂
,光解水能量转化形式为光能转化为化学能,故答案为:光能转化为化学能。
(2)若将该催化剂置于Na SO 溶液中,产物之一为SO2-,SO2-被氧化成SO2-,则H+被还原为
2 3 4 3 4
H ,即另一产物为H ;若将该催化剂置于AgNO 溶液中,产物之一为O ,氧元素的化合价升
2 2 3 2
高,O 为氧化产物,则生成另一产物的反应为还原反应,由于Ag+得电子能力大于H+,故生
2
成另一产物的离子反应式为Ag++e-=Ag,故答案为:H ,Ag++e-=Ag。
2
II.(3) CO 和H 的起始浓度分别为 a mol‧L-1和3 a mol‧L-
2 2
1,CH OH的产率为b,则生成的CH OH物质的量浓度为abmol/L,根据三段式
3 3
CO(g) +3H(g) CH OH(g) +H O(g)
2 2 ƒ 3 2
c(起始)(mol/L) a 3a 0 0
c(转化)(mol/L) ab 3ab ab ab
c(平衡)(mol/L) a(1-b) 3a(1-b) ab ab
c(CH OH)×c(H O) ab´ab b2
则反应的平衡常数K= 3 2 = = ,故答案为:
c(CO )×c3(H ) a(1-b)[3a(1-b)]3 27a2(1-b)4
2 2
b2
。
27a2(1-b)4
(4)①该反应为放热反应(∆H<0),温度升高,平衡逆向移动(或平衡常数减小),故甲醇平衡
产率随温度升高而降低,故答案为:该反应为放热反应,温度升高,平衡逆向移动(或平衡
常数减小);
②因为分子筛膜能选择性分离出H O,c(H O)减小,有利于反应正向进行,甲醇产率升高
2 2
,故P点甲醇产率高于T点,故答案为:分子筛膜从反应体系中不断分离出H O,有利于反应
2
正向进行,甲醇产率升高。
③根据图示,使用该分子筛膜210℃时甲醇的产率最大,故在此条件下采用该分子筛膜时的
最佳反应温度为210℃,故答案为:210。
第- 20 -页 | 共21页1
III.(5)CO2-中C的孤电子对数为 ×(4+2-
3 2
3×2)=0,σ键电子对数为3,价层电子对数为3,C上没有孤电子对,故CO2-的空间构型为平
3
面正三角形;H CO 的电离方程式为H CO ⇌H++HCO- 、HCO- ⇌ H++CO2-,则K =
2 3 2 3 3 3 3 a1
c(H+)c(HCO-) c(H+)c(CO2-)
3 、K = 3 ,当溶液的pH=12时,c(H+)=1×10-
c(H CO ) a2 c(HCO-)
2 3 3
12mol/L,将其代入K 、K 中分别求出c(HCO- )=1012K c(H CO )、c(CO2-)=1012K
a1 a2 3 a1 2 3 3 a2
c(HCO- )=1024K K c(H CO ),则c(H CO ):c(HCO- ):c(CO2-)
3 a1 a2 2 3 2 3 3 3
=1:(1012K ):(1024K K ),故答案为:平面正三角形,1012K ,1024K K 。
a1 a1 a2 a1 a1 a2
【点睛】本题考查的知识点较多,但难度都不是很大,学生只要充分利用题给信息、结合所
学的基本原理和方法即可作答。
第- 21 -页 | 共21页