文档内容
2 0 2 4 年 上 教 师 资 格 笔 试 · 化 学 学 科 知 识 与 教 学 能 力
理 论 精 讲 - 化 学 基 本 概 念 3
讲师:沈蕾
更多干货关注 粉笔教师教育 粉笔教师物质的组成、分类及变化P18
(二)胶体
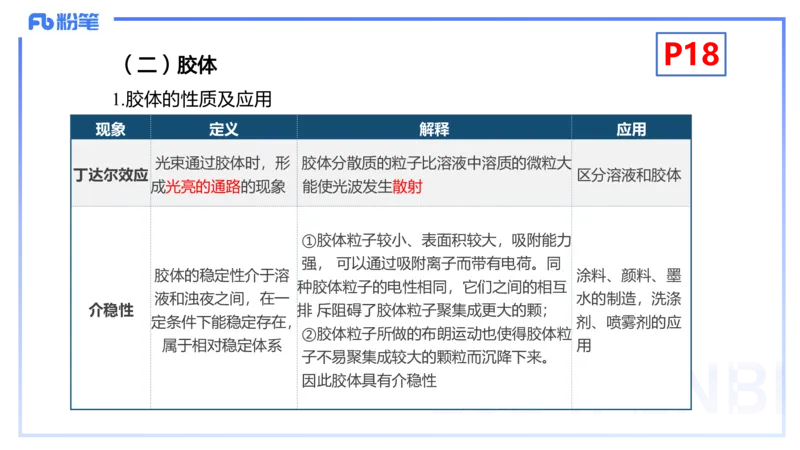
1.胶体的性质及应用
现象 定义 解释 应用
光束通过胶体时,形 胶体分散质的粒子比溶液中溶质的微粒大,
丁达尔效应 区分溶液和胶体
成光亮的通路的现象 能使光波发生散射
①胶体粒子较小、表面积较大,吸附能力
强, 可以通过吸附离子而带有电荷。同
胶体的稳定性介于溶 涂料、颜料、墨
种胶体粒子的电性相同,它们之间的相互
液和浊夜之间,在一 水的制造,洗涤
介稳性 排 斥阻碍了胶体粒子聚集成更大的颗;
定条件下能稳定存在, 剂、喷雾剂的应
②胶体粒子所做的布朗运动也使得胶体粒
属于相对稳定体系 用
子不易聚集成较大的颗粒而沉降下来。
因此胶体具有介稳性P19
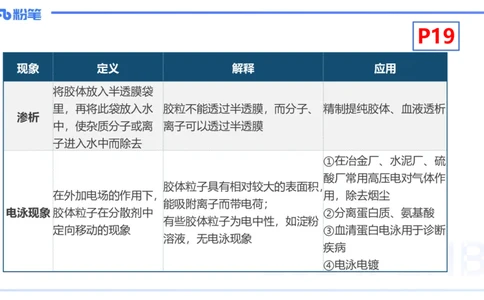
现象 定义 解释 应用
将胶体放入半透膜袋
里,再将此袋放入水 胶粒不能透过半透膜,而分子、 精制提纯胶体、血液透析
渗析
中,使杂质分子或离 离子可以透过半透膜
子进入水中而除去
①在冶金厂、水泥厂、硫
酸厂常用高压电对气体作
胶体粒子具有相对较大的表面积,
在外加电场的作用下, 用,除去烟尘
能吸附离子而带电荷;
电泳现象 胶体粒子在分散剂中 ②分离蛋白质、氨基酸
有些胶体粒子为电中性,如淀粉
定向移动的现象 ③血清蛋白电泳用于诊断
溶液,无电泳现象
疾病
④电泳电镀P19
【粉笔提示】
胶体的电泳现象:
1.电泳现象表明胶体粒子带电荷,而整个胶体分散系呈电中性。
2.胶体粒子带电,是胶体具有介稳性的重要原因。
3.由于带电的离子如MnO -在通电时也能发生定向移动,故不能
4
用电泳现象来区别溶液与胶体。
4. 利用电泳现象能够判断胶粒所带电荷种类。P19
2.胶体的聚沉
胶体粒子聚集成为较大的颗粒,从而形成沉淀从分散剂中析出,
这个过程叫作胶体的聚沉。
卤水点豆腐 三角洲的形成P19
聚沉方法:
(1)加入电解质溶液
在胶体中加入电解质,增加了胶体中离子的浓度,而给带电荷的
胶体粒子创造了吸引相反电荷的有利条件,从而减少或中和了原来胶
粒所带电荷。再加上粒子在不停地做布朗运动,就可以聚集起来,迅
速沉降。
一般说来,在加入电解质溶液时,高价离子比低价离子使胶体聚
沉的效率高。
如聚沉能力:Fe3+>Ca2+>Na+
PO 3->SO 2->Cl-
4 4P19
(2)加入带有相反电荷的胶体粒子
若两种胶体的胶粒带有相反的电荷,相遇时所带电荷就会互相中
和,从而聚集成大颗粒而沉降。
如把 Fe(OH) 胶体(胶粒带正电)加入硅酸胶体(胶粒带负电)
3
中,两种胶体均会发生聚沉。
胶体粒子带电规律:金属氧化物、氢氧化物常带正电;非金属氧
化物、金属硫化物、硅酸胶体粒子、土壤胶体粒子常带负电。P20
(3)加热
加热时,能量升高,胶粒布朗运动加剧,碰撞机会增多,导致胶
粒凝聚。如长时间加热时,Fe(OH) 胶体就发生凝聚而出现红褐色沉淀。
3P20
3.胶体的制备
(1)Fe(OH) (胶体)
3
将少量氯化铁的饱和溶液逐滴滴加到沸腾的蒸馏水中,继续加热
至液体呈红褐色,就制得了氢氧化铁胶体。
FeCl +3H O Fe(OH) (胶体)+3HCl
3 2 3
(2)Al(OH) (胶体)
3
将明矾等铝盐溶于水就制得了浓度较小的氢氧化铝胶体。
Al3++3H O Al(OH) (胶体)+3H+
2 3P21
四、物质的性质与变化
物理变化 化学变化
特征 没有新物质生成 有新物质生成
实质 构成物质的粒子没有发生变化 物质的组成、结构发生变化,分子中原子重新组合
关系 化学变化中一定伴随着物理变化的发生,但物理变化过程中不一定有化学变化
三馏 蒸馏、分馏 干馏
四色 焰色反应 显色反应、颜色反应、指示剂变色反应
七解 溶解、潮解 分解、电解、水解、裂解、降解
氢化、氧化、水化、风化、炭化、钝化、催化、皂
二十化 熔化、汽化、液化、酸化 化、歧化、卤化、硝化、酯化、裂化、(油脂)硬
化、硫化、老化P21
【粉笔提示】
1.化学变化中一定存在化学键的断裂和形成,但存在化学键断裂
的变化不一定是化学变化,如金属熔化破坏金属键、NaCl溶于水破坏
晶体中的离子键、液态NaCl降温析出晶体时形成离子键,以上变化均
属于物理变化。
2.原子的裂变、聚变中虽有新物质形成,但它不属于中学化学变化
研究的范畴。P21
3.易忽视的化学变化:
①同种元素形成的不同单质之间的转化(如O 转化为O );
3 2
②电解质溶液导电;
③NO 气体受热或遇冷时颜色变化等。
2
4.化学变化中常伴随着发光、放热和颜色变化,但有发光、放热或
颜色变化的变化不一定是化学变化,如在常温下将氧气冷却到-184 ℃
时,O 变为淡蓝色的液体等。
2P22
归纳与反思是学习化学的重要环节。下表是某同学对所学内容的归纳,
其中正确的是( )。离子反应P22
一、离子反应
(一)概念
有离子参加或有离子生成的反应统称为离子反应。
(二)离子反应的条件
1.生成难溶的物质,如 BaSO 、CaCO 、AgCl 等。
4 3
2.生成难电离的物质,如弱酸、弱碱、水等。
3.生成易挥发的物质,如 CO 、SO 等。
2 2
4.发生氧化还原反应。强氧化剂转变为弱还原剂,强还原剂转化为
弱氧化剂。如 FeCl 溶液中加入 Cu 的反应。
3P29
1. 向某溶液中加入过量盐酸生成白色沉淀,过滤后向滤液中加入过量
的氨水(使溶液呈碱性),又有白色沉淀生成;再过滤后向滤液中加入碳
酸钠溶液,又生成白色沉淀。则原溶液中含有的离子可能是( )。
A. Ag+、Cu2+、Ba2+ B. Ag+、Ba2+、Al3+
C. K+、Al3+、Ca2+ D. Al3+、K+、Mg2+P23
二、离子方程式
(一)概念
用实际参加反应的离子符号来表示反应的式子。
离子方程式可以表示同一类型的离子反应,而化学方程式只能表
示一个化学反应。P23
(二)离子方程式书写
1.书写步骤
①写:写出反应的化学方程式。
②拆:将易溶于水且易电离的物质改写成离子形式;将难溶物、
难电离的物质、气体、单质、氧化物等均写成化学式。
③删:从方程式两边删去相等个数的同种未参加反应的离子,并
使化学计量数最简化。
④查:检查方程式两边各元素得失电子是否守恒、电荷是否守恒、
原子个数是否守恒。P23
2.离子方程式正误判断:
(1)检查方程式是否符合客观反应事实,得失电子、电荷、原子
是否守恒。
(2)观察物质的存在形式和产物是否正确。
①微溶物处理方式有三种:
a.出现在生成物中写化学式;
b.作反应物处于溶液状态时写离子符号;
c.作反应物处于浊液或固态时写化学式。P23
②浓盐酸、浓 HNO 拆开写成离子形成,浓 H SO 写化学式。
3 2 4
③HCO -、HS-、HSO -等弱酸盐的酸式酸根离子不能拆开写,强
3 3
酸盐的酸式酸根离子拆写成离子形式。
④难电离的物质不拆开写。P23
(3)看“ ”、“ ”、“↑”、“↓”用的是否恰当;
盐类水解产生的沉淀,不写“↓”,气体不写“↑”,双水解都要
写成“↑”、“↓”。
(4)看是否符合题设条件及要求。如“过量”“少量”“等物质
的量”“适量”“任意量”以及“滴加顺序”等;
(5)看是否漏掉了某些离子反应。P24
【粉笔提示】
反应物量不同产物不同时,利用 “少定多变” 原则配平,谁少定谁
系数为1。
Ca(HCO ) 溶液中加入少量的NaOH溶液:
3 2
Ca2++OH-+HCO - CaCO ↓+H O
3 3 2
Ca(HCO ) 溶液中加入过量的NaOH溶液:
3 2
Ca2++2OH-+2HCO - CaCO ↓+2H O+CO 2-
3 3 2 3P29
3. 下列反应的离子方程式正确的是( )。
A. 石灰石和醋酸溶液反应:CaCO +2H+ Ca2++H O+ CO ↑
3 2 2
B. 铜与浓硝酸反应:Cu+4H++2NO- 3Cu2++2NO ↑+2H O
2 2
C. 向 NaHCO 溶液中滴加酚酞溶液,溶液变红:HCO - H++CO 2-
3 3 3
D. Ca(HCO ) 溶液中加入过量 NaOH 溶液:Ca2++HCO - +OH-
3 2 3
CaCO ↓+H O
3 2P24
三、离子共存
(一)离子共存
所谓几种离子在同一溶液中能大量共存,就是指离子之间不发生
任何反应;若离子之间能发生反应,则不能大量共存。P24
(二)判断溶液中离子能否大量共存的规律
多种离子能否大量共存于同一溶液中,归纳起来就是一句话:一
色、二性、四反应。
1.一色(溶液颜色)
若题中限定条件为无色溶液,则注意 MnO − 、Cu2+、Fe2+、Fe3+、
4
Cr2+、Cr3+、Cr O 2− 、CrO 2−等有色离子不能存在。
2 7 4P24
2.二性(溶液的酸性和碱性)
在强酸性溶液中,OH-及弱酸根阴离子(如CO 2-、SO 2-、S2-、
3 3
CH COO-、S O 2-等)均不能大量存在;
3 2 3
在强碱性溶液中,H+及弱碱阳离子(NH + 、Mg2+ 、Al3+ 、Cu2+ 、
4
Fe3+ 、Fe2+等)均不能大量存在;
酸式弱酸根离子(HCO -、HSO -、HS-等)在强酸性或强碱性
3 3
溶液中均不能大量存在。P25
3.四反应
指离子间通常能发生的四种类型的反应,能相互反应的离子显然
不能大量共存。
氧化还原反应
复分解反应
A B
双水解反应
络合反应
C DP25
(1)复分解反应
①有气体产生:OH-与NH + ;H+与CO 2-、HCO -、SO 2-、
4 3 3 3
HSO -、S -、HS-等。
3 2
②有沉淀产生:如Ba2+与SO 2-等。
4
③有弱电解质生成:
生成弱酸:H+与CO 2-、SO 2-、CH COO-、F-等。
3 3 3
生成弱碱:OH-与NH +、Al3+、Mg2+、Fe3+、Fe2+、Cu2+等。
4
生成水:OH-与H+P25
(2)氧化还原反应
某些氧化性离子与还原性离子能发生反应。
氧化性:MnO -、Cr O 2-、ClO-、NO -(H+)、Fe3+
4 2 7 3
还原性:S2-(HS-)、SO 2-(HSO -)、I-、Fe2+、Br-、Cl-
3 3P25
(3)双水解反应
当弱酸的酸根与弱碱的阳离子同时存在于水溶液中时,弱酸的酸
根水解生成的氢氧根离子与弱碱的阳离子水解生成的氢离子反应生成
水,而使两种离子的水解平衡向水解方向移动,互相促进水解,使水
解完全。
Al3++3H O Al(OH) +3H+
2 3
HCO - +H O H CO +OH-
3 2 2 3
Al3++3HCO - Al(OH) ↓+3CO ↑
3 3 2P25
熟记下列因双水解不能大量共存的离子组合:
(1)Al3+与 HCO -、CO 2-、AlO -、SiO 2-、HS-、S2-、ClO-
3 3 2 3
(2)Fe3+与 HCO -、CO 2-、AlO - 、SiO 2-、ClO-。
3 3 2 3
(3)NH +与 SiO 2-、AlO -
4 3 2P25
(4)络合反应
如Fe3+与CN-、SCN-、F-、C H O-等;
6 5
Ag+、Cu2+与NH ·H O等。
3 2P29
2. 在水溶液中能大量共存的一组离子是( )。
A. H+、Na+、SO 2−、HCO −
4 3
B. H+、Fe2+、Cl–、NO −
3
C. K+、Fe3+、NO −、MnO −
3 4
D. NH +、Ca2+、Cl–、CO 2−
4 3P29
4. 下列实验过程中,始终无明显现象的是( )。
A. CO 通入 CaCl 溶液中
2 2
B. NO 通入 FeSO 溶液中
2 4
C. NH 通入 AlCl 溶液中
3 3
D. SO 通入酸化的 Ba(NO ) 溶液中
2 3 2