文档内容
2018年深圳市初中毕业生学业考试
化 学
可能用到的相对原子质量:H-1 C-12 O-16 Ca-40 Cl-35.5
一.选择题(共10小题,每小题1.5分,共15分,在每小题给出的4个选项中,只有一项是符
合题目要求的。)
1.下列化学用语表达正确的是( )
A.三个钡离子:3Ba2+ B.两个氧原子:O
2
C.四个硫酸根离子:4SO 2- D.五个一氧化碳分子:5Co
3
答案:A
解析:Ba2+表示钡离子,3个钡离子为3 Ba2+,故A正确;两个氧原子为2O,O2表示氧气或氧
气分子,故B错误;4SO 2-表示4个亚硫酸根离子,四个硫酸根离子为4SO 2-,故C错误;CO
3 4
表示一氧化碳分子,而Co表示钴原子,故D错误。
2.6月5日是世界环境日,2018年我国的主题是“美丽中国,我是行动者”。下列做法错误
的是( )
A.减少使用不必要的塑料制品,如用布袋代替塑料袋
B.节约用水提高水的使用效益,如用洗过菜的水浇花
C.养成将垃圾分类处理的习惯,如废旧报纸回收利用
D.过度施用农药化肥提高产量,如喷洒过量农药杀虫
答案:D
解析:农药和化肥均要适度使用,如果过量施用农药会造成药物残留,对人体造成伤害,故D
错误。
3.归纳总结是学习化学的重要方法之一。下列排序正确的是( )
A.金属活动性顺序:
B.溶液的pH:
C.地壳中的元素含量:
D.气体的密度:答案:A
解析:在金属活动性顺序排列中,K>Mg>(H)>Cu>Ag,故A正确;pH值越大,碱性越强,pH
值越小,酸性越强,pH值由大到小的顺序应为NaOH>NaCl>HCl,故B错;地壳中元素的含量
顺序应为O、Si、Al、Fe,故C错;气体密度大小与其相对分子质量一致,故由大到小的顺序为
CO、O、H,故D错误。
2 2 2
4.下列说法正确的是( )
A.将pH试纸直接浸入待测液中测其pH
B.能与盐酸反应生成CO 气体的盐一定是NaHCO
2 3
C.铁制品锈蚀是铁在潮湿空气中缓慢氧化的过程
D.在测定空气里氧气含量的实验中,红磷燃烧产生大量白雾
答案:C
解析:A会污染待测液,故错;B可以是其他碳酸氢盐,如KHCO 、Ca(HCO ) 等,也可以是碳
3 3 2
酸盐,如NaCO、CaCO 等,故B错;铁锈蚀是铁与氧气、水发生化学反应的结果,由于有氧
2 3 3
气参加,是氧化反应,故C正确;红磷在空气中燃烧会产生大量白烟,烟是固体小颗粒,而雾
是液体小颗粒,故D错。
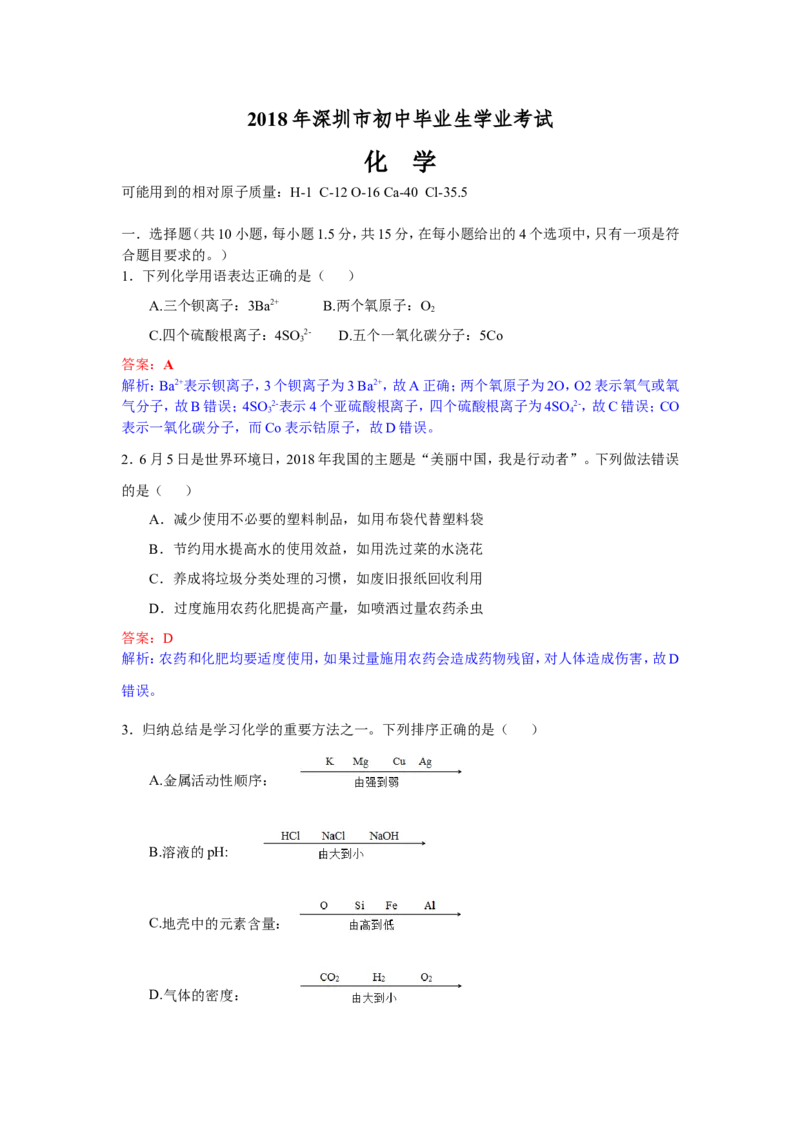
5.下列实验均与水有关,其相应描述正确的是( )
A.属于化学变化 B.净化后可得纯水 C.证明水的组成 D.吸收大量热
答案:C
解析:A中水由液体变成气体的水蒸汽,再由水蒸汽变成液体的水,这是物理变化,故A错;
过滤只除去不溶性杂质,活性炭的吸附只除去有颜色和气味的可溶性物质,但水的其他可溶
性杂质没有除去,故B错;通过电解水得到氧气和氢气,可以证明水的组成,故C正确;D是
稀释浓硫酸,水是作为溶剂使用的,故D错。
6.锌是促进人体生长发育的必须微量元素。下图为锌元素在元素周期表中的相关信息及原
子结构示意图。下列说法正确的是( )A.锌属于非金属元素 B.锌原子的中子数为30
C.锌的相对原子质量为65.38g D. 锌原子在化学反应中易失去电子形成Zn2+
答案:D
解析:锌是金字旁,最外层电子数少于4,为金属元素,故A错;锌原子的中子数=相对原子质
量-质子数=65-30=35,故B错;相对原子质量的单位为1,故C错;金属元素在化学反应中容
易失去电子,形成阳离子,阳离子所带的电荷数为所失的电子数,故D正确。
7.维生素可以起到调节新陈代谢、预防疾病、维持身体健康的重要作用。缺乏维生素 A
1
(C H O),会引起夜盲症。下列关于维生素A 的说法中正确的是( )
20 30 1
A.维生素A 属于无机化合物
1
B.维生素A 中O元素的质量分数最低
1
C.维生素A 中碳、氢元素的质量比为2:3
1
D.维生素A1由20个碳原子、30个氢原子、1个氧原子构成
答案:B
解析:含C化合物称为有机物,故A错;维生素A中O元素的质量为16,H元素的质量为
30,C元素的质量为240,所以,维生素A中O元素的质量健康最小,故B正确;维生素A中,
碳、氢元素的质量比为240:30 = 8:1,故C错;D是错误的,其正确表述应为:1个维生素A
分子是由20个碳原子、30个氢原子、1个氧原子构成。
8.最近,我国科学家成功合成新型催化剂,将CO 高效转化为甲醇(CHOH)。这不仅可以缓
2 3
解碳排放引起的温室效应,还将成为理想的能源补充形式。该化学反应的微观过程如下图所
示。下列说法正确的是( )
A.该反应中四种物质均为化合物 B.反应前后H元素的化合价不变
C.参加反应的甲、乙分子个数比为1:3 D.反应前后原子数目发生改变
答案:C解析:四种物质中乙为单质,故A错;反应前H元素集中在H 中,其化合价为零,反应后,其
2
化合价为+1价,故B错;该反应的化学方程式为CO + 3H CHOH + HO,参加反
2 2 3 2
应的甲、乙分子个数比为1:3,故C正确;根据质量守恒定律,反应前后原子的种类、数目和质
量不变,故D错。
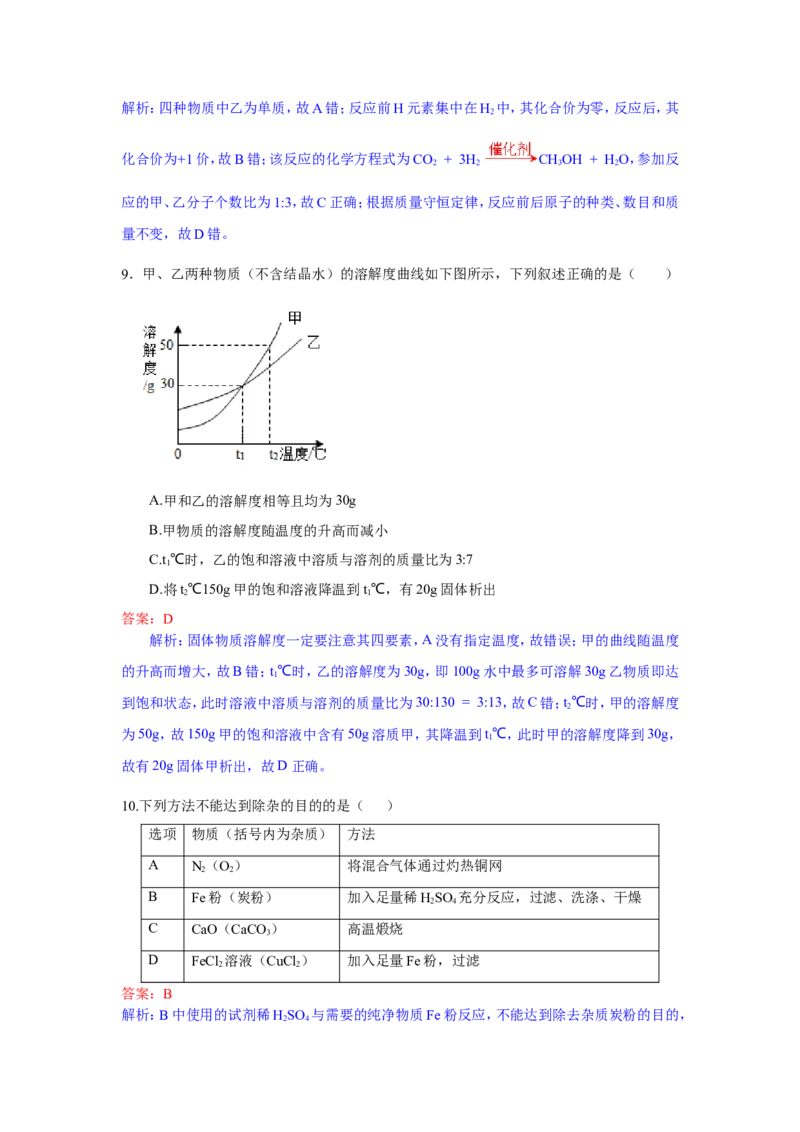
9.甲、乙两种物质(不含结晶水)的溶解度曲线如下图所示,下列叙述正确的是( )
A.甲和乙的溶解度相等且均为30g
B.甲物质的溶解度随温度的升高而减小
C.t℃时,乙的饱和溶液中溶质与溶剂的质量比为3:7
1
D.将t℃150g甲的饱和溶液降温到t℃,有20g固体析出
2 1
答案:D
解析:固体物质溶解度一定要注意其四要素,A没有指定温度,故错误;甲的曲线随温度
的升高而增大,故B错;t℃时,乙的溶解度为30g,即100g水中最多可溶解30g乙物质即达
1
到饱和状态,此时溶液中溶质与溶剂的质量比为30:130 = 3:13,故C错;t℃时,甲的溶解度
2
为50g,故150g甲的饱和溶液中含有50g溶质甲,其降温到t℃,此时甲的溶解度降到30g,
1
故有20g固体甲析出,故D正确。
10.下列方法不能达到除杂的目的的是( )
选项 物质(括号内为杂质) 方法
A N(O) 将混合气体通过灼热铜网
2 2
B Fe粉(炭粉) 加入足量稀HSO 充分反应,过滤、洗涤、干燥
2 4
C CaO(CaCO ) 高温煅烧
3
D FeCl 溶液(CuCl ) 加入足量Fe粉,过滤
2 2
答案:B
解析:B中使用的试剂稀HSO 与需要的纯净物质Fe粉反应,不能达到除去杂质炭粉的目的,
2 4故B错。
二.非选择题(共3题,第11题8分,第12题8分,第13题9分,共25分)
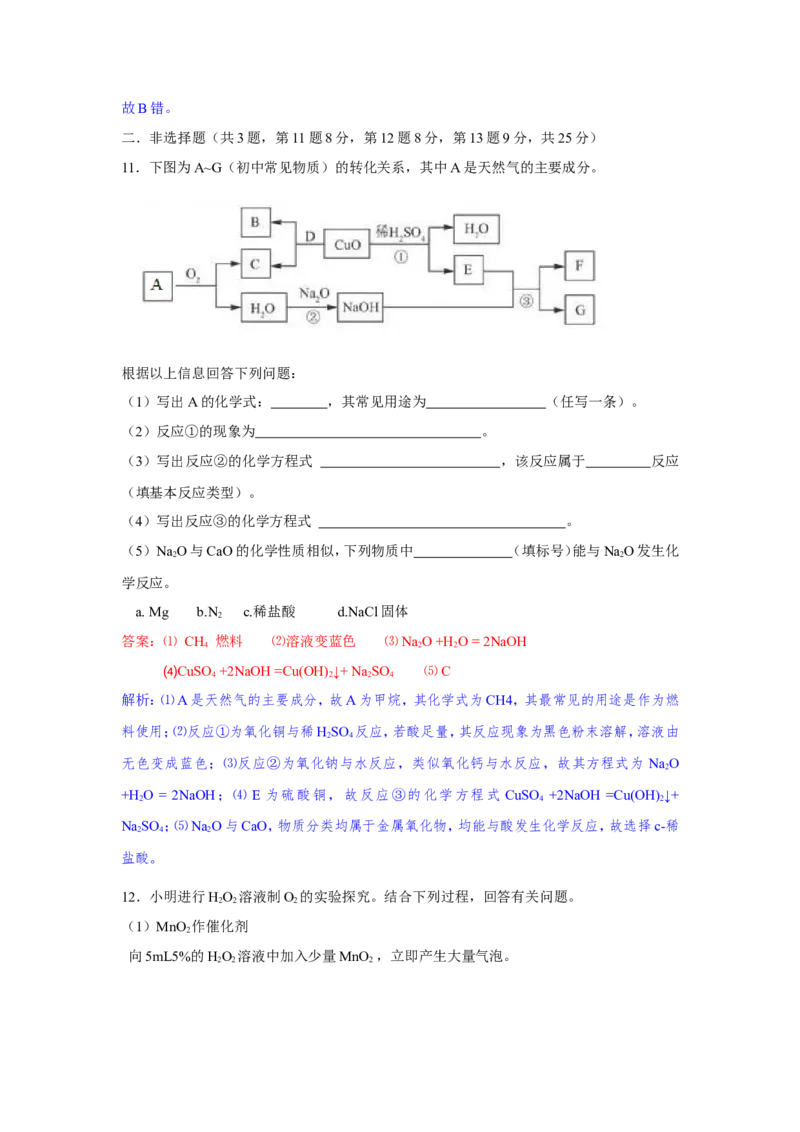
11.下图为A~G(初中常见物质)的转化关系,其中A是天然气的主要成分。
根据以上信息回答下列问题:
(1)写出A 的化学式: ,其常见用途为 (任写一条)。
(2)反应①的现象为 。
(3)写出反应②的化学方程式 ,该反应属于 反应
(填基本反应类型)。
(4)写出反应③的化学方程式 。
(5)NaO与CaO的化学性质相似,下列物质中 (填标号)能与NaO发生化
2 2
学反应。
a. Mg b.N c.稀盐酸 d.NaCl固体
2
答案:⑴ CH 燃料 ⑵溶液变蓝色 ⑶NaO +H O = 2NaOH
4 2 2
⑷CuSO +2NaOH =Cu(OH) ↓+ Na SO ⑸C
4 2 2 4
解析:⑴A是天然气的主要成分,故A为甲烷,其化学式为CH4,其最常见的用途是作为燃
料使用;⑵反应①为氧化铜与稀HSO 反应,若酸足量,其反应现象为黑色粉末溶解,溶液由
2 4
无色变成蓝色;⑶反应②为氧化钠与水反应,类似氧化钙与水反应,故其方程式为 NaO
2
+H O = 2NaOH;⑷ E 为硫酸铜,故反应③的化学方程式 CuSO +2NaOH =Cu(OH) ↓+
2 4 2
NaSO ;⑸NaO与CaO,物质分类均属于金属氧化物,均能与酸发生化学反应,故选择c-稀
2 4 2
盐酸。
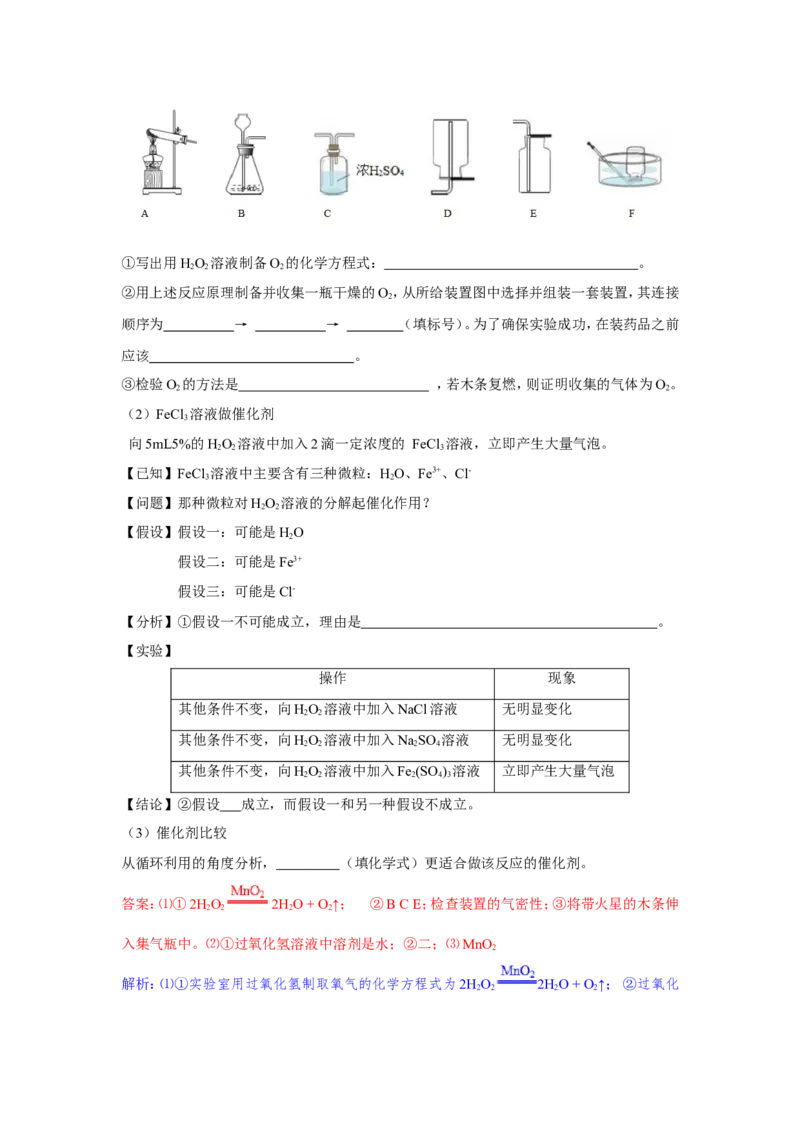
12.小明进行HO 溶液制O 的实验探究。结合下列过程,回答有关问题。
2 2 2
(1)MnO 作催化剂
2
向5mL5%的HO 溶液中加入少量MnO ,立即产生大量气泡。
2 2 2①写出用HO 溶液制备O 的化学方程式: 。
2 2 2
②用上述反应原理制备并收集一瓶干燥的O,从所给装置图中选择并组装一套装置,其连接
2
顺序为 → → (填标号)。为了确保实验成功,在装药品之前
应该 。
③检验O 的方法是 ,若木条复燃,则证明收集的气体为O。
2 2
(2)FeCl 溶液做催化剂
3
向5mL5%的HO 溶液中加入2滴一定浓度的 FeCl 溶液,立即产生大量气泡。
2 2 3
【已知】FeCl 溶液中主要含有三种微粒:HO、Fe3+、Cl-
3 2
【问题】那种微粒对HO 溶液的分解起催化作用?
2 2
【假设】假设一:可能是HO
2
假设二:可能是Fe3+
假设三:可能是Cl-
【分析】①假设一不可能成立,理由是 。
【实验】
操作 现象
其他条件不变,向HO 溶液中加入NaCl溶液 无明显变化
2 2
其他条件不变,向HO 溶液中加入NaSO 溶液 无明显变化
2 2 2 4
其他条件不变,向HO 溶液中加入Fe (SO ) 溶液 立即产生大量气泡
2 2 2 4 3
【结论】②假设 成立,而假设一和另一种假设不成立。
(3)催化剂比较
从循环利用的角度分析, (填化学式)更适合做该反应的催化剂。
答案:⑴①2HO 2H O + O↑; ②B C E;检查装置的气密性;③将带火星的木条伸
2 2 2 2
入集气瓶中。⑵①过氧化氢溶液中溶剂是水;②二;⑶MnO
2
解析:⑴①实验室用过氧化氢制取氧气的化学方程式为2HO 2HO + O↑; ②过氧化
2 2 2 2氢制取氧气为固体与液体在常温下反应,故发生装置选择B,由于要制取干燥的氧气,这需
要浓硫酸进行干燥,故需要连接装置C,收集干燥的氧气,故只能使用排空气法进行收集,氧
气的密度比空气的密度大,故选用向上排空气法进行收集,故选用E;所有涉及气体生成并
收集的化学实验,均需要检查装置的气密性;③检验氧气的方法是将带火星的木条伸入集气
瓶中,木条复燃,则表示集满。⑵①若假设一成立,由于过氧化氢溶液中溶剂是水,故过氧化
氢溶液就自动快速分解了;②实验顺序1中排除了Cl-;2中排除了SO 2-;3中则证明了Fe3+能
4
加速HO 的分解速率,故假设二成立;⑶相对于FeCl 而言,MnO 是固体,不溶于水,能回收,
2 2 3 2
故MnO 更好。
2
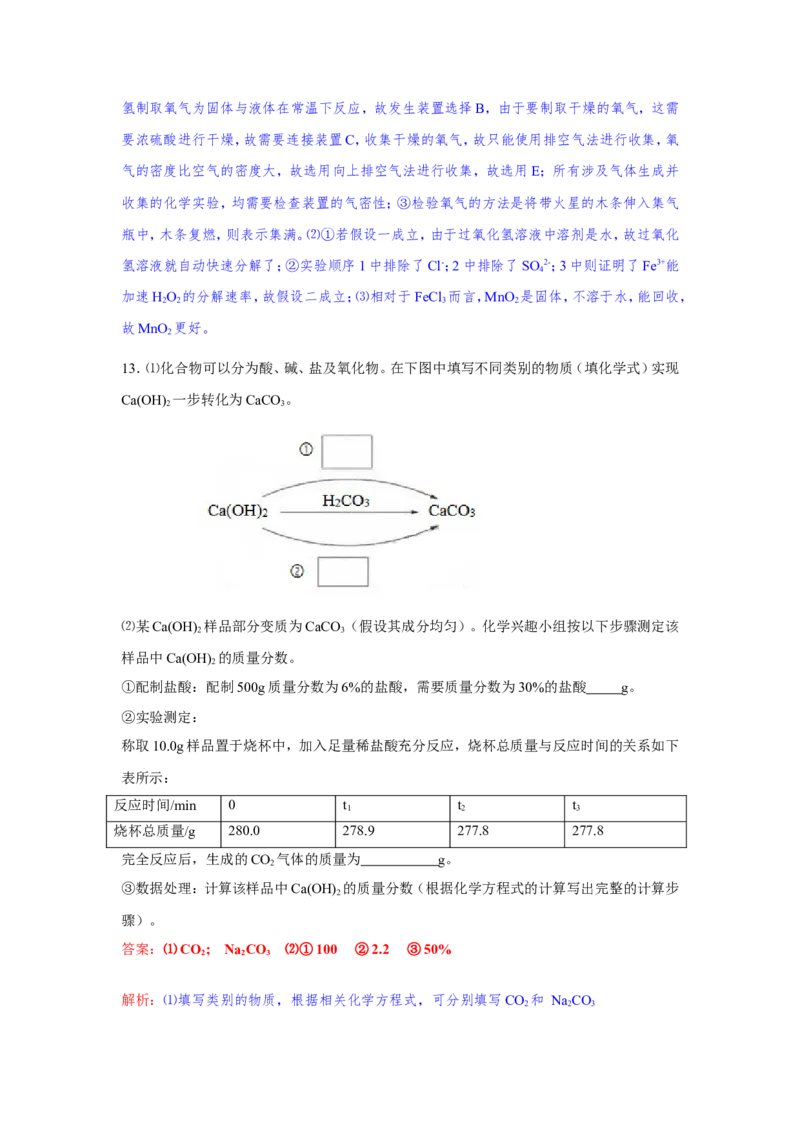
13.⑴化合物可以分为酸、碱、盐及氧化物。在下图中填写不同类别的物质(填化学式)实现
Ca(OH) 一步转化为CaCO 。
2 3
⑵某Ca(OH) 样品部分变质为CaCO (假设其成分均匀)。化学兴趣小组按以下步骤测定该
2 3
样品中Ca(OH) 的质量分数。
2
①配制盐酸:配制500g质量分数为6%的盐酸,需要质量分数为30%的盐酸 g。
②实验测定:
称取10.0g样品置于烧杯中,加入足量稀盐酸充分反应,烧杯总质量与反应时间的关系如下
表所示:
反应时间/min 0 t t t
1 2 3
烧杯总质量/g 280.0 278.9 277.8 277.8
完全反应后,生成的CO 气体的质量为 g。
2
③数据处理:计算该样品中Ca(OH) 的质量分数(根据化学方程式的计算写出完整的计算步
2
骤)。
答案:⑴CO ; Na CO ⑵①100 ②2.2 ③50%
2 2 3
解析:⑴填写类别的物质,根据相关化学方程式,可分别填写CO 和 NaCO
2 2 3⑵①配制500g质量分数为6%的盐酸,需要质量分数为30%的盐酸为X,则稀释前后溶质的
质量不变,故有 500g×6%=X×30% X=100g
②系统中有气体生成,根据质量守恒定律,生成气体的质量等于反应前后系统质量的减少值,
故生成CO 的质量为280.0g-277.8g=2.2g
2
③解:设样品中CaCO 的质量为X
3