文档内容
2 0 2 5 年 上 教 师 资 格 · 化 学 学 科 笔 试
主讲老师 王双奕
粉笔教师教育 粉笔教师目
录
content
1 化学反应与能量
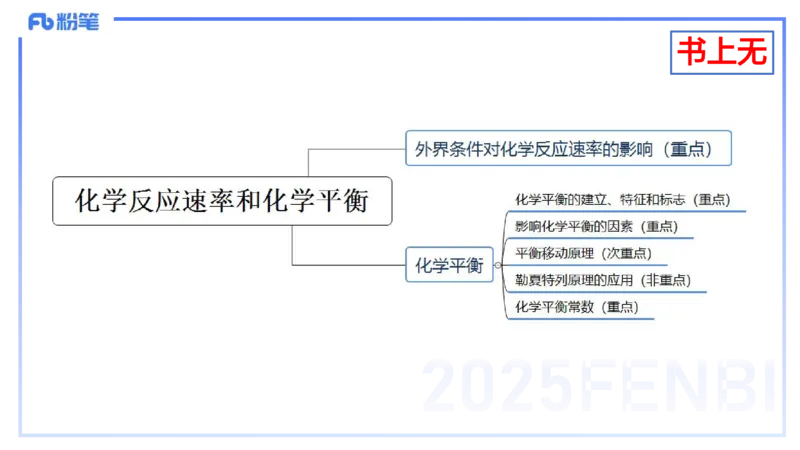
2 化学反应速率和化学平衡
3 水溶液中的离子平衡
4 电化学基础化学反应速率和化学平衡P129
二、影响化学反应速率的因素
(一)有效碰撞理论
1.碰撞理论
1918年,路易斯(lewis)根据气体分子运动论,提出了碰撞理论。
碰撞理论的要点:
(1)反应物分子间只有发生碰撞才有可能发生反应,或者说碰撞是反应发生的
先决条件。
(2)只有少部分碰撞能引发化学反应,大多数反应物微粒之间的碰撞是无效碰撞。
(3)单位时间内有效碰撞的次数越多,反应速率越快。
(4)活化能越大,活化分子越少,反应速率就越慢。P129
2.有效碰撞及其条件
有效碰撞:能导致化学反应发生的碰撞。
要发生有效碰撞必须具备以下两个条件:
(1)反应物分子必须具有足够大的能量。
(2)反应物分子碰撞的几何方位要适当。P130
3.活化分子与活化能
活化分子:能够发生有效碰撞的分子。
活化能:活化分子比普通分子多出的那部分能量(或普通分子转化成活化
分子所需的最低能量)。P130
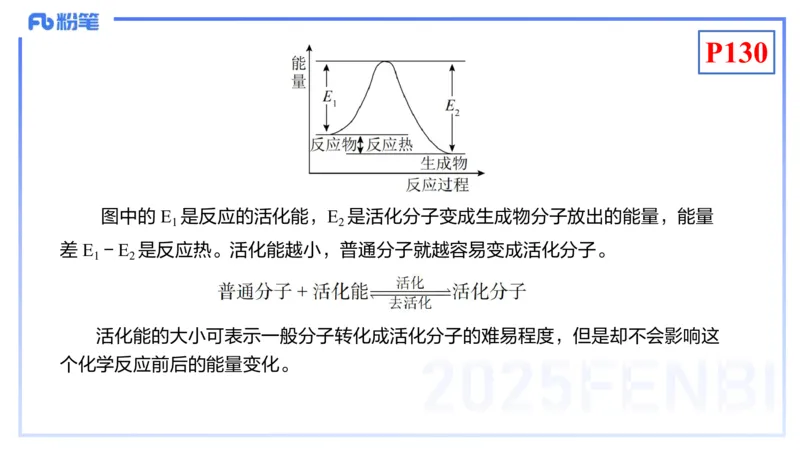
图中的 E 是反应的活化能,E 是活化分子变成生成物分子放出的能量,能量
1 2
差 E -E 是反应热。活化能越小,普通分子就越容易变成活化分子。
1 2
活化能的大小可表示一般分子转化成活化分子的难易程度,但是却不会影响这
个化学反应前后的能量变化。P130
活化能低→普通分子易变成活化分子→活化分子百分数大→有效碰撞
次数多→反应速率快。
【粉笔提示】
有关活化能需要了解:
1.温度对某反应的速率的影响程度,大致反映了该反应的活化能的大小。
2.自然条件下活化能较高的反应:岩石的风化、溶洞的形成、矿物的形
成等。P130
3.有些反应,速率极大,当反应物相互接触时,瞬间发生反应,而且温度
对其反应速率几乎没有什么影响,其活化能接近于零。
例如:
(1)离子反应:H+和OH-、Ag+和Cl-在水溶液中混合时,反应几乎都
是在瞬间内完成的;
(2)距地面约50~85km的大气层,平均温度只有-50℃,但是存在于其
中的大量自由原子之间的反应,却几乎不需要“克服”活化能。
这两类反应活化能几乎为零的原因,是在反应之前反应物已经成为自由
的离子或原子,不再需要破坏或减弱化学键。P131
(二)外界条件对化学反应速率的影响
1.决定反应速率的主要因素(内因)
反应物本身的性质。
2.影响反应速率的因素(外因)
(1)反应物的浓度:增加反应物的浓度,反应速率增大。P131
【粉笔提示】
改变固体或纯液体的量对化学反应速率无影响,但改变固体的表面
积,会影响化学反应速率。
当固体或纯液体参加反应时,反应速率与接触面积、扩散速率的大
小有关,所以增大接触面积(将固体研碎)或加快扩散速率(搅拌)均
可提高反应速率。P131
(2)温度
温度对化学反应速率的影响是绝对的,升高温度,可以加快反应速率。
对于可逆反应来说:
①升高温度,正、逆反应速率都增大,但吸热反应速率增大的程度大。
②降低温度,正、逆反应速率都减小,但吸热反应速率减小的程度大。P131
(3)压强
对于有气体参加的反应,讨论压强对反应速率的影响时,应区分引起压强改变
的原因,这种改变对反应体系的浓度产生何种影响,由此判断出对反应速率有何影
响。具体如下:
①恒温时:增大压强 → 体积缩小 → 浓度增大 → 反应速率加快。
②恒温恒容时:
a.充入气体反应物 → 浓度增大 →反应速率加快;
b.充入“惰性气体” → 总压强增大,但各气体分压不变,即参与反应的各物质
的浓度不变,反应速率不变。
③恒温恒压时:充入“惰性气体” → 体积增大 → 参与反应的各物质的浓度减
小 → 反应速率减慢。P131
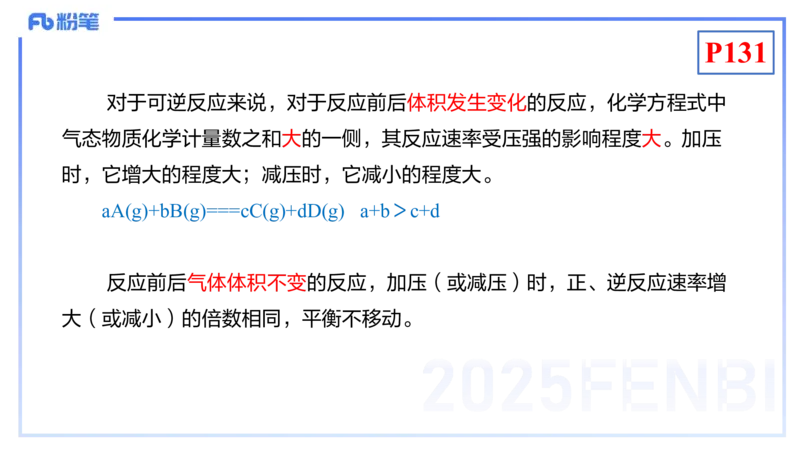
对于可逆反应来说,对于反应前后体积发生变化的反应,化学方程式中
气态物质化学计量数之和大的一侧,其反应速率受压强的影响程度大。加压
时,它增大的程度大;减压时,它减小的程度大。
aA(g)+bB(g)===cC(g)+dD(g) a+b>c+d
反应前后气体体积不变的反应,加压(或减压)时,正、逆反应速率增
大(或减小)的倍数相同,平衡不移动。P132
(4)催化剂
催化剂能够降低反应的活化能,增加活化分子的百分数,同等程度地提
高正、逆反应的速率。
(5)其它条件:如光、反应物颗粒大小、溶剂、反应物的状态等都可
以影响化学反应速率。P132
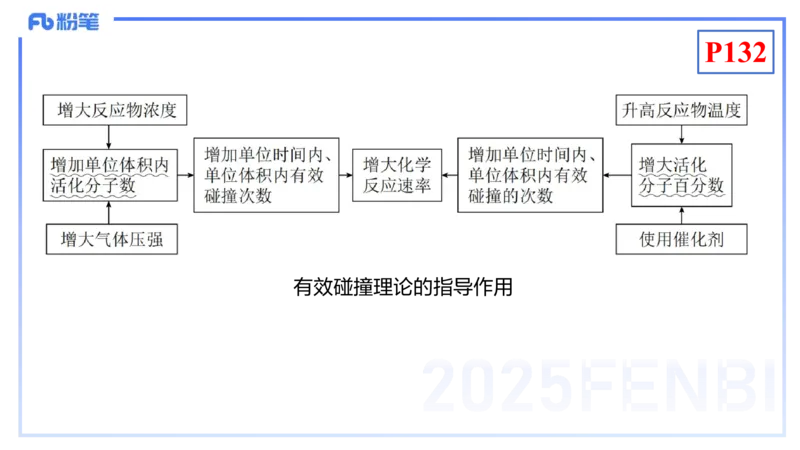
有效碰撞理论的指导作用P132
三、化学平衡
(一)化学平衡的建立、特征和标志
1.可逆反应
在相同条件下,既能向正反应方向又能向逆反应方向进行的反应叫作
可逆反应。
可逆反应必须是同一条件下既能向正反应方向又能向逆反应方向进行
的反应,对于在不同条件下进行的反应物、生成物正好相反的反应,不能
认为是可逆反应。
可逆反应是不能进行到底的,不能实现完全转化。P132
2.化学平衡的建立
当 ν(正)= ν(逆)时,单位时间内同一物质消耗的量与生成的量完全
相等,因而各物质的浓度和百分含量保持一定,即达到化学平衡状态——在
一定条件下的可逆反应里,正反应和逆反应速率相等,反应混合物中各组分
的浓度保持不变的状态。
aA(g)+bB(g) cC(g)+dD(g)P132
3.化学平衡的特征
(1)逆:只有可逆反应才能达到化学平衡状态。
(2)等:ν(正)= ν(逆)(同一物质)
(3)动:ν(正)= ν(逆)≠ 0,是动态平衡,正、逆反应仍在不断进行。
(4)定:达到平衡后,各组分的浓度及百分含量保持一定。P132
(5)变:当影响化学平衡的外界条件发生变化,使 ν(正)≠ ν(逆)时,
平衡便会发生移动而使各组分的浓度、百分含量发生变化,直至建立新的平
衡。
(6)同:如果外界条件不变时,不论采取何种途径,即反应是由反应物
开始或由生成物开始,是一次投料或是分步投料,最后所达到的化学平衡状
态是相同的,即化学平衡状态只与反应条件有关而与反应途径无关。P133
4.化学平衡的标志——判断可逆反应达到平衡状态的方法和依据
反应 mA(g)+nB(g) pC(g)+qD(g)
①各物质的物质的量或物质的量分数一定 平衡
混合物
②各物质的质量或质量分数一定 平衡
体系中
各成分
③各气体的体积或体积分数一定 平衡
的含量
④总体积、总压强、总物质的量一定 不一定平衡P133
反应 mA(g)+nB(g) pC(g)+qD(g)
①在单位时间内消耗了 m mol A,同时生成了 m mol A,
平衡
即 ν(正)= ν(逆)
②在单位时间内消耗了 n mol B,同时消耗了 p mol C,则
平衡
ν(正)= ν(逆)
正、逆反应
③ν(A):ν(B):ν(C):ν(D) = m:n:p:q,ν(正)不一定等于ν(逆)不一定平衡
速率的关系
④在单位时间内生成了 n mol B,同时消耗了 q mol D,
不一定平衡
均指 ν(逆)
⑤在单位时间内同一物质断裂的化学键与生成的化学键的
平衡
物质的量相等P133
反应 mA(g)+nB(g) pC(g)+qD(g)
①m+n ≠ p+q时,混合气体的平均相对分子质量一定 平衡
混合气体的平均
相对分子质量
②m+n = p+q时,混合气体的平均相对分子质量一定 不一定平衡P133
反应 mA(g)+nB(g) pC(g)+qD(g)
任何化学反应都伴随着能量变化,当体系温度一定时
温度 平衡
(其他条件不变)
体系的密度 密度一定 不一定平衡
颜色 含有有色物质的体系颜色不再变化 平衡书上无
可逆反应 2HI(g) H (g)+I (g) 在固定体积的密闭容器中进行,达到
2 2
平衡状态的标志是( )。
A.单位时间内生成 nmol H 的同时,生成 nmol I
2 2
B.混合气体的颜色不再改变的状态
C.混合气体的密度不再改变的状态
D.混合气体的平均相对分子质量不再改变的状态P133
【粉笔提示】
“三段式”法解化学平衡计算
在化学平衡的计算中,常常要计算反应物的转化率、各组分的转化浓
度、转化的物质的量、平衡浓度、平衡时物质的量等。若在反应的化学方
程式下用“三段式”法列出各物质的起始、转化、平衡的量,理顺关系,
找出已知量与未知量的关系,对正确分析和解决问题有很大帮助。下面以
求解转化率为例说明“三段式”法的具体应用。P134
例:在 2L 的密闭容器中加入 2molSO 、1.2molO ,一定条件下使其充
2 2
分反应后,测得 SO 为 1.8mol,则 SO 的转化率为多少?
3 2P134
(二)影响化学平衡的因素
可逆反应中旧的化学平衡被破坏、新的化学平衡建立的过程就是化学
平衡的移动。平衡移动的根本原因是 ν(正)≠ ν(逆)。移动的结果是
ν(正)、ν(逆)又相等。P134
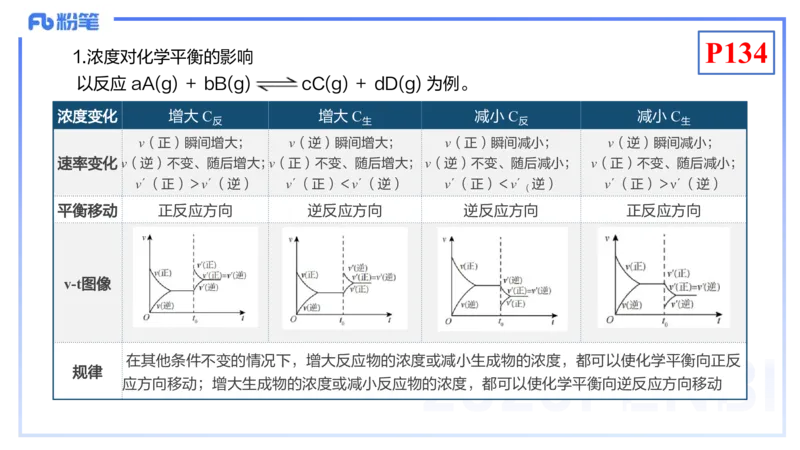
1.浓度对化学平衡的影响
以反应 aA(g) + bB(g) cC(g) + dD(g) 为例。
浓度变化 增大 C 增大 C 减小 C 减小 C
反 生 反 生
ν(正)瞬间增大; ν(逆)瞬间增大; ν(正)瞬间减小; ν(逆)瞬间减小;
速率变化 ν(逆)不变、随后增大;ν(正)不变、随后增大; ν(逆)不变、随后减小; ν(正)不变、随后减小;
ν´(正)>ν´(逆) ν´(正)<ν´(逆) ν´(正)<ν´ 逆) ν´(正)>ν´(逆)
(
平衡移动 正反应方向 逆反应方向 逆反应方向 正反应方向
v-t图像
在其他条件不变的情况下,增大反应物的浓度或减小生成物的浓度,都可以使化学平衡向正反
规律
应方向移动;增大生成物的浓度或减小反应物的浓度,都可以使化学平衡向逆反应方向移动P135
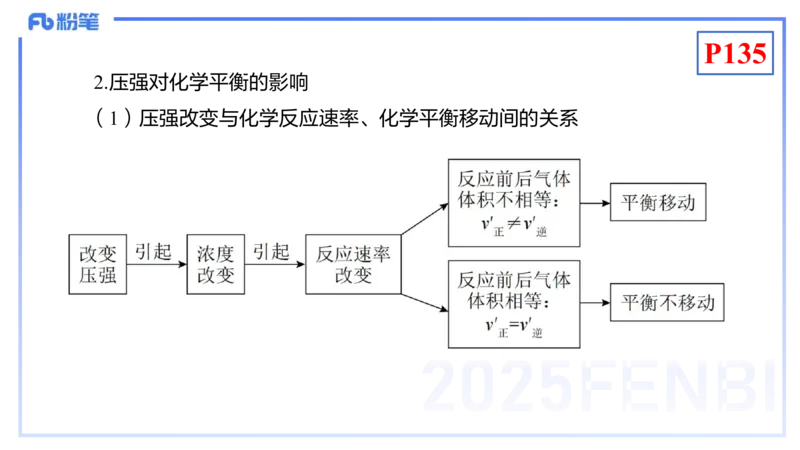
2.压强对化学平衡的影响
(1)压强改变与化学反应速率、化学平衡移动间的关系P135
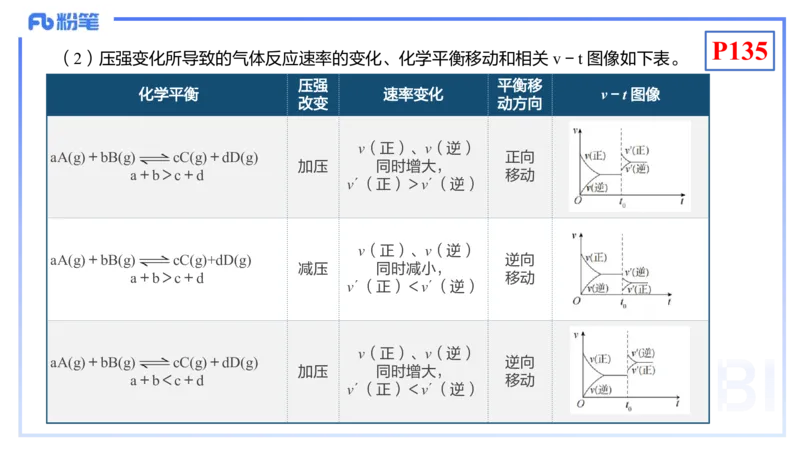
(2)压强变化所导致的气体反应速率的变化、化学平衡移动和相关 v-t 图像如下表。
压强 平衡移
化学平衡 速率变化 v-t 图像
改变 动方向
ν(正)、ν(逆)
aA(g)+bB(g) cC(g)+dD(g) 正向
加压 同时增大,
a+b>c+d 移动
ν´(正)>ν´(逆)
ν(正)、ν(逆)
aA(g)+bB(g) cC(g)+dD(g) 逆向
减压 同时减小,
a+b>c+d 移动
ν´(正)<ν´(逆)
ν(正)、ν(逆)
aA(g)+bB(g) cC(g)+dD(g) 逆向
加压 同时增大,
a+b<c+d 移动
ν´(正)<ν´(逆)P135
压强 平衡移
化学平衡 速率变化 v-t 图像
改变 动方向
ν(正)、ν(逆)
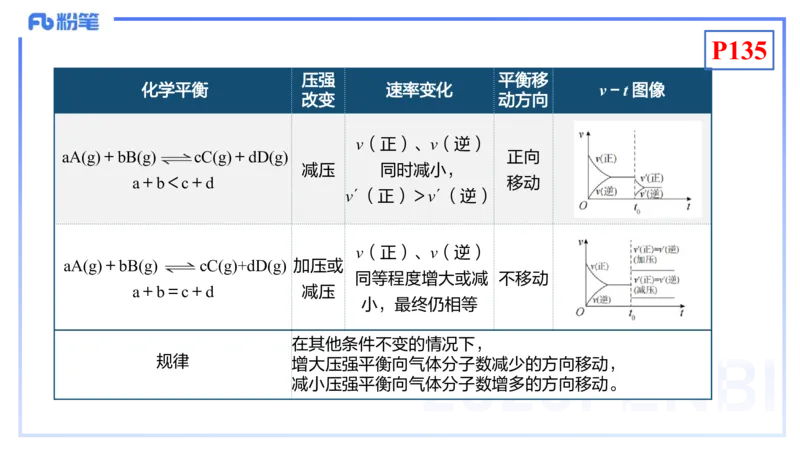
aA(g)+bB(g) cC(g)+dD(g) 正向
减压 同时减小,
a+b<c+d 移动
ν
´(正)>ν ´(逆)
ν(正)、ν(逆)
aA(g)+bB(g) cC(g)+dD(g) 加压或
同等程度增大或减 不移动
a+b=c+d 减压
小,最终仍相等
在其他条件不变的情况下,
规律
增大压强平衡向气体分子数减少的方向移动,
减小压强平衡向气体分子数增多的方向移动。3.温度变化对化学平衡的影响
P136
化学 aA(g)+bB(g) aA(g)+bB(g) aA(g)+bB(g) aA(g)+bB(g)
平衡 cC(g)+dD(g) △H>0 cC(g)+dD(g) △H<0 cC(g)+dD(g) △H<0 cC(g)+dD(g) △H>0
体系温
升温 升温 降温 降温
度改变
ν(正)、ν(逆) ν(正)、ν(逆) ν(正)、ν(逆) ν(正)、ν(逆)
速率
同时增大, 同时增大, 同时减小, 同时减小,
变化
ν´(正)>ν´(逆) ν´(正)<ν´(逆) ν´(正)>ν´(逆) ν´(正)<ν´(逆)
平衡移
正反应方向 逆反应方向 正反应方向 逆反应方向
动方向
v-t 图像
规律 在其他条件不变的情况下,升高温度平衡向吸热方向移动,降低温度平衡向放热方向移动P136
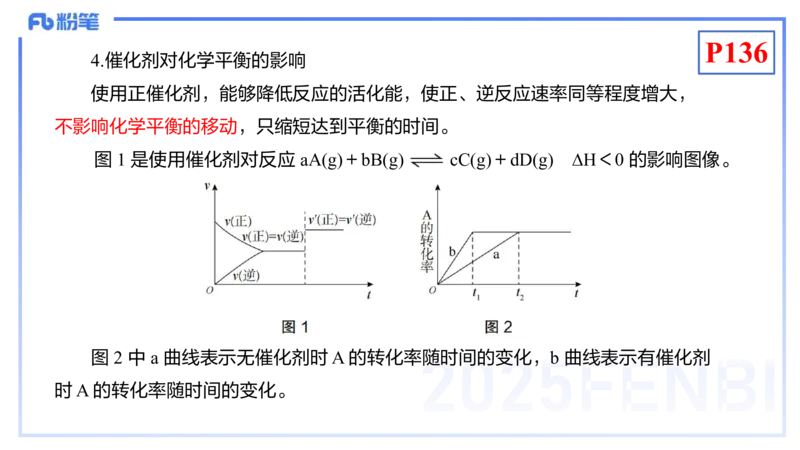
4.催化剂对化学平衡的影响
使用正催化剂,能够降低反应的活化能,使正、逆反应速率同等程度增大,
不影响化学平衡的移动,只缩短达到平衡的时间。
图 1 是使用催化剂对反应 aA(g)+bB(g) cC(g)+dD(g) ∆H<0 的影响图像。
图 2 中 a 曲线表示无催化剂时 A 的转化率随时间的变化,b 曲线表示有催化剂
时 A 的转化率随时间的变化。P137
(三)平衡移动原理
1.平衡移动原理——勒夏特列原理
如果改变影响平衡的一个条件(如浓度、压强或温度),平衡将向着能
够减弱这种改变的方向移动。
2.勒夏特列原理应用的注意事项
(1)勒夏特列原理适用的范围:已达到平衡的体系,例如化学平衡、电
离平衡、水解平衡、沉淀溶解平衡等。P137
(2)勒夏特列原理适用的条件:只限于改变影响平衡的一个条件。当有
两个或两个以上的条件同时改变时,如果这些条件对平衡移动方向的影响是
一致的,则可判断平衡移动的方向。但如果这些条件对平衡移动方向的影响
不一致,则需分析哪一个条件变化是影响平衡移动的主要因素。
(3)平衡向“减弱”外界条件改变的方向移动,但不能“抵消”这种改
变。
(4)存在平衡且平衡发生移动时才能应用平衡移动原理,如果不存在平
衡(如铁的电化学腐蚀)或虽存在平衡但不发生移动,均不能应用平衡移动
原理。P137
(四)勒夏特列原理的应用 ——合成氨的适宜条件
1.合成氨的适宜条件及选择依据
(1)合成氨反应的特点:N +3H 2NH 是一个放热的、气体体
2 2 3
积减小的可逆反应。
(2)合成氨反应的理想状态:①反应速率较快;②平衡混合物中 NH 的
3
含量较高。P137
2.合成氨条件的选择
(1)原理:N (g)+3H (g) 2NH (g) ∆H=-92.2kJ/mol。
2 2 3
(2)根据合成氨反应的特点,应采取以下措施提高反应的平衡转化率和
反应速率。
提高化学反应的平衡转化率 提高化学反应的速率
性质 措施 性质 措施
放热(∆H<0) 降低温度 活化能高 升高温度
分子数减少 增大压强 低温时反应速率慢 使用催化剂
减小生成物浓度能使 原料气浓度增加能加快
及时分离氨 增加 N 的浓度
2
平衡向右移动 反应速率P138
(3)运用化学反应速率和化学平衡原理,同时考虑合成氨生产中的动
力、材料、设备等因素,合成氨工业中实际采用的适宜条件是:
使用铁触媒作催化剂,温度为400 ~ 500℃左右,压强可根据反应器钢
材质量及综合指标来选择 10 ~ 30Mpa,及时分离出氨,不断补充 N 和 H 。
2 2P138
(五)化学平衡常数
1.定义
在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与
反应物浓度幂之积的比值是一个常数,这个常数就是该反应的化学平衡常数
(简称平衡常数),用符号 K 表示。
对于一般的可逆反应:
aA(g)+bB(g) cC(g)+dD(g)
在一定温度下达到平衡时,可以得出:P138
【粉笔提示】
1.化学平衡常数只与温度有关,与反应物或生成物的浓度无关。
2.反应物或生成物中有固体或纯液体存在时,其浓度可看作“1”而不代
入公式。
3.化学平衡常数是指某一具体反应的平衡常数。若反应方向改变,则平衡
常数改变。若方程式中各物质的化学计量数等倍扩大或缩小,尽管是同一反
应,平衡常数也会改变。P138
2.化学平衡常数的应用
(1)K 值越大,说明平衡体系中生成物所占的比例越大,它的正向反应
进行的程度越大,即该反应进行得越完全,反应物转化率越大;反之,反应
进行得就越不完全,反应物转化率就越小。
(2)若用任意状态的浓度幂之积的比值(称为浓度商,用 Q 表示)与K
c
比较,可判断可逆反应是否达到平衡状态和反应进行的方向。P138
对于一般的可逆反应 aA(g) + bB(g) cC(g) + dD(g) :
Q < K,反应向正反应方向进行;
c
Q = K,反应达到平衡状态;
c
Q > K,反应向逆反应方向进行。
cP141P139
(3)利用 K 可判断反应的热效应。
若升高温度,K 值增大,则反应正向进行,正反应为吸热反应;
若升高温度,K 值减小,则反应逆向进行,正反应为放热反应。
(4)计算转化率
依据起始浓度(或平衡浓度)和平衡常数可以计算平衡浓度(或起始浓
度),从而计算反应物的转化率。(结合三段式法)P142P141书上无