文档内容
2012年普通高等学校招生全国统一考试(安徽卷)
理综化学
【试卷总评】1、试题紧扣2012年安徽高考《考试说明》,化学试题秉承往年的命题传统,
稳中求变、稳中求新,第13题、25题等体现《考试说明》上内容与要求的变化,如质量数、
核磁共振氢谱等;体现样题的变化,如13题与样题例6(新增加的内容)相近,试题结构、
试题难度与往年非常相近。第I卷试题考查氧化还原反应、化学平衡、离子共存、化学实验
基本操作、反应热、电化学等基本概念、基本理论、化学实验等。第II卷注重基本原理、基
本理论的掌握与运用能力的考查,分别针对元素周期表和周期律、元素化合物、有机框图推
断、化学实验、工艺流程进行重点考查。
2、注重对基础特别是对主干知识和核心知识的考查,考点均为教材中的重点内容,注
重实验细节,强调对实验原理的理解,方案的设计,实验分量加重(10题、27题、28题)
考点分布合理,覆盖面较广。
3、试题考查了学生多方面的能力如迁移能力(26题)、计算能力(27题、28题)、正
向逆向思维能力、观察能力、推理能力、实验能力、发散思维能力,利用所学知识分析问题
和解决实际问题的能力等,体现了化学学科特点,符合对化学学习能力的要求。
[来源:学&科&网Z&X&X&K]
3、试题结合了社会热点、生活生产实际,科技新成果,有时代气息如7、26、27、28题
等,试卷整体以中档试题为主,试卷总体难度约0.69左右。
7.科学家最近研究出一种环保、安全的储氢方法,其原理可表示为:
储氢
NaHCO +H HCOONa+H O下列有关说法正确的是
3 2 2
释氢
A.储氢、释氢过程均无能量变化
B.NaHCO 、HCOONa均含有离子键和共价键
3
C.储氢过程中,NaHCO 被氧化
3
D.释氢过程中,每消耗0.1molH O放出2.24L的H
2 2
8.下列离子或分子在溶液中能大量共存,通入CO 后仍能大量共存的一组是
2
第1页 | 共11页A.K+、Na+、Cl—、NO — B.K+、Na+、Br—、SiO 2—
3 3
C.H+、Fe2+、SO 2—、Cl D.K+、Ag+、NH ·H O、NO —
4 2 3 2 3
9.一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
催化剂
SO (g)+2CO(g) 2CO (g)+S(l) △H<0 若反应在恒容的密闭容器中进行,下列有关
2 2
说法正确的是
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,升高温度可提高SO 的转化率
2
D.其他条件不变,使用不同催化剂,该反应平衡常数不变
10.仅用下表提供的玻璃容器(非玻璃容器任选)就能实现相应实验目的的是
选项 实验目的 玻璃容器
A 分离乙醇和乙酸乙酯的混合物 分液漏斗、烧杯
用pH=1的盐酸配置100mL,pH=2的
B 100mL容量瓶、烧杯、玻璃棒、胶头滴管
盐酸
[来源:学|科|网Z|X|X|K]
用溴水、淀粉—KI溶液比较Br 与I 的
C 2 2 试管、胶头滴管
氧化性强弱
用NH Cl固体和Ca(OH) 固体制备并
D 4 2 酒精灯、烧杯、导管、集气瓶
收集NH
3
10、【答案】C
【解析】分液漏斗和烧杯组合常用于分液操作,而乙酸乙酯和乙醇互溶,因此二者的分离不
可采用分液的方法,而应采取蒸馏的方法(需用到蒸馏烧瓶、冷凝管、尾接管等玻璃仪器),
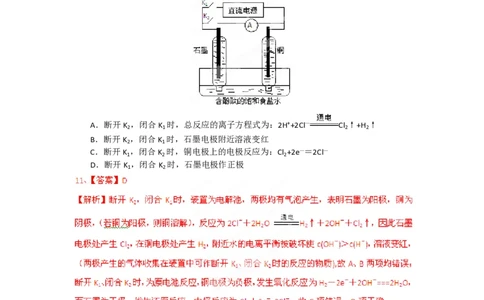
第2页 | 共11页11.某兴趣小组设计如下微型实验装置。实验时,现断开K ,闭合K ,两极均有气泡产生;
2 1
一段时间后,断开K ,闭合K ,发现电流表指针偏转,下列有关描述正确的是
1 2
A.断开K ,闭合K 时,总反应的离子方程式为:2H++2Cl— Cl ↑+H ↑
2 1 2 2
B.断开K ,闭合K 时,石墨电极附近溶液变红
2 1
C.断开K ,闭合K 时,铜电极上的电极反应为:Cl +2e—=2Cl—
1 2 2
D.断开K ,闭合K 时,石墨电极作正极
1 2 [来源:学科网ZXXK]
12.氢氟酸是一种弱酸,可用来刻蚀玻璃。已知25℃时
①HF(aq)+OH—(aq)=F—(aq)+H O(l) △H=—67.7KJ·mol—1
2
②H+(aq)+OH—(aq)=H O(l) △H=—57.3KJ·mol—1
2
在20mL0.1·molL—1氢氟酸中加入VmL0.1mol·L—1NaOH溶液,下列有关说法正确的是
A.氢氟酸的电离方程式及热效应可表示为:
HF(aq)=H+(aq) +F−(aq) △H=+10.4KJ·mol—1
第3页 | 共11页B.当V=20时,溶液中:c(OH—)=c(HF) +c(H+)
C.当V=20时,溶液中:c(F—)<c(Na+)=0.1mol·L—1
D.当V>0时,溶液中一定存在:c(Na+)>c(F—)>c(OH—)>c(H+)
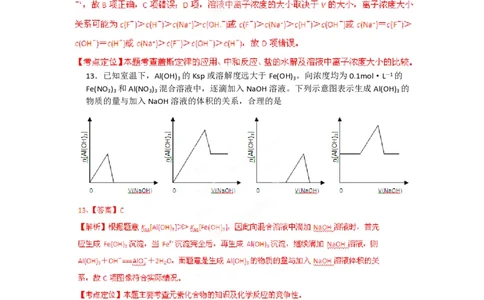
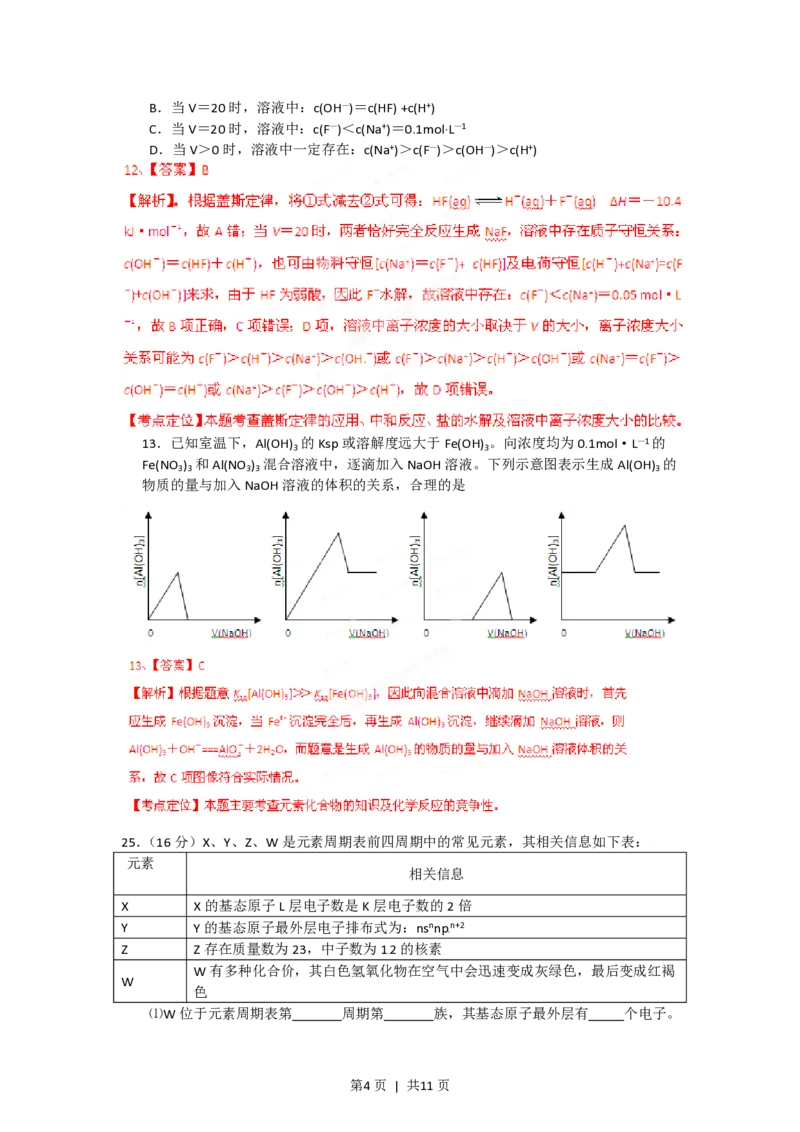
13.已知室温下,Al(OH) 的Ksp或溶解度远大于Fe(OH) 。向浓度均为0.1mol·L—1的
3 3
Fe(NO ) 和Al(NO ) 混合溶液中,逐滴加入NaOH溶液。下列示意图表示生成Al(OH) 的
3 3 3 3 3
物质的量与加入NaOH溶液的体积的关系,合理的是
25.(16分)X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如下表:
[来源:Zxxk.Com]
元素
[来源:学&科&网 相关信息
Z&X&X&K]
X X的基态原子L层电子数是K层电子数的2倍
Y Y的基态原子最外层电子排布式为:nsnnpn+2
Z Z存在质量数为23,中子数为12的核素
W有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐
W
色
⑴W位于元素周期表第 周期第 族,其基态原子最外层有 个电子。
第4页 | 共11页⑵X的电负性比Y的 (填“大”或“小”);X和Y的气态氢化物中,较稳定的
是 (写化学式)
⑶写出Z Y 与XY 反应的化学方程式,并标出电子转移的方向和数目: 。
2 2 2
⑷在X原子与氢原子形成的多种分子中,有些分子的核磁共振氢谱显示有两种氢,写出
其中一种分子的名称: 。氢元素、X、Y的原子也可共同形成多种分
子和某种常见无机阴离子,写出其中一种分子与该无机阴离子反应的离子方程式:
。
26.(14分)PBS是一种可降解的聚酯类高分子材料,可由马来酸酐等原料经下列路线合成:
第5页 | 共11页H O H
2 HOOCCH=CHCOOH 2 B
△ A 催化剂
一定条件
(马来酸酐) PBS
HC≡CH
H—C—H
C H 2 HOCH CH CH CH OH
一定条件 催化剂 2 2 2 2
D
OH
O
(已知: RC≡CH + 一定条件 R C C C R )
1
R -C-R
1 2
R
2
(1)A→B的反应类型是 ;B的结构简式是 。
(2)C中含有的官能团名称是 ;D的名称(系统命名)是 。
(3)半方酸是马来酸酐的同分异构体,分子中含1个环(四元碳环)和1个羟基,但不含
—O—O—键。半方酸的结构简式是 。
(4)由D和B合成PBS的化学方程式是 。
(5)下列关于A的说法正确的是 。
a.能使酸性KMnO 溶液或溴的CCl 溶液褪色
4 4
b.能与Na CO 反应,但不与HBr反应
2 3
c.能与新制Cu(OH) 反应
2
1molA完全燃烧消耗5molO
d. 2
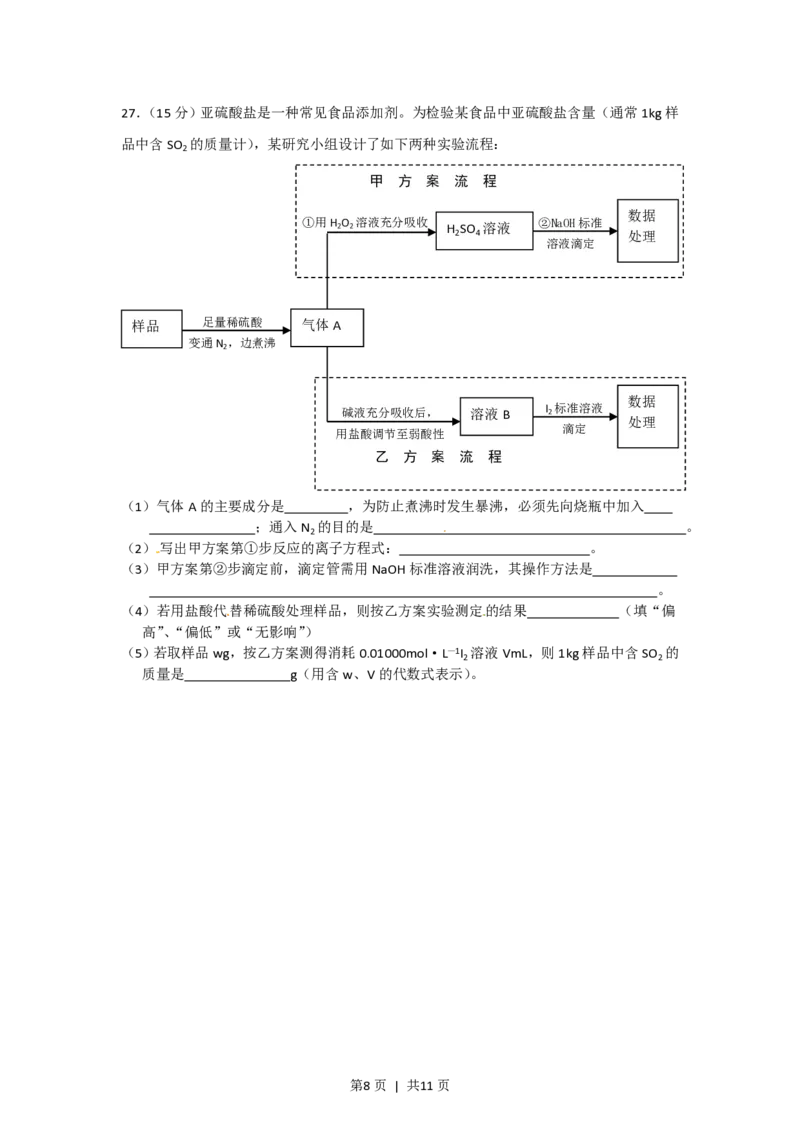
第6页 | 共11页第7页 | 共11页27.(15分)亚硫酸盐是一种常见食品添加剂。为检验某食品中亚硫酸盐含量(通常1kg样
品中含SO 的质量计),某研究小组设计了如下两种实验流程:
2
甲 方 案 流 程
数据
①用H 2 O 2 溶液充分吸收 H SO 溶液 ②NaOH标准
2 4 处理
溶液滴定
样品 足量稀硫酸 气体A
变通N ,边煮沸
2
数据
碱液充分吸收后, 溶液B I 2 标准溶液
处理
滴定
用盐酸调节至弱酸性
乙 方 案 流 程
(1)气体A的主要成分是 ,为防止煮沸时发生暴沸,必须先向烧瓶中加入
;通入N 的目的是 。
2
(2)写出甲方案第①步反应的离子方程式: 。
(3)甲方案第②步滴定前,滴定管需用NaOH标准溶液润洗,其操作方法是
。
(4)若用盐酸代替稀硫酸处理样品,则按乙方案实验测定的结果 (填“偏
高”、“偏低”或“无影响”)
(5)若取样品wg,按乙方案测得消耗0.01000mol·L—1I 溶液VmL,则1kg样品中含SO 的
2 2
质量是 g(用含w、V的代数式表示)。
第8页 | 共11页28.(13分)工业上从废铅酸电池的铅膏回收铅的过程中,可用碳酸盐溶液与铅膏(主要成
分为PbSO )发生反应:PbSO (s)+CO 2—(aq) PbCO (s)+SO 2—(aq)。某课题组用PbSO 为原
4 4 3 3 4 4
料模拟该过程,探究上述反应的实验条件及固体产物的成分。
(1)上述反应的平衡常数表达式:K= 。
(2)室温时,向两份相同的样品中分别加入同体积、同浓度的Na CO 和NaHCO 溶液
2 3 3
均可实现上述转化,在 溶液中PbSO 转化率较大,理由是 。
4
(3)查阅文献:上述反应还可能生成碱式碳酸铅[2PbCO ·Pb(OH) ],它和PbCO 受热都
3 2 3
易分解生成PbO。该课题组对固体产物(不考虑PbSO )的成分提出如下假设,请
4
你完成假设二和假设三:
假设一:全部为PbCO ;
3
假设二: ;
第9页 | 共11页假设三: 。
(4)为验证假设一是否成立,课题组进行如下研究。
①定性研究:请你完成下表中内容。
实验步骤(不要求写出具体操作过程) 预期的实验现象和结论
取一定量样品充分干燥,……
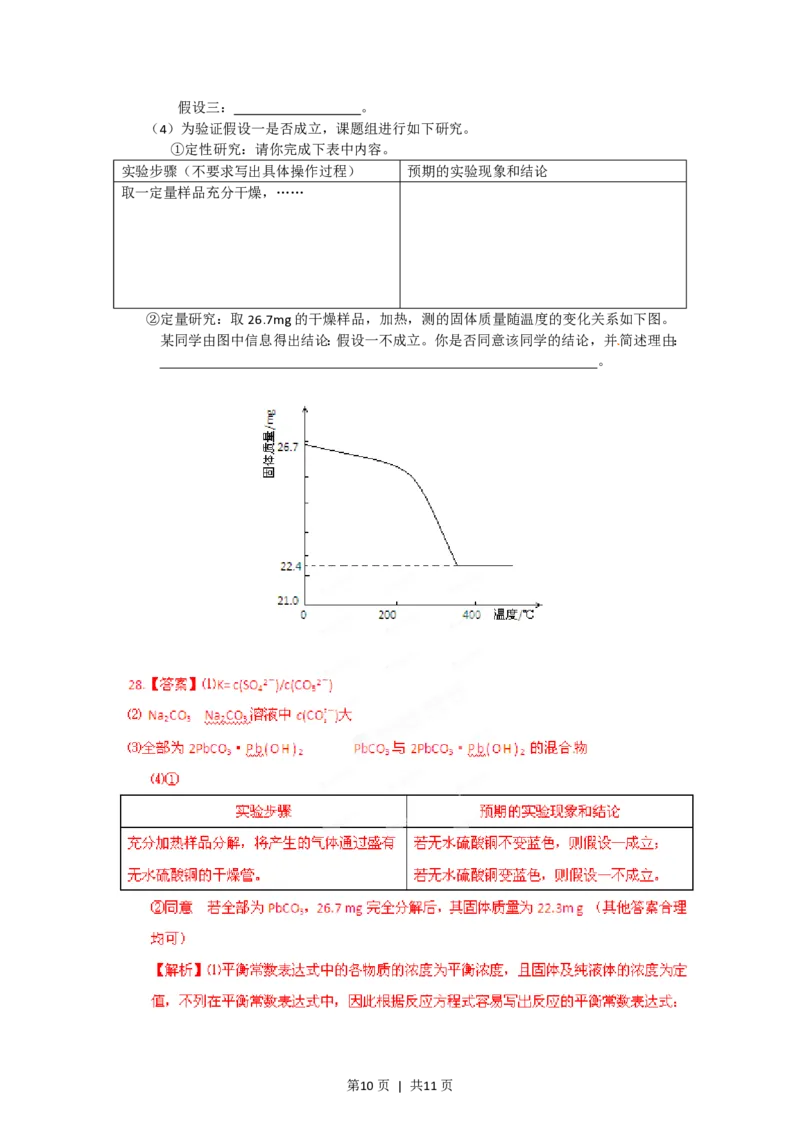
②定量研究:取26.7mg的干燥样品,加热,测的固体质量随温度的变化关系如下图。
某同学由图中信息得出结论:假设一不成立。你是否同意该同学的结论,并简述理由:
。
第10页 | 共11页第11页 | 共11页