文档内容
五年(2019-2023)年高考真题分项汇编
专题 06 物质结构与性质 元素推断
〖2023年高考真题〗
考点一 原子结构和化学键
1.(2023·北京卷)下列事实不能通过比较氟元素和氯元素的电负性进行解释的是
A. 键的键能小于 键的键能
B.三氟乙酸的 大于三氯乙酸的
C.氟化氢分子的极性强于氯化氢分子的极性
D.气态氟化氢中存在 ,而气态氯化氢中是 分子
【答案】A
【详解】A.F原子半径小,电子云密度大,两个原子间的斥力较强, 键不稳定,因此 键的键能
小于 键的键能,与电负性无关,A符合题意;
B.氟的电负性大于氯的电负性。 键的极性大于 键的极性,使 —的极性大于 —的极性,
导致三氟乙酸的羧基中的羟基极性更大,更容易电离出氢离子,酸性更强,B不符合题意;
C.氟的电负性大于氯的电负性, 键的极性大于 键的极性,导致 分子极性强于 ,C不
符合题意;
D.氟的电负性大于氯的电负性,与氟原子相连的氢原子可以与另外的氟原子形成分子间氢键,因此气态
氟化氢中存在 ,D不符合题意;
故选A。
考点二 元素推断
2.(2023·全国甲卷)W、X、Y、Z为短周期主族元素,原子序数依次增大,最外层电子数之和为19。Y
的最外层电子数与其K层电子数相等,WX 是形成酸雨的物质之一。下列说法正确的是
2
A.原子半径: B.简单氢化物的沸点:
C. 与 可形成离子化合物 D. 的最高价含氧酸是弱酸
【答案】C
【分析】W、X、Y、Z为短周期主族元素,原子序数依次增大,WX 是形成酸雨的物质之一,根据原子序
2
数的规律,则W为N,X为O,Y的最外层电子数与其K层电子数相等,又因为Y的原子序数大于氧的,
则Y电子层为3层,最外层电子数为2,所以Y为Mg,四种元素最外层电子数之和为19,则Z的最外层
电子数为6,Z为S,据此解答。
【详解】A.X为O,W为N,同周期从左往右,原子半径依次减小,所以半径大小为W>X,A错误;
B.X为O,Z为S,X的简单氢化物为HO,含有分子间氢键,Z的简单氢化物为HS,没有氢键,所以
2 2
简单氢化物的沸点为X>Z,B错误;C.Y为Mg,X为O,他们可形成MgO,为离子化合物,C正确;
D.Z为S,硫的最高价含氧酸为硫酸,是强酸,D错误;
故选C。
3.(2023·全国乙卷)一种矿物由短周期元素W、X、Y组成,溶于稀盐酸有无色无味气体生成。W、X、
Y原子序数依次增大。简单离子 与 具有相同的电子结构。下列叙述正确的是
A.X的常见化合价有 、 B.原子半径大小为
C.YX的水合物具有两性 D.W单质只有4种同素异形体
【答案】A
【分析】W、X、Y为短周期元素,原子序数依次增大,简单离子X2-与Y2+具有相同的电子结构,则它们
均为10电子微粒, X为O,Y为Mg,W、X、Y组成的物质能溶于稀盐酸有无色无味的气体产生,则W
为C,产生的气体为二氧化碳,据此解答。
【详解】A.X为O,氧的常见价态有-1价和-2价,如HO 和HO,A正确;
2 2 2
B.W为C,X为O,Y为Mg,同主族时电子层数越多,原子半径越大,电子层数相同时,原子序数越小,
原子半径越大,所以原子半径大小为:Y>W>X,B错误;
C.Y为Mg,X为O,他们可形成MgO,水合物为Mg(OH) ,Mg(OH) 只能与酸反应生成盐和水,不能与
2 2
碱反应,所以YX的水合物没有两性,C错误;
D.W为C,碳的同素异形体有:金刚石、石墨、石墨烯、富勒烯、碳纳米管等,种类不止四种,D错误;
故选A。
4.(2023·湖南卷)日光灯中用到的某种荧光粉的主要成分为3W3(ZX4)2·WY2。已知:X、Y、Z和W为
原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,
基态X、Y、Z原子的未成对电子数之比为2:1:3。下列说法正确的是
A.电负性:X>Y>Z>W
B.原子半径:XX>Z>W,A错误;
B.同一周期原子半径从左到右依次减小,同一主族原子半径从上到下依次增大,故四种原子的原子半径大小为:YO>C,B错误;
C.Q为Al,Al O 为两性氧化物,C正确;
2 3
D.该阴离子中L与Q之间形成配位键,D正确;
故答案选AB。
7.(2023·湖北卷)W、X、Y、Z为原子序数依次增加的同一短周期元素,其中X、Y、Z相邻,W的核
外电子数与X的价层电子数相等, 是氧化性最强的单质,4种元素可形成离子化合物 。下
列说法正确的是
A.分子的极性: B.第一电离能:XH,C-F键极性大于C-H键,使得羧基上的羟基极性增强,氢原子更容易电离,酸性增
强,故C正确;
D.碳酸氢钠在水中的溶解度比碳酸钠小的原因是碳酸氢钠晶体中HCO 间存在氢键,与晶格能大小无关,
即与阴离子电荷无关,故D错误;
答案选D。
考点四 晶体结构与性质
12.(2023·北京卷)中国科学家首次成功制得大面积单晶石墨炔,是碳材料科学的一大进步。
下列关于金刚石、石墨、石墨炔的说法正确的是
A.三种物质中均有碳碳原子间的 键 B.三种物质中的碳原子都是 杂化
C.三种物质的晶体类型相同 D.三种物质均能导电
【答案】A
【详解】A.原子间优先形成 键,三种物质中均存在 键,A项正确;
B.金刚石中所有碳原子均采用 杂化,石墨中所有碳原子均采用 杂化,石墨炔中苯环上的碳原子采
用 杂化,碳碳三键上的碳原子采用 杂化,B项错误;
C.金刚石为共价晶体,石墨炔为分子晶体,石墨为混合晶体,C项错误;
D.金刚石中没有自由移动电子,不能导电,D项错误;故选A。
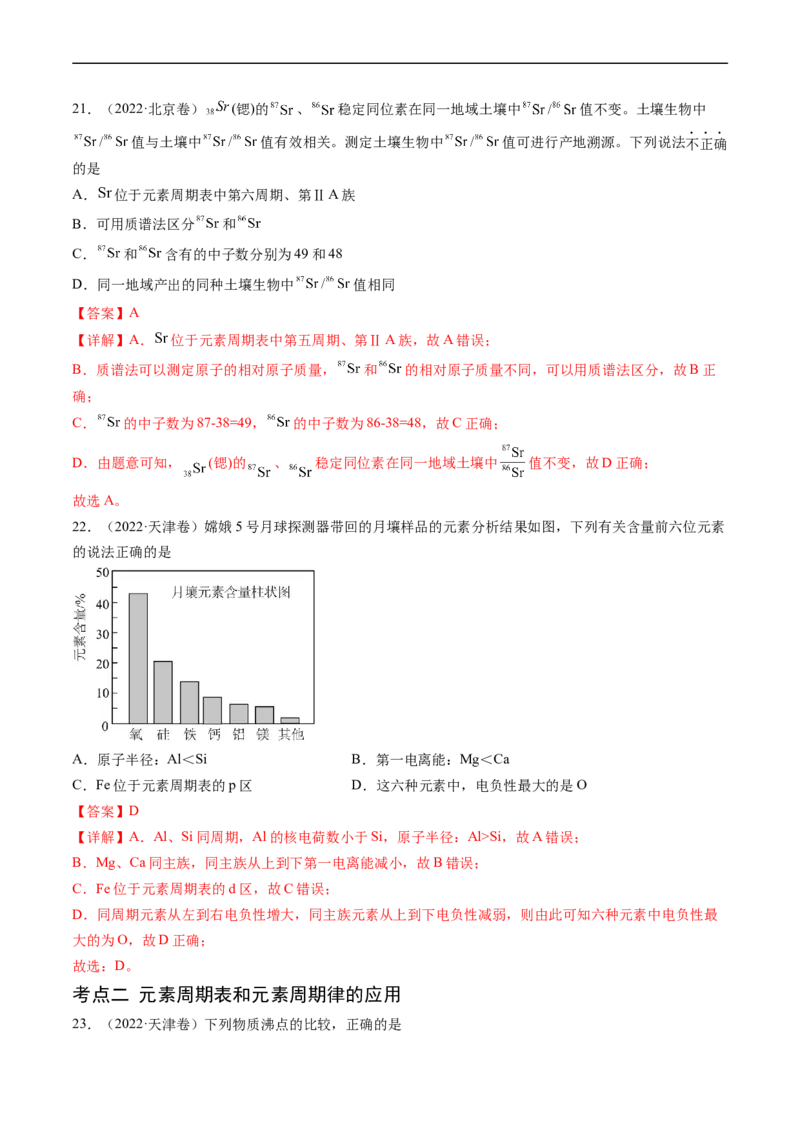
13.(2023·山东卷)石墨与F2在450℃反应,石墨层间插入F得到层状结构化合物(CF)x,该物质仍具润
滑性,其单层局部结构如图所示。下列关于该化合物的说法正确的是
A.与石墨相比,(CF) 导电性增强
x
B.与石墨相比,(CF) 抗氧化性增强
x
C.(CF) 中 的键长比 短
x
D.1mol(CF) 中含有2xmol共价单键
x
【答案】B
【详解】A.石墨晶体中每个碳原子上未参与杂化的1个2p轨道上电子在层内离域运动,故石墨晶体能导
电,而(CF) 中没有未参与杂化的2p轨道上的电子,故与石墨相比,(CF) 导电性减弱,A错误;
x x
B.(CF) 中C原子的所有价键均参与成键,未有未参与成键的孤电子或者不饱和键,故与石墨相比,(CF)
x x
抗氧化性增强,B正确;
C.已知C的原子半径比F的大,故可知(CF) 中 的键长比 长,C错误;
x
D.由题干结构示意图可知,在(CF) 中C与周围的3个碳原子形成共价键,每个C-C键被2个碳原子共用,
x
和1个F原子形成共价键,即1mol(CF) 中含有2.5xmol共价单键,D错误;
x
故答案为:B。
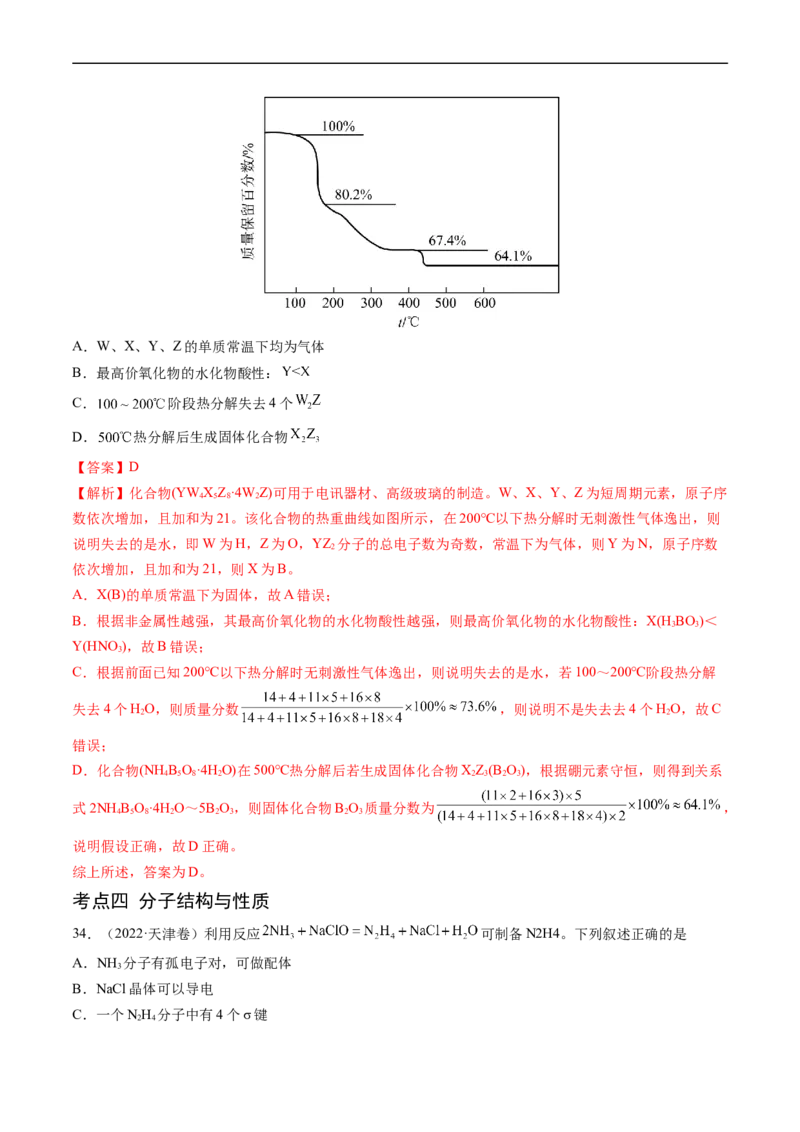
14.(2023·湖南卷)科学家合成了一种高温超导材料,其晶胞结构如图所示,该立方晶胞参数为 。阿
伏加德罗常数的值为 。下列说法错误的是
A.晶体最简化学式为
B.晶体中与 最近且距离相等的 有8个
C.晶胞中B和C原子构成的多面体有12个面D.晶体的密度为
【答案】C
【详解】A.根据晶胞结构可知,其中K个数:8× =1,其中Ca个数:1,其中B个数:12× =6,其中C
个数:12× =6,故其最简化学式为 ,A正确;
B.根据晶胞结构可知, 位于晶胞体心,Ca位于定点,则晶体中与 最近且距离相等的 有8个,
B正确;
C.根据晶胞结构可知,晶胞中B和C原子构成的多面体有14个面,C错误;
D.根据选项A分析可知,该晶胞最简化学式为 ,则1个晶胞质量为: ,晶胞体积为a3×10-
30cm3,则其密度为 ,D正确;
故选C。
15.(2023·湖北卷)镧La和H可以形成一系列晶体材料 ,在储氢和超导等领域具有重要应用。
,属于立方晶系,晶胞结构和参数如图所示。高压下, 中的每个H结合4个H形成类似 的
结构,即得到晶体 。下列说法错误的是
A. 晶体中La的配位数为8
B.晶体中H和H的最短距离:
C.在 晶胞中,H形成一个顶点数为40的闭合多面体笼
D. 单位体积中含氢质量的计算式为
【答案】C
【详解】A.由 的晶胞结构可知,La位于顶点和面心,晶胞内8个小立方体的中心各有1个H原子,
若以顶点La研究,与之最近的H原子有8个,则La的配位数为8,故A正确;
B.由 晶胞结构可知,每个H结合4个H形成类似 的结构,H和H之间的最短距离变小,则晶体
中H和H的最短距离: ,故B正确;
C.由题干信息可知,在 晶胞中,每个H结合4个H形成类似 的结构,这样的结构有8个,顶点数为4 8=32,且不是闭合的结构,故C错误;
D.1个 晶胞中含有5 8=40个H原子,含H质量为 g,晶胞的体积为(484.0 10-10cm)3=(4.84 10-
8)3cm3,则 单位体积中含氢质量的计算式为 ,故D正确;
答案选C。
16.(2023·辽宁卷)晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是立方体(图1),
进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法错误的是
A.图1晶体密度为 g∙cm-3 B.图1中O原子的配位数为6
C.图2表示的化学式为 D. 取代产生的空位有利于 传导
【答案】C
【详解】A.根据均摊法,图1的晶胞中含Li:8× +1=3,O:2× =1,Cl:4× =1,1个晶胞的质量为
g= g,晶胞的体积为(a×10-10cm)3=a3×10-30cm3,则晶体的密度为 g÷(a3×10-30cm3)=
g/cm3,A项正确;
B.图1晶胞中,O位于面心,与O等距离最近的Li有6个,O原子的配位数为6,B项正确;
C.根据均摊法,图2中Li:1,Mg或空位为8× =2。O:2× =1,Cl或Br:4× =1,Mg的个数小于
2,根据正负化合价的代数和为0,图2的化学式为LiMgOCl Br ,C项错误;
x 1-x
D.进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料,说明Mg2+取代产生的空位有利于
Li+的传导,D项正确;
答案选C。
17.(2023·新课标卷)一种可吸附甲醇的材料,其化学式为 ,部分晶体结构
如下图所示,其中 为平面结构。下列说法正确的是
A.该晶体中存在N-H…O氢键 B.基态原子的第一电离能:
C.基态原子未成对电子数: D.晶体中B、N和O原子轨道的杂化类型相同
【答案】A
【详解】A.由晶体结构图可知, 中的 的 与 中的 形成氢键,因此,该晶
体中存在 氢键,A说法正确;
B.同一周期元素原子的第一电离能呈递增趋势,但是第ⅡA、ⅤA元素的原子结构比较稳定,其第一电
离能高于同周期的相邻元素的原子,因此,基态原子的第一电离能从小到大的顺序为C< O < N,B说法不
正确;
C.B、C、O、N的未成对电子数分别为1、2、2、3,因此,基态原子未成对电子数BSi,故A错误;
B.Mg、Ca同主族,同主族从上到下第一电离能减小,故B错误;
C.Fe位于元素周期表的d区,故C错误;
D.同周期元素从左到右电负性增大,同主族元素从上到下电负性减弱,则由此可知六种元素中电负性最
大的为O,故D正确;
故选:D。
考点二 元素周期表和元素周期律的应用
23.(2022·天津卷)下列物质沸点的比较,正确的是A. B.HF>HCl
C. D.
【答案】B
【详解】A.甲烷和乙烷组成结构相似,相对分子质量越大,范德华力越大,沸点越高,因此沸点
,故A错误;
B.HF存在分子间氢键,因此沸点HF>HCl,故B正确;
C. 组成结构相似,相对分子质量越大,范德华力越大,沸点越高,因此沸点 ,故C
错误;
D.相同碳原子的烷烃,支链越多,沸点越低,因此 ,故D错误。
综上所述,答案为B。
24.(2022·辽宁卷)下列类比或推理合理的是
已知 方法 结论
A 沸点: 类比 沸点:
B 酸性: 类比 酸性:
C 金属性: 推理 氧化性:
D : 推理 溶解度:
【答案】A
【详解】A. 、 、 的相对分子质量逐渐增大,沸点逐渐升高,可推知分子晶体的相对分子质量越
大,分子间作用力越大,沸点越高,由于相对分子质量: ,所以沸点: ,故A
正确;
B.非金属元素最高价含氧酸的酸性与非金属性有关,元素的非金属性越强,最高价含氧酸的酸性越强,
所以酸性: ,酸性: ,故B错误;
C.由金属性: ,可推出氧化性 ;由离子方程式 可得,氧化性:
,故C错误;
D. 和 的阴、阳离子个数比不相同,不能通过 大小来比较二者在水中的溶解度,故D错
误;
选A。
25.(2022·江苏卷)工业上电解熔融 和冰晶石 的混合物可制得铝。下列说法正确的是
A.半径大小: B.电负性大小:C.电离能大小: D.碱性强弱:
【答案】A
【详解】A.核外电子数相同时,核电荷数越大半径越小,故半径大小为 ,故A正确;
B.同周期元素核电荷数越大电负性越大,故 ,故B错误;
C.同周期从左往右第一电离能呈增大趋势,同主族从上往下第一电离能呈减小趋势,故电离能大小为
,故C错误;
D.元素金属性越强,其最高价氧化物对应水化物的碱性越强,故碱性强弱为 ,故D错误;
故选A。
考点三 元素推断
26.(2022·广东卷)甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对
应的水化物为强酸。下列说法不正确的是
A.原子半径:丁>戊>乙
B.非金属性:戊>丁>丙
C.甲的氢化物遇氯化氢一定有白烟产生
D.丙的最高价氧化物对应的水化物一定能与强碱反应
【答案】C
【解析】甲~戊是短周期元素,戊中的最高价氧化物对应水化物为强酸,则可能是硫酸或高氯酸,若是高
氯酸,则戊为Cl,甲为N、乙为F、丙为P、丁为S,若是硫酸,则戊为S,甲为C、乙为O、丙为Si、丁
为P。
A.根据层多径大,同电子层结构核多径小原则,则原子半径:丁>戊>乙,故A正确;
B.根据同周期从左到右非金属性逐渐增强,则非金属性:戊>丁>丙,故B正确;
C.甲的氢化物可能为氨气,可能为甲烷、乙烷等,若是氨气,则遇氯化氢一定有白烟产生;若是甲烷、
乙烷等,则遇氯化氢不反应,没有白烟生成,故C错误;
D.丙的最高价氧化物对应的水化物可能是硅酸、也可能是磷酸,都一定能与强碱反应,故D正确。
综上所述,答案为C。
27.(2022·全国甲卷)Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外层电子数之和为
19。Q与X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是Q原子内层电子数的2倍。下列说
法正确的是
A.非金属性: B.单质的熔点:
C.简单氢化物的沸点: D.最高价含氧酸的酸性:
【答案】D【解析】Q、X、Y、Z为原子序数依次增大的短周期主族元素,Q与X、Y、Z不在同一周期,Y原子最外
层电子数为Q元原子内层电子数的2倍,则Q应为第二周期元素,X、Y、Z位于第三周期,Y的最外层电
子数为4,则Y为Si元素,X、Y相邻,且X的原子序数小于Y,则X为Al元素,Q、X、Y、Z的最外层
电子数之和为19,则Q、Z的最外层电子数之和为19-3-4=12,主族元素的最外层电子数最多为7,若Q的
最外层电子数为7,为F元素,Z的最外层电子数为5,为P元素,若Q的最外层电子数为6,为O元素,
则Z的最外层电子数为6,为S元素,若Q的最外层电子数为5,为N元素,Z的最外层电子数为7,为Cl
元素;综上所述,Q为N或O或F,X为Al,Y为Si,Z为Cl或S或P,据此分析解题。
A.X为Al,Q为N或O或F,同一周期从左往右元素非金属性依次增强,同一主族从上往下依次减弱,
故非金属性:Q>X,A错误;
B.由分析可知,X为Al属于金属晶体,Y为Si属于原子晶体或共价晶体,故单质熔点Si>Al,即Y>X,
B错误;
C.含有氢键的物质沸点升高,由分析可知Q为N或O或F,其简单氢化物为HO或NH 或HF,Z为Cl
2 3
或S或P,其简单氢化物为HCl或HS或PH ,由于前者物质中存在分子间氢键,而后者物质中不存在,
2 3
故沸点Q>Z,C错误;
D.元素的非金属性越强,其最高价含氧酸的酸性越强,P、S、Cl的非金属性均强于Si,因此最高价含氧
酸酸性:Z>Y,D正确;
故答案为:D。
28.(2022·重庆卷)R、X、Y、Z均为短周期主族元素,Y与Z同主族且Z的原子序数大于Y。R和X的
原子获得1个电子均可形成稀有气体原子的电子层结构,R的最高化合价为+1。1mol化合物RZY X含
3
58mol电子。下列说法正确的是
A.R与X形成的化合物水溶液呈碱性 B.X是四种元素中原子半径最大的
C.Y单质的氧化性比Z单质的弱 D.Z的原子最外层电子数为6
【答案】D
【分析】由题干信息可知,R、X、Y、Z均为短周期主族元素,Y与Z同主族且Z的原子序数大于Y,R
和X的原子获得1个电子均可形成稀有气体原子的电子层结构,R的最高化合价为+1,则R为H,X为Cl
或F;1mol化合物RZY X含58mol电子,设Y的原子序数为a,则Z的原子序数为a+8;若X为F,则有
3
1+9+a+8+3a=58,解得a=10,则Y为Ne,不符合题意;若X为Cl,则有1+17+a+8+3a=58,解得a=8,则
Y为O,Z为S;故R为H、X为Cl、Y为O、Z为S,据此分析解题。
【详解】A.由分析可知,R为H、X为Cl,故R与X形成的化合物即HCl水溶液呈酸性,A错误;
B.由分析可知,R为H、X为Cl、Y为O、Z为S,故S是四种元素中原子半径最大的,B错误;
C.由分析可知,Y为O、Z为S,由于O的非金属性比S强,故O 的氧化性比S强,C错误;
2
D.由分析可知,Z为S,是16号元素,S原子最外层电子数为6,D正确;
故答案为:D。
29.(2022·福建卷)某非线性光学晶体由钾元素(K)和原子序数依次增大的X、Y、Z、W四种短周期元素
组成。X与Y、Z与W均为同周期相邻元素,X的核外电子总数为最外层电子数的2倍,Z为地壳中含量
最多的元素。下列说法正确的是A.简单氢化物沸点: B. 分子的空间构型为三角锥形
C.原子半径: D.最高价氧化物对应水化物的碱性:
【答案】A
【分析】X的核外电子总数为最外层电子数的2倍,X为Be;Z为地壳中含量最多的元素,Z为O,X与
Y、Z与W均为同周期相邻元素,Y为B,W为F,据此解答。
【详解】A. 常温下为液态,HF常温下为气体,沸点 ,故A正确;
B. 为BF,中心B原子有3对价电子且没有孤电子对,空间构型为平面三角形,故B错误;
3
C.四种元素为同周期元素,随核电荷数增大原子半径减小,原子半径:Be>B>O>F,故C错误;
D.Be最高价氧化物水化物为Be(OH) ,溶液显两性,B最高价氧化物的水化物为HBO,溶液显酸性,
2 3 3
故D错误;
故选:A。
30.(2022·辽宁卷)短周期元素X、Y、Z、W、Q原子序数依次增大。基态X、Z、Q原子均有两个单电
子,W简单离子在同周期离子中半径最小,Q与Z同主族。下列说法错误的是
A.X能与多种元素形成共价键 B.简单氢化物沸点:
C.第一电离能: D.电负性:
【答案】B
【分析】短周期元素X、Y、Z、W、Q原子序数依次增大,W简单离子在同周期离子中半径最小,说明W
为第三周期元素Al。短周期元素的基态原子中有两个单电子,可分类讨论:①为第二周期元素时,最外层
电子排布为2s22p2或2s22p4,即C或O;②为第三周期元素时,最外层电子排布为3s23p2或3s23p4,即Si或
S。Q与Z同主族,结合原子序数大小关系可知,则X、Z、Q分别为C、O和S,则Y为N。
【详解】A.X为C,能与多种元素(H、O、N、P、S等)形成共价键,A正确;
B.Z和Q形成的简单氢化物为HO和HS,由于HO分子间能形成氢键,故HO沸点高于HS,B错误;
2 2 2 2 2
C.Y为N,Z为O,N的最外层p轨道电子为半充满结构,比较稳定,故其第一电离能比O大,C正确;
D.W为Al,Z为O,O的电负性更大,D正确;
故选B。
31.(2022·湖南卷)科学家合成了一种新的共价化合物(结构如图所示),X、Y、Z、W为原子序数依次增
大的短周期元素,W的原子序数等于X与Y的原子序数之和。下列说法错误的是
A.原子半径:
B.非金属性:
C.Z的单质具有较强的还原性
D.原子序数为82的元素与W位于同一主族【答案】C
【解析】由共价化合物的结构可知,X、W形成4个共价键,Y形成2个共价键,Z形成1个共价键,X、
Y、Z、W是原子序数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和,则X为C元素、
Y为O元素、Z为F元素、W为Si元素。
A.同周期元素,从左到右原子半径依次减小,则C、O、F的原子半径大小顺序为C>O>F,故A正确;
B.同周期元素,从左到右元素的非金属性依次增强,同主族元素,从上到下元素的非金属性依次减弱,
则C、O、Si的非金属性强弱顺序为O>C>Si,故B正确;
C.位于元素周期表右上角的氟元素的非金属性最强,单质具有很强的氧化性,故C错误;
D.原子序数为82的元素为铅元素,与硅元素都位于元素周期表ⅣA族,故D正确;
故选C。
32.(2022·浙江卷)X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。X的核外电子数等于其
周期数, 分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q是同周期
中非金属性最强的元素。下列说法正确的是
A.X与Z形成的10电子微粒有2种
B.Z与Q形成的一种化合物可用于饮用水的消毒
C. 与 的晶体类型不同
D.由X、Y、Z三种元素组成的化合物的水溶液均显酸性
【答案】B
【解析】X的核外电子数等于其周期数,X为H,YX 分子呈三角锥形,Y为N,Z的核外电子数等于X、
3
Y核外电子数之和,则Z为O,M与X同主族,则M为Na,Q是同周期中非金属性最强的元素,则Q为
Cl,综合分析,X为H,Y为N,Z为O,M为Na,Q为Cl,以此解题。
A.由分析可知X为H,Z为O,则其形成的10电子微粒有HO、OH-、HO+,A错误;
2 3
B.由分析可知Z为O,Q为Cl,可形成ClO ,有氧化性,可用于自来水消毒,B正确;
2
C.由分析可知Z为O,M为Na,Q为Cl,则MZ为NaO,为离子晶体,MQ为NaCl,为离子晶体,晶
2 2
体类型相同,C错误;
D.由分析可知X为H,Y为N,Z为O,这三种元素可以形成NH₃·H₂O,其溶液显碱性,D错误;
故选B。
33.(2022·全国乙卷)化合物 可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短
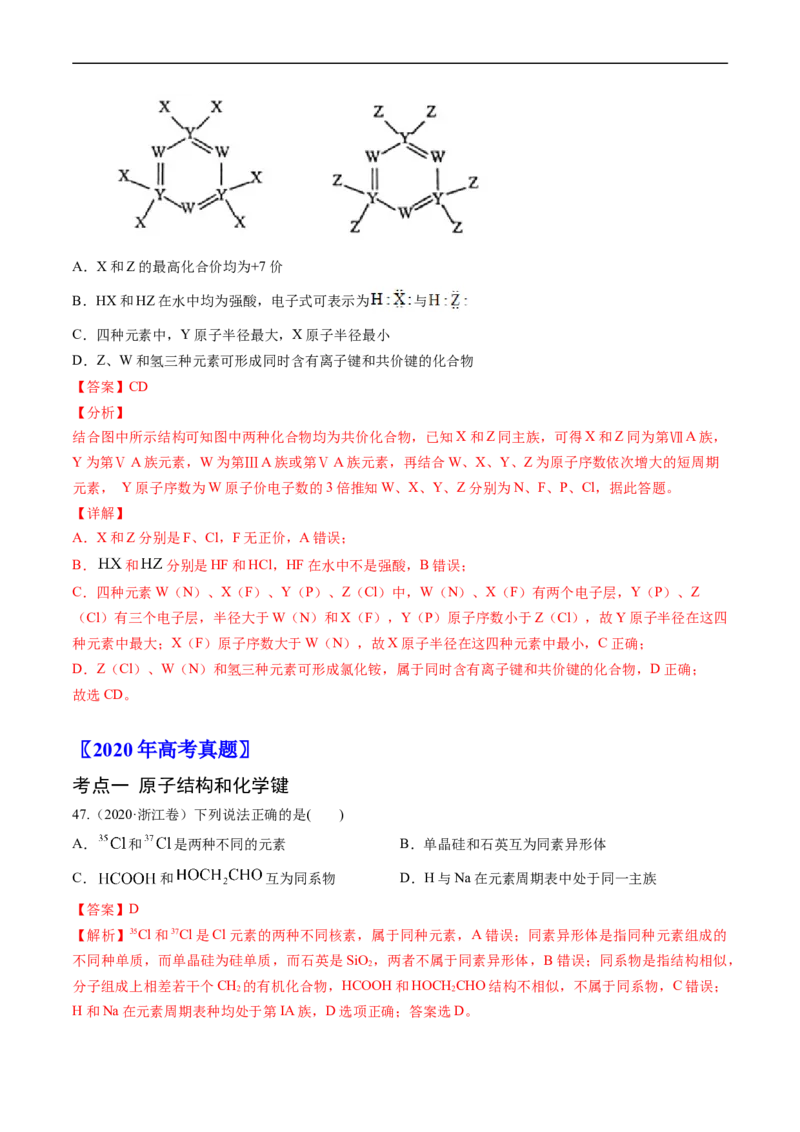
周期元素,原子序数依次增加,且加和为21。 分子的总电子数为奇数常温下为气体。该化合物的热重
曲线如图所示,在 以下热分解时无刺激性气体逸出。下列叙述正确的是A.W、X、Y、Z的单质常温下均为气体
B.最高价氧化物的水化物酸性:
C. 阶段热分解失去4个
D. 热分解后生成固体化合物
【答案】D
【解析】化合物(YW XZ·4W Z)可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周期元素,原子序
4 5 8 2
数依次增加,且加和为21。该化合物的热重曲线如图所示,在200℃以下热分解时无刺激性气体逸出,则
说明失去的是水,即W为H,Z为O,YZ 分子的总电子数为奇数,常温下为气体,则Y为N,原子序数
2
依次增加,且加和为21,则X为B。
A.X(B)的单质常温下为固体,故A错误;
B.根据非金属性越强,其最高价氧化物的水化物酸性越强,则最高价氧化物的水化物酸性:X(H BO)<
3 3
Y(HNO ),故B错误;
3
C.根据前面已知200℃以下热分解时无刺激性气体逸出,则说明失去的是水,若100~200℃阶段热分解
失去4个HO,则质量分数 ,则说明不是失去去4个HO,故C
2 2
错误;
D.化合物(NH B O·4H O)在500℃热分解后若生成固体化合物XZ(B O),根据硼元素守恒,则得到关系
4 5 8 2 2 3 2 3
式2NH B O·4H O~5B O,则固体化合物B O 质量分数为 ,
4 5 8 2 2 3 2 3
说明假设正确,故D正确。
综上所述,答案为D。
考点四 分子结构与性质
34.(2022·天津卷)利用反应 可制备N2H4。下列叙述正确的是
A.NH 分子有孤电子对,可做配体
3
B.NaCl晶体可以导电
C.一个NH 分子中有4个σ键
2 4D.NaClO和NaCl均为离子化合物,他们所含的化学键类型相同
【答案】A
【详解】A.NH 中N原子的孤电子对数= =1,可以提供1对孤电子对,可以做配体,A正确;
3
B.导电需要物质中有可自由移动的离子或电子,NaCl晶体中没有自由移动的电子或者离子,故不能导电,
B错误;
C.单键属于σ键,双键中含有1个σ键和1个π键,三键中含有1个σ键和2个π键;NH 的结构式为
2 4
,分子中含有5个σ键,C错误;
D.NaClO含有离子键和共价键,NaCl只含有离子键,都是离子化合物,但所含的化学键类型不同,D错
误;
故选A。
35.(2022·辽宁卷)理论化学模拟得到一种 离子,结构如图。下列关于该离子的说法错误的是
A.所有原子均满足8电子结构 B.N原子的杂化方式有2种
C.空间结构为四面体形 D.常温下不稳定
【答案】B
【详解】A.由 的结构式可知,所有N原子均满足8电子稳定结构,A正确;
B.中心N原子为 杂化,与中心N原子直接相连的N原子为 杂化,与端位N原子直接相连的N原子
为 杂化,端位N原子为 杂化,则N原子的杂化方式有3种,B错误;
C.中心N原子为 杂化,则其空间结构为四面体形,C正确;
D. 中含叠氮结构( ),常温下不稳定,D正确;
故答案选B。
36.(2022·江苏卷)下列说法正确的是
A.金刚石与石墨烯中的 夹角都为
B. 、 都是由极性键构成的非极性分子
C.锗原子( )基态核外电子排布式为
D.ⅣA族元素单质的晶体类型相同
【答案】B
【详解】A.金刚石中的碳原子为正四面体结构, 夹角为109°28′,故A错误;B. 的化学键为Si-H,为极性键,为正四面体,正负电荷中心重合,为非极性分子; 的化学键为
Si-Cl,为极性键,为正四面体,正负电荷中心重合,为非极性分子,故B正确;
C.锗原子( )基态核外电子排布式为[Ar]3d10 ,故C错误;
D.ⅣA族元素中的碳元素形成的石墨为混合晶体,而硅形成的晶体硅为原子晶体,故D错误;
故选B。
考点五 晶体结构与性质
37.(2022·山东卷) 、 属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在
键、 键。下列说法错误的是
A. 的熔点高于 B.晶体中所有化学键均为极性键
C.晶体中所有原子均采取 杂化 D.晶体中所有原子的配位数均相同
【答案】A
【解析】Al和Ga均为第ⅢA元素,N属于第ⅤA元素,AlN、GaN的成键结构与金刚石相似,则其为共
价晶体,且其与金刚石互为等电子体,等电子体之间的结构和性质相似。AlN、GaN晶体中,N原子与其
相邻的原子形成3个普通共价键和1个配位键。
A.因为AlN、GaN为结构相似的共价晶体,由于Al原子的半径小于Ga,N—Al的键长小于N—Ga的,
则N—Al的键能较大,键能越大则其对应的共价晶体的熔点越高,故GaN的熔点低于AlN,A说错误;
B.不同种元素的原子之间形成的共价键为极性键,故两种晶体中所有化学键均为极性键,B说法正确;
C.金刚石中每个C原子形成4个共价键(即C原子的价层电子对数为4),C原子无孤电子对,故C原子
均采取sp3杂化;由于AlN、GaN与金刚石互为等电子体,则其晶体中所有原子均采取sp3杂化,C说法正
确;
D.金刚石中每个C原子与其周围4个C原子形成共价键,即C原子的配位数是4,由于AlN、GaN与金
刚石互为等电子体,则其晶体中所有原子的配位数也均为4,D说法正确。
综上所述,本题选A。
38.(2022·山东卷) 是一种钠离子电池正极材料,充放电过程中正极材料立方晶胞(示意图)的组成
变化如图所示,晶胞内未标出因放电产生的0价Cu原子。下列说法正确的是
A.每个 晶胞中 个数为x
B.每个 晶胞完全转化为 晶胞,转移电子数为8
C.每个 晶胞中0价Cu原子个数为D.当 转化为 时,每转移 电子,产生 原子
【答案】BD
【解析】A.由晶胞结构可知,位于顶点和面心的硒离子个数为8× +6× =4,位于体内的铜离子和亚铜
离子的个数之和为8,设晶胞中的铜离子和亚铜离子的个数分别为a和b,则a+b=8-4x,由化合价代数和为
0可得2a+b=4×2,解得a=4x,故A错误;
B.由题意可知,NaSe转化为Cu Se的电极反应式为NaSe-2e-+(2-x)Cu=Cu Se+2Na+,由晶胞结构可知,
2 2-x 2 2-x
位于顶点和面心的硒离子个数为8× +6× =4,则每个晶胞中含有4个NaSe,转移电子数为8,故B正确;
2
C.由题意可知,Cu Se转化为NaCuSe的电极反应式为Cu Se+ e-+Na+=NaCuSe+(1-x)Cu,由晶胞结构可
2-x 2-x
知,位于顶点和面心的硒离子个数为8× +6× =4,则每个晶胞中含有4个NaCuSe,晶胞中0价铜而个数
为(4-4x),故C错误;
D.由题意可知,NaCu Se转化为NaCuSe的电极反应式为NaCu Se+(1-y) e-+ Na+=NaCuSe+(1-x)Cu,所
y 2-x y 2-x
以每转移(1-y)电子,产生(1-x)mol铜,故D正确;
故选BD。
〖2021年高考真题〗
考点一 原子结构和化学键
39.(2021·河北)用中子轰击 X原子产生α粒子(即氮核 He)的核反应为: X+ n→ Y+ He。已知元
素Y在化合物中呈+1价。下列说法正确的是
A.HXO 可用于中和溅在皮肤上的NaOH溶液
3 3
B.Y单质在空气中燃烧的产物是YO
2 2
C.X和氢元素形成离子化合物
D.6Y和7Y互为同素异形体
【答案】A
【分析】
根据核反应为: 可知,X的质量数N为4+7-1=10,又因为Y在化合物中呈 价,
则推知Y位于IA族,质量数=质子数+中子数,Y的质量数为7,所以得出Y为Li,其质子数p=3,所以X
的质子数Z=3+2-0=5,核电荷数=原子序数=核内质子数=5,则推知X属于B元素,据此分析解答。
【详解】
A. 为硼酸,氢氧化钠溶液具有腐蚀性,若不慎将 溶液溅到皮肤上,则需用大量水冲洗,
同时涂抹 ,以中和碱液,A正确;
B.Y为Li,在空气中燃烧的产物只有LiO,B错误;
2
C.X为B,与氢元素会形成BH 或B H 等硼氢化合物,B元素与H元素以共价键结合,属于共价化合物,
3 2 4C错误;
D. 和 两者的质子数均为3,中子数不同,所以两者互为同位素,D错误;
故选A。
考点二 元素推断
40.(2021·全国乙)我国嫦娥五号探测器带回 的月球土壤,经分析发现其构成与地球土壤类似土
壤中含有的短周期元素W、X、Y、Z,原子序数依次增大,最外层电子数之和为15。X、Y、Z为同周期
相邻元素,且均不与W同族,下列结论正确的是
A.原子半径大小顺序为
B.化合物XW中的化学键为离子键
C.Y单质的导电性能弱于Z单质的
D.Z的氧化物的水化物的酸性强于碳酸
【答案】B
【分析】
由短周期元素W、X、Y、Z,原子序数依次增大,最外层电子数之和为15, X、Y、Z为同周期相邻元素,
可知W所在主族可能为第ⅢA族或第ⅥA族元素,又因X、Y、Z为同周期相邻元素,且均不与W同族,
故W一定不是第ⅢA族元素,即W一定是第ⅥA族元素,进一步结合已知可推知W、X、Y、Z依次为
O、Mg、Al、Si,据此答题。
【详解】
A.O原子有两层,Mg、Al、Si均有三层且原子序数依次增大,故原子半径大小顺序为Mg>Al>Si>O,
即 ,A错误;
B.化合物XW即MgO为离子化合物,其中的化学键为离子键,B正确;
C.Y单质为铝单质,铝属于导体,导电性很强,Z单质为硅,为半导体,半导体导电性介于导体和绝缘体
之间,故Y单质的导电性能强于Z单质的,C错误;
D.Z的氧化物的水化物为硅酸,硅酸酸性弱于碳酸,D错误;
故选B。
41.(2021·山东)X、Y为第三周期元素、Y最高正价与最低负价的代数和为6,二者形成的一种化合物
能以[XY ]+[XY ]-的形式存在。下列说法错误的是
4 6
A.原子半径:X>Y
B.简单氢化物的还原性:X>Y
C.同周期元素形成的单质中Y氧化性最强
D.同周期中第一电离能小于X的元素有4种
【答案】D
【分析】
Y位于第三周期,且最高正价与最低负价的代数和为6,则Y是Cl元素,由X、Y形成的阴离子和阳离子
知,X与Y容易形成共价键,根据化合物的形式知X是P元素。【详解】
A.P与Cl在同一周期,则P半径大,即X>Y,A项不符合题意;
B.两者对应的简单氢化物分别是PH 和HCl,半径是P3->Cl-,所以PH 的失电子能力强,还原性强,即
3 3
X>Y,B项不符合题意;
C.同周期元素从左往右,金属性减弱,非金属性增强,各元素对应的金属单质还原性减弱,非金属单质
的氧化性增强,所以Cl 的氧化性最强,C项不符合题意;
2
D.同一周期,从左到右,第一电离能呈现增大的趋势,第VA族元素的第一电离能大于相邻元素的第一电
离能;所以第三周期第一电离能从小到大依次为Na、Al、Mg、Si、S、P、Cl,所以有5种,D项符合题
意;
故选D。
42.(2021·浙江)已知短周期元素X、Y、Z、M、Q和R在周期表中的相对位置如下所示,其中Y的最
高化合价为+3。下列说法不正确的是
A.还原性:
B.X能从 中置换出Z
C.Y能与 反应得到Fe
D.M最高价氧化物的水化物能与其最低价氢化物反应
【答案】A
【分析】
根据短周期元素X、Y、Z、M、Q和R在周期表中的相对位置,以及Y的最高化合价为+3,可推知,X为:
,Y为: ,Z为:C,M为:N,Q为:S,R为: ,据此分析答题。
【详解】
A. 为: , 为: , 中硫的还原性强于 中的氯元素,A错误;
B. 和 发生下述反应: ,B正确;
C. 和 发生铝热反应如下: ,C正确;
D.M为:N,N的最高价氧化物的水化物为: ,最低价氢化物为: ,二者发生如下反应:
,D正确;
答案为:A。
43.(2021·全国甲)W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子数是W和X
的最外层电子数之和,也是Y的最外层电子数的2倍。W和X的单质常温下均为气体。下列叙述正确的是A.原子半径:
B.W与X只能形成一种化合物
C.Y的氧化物为碱性氧化物,不与强碱反应
D.W、X和Z可形成既含有离子键又含有共价键的化合物
【答案】D
【分析】
W.X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子数是W和X的最外层电子数之和,
也是Y的最外层电子数的2倍,则分析知,Z的最外层电子数为偶数,W和X的单质常温下均为气体,则
推知W和X为非金属元素,所以可判断W为H元素,X为N元素,Z的最外层电子数为1+5=6,Y的最
外层电子数为 =3,则Y为Al元素,Z为S元素,据此结合元素及其化合物的结构与性质分析解答。
【详解】
根据上述分析可知,W为H元素,X为N元素,Y为Al元素,Z为S元素,则
A.电子层数越多的元素原子半径越大,同周期元素原子半径依次减弱,则原子半径:Y(Al)>Z(S)>X(N)
>W(H),A错误;
B.W为H元素,X为N元素,两者可形成NH 和NH,B错误;
3 2 4
C.Y为Al元素,其氧化物为两性氧化物,可与强酸、强碱反应,C错误;
D.W、X和Z可形成(NH )S、NH HS,两者既含有离子键又含有共价键,D正确。
4 2 4
故选D。
44.(2021·广东)一种麻醉剂的分子结构式如图所示。其中, 的原子核只有1个质子;元素 、 、
原子序数依次增大,且均位于 的下一周期;元素 的原子比 原子多8个电子。下列说法不正确的
是
A. 是一种强酸
B.非金属性:
C.原子半径:
D. 中, 的化合价为+2价
【答案】C
【分析】
题给化合物结构中X、W、E均形成1个共价键、Y形成4个共价键、Z形成2个共价键。
的原子核只有1个质子,则X为H元素;元素 、 、 原子序数依次增大,且均位于 的下一周期,
即第二周期元素,则Y为C元素,Z为O元素,W为F元素;元素 的原子比 原子多8个电子,则E为Cl元素,综合以上分析可知,X、Y、Z、W、E分别为H、C、O、F、Cl元素。
据此分析解答。
【详解】
A.氯元素非金属性较强,其最高价氧化物的水化物HClO 是一种强酸,故A正确;
4
B.同一周期元素从左到右非金属性逐渐增强,所以非金属性:F>O>C,故B正确;
C.同一周期从左到右原子半径逐渐减小,同一主族从上到下原子半径逐渐增大,电子层越多半径越大,
所以原子半径:Cl>C>F,故C错误;
D.OF 中,F为-1价,则O的化合价为+2价,故D正确;
2
答案选C。
45.(2021·湖南)W、X、Y、Z为原子序数依次增大的短周期主族元素,Y的原子序数等于W与X的原
子序数之和,Z的最外层电子数为K层的一半,W与X可形成原子个数比为2:1的 分子。下列说法
正确的是
A.简单离子半径:
B.W与Y能形成含有非极性键的化合物
C.X和Y的最简单氢化物的沸点:
D.由W、X、Y三种元素所组成化合物的水溶液均显酸性
【答案】B
【分析】
Z的最外层电子数为K层的一半,则Z的核外有3个电子层,最外层电子数为1,即为Na,W与X能形成
原子个数比为2:1的18电子的分子,则形成的化合物为NH,所以W为H,X为N,Y的原子序数是W
2 4
和X的原子序数之和,则Y为O。据此分析解答。
【详解】
由分析可知,W为H,X为N,Y为O,Z为Na。
A.离子的电子层数相同时,原子序数越小,半径越大,即离子半径大小为:N3->O2->Na+,即简单离子
半径为:X>Y>Z,故A错误;
B.W为H,Y为O,能形成HO,含有极性共价键和非极性共价键,故B正确;
2 2
C.X的最简单氢化物为氨气,Y的最简单氢化物为水,水的沸点高于氨气,即最简单氢化物的沸点为Y>
X,故C错误;
D.由W、X、Y三种元素形成的化合物有硝酸,硝酸铵,氨水等,硝酸,硝酸铵显酸性,氨水显碱性,
故由W、X、Y三种元素形成的化合物不一定都是酸性,故D错误;
故选B。
46.(2021·河北)如图所示的两种化合物可应用于阻燃材料和生物材料的合成。其中W、X、Y、Z为原
子序数依次增大的短周期元素,X和Z同主族,Y原子序数为W原子价电子数的3倍。下列说法正确的是A.X和Z的最高化合价均为+7价
B.HX和HZ在水中均为强酸,电子式可表示为 与
C.四种元素中,Y原子半径最大,X原子半径最小
D.Z、W和氢三种元素可形成同时含有离子键和共价键的化合物
【答案】CD
【分析】
结合图中所示结构可知图中两种化合物均为共价化合物,已知X和Z同主族,可得X和Z同为第ⅦA族,
Y为第ⅤA族元素,W为第ⅢA族或第ⅤA族元素,再结合W、X、Y、Z为原子序数依次增大的短周期
元素, Y原子序数为W原子价电子数的3倍推知W、X、Y、Z分别为N、F、P、Cl,据此答题。
【详解】
A.X和Z分别是F、Cl,F无正价,A错误;
B. 和 分别是HF和HCl,HF在水中不是强酸,B错误;
C.四种元素W(N)、X(F)、Y(P)、Z(Cl)中,W(N)、X(F)有两个电子层,Y(P)、Z
(Cl)有三个电子层,半径大于W(N)和X(F),Y(P)原子序数小于Z(Cl),故Y原子半径在这四
种元素中最大;X(F)原子序数大于W(N),故X原子半径在这四种元素中最小,C正确;
D.Z(Cl)、W(N)和氢三种元素可形成氯化铵,属于同时含有离子键和共价键的化合物,D正确;
故选CD。
〖2020年高考真题〗
考点一 原子结构和化学键
47.(2020·浙江卷)下列说法正确的是( )
A. 和 是两种不同的元素 B.单晶硅和石英互为同素异形体
C. 和 互为同系物 D.H与Na在元素周期表中处于同一主族
【答案】D
【解析】35Cl和37Cl是Cl元素的两种不同核素,属于同种元素,A错误;同素异形体是指同种元素组成的
不同种单质,而单晶硅为硅单质,而石英是SiO ,两者不属于同素异形体,B错误;同系物是指结构相似,
2
分子组成上相差若干个CH 的有机化合物,HCOOH和HOCH CHO结构不相似,不属于同系物,C错误;
2 2
H和Na在元素周期表种均处于第IA族,D选项正确;答案选D。考点二 元素推断
48.(2020·新课标Ⅰ)1934年约里奥–居里夫妇在核反应中用α粒子(即氦核 )轰击金属原子 ,得到
核素 ,开创了人造放射性核素的先河: + → + 。其中元素X、Y的最外层电子数之和
为8。下列叙述正确的是
A. 的相对原子质量为26
B.X、Y均可形成三氯化物
C.X的原子半径小于Y的
D.Y仅有一种含氧酸
【答案】B
【解析】原子轰击实验中,满足质子和质量数守恒,因此W+4=30+1,则W=27,X与Y原子之间质子数
相差2,因X元素为金属元素,Y的质子数比X大,则Y与X位于同一周期,且Y位于X右侧,且元素
X、Y的最外层电子数之和为8,设X最外层电子数为a,则Y的最外层电子为a+2,解得a=3,因此X为
Al,Y为P,以此解答。 的质量数为27,则该原子相对原子质量为27,故A错误;Al元素均可形成
AlCl ,P元素均可形成PCl ,故B正确;Al原子与P原子位于同一周期,且Al原子序数大于P原子序数,
3 3
故原子半径Al>P,故C错误;P的含氧酸有HPO 、HPO 、HPO 等,故D错误;故答案为B。
3 4 3 3 3 2
49.(2020·新课标Ⅱ)一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素
W、X、Y、Z的原子序数依次增大、且总和为24。下列有关叙述错误的是
A.该化合物中,W、X、Y之间均为共价键
B.Z的单质既能与水反应,也可与甲醇反应
C.Y的最高化合价氧化物的水化物为强酸
D.X的氟化物XF 中原子均为8电子稳定结构
3
【答案】D
【解析】一种由短周期主族元素形成的化合物,具有良好的储氢性能,其中元素W、X、Y、Z的原子序数
依次增大,且总和为24,根据图示,W为1价形成共价键,W为氢,Z为+1价阳离子,Z为Na,Y为3
价,Y为N,24−1−11−7=5,X为B元素。该化合物中,H、B、N之间均以共用电子对形成共价键,故A
正确;Na单质既能与水反应生成氢氧化钠和氢气,也能与甲醇反应生成甲醇钠和氢气,故B正确;N的最
高价氧化物的水化物HNO 为强酸,故C正确;B的氟化物BF 中B原子最外层只有6个电子,达不到8电
3 3
子稳定结构,故D错误;故选D。
50.(2020·新课标Ⅲ)W、X、Y、Z为原子序数依次增大的短周期元素,四种元素的核外电子总数满足
X+Y=W+Z;化合物XW 与WZ相遇会产生白烟。下列叙述正确的是
3
A.非金属性:W> X>Y> Z B.原子半径:Z>Y>X>WC.元素X的含氧酸均为强酸 D.Y的氧化物水化物为强碱
【答案】D
【解析】根据题干信息可知,W、X、Y、Z为原子序数依次增大的短周期元素,化合物XW 与WZ相遇会
3
产生白烟,则WX 为NH ,WZ为HCl,所以W为H元素,X为N元素,Z为Cl元素,又四种元素的核
3 3
外电子总数满足X+Y=W+Z,则Y的核外电子总数为11,Y为Na元素,据此分析解答。根据上述分析可
知,W为H元素,X为N元素,Y为Na元素,Z为Cl元素,则Na为金属元素,非金属性最弱,非金属
性Y<Z,A选项错误;同周期元素从左至右原子半径依次减小,同主族元素至上而下原子半径依次增大,
则原子半径:Na>Cl>N>H,B选项错误;N元素的含氧酸不一定全是强酸,如HNO 为弱酸,C错误;
2
Y的氧化物水化物为NaOH,属于强碱,D正确。
51.(2020·山东卷)短周期主族元素X、Y、Z、W的原子序数依次增大,基态X原子的电子总数是其最高
能级电子数的2倍,Z可与X形成淡黄色化合物ZX,Y、W最外层电子数相同。下列说法正确的是
2 2
A.第一电离能:W>X>Y>Z B.简单离子的还原性:Y>X>W
C.简单离子的半径:W>X>Y>Z D.氢化物水溶液的酸性:Y>W
【答案】C
【解析】四种短周期主族元素,基态X原子的电子总数是其最高能级电子数的2倍,设若X为第二周期元
素原子,则X可能为Be或O,若X为第三周期元素原子,则均不满足题意,Z与X能形成ZX 的淡黄色
2 2
化合物,该淡黄色固体为NaO,则X为O元素,Z为Na元素;Y与W的最外层电子数相同,则Y为F
2 2
元素,W为Cl元素,据此分析。同一周期从左向右第一电离能总趋势为逐渐增大,同一主族从上到下第
一电离能逐渐减小,故四种元素中第一电离能从大到小的顺序为F>O>Cl>Na,A错误;单质的氧化性
越强,简单离子的还原性越弱,O、F、Cl三种元素中F 的氧化性最强O 的氧化性最弱,故简单离子的还
2 2
原性O2−>Cl−>F−,B错误;电子层数越多简单离子半径越大,相同结构的离子,原子序数越大半径越小,
故四种元素中离子半径从大到小的顺序为Cl−>O2−>F−>Na+,C正确;F元素的非金属性强于Cl元素,则
形成氢化物后F原子束缚H原子的能力强于Cl原子,在水溶液中HF不容易发生电离,故HCl的酸性强于
HF,D错误;故选C。
52.(2020·浙江卷)X、Y、Z、M、Q五种短周期元素,原子序数依次增大。Y元素的最高正价为+4价,Y
元素与Z、M元素相邻,且与M元素同主族;化合物 的电子总数为18个;Q元素的原子最外层电子
数比次外层少一个电子。下列说法不正确的是( )
A.原子半径:
B.最高价氧化物对应水化物的酸性:
C. 易溶于水,其水溶液呈碱性
D.X、Z和Q三种元素形成的化合物一定是共价化合物
【答案】D
【解析】X、Y、Z、M、Q为五种短周期元素,原子序数依次增大。Y元素的最高正价为+4价,则证明该
元素为第IVA族元素,又知Y元素与Z、M元素相邻,且与M同族,则在元素周期表位置应为
IVA族 VA族Y Z
M
故推知Y为C元素,Z为N元素,M为Si元素;化合物ZX 的电子总数为18,则推知,X为H,该化合
2 4
物为NH;Q元素的原子最外层电子总数比次外层电子数少一个电子,推出Q为Cl元素,据此结合元素
2 4
周期律与物质的结构与性质分析作答。根据上述分析可知,X为H、Y为C元素、Z为N元素、M为Si元
素、Q为Cl元素,则同周期元素从左到右原子半径依次减小,同主族元素从上到下原子半径依次增大,则
原子半径比较:Z(N)Al
D.碱性:In(OH) >RbOH
3
【答案】D【解析】根据原子核外电子排布规则,该原子结构示意图为 ,因此In位于元素周
期表第五周期第IIIA族,故A不符合题意;质量数=质子数+中子数,元素符号的左上角为质量
数、左下角为质子数,因此该原子的质子数=电子数=49,中子数为115−49=66,所以中子数与电
子数之差为66−49=17,故B不符合题意;Al位于元素周期表的三周期IIIA族,In位于元素周期
表第五周期IIIA族,同主族元素的原子,从上到下,电子层数逐渐增多,半径逐渐增大,因此原
子半径In>Al,故C不符合题意;In位于元素周期表第五周期,铷(Rb)位于元素周期表第五周
期第IA族,同周期元素,核电荷数越大,金属性越越弱,最高价氧化物对应水化物的碱性越弱,
因此碱性:In(OH) <RbOH,故D符合题意;综上所述,本题应选D。
3
考点二 元素推断
55.[2019新课标Ⅰ]科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,
Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是( )
A.WZ的水溶液呈碱性
B.元素非金属性的顺序为X>Y>Z
C.Y的最高价氧化物的水化物是中强酸
D.该新化合物中Y不满足8电子稳定结构
【答案】C
【解析】氯化钠为强酸强碱盐,水溶液呈中性,A错误;同周期元素从左到右,非金属性依次增
强,则非金属性的强弱顺序为Cl>S>P,B错误;P元素的最高价氧化物对应水化物为磷酸,磷
酸是三元中强酸,C正确;新化合物中P元素化合价为−3价,满足8电子稳定结构,故D错误。
56.[2019新课标Ⅱ] 今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,W、X、
Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是( )
A.原子半径:W r(Z)> r(Y)> r(X)
B.由X、Y组成的化合物是离子化合物
C.Z的最高价氧化物对应水化物的酸性比W的强
D.W的简单气态氢化物的热稳定性比X的强
【答案】B
【解析】X是地壳中含量最多的元素,因此X为O元素,Y的最外层有两个电子,且Y是短周期
元素,原子序数大于O,因此Y为Mg元素,Z的单质晶体是广泛应用的半导体材料,所以Z为
Si元素,W与X同主族,且W是短周期元素,原子序数大于X,所以W为S元素。元素周期表
中,同族元素原子半径随核电荷数增加而增加,O位于第二周期,其他元素位于第三周期,因此
O的原子半径最小,同周期元素,核电荷数越大,原子半径越小,因此原子半径应为r(Mg)>r(Si)
>r(S)>r(O),A错误;X为O元素,Y为Mg元素,两者组成的化合物氧化镁为离子化合物,B
正确;Z为Si元素,W为S元素,因为S的非金属性强于Si,所以S的最高价氧化物对应水化物
的酸性强于Si的,C错误;W为S元素,X为O元素,因为O的非金属性强于S,所以O的气态
氢化物的热稳定性强于S的,D错误。