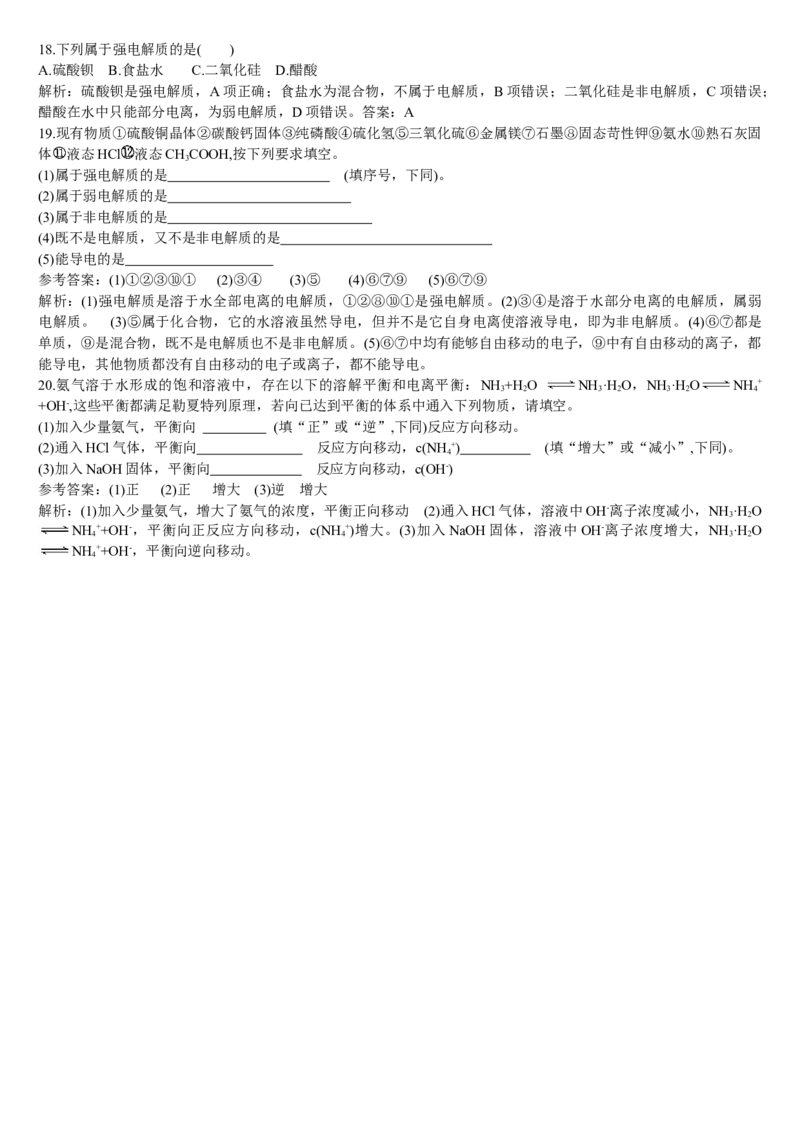文档内容
第一节 电离平衡基础练习题
1.下列物质的分类组合中全部正确的是 ( )
选项 强电解质 弱电解质 非电解质
A NaCl HF Cl
2
B NaHCO NH ·H O CCl
3 3 2 4
C Ba(OH) HCl Cu
2
D AgCl HS CHCOOH
2 3
2.下列叙述正确的是 ( )
A.强电解质的饱和溶液导电能力一定强
B.凡是能导电的物质都是电解质
C.强电解质在水溶液中的电离过程是不可逆的
D.强酸溶液的酸性一定强于弱酸溶液的酸性水
3.下列电离方程式中,书写正确的是 ( )
A.Ba(OH) Ba2++2OH-
2
B. HPO 3H++PO3-
3 4 4
C.HF=H++F-
D.NH·HO NH++OH-
3 2 4
4.在氨水中,NH ·H O的电离达到平衡的标志是( )
3 2
A.溶液显电中性
B.溶液中无氨水分子
C.OH-浓度保持不变
D.溶液中NH +和OH-共存
4
5.下列事实能说明醋酸是弱电解质的是( )
A.醋酸能使石蕊溶液变红
B.25℃时,0.1mol/L醋酸的pH约为3
C.向醋酸中加入氢氧化钠溶液,溶液pH增大
D.醋酸能与碳酸钙反应产生CO 气体
2
6.(双选)下列说法中正确的是( )
A.CO 溶于水能导电,但CO 不是电解质
2 2
B.KHSO 只有在电流作用下才能电离成K+、H+和SO 2-
4 4
C.强电解质溶液的导电能力不一定都强;弱电解质溶液的导电能力不一定都弱
D.AgCl难溶于水,所以AgCl是弱电解质;醋酸铅易溶于水,所以醋酸铅是强电解质
7.把0.05 mol NaOH固体分别加入100mL下列液体中,溶液的导电能力变化最小的是 ( )
A.自来水
B.0.5mol·L-1盐酸
C.0.5mol·L-1CHCOOH溶液
3
D.0.5mol·L-1KCl溶液
8.某浓度的氨水中存在下列平衡:NH ·H O NH ++OH-,如想减小NH +的浓度,而增大OH-的浓度,采取措施有效
3 2 4 4
的是( )
A.通入HCl
B.加入NH Cl固体
4
C.加入少量FeCl
3
D.加入少量NaOH
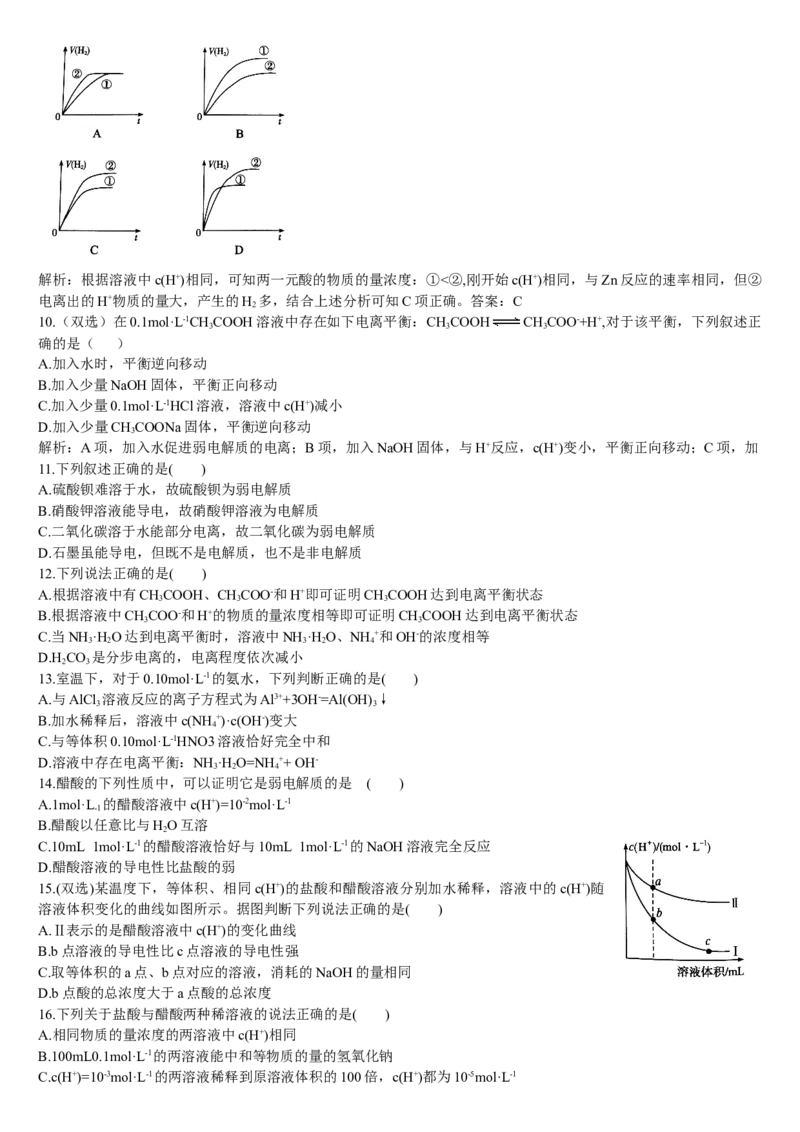
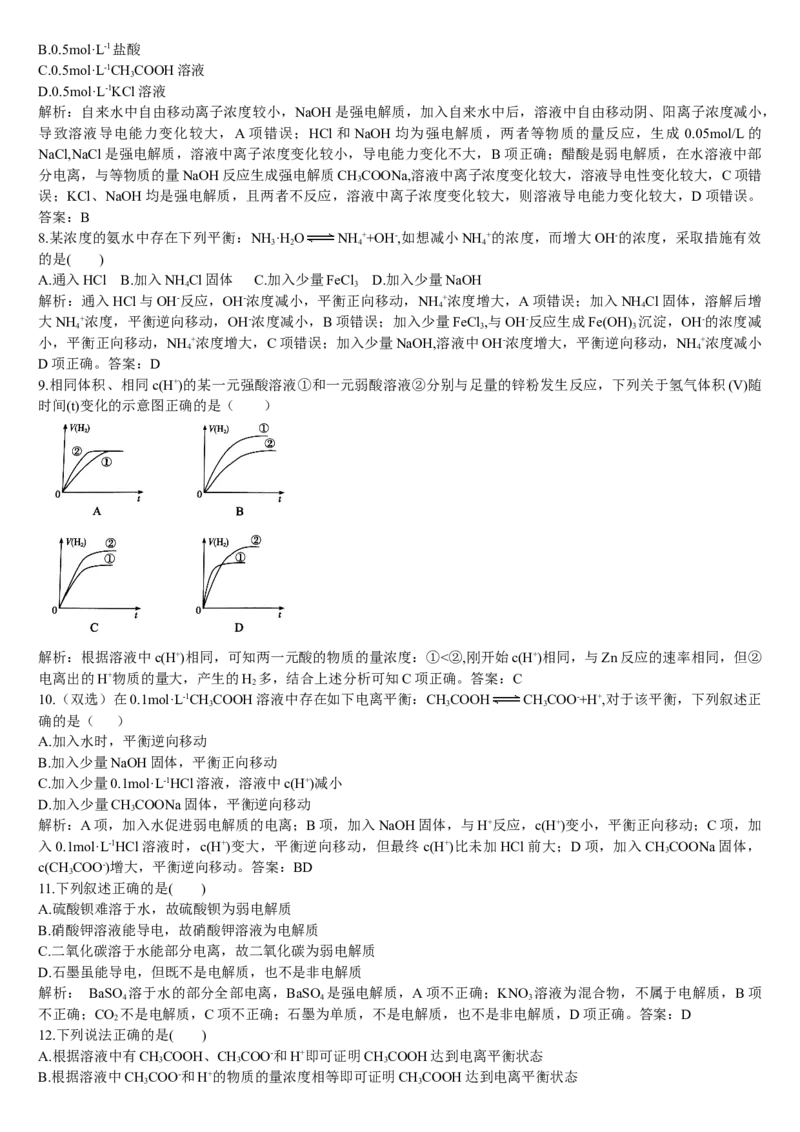
9.相同体积、相同c(H+)的某一元强酸溶液①和一元弱酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随
时间(t)变化的示意图正确的是( )解析:根据溶液中c(H+)相同,可知两一元酸的物质的量浓度:①<②,刚开始c(H+)相同,与Zn反应的速率相同,但②
电离出的H+物质的量大,产生的H 多,结合上述分析可知C项正确。答案:C
2
10.(双选)在0.1mol·L-1CHCOOH溶液中存在如下电离平衡:CHCOOH CHCOO-+H+,对于该平衡,下列叙述正
3 3 3
确的是( )
A.加入水时,平衡逆向移动
B.加入少量NaOH固体,平衡正向移动
C.加入少量0.1mol·L-1HCl溶液,溶液中c(H+)减小
D.加入少量CHCOONa固体,平衡逆向移动
3
解析:A项,加入水促进弱电解质的电离;B项,加入NaOH固体,与H+反应,c(H+)变小,平衡正向移动;C项,加
11.下列叙述正确的是( )
A.硫酸钡难溶于水,故硫酸钡为弱电解质
B.硝酸钾溶液能导电,故硝酸钾溶液为电解质
C.二氧化碳溶于水能部分电离,故二氧化碳为弱电解质
D.石墨虽能导电,但既不是电解质,也不是非电解质
12.下列说法正确的是( )
A.根据溶液中有CHCOOH、CHCOO-和H+即可证明CHCOOH达到电离平衡状态
3 3 3
B.根据溶液中CHCOO-和H+的物质的量浓度相等即可证明CHCOOH达到电离平衡状态
3 3
C.当NH ·H O达到电离平衡时,溶液中NH ·H O、NH +和OH-的浓度相等
3 2 3 2 4
D.HCO 是分步电离的,电离程度依次减小
2 3
13.室温下,对于0.10mol·L-1的氨水,下列判断正确的是( )
A.与AlCl 溶液反应的离子方程式为Al3++3OH-=Al(OH) ↓
3 3
B.加水稀释后,溶液中c(NH +)·c(OH-)变大
4
C.与等体积0.10mol·L-1HNO3溶液恰好完全中和
D.溶液中存在电离平衡:NH ·H O=NH ++ OH-
3 2 4
14.醋酸的下列性质中,可以证明它是弱电解质的是 ( )
A.1mol·L 的醋酸溶液中c(H+)=10-2mol·L-1
-1
B.醋酸以任意比与HO互溶
2
C.10mL 1mol·L-1的醋酸溶液恰好与10mL 1mol·L-1的NaOH溶液完全反应
D.醋酸溶液的导电性比盐酸的弱
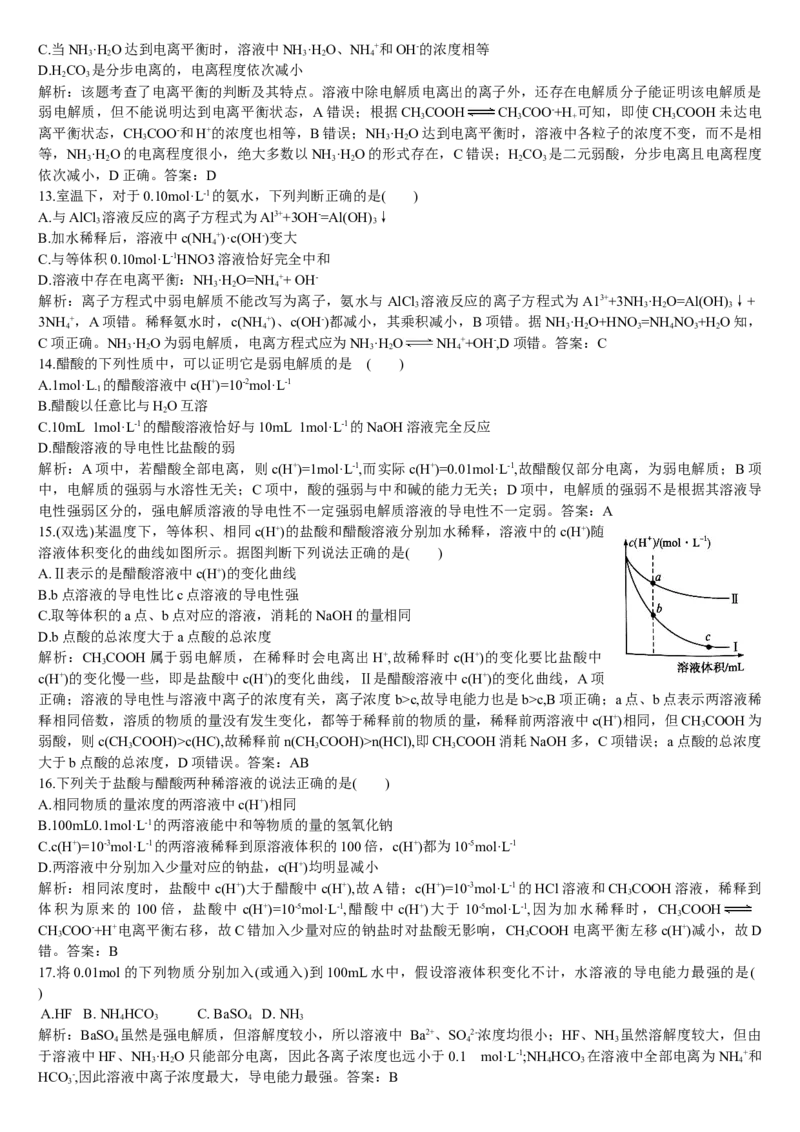
15.(双选)某温度下,等体积、相同c(H+)的盐酸和醋酸溶液分别加水稀释,溶液中的c(H+)随
溶液体积变化的曲线如图所示。据图判断下列说法正确的是( )
A.Ⅱ表示的是醋酸溶液中c(H+)的变化曲线
B.b点溶液的导电性比c点溶液的导电性强
C.取等体积的a点、b点对应的溶液,消耗的NaOH的量相同
D.b点酸的总浓度大于a点酸的总浓度
16.下列关于盐酸与醋酸两种稀溶液的说法正确的是( )
A.相同物质的量浓度的两溶液中c(H+)相同
B.100mL0.1mol·L-1的两溶液能中和等物质的量的氢氧化钠
C.c(H+)=10-3mol·L-1的两溶液稀释到原溶液体积的100倍,c(H+)都为10-5mol·L-1D.两溶液中分别加入少量对应的钠盐,c(H+)均明显减小
17.将0.01mol的下列物质分别加入(或通入)到100mL水中,假设溶液体积变化不计,水溶液的导电能力最强的是(
)
A.HF
B. NH HCO
4 3
C. BaSO
4
D. NH
3
18.下列属于强电解质的是( )
A.硫酸钡
B.食盐水
C.二氧化硅
D.醋酸
19.现有物质①硫酸铜晶体②碳酸钙固体③纯磷酸④硫化氢⑤三氧化硫⑥金属镁⑦石墨⑧固态苛性钾⑨氨水⑩熟石灰固
体 液态HCl 液态CHCOOH,按下列要求填空。
3
(1)属于强电解质的是 (填序号,下同)。
(2)属于弱电解质的是
(3)属于非电解质的是
(4)既不是电解质,又不是非电解质的是
(5)能导电的是
20.氨气溶于水形成的饱和溶液中,存在以下的溶解平衡和电离平衡:NH +H O NH ·H O,NH ·H O NH +
3 2 3 2 3 2 4
+OH-,这些平衡都满足勒夏特列原理,若向已达到平衡的体系中通入下列物质,请填空。
(1)加入少量氨气,平衡向 (填“正”或“逆”,下同)反应方向移动。
(2)通入HCl气体,平衡向 反应方向移动,c(NH +) (填“增大”或“减小”,下同)。
4
(3)加入NaOH固体,平衡向 反应方向移动,c(OH-)第一节 电离平衡基础练习题解析版
1.下列物质的分类组合中全部正确的是 ( )
选项 强电解质 弱电解质 非电解质
A NaCl HF Cl
2
B NaHCO NH ·H O CCl
3 3 2 4
C Ba(OH) HCl Cu
2
D AgCl HS CHCOOH
2 3
解析: Cl 、Cu均属于单质,既不是电解质也不是非电解质,且HCl为强电解质,A、C两项错误; NaHCO 在溶液
2 3
中完全电离为强电解质,NH ·H O部分电离为弱电解质,CCl 不能发生电离,属于非电解质,B项正确;CHCOOH
3 2 4 3
部分电离为弱电解质,D项错误。答案:B
2.下列叙述正确的是 ( )
A.强电解质的饱和溶液导电能力一定强
B.凡是能导电的物质都是电解质
C.强电解质在水溶液中的电离过程是不可逆的
D.强酸溶液的酸性一定强于弱酸溶液的酸性
解析:电解质溶液的导电能力与溶液中自由移动的离子浓度及所带电荷的多少有关,与电解质溶液的强弱无关,A项
错误;能导电的物质不一定是电解质,如石墨、金属单质等,B项错误;强电解质在溶液中完全电离,其电离过程是
不可逆的,C项正确;溶液的酸性强弱,主要看溶液中c(H+)的大小,与酸溶液的强弱无直接关系,D项错误。答案:
C
3.下列电离方程式中,书写正确的是 ( )
A.Ba(OH) Ba2++2OH- B. HPO 3H++PO3- C.HF=H++F- D.NH·HO NH++OH-
2 3 4 4 3 2 4
解析: Ba(OH) 为强电解质,在溶液中完全电离,即 Ba(OH) =Ba2++2OH-,A项错误;HPO 为弱电解质,在溶液中
2 2 3 4
部分电离,且以第一步为主,即HPO H++HPO -,B项错误;HF为弱酸,在溶液中部分电离即HF H++F-,C
3 4 2 4
项错误;NH ·H O为弱碱,在溶液中部分电离,即NH·HO NH++OH- ,D项正确。答案:D
3 2 3 2 4
4.在氨水中,NH ·H O的电离达到平衡的标志是( )
3 2
A.溶液显电中性 B.溶液中无氨水分子 C.OH-浓度保持不变 D.溶液中NH +和OH-共存
4
解析:任何溶液都呈电中性,据此不能判断是否达到平衡,A项错误;溶液中无氨水分子,可说明NH ·H O是强电解
3 2
质,B项错误;溶液中OH-保持不变,则溶液中NH ·H O和NH +均不变,即达到了电离平衡,C项正确;NH +和OH-
3 2 4 4
共存,只能说明NH ·H O发生了电离,但无法确定是否达到电离平衡,D项错误。答案:C
3 2
5.下列事实能说明醋酸是弱电解质的是( )
A.醋酸能使石蕊溶液变红
B.25℃时,0.1mol/L醋酸的pH约为3
C.向醋酸中加入氢氧化钠溶液,溶液pH增大
D.醋酸能与碳酸钙反应产生CO 气体
2
解析:使石蕊变红只能说明醋酸在溶液中已电离,但不能判断是否完全电离,A项错误0.1mol/L醋酸溶液pH约为3,
即c(H+)为0.001mol/L,说明醋酸未完全电离,属于弱电解质,B项正确;醋酸中加入NaOH溶液,因发生中和反应使
c(H+)减小,溶液pH增大,使醋酸电离程度完全,C项错误;与碳酸钙反应产生CO 气体,只可证明醋酸酸性强于碳
2
酸,但无法判断醋酸是否完全电离,D项错误。答案:B
6.(双选)下列说法中正确的是( )
A.CO 溶于水能导电,但CO 不是电解质
2 2
B.KHSO 只有在电流作用下才能电离成K+、H+和SO 2-
4 4
C.强电解质溶液的导电能力不一定都强;弱电解质溶液的导电能力不一定都弱
D.AgCl难溶于水,所以AgCl是弱电解质;醋酸铅易溶于水,所以醋酸铅是强电解质
解析:CO 溶于水能导电,说明碳酸是电解质,但 CO 属于非电解质,A项正确;KHSO 在水作用下能电离成K+、
2 2 4
H+和SO 2-,B项错误;电解质溶液导电能力与离子浓度和离子所带电荷等因素成正比,与电解质强弱无关,C项正确;
4
电解质强弱与溶解性无关,虽AgCl难溶于水,但属于强电解质;醋酸铅易溶于水,但属于弱电解质,D项错误。答
案:AC
7.把0.05 mol NaOH固体分别加入100mL下列液体中,溶液的导电能力变化最小的是 ( )
A.自来水B.0.5mol·L-1盐酸
C.0.5mol·L-1CHCOOH溶液
3
D.0.5mol·L-1KCl溶液
解析:自来水中自由移动离子浓度较小,NaOH是强电解质,加入自来水中后,溶液中自由移动阴、阳离子浓度减小,
导致溶液导电能力变化较大,A项错误;HCl和NaOH均为强电解质,两者等物质的量反应,生成 0.05mol/L的
NaCl,NaCl是强电解质,溶液中离子浓度变化较小,导电能力变化不大,B项正确;醋酸是弱电解质,在水溶液中部
分电离,与等物质的量NaOH反应生成强电解质CHCOONa,溶液中离子浓度变化较大,溶液导电性变化较大,C项错
3
误;KCl、NaOH均是强电解质,且两者不反应,溶液中离子浓度变化较大,则溶液导电能力变化较大,D项错误。
答案:B
8.某浓度的氨水中存在下列平衡:NH ·H O NH ++OH-,如想减小NH +的浓度,而增大OH-的浓度,采取措施有效
3 2 4 4
的是( )
A.通入HCl B.加入NH Cl固体 C.加入少量FeCl D.加入少量NaOH
4 3
解析:通入HCl与OH-反应,OH-浓度减小,平衡正向移动,NH +浓度增大,A项错误;加入NH Cl固体,溶解后增
4 4
大NH +浓度,平衡逆向移动,OH-浓度减小,B项错误;加入少量FeCl ,与OH-反应生成Fe(OH) 沉淀,OH-的浓度减
4 3 3
小,平衡正向移动,NH +浓度增大,C项错误;加入少量NaOH,溶液中OH-浓度增大,平衡逆向移动,NH +浓度减小
4 4
D项正确。答案:D
9.相同体积、相同c(H+)的某一元强酸溶液①和一元弱酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随
时间(t)变化的示意图正确的是( )
解析:根据溶液中c(H+)相同,可知两一元酸的物质的量浓度:①<②,刚开始c(H+)相同,与Zn反应的速率相同,但②
电离出的H+物质的量大,产生的H 多,结合上述分析可知C项正确。答案:C
2
10.(双选)在0.1mol·L-1CHCOOH溶液中存在如下电离平衡:CHCOOH CHCOO-+H+,对于该平衡,下列叙述正
3 3 3
确的是( )
A.加入水时,平衡逆向移动
B.加入少量NaOH固体,平衡正向移动
C.加入少量0.1mol·L-1HCl溶液,溶液中c(H+)减小
D.加入少量CHCOONa固体,平衡逆向移动
3
解析:A项,加入水促进弱电解质的电离;B项,加入NaOH固体,与H+反应,c(H+)变小,平衡正向移动;C项,加
入0.1mol·L-1HCl溶液时,c(H+)变大,平衡逆向移动,但最终c(H+)比未加HCl前大;D项,加入CHCOONa固体,
3
c(CHCOO-)增大,平衡逆向移动。答案:BD
3
11.下列叙述正确的是( )
A.硫酸钡难溶于水,故硫酸钡为弱电解质
B.硝酸钾溶液能导电,故硝酸钾溶液为电解质
C.二氧化碳溶于水能部分电离,故二氧化碳为弱电解质
D.石墨虽能导电,但既不是电解质,也不是非电解质
解析: BaSO 溶于水的部分全部电离,BaSO 是强电解质,A项不正确;KNO 溶液为混合物,不属于电解质,B项
4 4 3
不正确;CO 不是电解质,C项不正确;石墨为单质,不是电解质,也不是非电解质,D项正确。答案:D
2
12.下列说法正确的是( )
A.根据溶液中有CHCOOH、CHCOO-和H+即可证明CHCOOH达到电离平衡状态
3 3 3
B.根据溶液中CHCOO-和H+的物质的量浓度相等即可证明CHCOOH达到电离平衡状态
3 3C.当NH ·H O达到电离平衡时,溶液中NH ·H O、NH +和OH-的浓度相等
3 2 3 2 4
D.HCO 是分步电离的,电离程度依次减小
2 3
解析:该题考查了电离平衡的判断及其特点。溶液中除电解质电离出的离子外,还存在电解质分子能证明该电解质是
弱电解质,但不能说明达到电离平衡状态,A错误;根据CHCOOH CHCOO-+H 可知,即使CHCOOH未达电
3 3 + 3
离平衡状态,CHCOO-和H+的浓度也相等,B错误;NH ·H O达到电离平衡时,溶液中各粒子的浓度不变,而不是相
3 3 2
等,NH ·H O的电离程度很小,绝大多数以NH ·H O的形式存在,C错误;HCO 是二元弱酸,分步电离且电离程度
3 2 3 2 2 3
依次减小,D正确。答案:D
13.室温下,对于0.10mol·L-1的氨水,下列判断正确的是( )
A.与AlCl 溶液反应的离子方程式为Al3++3OH-=Al(OH) ↓
3 3
B.加水稀释后,溶液中c(NH +)·c(OH-)变大
4
C.与等体积0.10mol·L-1HNO3溶液恰好完全中和
D.溶液中存在电离平衡:NH ·H O=NH ++ OH-
3 2 4
解析:离子方程式中弱电解质不能改写为离子,氨水与 AlCl 溶液反应的离子方程式为A13++3NH·H O=Al(OH) ↓+
3 3 2 3
3NH +,A项错。稀释氨水时,c(NH +)、c(OH-)都减小,其乘积减小,B项错。据NH ·H O+HNO =NHNO +H O知,
4 4 3 2 3 4 3 2
C项正确。NH ·H O为弱电解质,电离方程式应为NH ·H O NH ++OH-,D项错。答案:C
3 2 3 2 4
14.醋酸的下列性质中,可以证明它是弱电解质的是 ( )
A.1mol·L 的醋酸溶液中c(H+)=10-2mol·L-1
-1
B.醋酸以任意比与HO互溶
2
C.10mL 1mol·L-1的醋酸溶液恰好与10mL 1mol·L-1的NaOH溶液完全反应
D.醋酸溶液的导电性比盐酸的弱
解析:A项中,若醋酸全部电离,则c(H+)=1mol·L-1,而实际c(H+)=0.01mol·L-1,故醋酸仅部分电离,为弱电解质;B项
中,电解质的强弱与水溶性无关;C项中,酸的强弱与中和碱的能力无关;D项中,电解质的强弱不是根据其溶液导
电性强弱区分的,强电解质溶液的导电性不一定强弱电解质溶液的导电性不一定弱。答案:A
15.(双选)某温度下,等体积、相同c(H+)的盐酸和醋酸溶液分别加水稀释,溶液中的c(H+)随
溶液体积变化的曲线如图所示。据图判断下列说法正确的是( )
A.Ⅱ表示的是醋酸溶液中c(H+)的变化曲线
B.b点溶液的导电性比c点溶液的导电性强
C.取等体积的a点、b点对应的溶液,消耗的NaOH的量相同
D.b点酸的总浓度大于a点酸的总浓度
解析:CHCOOH属于弱电解质,在稀释时会电离出H+,故稀释时c(H+)的变化要比盐酸中
3
c(H+)的变化慢一些,即是盐酸中c(H+)的变化曲线,Ⅱ是醋酸溶液中c(H+)的变化曲线,A项
正确;溶液的导电性与溶液中离子的浓度有关,离子浓度 b>c,故导电能力也是b>c,B项正确;a点、b点表示两溶液稀
释相同倍数,溶质的物质的量没有发生变化,都等于稀释前的物质的量,稀释前两溶液中c(H+)相同,但CHCOOH为
3
弱酸,则c(CHCOOH)>c(HC),故稀释前n(CHCOOH)>n(HCl),即CHCOOH消耗NaOH多,C项错误;a点酸的总浓度
3 3 3
大于b点酸的总浓度,D项错误。答案:AB
16.下列关于盐酸与醋酸两种稀溶液的说法正确的是( )
A.相同物质的量浓度的两溶液中c(H+)相同
B.100mL0.1mol·L-1的两溶液能中和等物质的量的氢氧化钠
C.c(H+)=10-3mol·L-1的两溶液稀释到原溶液体积的100倍,c(H+)都为10-5mol·L-1
D.两溶液中分别加入少量对应的钠盐,c(H+)均明显减小
解析:相同浓度时,盐酸中c(H+)大于醋酸中c(H+),故A错;c(H+)=10-3mol·L-1的HCl溶液和CHCOOH溶液,稀释到
3
体积为原来的 100 倍,盐酸中 c(H+)=10-5mol·L-1,醋酸中 c(H+)大于 10-5mol·L-1,因为加水稀释时,CHCOOH
3
CHCOO-+H+电离平衡右移,故C错加入少量对应的钠盐时对盐酸无影响,CHCOOH电离平衡左移c(H+)减小,故D
3 3
错。答案:B
17.将0.01mol的下列物质分别加入(或通入)到100mL水中,假设溶液体积变化不计,水溶液的导电能力最强的是(
)
A.HF B. NH HCO C. BaSO D. NH
4 3 4 3
解析:BaSO 虽然是强电解质,但溶解度较小,所以溶液中 Ba2+、SO 2-浓度均很小;HF、NH 虽然溶解度较大,但由
4 4 3
于溶液中HF、NH ·H O只能部分电离,因此各离子浓度也远小于0.1 mol·L-1;NHHCO 在溶液中全部电离为NH +和
3 2 4 3 4
HCO -,因此溶液中离子浓度最大,导电能力最强。答案:B
318.下列属于强电解质的是( )
A.硫酸钡 B.食盐水 C.二氧化硅 D.醋酸
解析:硫酸钡是强电解质,A项正确;食盐水为混合物,不属于电解质,B项错误;二氧化硅是非电解质,C项错误;
醋酸在水中只能部分电离,为弱电解质,D项错误。答案:A
19.现有物质①硫酸铜晶体②碳酸钙固体③纯磷酸④硫化氢⑤三氧化硫⑥金属镁⑦石墨⑧固态苛性钾⑨氨水⑩熟石灰固
体 液态HCl 液态CHCOOH,按下列要求填空。
3
(1)属于强电解质的是 (填序号,下同)。
(2)属于弱电解质的是
(3)属于非电解质的是
(4)既不是电解质,又不是非电解质的是
(5)能导电的是
参考答案:(1)①②③⑩① (2)③④ (3)⑤ (4)⑥⑦⑨ (5)⑥⑦⑨
解析:(1)强电解质是溶于水全部电离的电解质,①②⑧⑩①是强电解质。(2)③④是溶于水部分电离的电解质,属弱
电解质。 (3)⑤属于化合物,它的水溶液虽然导电,但并不是它自身电离使溶液导电,即为非电解质。(4)⑥⑦都是
单质,⑨是混合物,既不是电解质也不是非电解质。(5)⑥⑦中均有能够自由移动的电子,⑨中有自由移动的离子,都
能导电,其他物质都没有自由移动的电子或离子,都不能导电。
20.氨气溶于水形成的饱和溶液中,存在以下的溶解平衡和电离平衡:NH +H O NH ·H O,NH ·H O NH +
3 2 3 2 3 2 4
+OH-,这些平衡都满足勒夏特列原理,若向已达到平衡的体系中通入下列物质,请填空。
(1)加入少量氨气,平衡向 (填“正”或“逆”,下同)反应方向移动。
(2)通入HCl气体,平衡向 反应方向移动,c(NH +) (填“增大”或“减小”,下同)。
4
(3)加入NaOH固体,平衡向 反应方向移动,c(OH-)
参考答案:(1)正 (2)正 增大 (3)逆 增大
解析:(1)加入少量氨气,增大了氨气的浓度,平衡正向移动 (2)通入HCl气体,溶液中OH-离子浓度减小,NH ·H O
3 2
NH ++OH-,平衡向正反应方向移动,c(NH +)增大。(3)加入NaOH固体,溶液中OH-离子浓度增大,NH ·H O
4 4 3 2
NH ++OH-,平衡向逆向移动。
4