文档内容
专题 10 化学反应原理综合题
专项训练
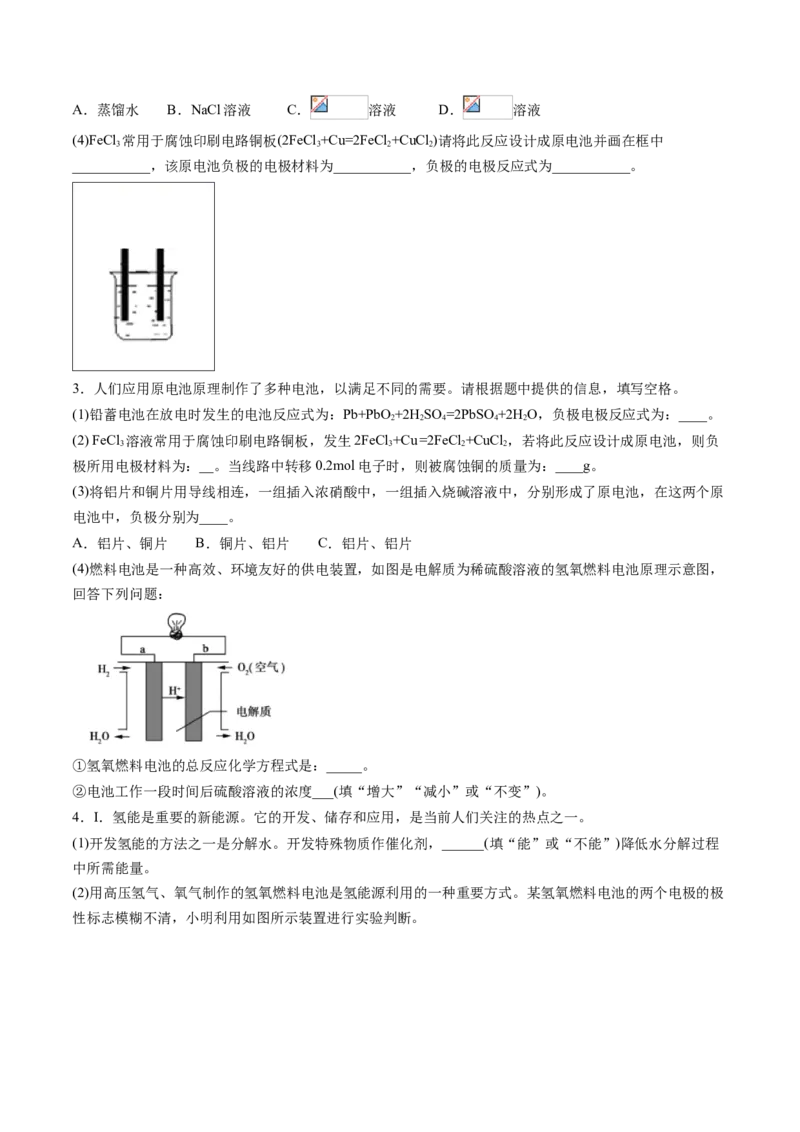
1.某温度时,在一个2L的密闭容器中,A、B、C三种气体物质的浓度随时间的变化曲线如图所示。
根据图中数据,试填写下列空白:
(1)该反应的化学方程式为_______;
(2)从开始至2min,B的平均反应速率为_______;平衡时,C的物质的量为_______;
(3)下列叙述能说明该反应已达到化学平衡状态的是_______(填序号);
A.A、B、C的物质的量之比为3:1:3
B.相同时间内消耗3molA,同时生成3molC
C.相同时间内消耗 ,同时消耗
D.混合气体的总质量不随时间的变化而变化
E.B的体积分数不再发生变化
(4)在某一时刻采取下列措施能使该反应速率减小的是_______(填序号)。
A.加催化剂
B.降低温度
C.容积不变,充入A
D.容积不变,从容器中分离出A
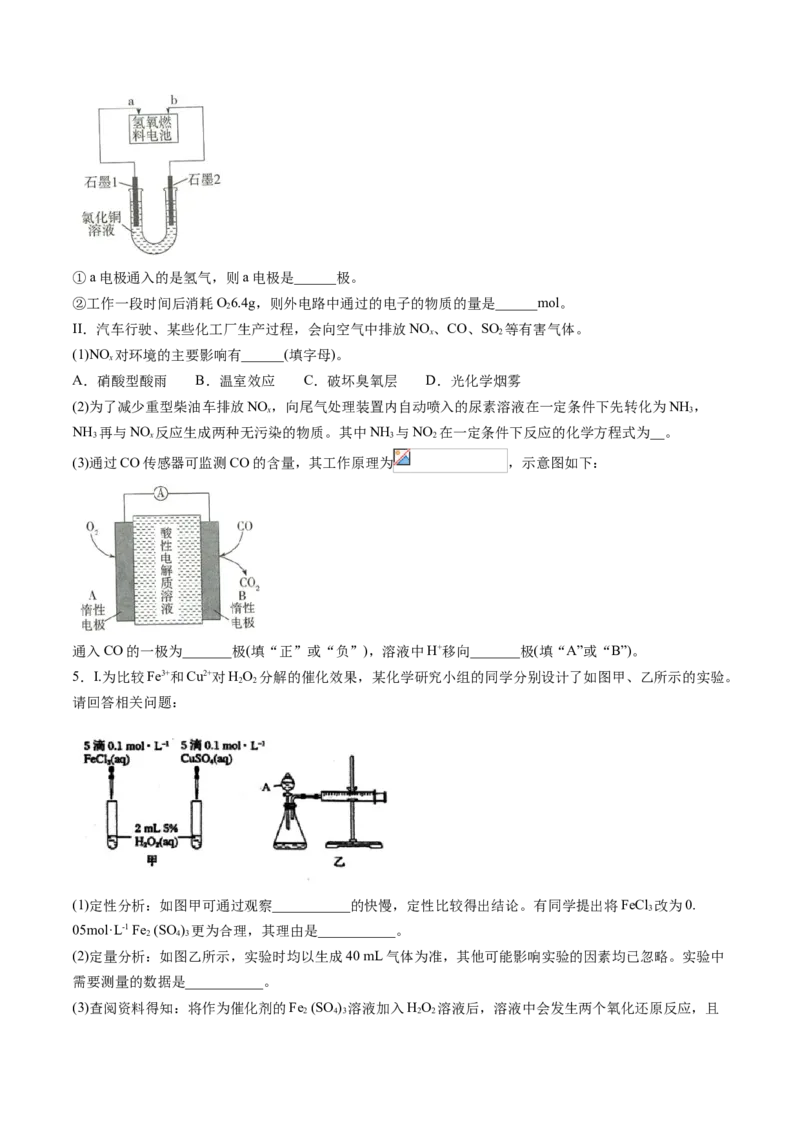
2.原电池是将化学能转化为电能的装置。如图,烧杯中是稀硫酸溶液
(1)当开关K断开时产生的现象为___________。
A.铜片不断溶解B.锌片不断溶解C.铜片上产生气泡D.锌片上产生气泡E.溶液逐渐变蓝
(2)闭合开关K,经过一段时间后,若导线中转移了0.4mol电子,则产生的气体在标况下的体积为
___________。
(3)如果反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,该同学在烧杯中分别加入等体积的下列
液体,你认为可行的是___________(填序号)。A.蒸馏水 B.NaCl溶液 C. 溶液 D. 溶液
(4)FeCl 常用于腐蚀印刷电路铜板(2FeCl +Cu=2FeCl +CuCl )请将此反应设计成原电池并画在框中
3 3 2 2
___________,该原电池负极的电极材料为___________,负极的电极反应式为___________。
3.人们应用原电池原理制作了多种电池,以满足不同的需要。请根据题中提供的信息,填写空格。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO+2H SO =2PbSO+2H O,负极电极反应式为:____。
2 2 4 4 2
(2) FeCl 溶液常用于腐蚀印刷电路铜板,发生2FeCl +Cu=2FeCl +CuCl ,若将此反应设计成原电池,则负
3 3 2 2
极所用电极材料为:__。当线路中转移0.2mol电子时,则被腐蚀铜的质量为:____g。
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原
电池中,负极分别为____。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
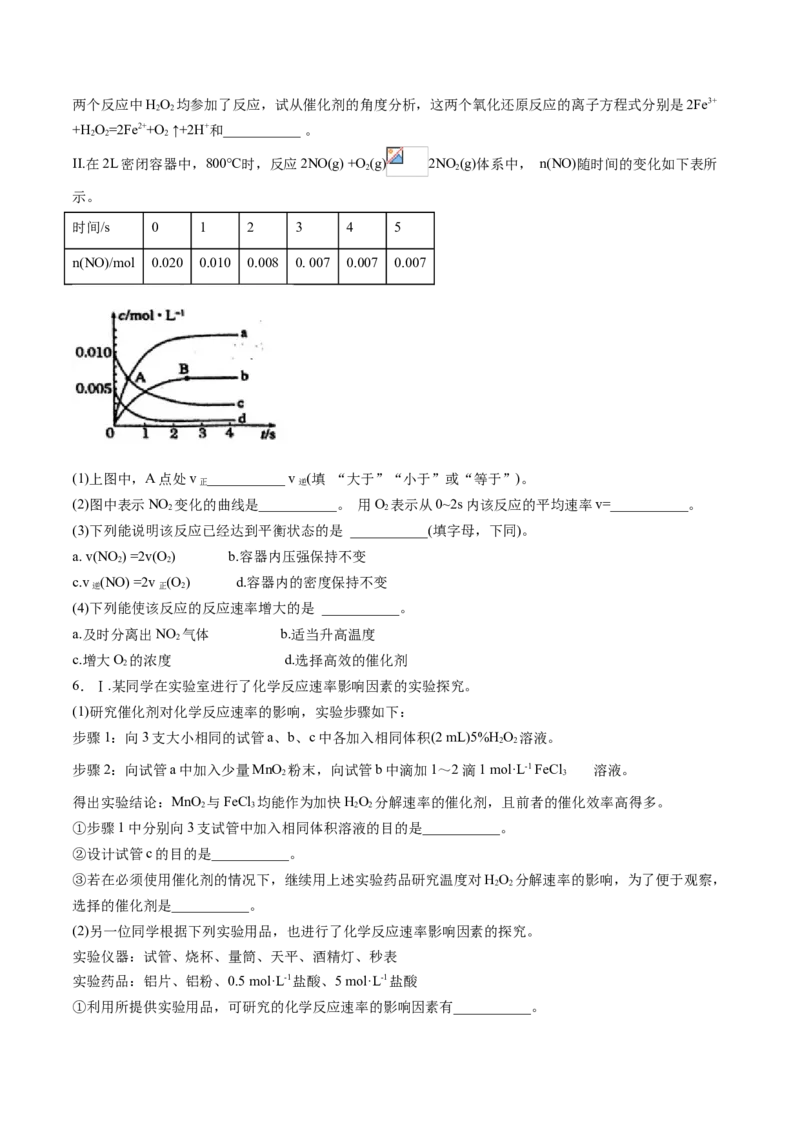
(4)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,
回答下列问题:
①氢氧燃料电池的总反应化学方程式是:_____。
②电池工作一段时间后硫酸溶液的浓度___(填“增大”“减小”或“不变”)。
4.I.氢能是重要的新能源。它的开发、储存和应用,是当前人们关注的热点之一。
(1)开发氢能的方法之一是分解水。开发特殊物质作催化剂,______(填“能”或“不能”)降低水分解过程
中所需能量。
(2)用高压氢气、氧气制作的氢氧燃料电池是氢能源利用的一种重要方式。某氢氧燃料电池的两个电极的极
性标志模糊不清,小明利用如图所示装置进行实验判断。①a电极通入的是氢气,则a电极是______极。
②工作一段时间后消耗O6.4g,则外电路中通过的电子的物质的量是______mol。
2
II.汽车行驶、某些化工厂生产过程,会向空气中排放NO、CO、SO 等有害气体。
x 2
(1)NO 对环境的主要影响有______(填字母)。
x
A.硝酸型酸雨 B.温室效应 C.破坏臭氧层 D.光化学烟雾
(2)为了减少重型柴油车排放NO,向尾气处理装置内自动喷入的尿素溶液在一定条件下先转化为NH ,
x 3
NH 再与NO 反应生成两种无污染的物质。其中NH 与NO 在一定条件下反应的化学方程式为__。
3 x 3 2
(3)通过CO传感器可监测CO的含量,其工作原理为 ,示意图如下:
通入CO的一极为_______极(填“正”或“负”),溶液中H+移向_______极(填“A”或“B”)。
5.I.为比较Fe3+和Cu2+对HO 分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。
2 2
请回答相关问题:
(1)定性分析:如图甲可通过观察___________的快慢,定性比较得出结论。有同学提出将FeCl 改为0.
3
05mol·L-1 Fe (SO) 更为合理,其理由是___________。
2 4 3
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中
需要测量的数据是___________。
(3)查阅资料得知:将作为催化剂的Fe (SO) 溶液加入HO 溶液后,溶液中会发生两个氧化还原反应,且
2 4 3 2 2两个反应中HO 均参加了反应,试从催化剂的角度分析,这两个氧化还原反应的离子方程式分别是2Fe3+
2 2
+H O=2Fe2++O ↑+2H+和___________ 。
2 2 2
II.在2L密闭容器中,800℃时,反应2NO(g) +O(g) 2NO (g)体系中, n(NO)随时间的变化如下表所
2 2
示。
时间/s 0 1 2 3 4 5
n(NO)/mol 0.020 0.010 0.008 0. 007 0.007 0.007
(1)上图中,A点处v ___________ v (填 “大于”“小于”或“等于”)。
正 逆
(2)图中表示NO 变化的曲线是___________。 用O 表示从0~2s内该反应的平均速率v=___________。
2 2
(3)下列能说明该反应已经达到平衡状态的是 ___________(填字母,下同)。
a. v(NO ) =2v(O ) b.容器内压强保持不变
2 2
c.v (NO) =2v (O ) d.容器内的密度保持不变
逆 正 2
(4)下列能使该反应的反应速率增大的是 ___________。
a.及时分离出NO 气体 b.适当升高温度
2
c.增大O 的浓度 d.选择高效的催化剂
2
6.Ⅰ.某同学在实验室进行了化学反应速率影响因素的实验探究。
(1)研究催化剂对化学反应速率的影响,实验步骤如下:
步骤1:向3支大小相同的试管a、b、c中各加入相同体积(2 mL)5%H O 溶液。
2 2
步骤2:向试管a中加入少量MnO 粉末,向试管b中滴加1~2 滴1 mol·L-1 FeCl 溶液。
2 3
得出实验结论:MnO 与FeCl 均能作为加快HO 分解速率的催化剂,且前者的催化效率高得多。
2 3 2 2
①步骤1中分别向3支试管中加入相同体积溶液的目的是___________。
②设计试管c的目的是___________。
③若在必须使用催化剂的情况下,继续用上述实验药品研究温度对HO 分解速率的影响,为了便于观察,
2 2
选择的催化剂是___________。
(2)另一位同学根据下列实验用品,也进行了化学反应速率影响因素的探究。
实验仪器:试管、烧杯、量筒、天平、酒精灯、秒表
实验药品:铝片、铝粉、0.5 mol·L-1盐酸、5 mol·L-1盐酸
①利用所提供实验用品,可研究的化学反应速率的影响因素有___________。②若要研究温度对化学反应速率的影响,还需用到的主要仪器是___________。
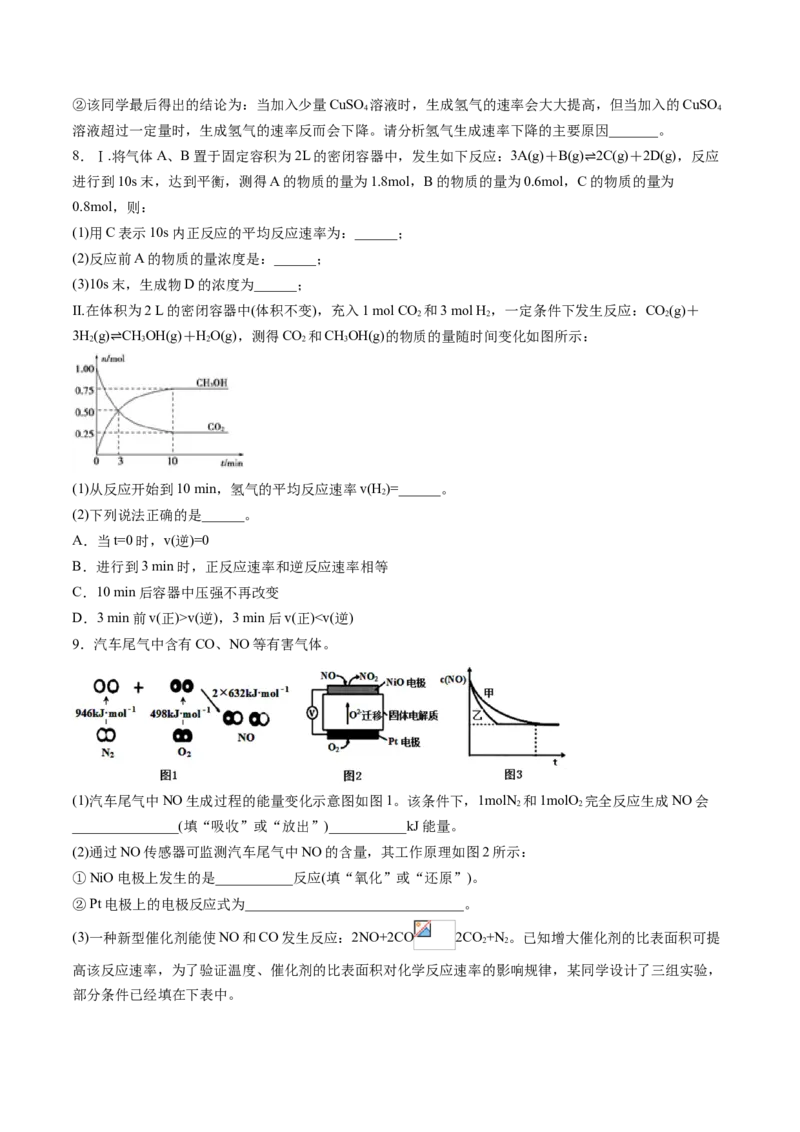
Ⅱ.某反应在体积为5 L的密闭容器中进行,0~3分钟各物质的物质的量的变化情况如图所示(A、B、C均为
气体)。
(1)该反应的化学方程式为___________。
(2)反应开始至2分钟时,B的平均反应速率为___________。
(3)在密闭容器里,通入a mol A(g)、b mol B(g)、c mol C(g),发生上述反应,当改变下列条件时,反应速率
会减小的是___________。
A.降低温度 B.加入催化剂 C.增大容器容积 D. 减小容器容积
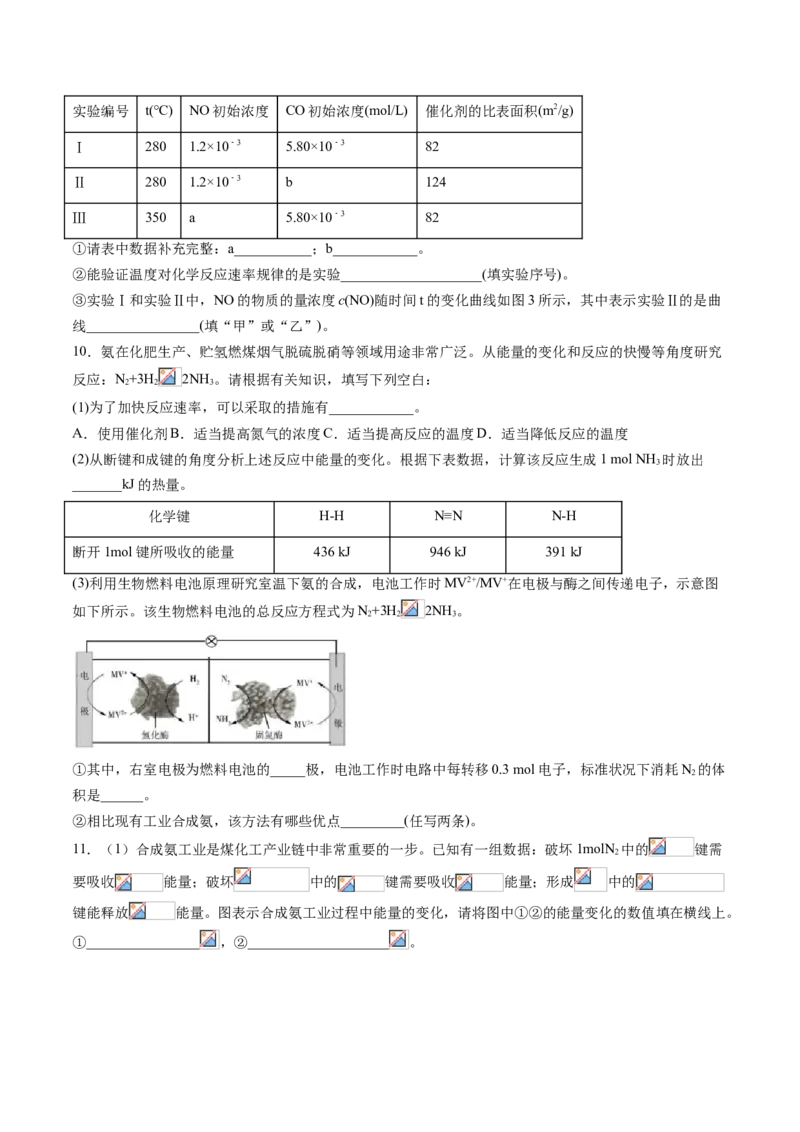
7.某反应在体积为5 L的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示(已知A、
B、C均为气体)。
(1)该反应的化学方程式为_______。
(2)反应开始至2 min时,B的平均反应速率为_______。
(3)能说明该反应已达到平衡状态的是_______。
A.υ(A)=2υ(B) B.容器内气体密度不变 C.υ (A)=υ (C) D.容器内温度保持恒定 E. 混合气体的平
逆 正
均相对分子质量不再改变的状态
(4)由图求得平衡时A的转化率为_______。
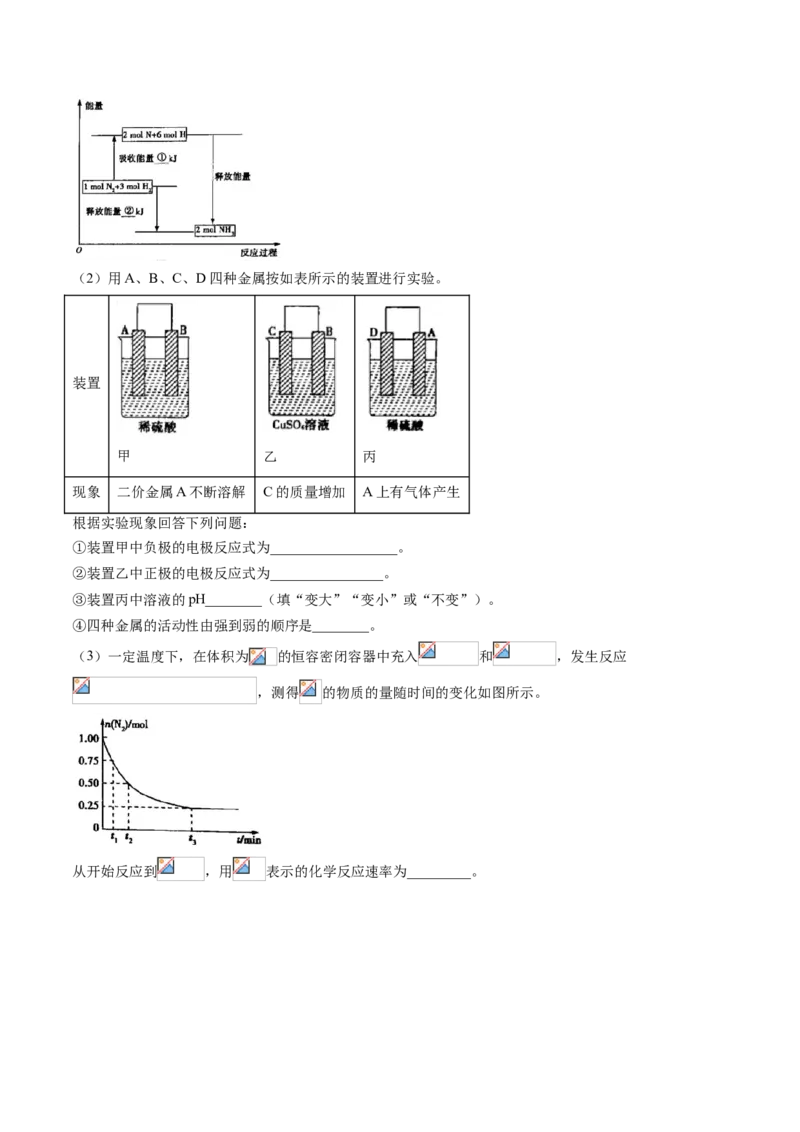
(5)为了研究硫酸铜的量对氢气生成速率的影响,某同学设计了如下一系列的实验:将表中所给的混合溶液
分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积的气体所需时间。
实验
A B C D E F
混合溶液
4 mol/L H SO (mL) 30 V V V V V
2 4 1 2 3 4 5
饱和CuSO 溶液(mL) 0 0.5 2.5 5 V 20
4 6
HO(mL) V V V V 10 0
2 7 8 9 10
①请完成此实验设计,其中:V=_______,V=_______。
1 6②该同学最后得出的结论为:当加入少量CuSO 溶液时,生成氢气的速率会大大提高,但当加入的CuSO
4 4
溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因_______。
8.Ⅰ.将气体A、B置于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g) 2C(g)+2D(g),反应
进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为
⇌
0.8mol,则:
(1)用C表示10s内正反应的平均反应速率为:______;
(2)反应前A的物质的量浓度是:______;
(3)10s末,生成物D的浓度为______;
Ⅱ.在体积为2 L的密闭容器中(体积不变),充入1 mol CO 和3 mol H ,一定条件下发生反应:CO(g)+
2 2 2
3H(g) CHOH(g)+HO(g),测得CO 和CHOH(g)的物质的量随时间变化如图所示:
2 3 2 2 3
⇌
(1)从反应开始到10 min,氢气的平均反应速率v(H )=______。
2
(2)下列说法正确的是______。
A.当t=0时,v(逆)=0
B.进行到3 min时,正反应速率和逆反应速率相等
C.10 min后容器中压强不再改变
D.3 min前v(正)>v(逆),3 min后v(正)