文档内容
2000 年上海高考化学真题及答案
第Ⅰ卷 (共66分)
考生注意:
第Ⅰ卷分三大题(第1-23小题),由机器阅郑,答案必须全部涂写在答题纸上,填涂
时用2B铅笔将选中项涂满涂黑。注意试题题号和答题纸上编号一一对应,答案需要
更改时,用塑料橡皮擦除干净。
相对原子质量 H-1 B-11 C-12 N-14 O-16 Na-23 Mg-24 Cl-35.5
Cu-64 Zn-65 Br-80 Ag-108
一、选择题(本题共16分),每小题2分,只有一个正确行项,答案涂写在答题纸上。
1.人体内所必需的下列元素中,因摄入量不足而导致骨质疏松的是
(A)K (B)Ca (C)Na (D)Fe
2.下列物质属于原子晶体的化合物是
(A)金刚石 (B)刚玉 (C)二氧化硅 (D)干冰
3.报道,某些建筑材料会产生放射性同位素氡222Rn,从而对人体产生伤害,该同位
86
素原子的中子数和质子数之差是
(A)136 (B)50 (C)86 (D)222
4.下列物质中,不属于合金的是
(A) 硬铝 (B)黄铜 (C) 钢铁 (D)水银
5.方法把固体物质加工到纳米级(1-100nm,1nm=10-9m)的超细粉末粒子,然后制得
纳米材料。下列分散系中的分散质的微粒直径和这种粒子具有相同数量级的是
A.溶液 B.悬浊液 C.胶体 D.乳浊液
6.有下列电子排布式的原子中,半径最大的是
A.ls22s22p63s23p? B.1s22s22p3
C.1s22s2sp2 D.1s22s22p63s23p4
7.列物质的水溶液能导电,但属于非电解质的是
A.CHCHCOOH B.Cl C.NHHCO D.SO
3 2 2 4 3 2
8.随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,
其首要原因是
A.利用电池外壳的金属材料
B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染
C.不使电池中渗泄的电解液腐蚀其他物品
D.回收其中石墨电极
二、选择题(本题共30分),每小题3分,只有一个正确选项,答案涂写在答题纸上。
9.下列实验操作中错误的是
A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
B.蒸馏时,应使温度计水银球靠近蒸烧瓶支管口
C.滴定时,大手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管
第1页 | 共11页中的液面
D.量时,称量物放在称量纸上,置于托盘天平的大盘,砝码放在托盘天平的右盘中
10.列反应的离子方程式错误的是
A.氯化铝溶液中加入过量的氨水 Al3++4NHHO→AlO+4NH+2HO
3 2 2 4 2
B.用氨水吸收过量的二氧化硫 NH·HO+SO→NH+HSO
3 2 2 4 3
C.碳酸钠溶液中加入过量的苯酚 OH+CO2→ O -+HCO
3 3
D.次氯酸钙溶液中通入过量的二氧化碳 ClO-+CO+HO→HCO+HclO
2 2 3
11.丁睛橡胶CHCH=CH-CHCHCH 具有优良的
2 2 2 n
耐油、耐高温性能,合成丁腈橡胶的原料是 CN
①CH=CH-CH=CH ②CH-C C-CH ③CH2=CH-CN
2 2 3 3
④CH-CH=CH ⑤CH-CH=CH ⑥CH-CH=CH-CH
3 3 2 3 3
│
CN
12.在外界提供相同电量的条件,Cu2+或Ag+分别按Cu2++2e→Cu或Ag++e→Ag在电极上
放电,基析出铜的质量为1.92g,则析出银的质量为
A.1.62g B.6.48g C.3.24g D.12.96g
13.维生素C的结构简式为HC-CC-OH,有关它的叙述错误的是
│ │
HO-CH-CH-CH C=O
2
│
HO O
A. 是一个环状的酯类化合物
B. 易起氧化及加成反应
C. 可以溶解于水
D. 在碱性溶液中能稳定地存在
14.水的电离过程为 HOH++OH-,在不同温度下其平衡常数为 K(25℃)=1.0×
2
10-14,K(35℃)=2.1×10-14。则下列叙述正确的是
A. C(H+)随着温度升高而降低
B. 在35℃时,C(H+)>C(OH-)
C. 水的电离度(25℃)>(35℃)
D. 水的电离是吸热的
15.由NaHPO 脱水形成聚磷酸盐Na HP O ,共脱去水分子的数目为
2 4 200 2 200 601
A.198个 B.199个 C.200个 D.201个
16.下列各组离子在溶液中能大量共存的是
A.Ca2+ 、HCO、Cl-、K+ B、Al3+、AlO、HCO、Na+
3 2 3
第2页 | 共11页C、Fe2+、NH、SO2、S2- D、Fe3+、SCN-、Na+、CO2
4 4 3
17.等物质的量浓度的下列溶液中,NH离子的浓度最大的是
4
A.NHCl B.NHHCO C.NHHSO D.NHNO
4 4 3 4 4 4 3
18.对下列事实的解释错误的是
A.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性
B.浓硝酸在光照下颜色变黄,说明浓硝酸不稳定
C.常温下,浓硝酸可以用铝?贮存,说明铝与浓硝酸不反应
D.反应CuSO+HS→CuS↓+HSO 能进行,说明硫化铜既不溶于水,也不溶于稀硫酸
4 2 2 4
三、选择题(本题共20分),每小题4分,每小题有一个或两个正确选项。只有一个
正确选项的,多选不给分;有两个正确选项的,选对一个给2分,选错一个该小题
不给分,答案涂写在答题纸上。
19.对于反应2SO+O 2SO,下列判断正确的是
2 2 3
A.体积2SO 和足量O 反应,必定生成2体积SO
2 2 3
B.其他条件不变,增大压强,平衡必定向右移动
C.平衡时,SO 消耗速度必定等于O 生成速度的两倍
2 2
D.平衡时,SO 浓度必定等于O 浓度的两倍
2 2
20.下列变化规律中正确的是
A.HS、HCl、PH 热稳定性由弱到强
2 3
B.物质的量浓度相等的NaCl、MgCl、AlCl 三种溶液的pH值由小到大
2 3
C.等质量的甲烷、乙稀、乙炔充分燃烧,所耗用氧气的量由多到少
D.CHCHOH、—OH、CHCOOH的酸性由弱到强
3 2 3
21.氯只有35Cl和37Cl两各稳定同位素,它们在氯气中的原子数之比35Cl:37Cl为3:
1。则分子量为70、72、74的氯气分子数之比可能是
A.5:2:1 B.5:2:2 C.9:3:1 D.9:3:2
22.取pH值均等于2的盐酸和醒酸各100ml分别稀释2倍后,再分别加入0.03g锌粉,
在相同条件下充分反应,有关叙述正确的是
A.醋酸与锌反应放出氢气多
B.盐酸和醋酸分别与锌反应放出的氢气一样多
C.醋酸与锌反应速率大
D.盐酸和醋分别与锌反应的速度一样大
23.铜和镁的合金4.6g完全溶于浓硝酸,若反应中硝酸被还原只产生4480mL的NO
2
气体和336mL的NO 气体(都已折算到标准状况),在反应后的溶液中,加入足量的
2 4
氢氧化钠溶液,生成沉淀的质量为
A.9.02g B.8.51g C.8.26g D.7.04g
2000年全国普通高等学校招生统一考试
上海 化学试卷
第3页 | 共11页第Ⅱ卷(共84分)
考生注意
第Ⅱ卷(第24-33小题),请按题目要求笔答在本试卷上。
四、(本题共28分)
24.KClO 和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯。其变化可个
3
表述为:
⑴请完成该化学方程式并配平(未知物化学和系数填入框内)
⑵浓盐酸在反应中显示出来的性质是_______(填写编号,多选倒扣)。
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
⑶产生0.1molCl,则转移的电子的物质的是为_________mol.
2
⑷ClO 具有很强的氧化性。因此,常被用作消毒剂,其消毒的效率(以单位质量
2
得到的电子数表示)是Cl 的_______倍。
2
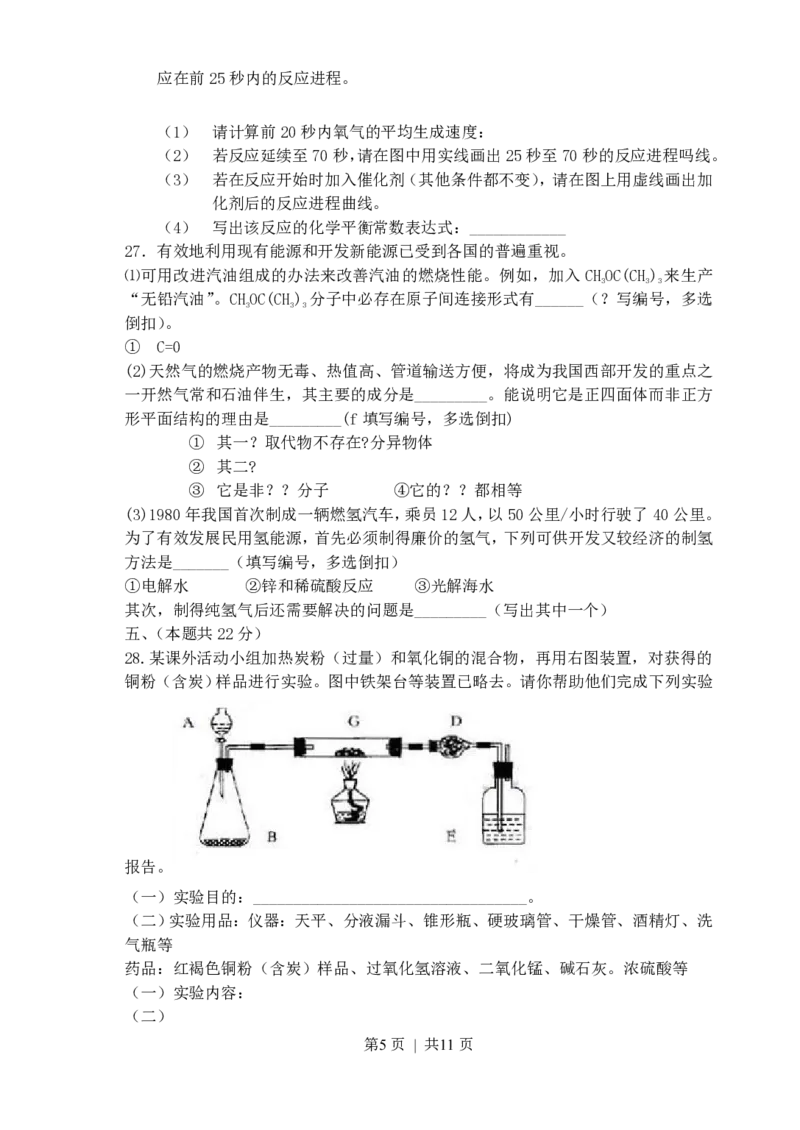
25.不同元素的气态原子失去最外层一个电子所需要的能量(设其为E)如右图
所示。试根据元素在周期表中的位置,分析
图中吗线的变化特点,并回答下列问题。
⑴同主族内不同元素的E值变化的特点是:
__________________________.
各主族中E值的这种变化特点体现了元素
性质的__________变化规律。
(2)同周期内,随原子序数增大,E 值增
大。但个别元素的E 值出现反常现试预测
下列关系式中正确的是______(填写编号,
多选倒扣)
①E(砷)>E(硒) ②E(砷)E(硒) ④E(溴)