文档内容
第一单元 物质及其变化
第三节 氧化还原反应(二)
一、基础巩固
1.下列反应中,氧化产物与还原产物为同一种物质的是( )
A.SO +2H S═3S↓+H O
2 2 2
B.2Na O +2H O═4NaOH+O ↑
2 2 2 2
C.HCl+NaOH═NaCl+H O
2
D.Zn+2HCl═ZnCl +H ↑
2 2
2.海洋是资源的宝库,下列生产过程中不涉及氧化还原反应的是( )
A.海水晒盐 B.电解饱和食盐水
C.海带提碘 D.用氯气制漂粉精
3.下列变化中,气体被氧化的是( )
A.C H 通入酸性KMnO 溶液
2 2 4
B.Cl 通入KBr溶液
2
C.H S通入CuSO 溶液
2 4
D.NH 通入AlCl 溶液
3 3
4.反应Cu+2H SO (浓) CuSO +SO ↑+2H O中,还原产物是( )
2 4 4 2 2
A.Cu B.H SO C.CuSO D.SO
2 4 4 2
5.下列氧化还原反应中,氧化剂和还原剂是同一种物质的是( )
A.2Na O +2CO ═2Na CO +O
2 2 2 2 3 2
B.SO +2H S═3S+2H O
2 2 2
C.Cl +2NaI═2NaCl+I
2 2
D.3Mg+N Mg N
2 3 2
6.向CuSO 溶液中加入H O 溶液,很快有大量气体逸出,同时放热,一段时间后,蓝色溶液变为红色浑
4 2 2
浊(Cu O),继续加入H O 溶液,红色浑浊又变为蓝色溶液,这个反应可以反复多次。下列关于上述过
2 2 2
程的说法不正确的是( )
A.Cu2+将H O 还原为O
2 2 2
B.H O 既表现氧化性又表现还原性
2 2
C.Cu2+是H O 分解反应的催化剂
2 2
D.发生了反应Cu O+H O +4H+═2Cu2++3H O
2 2 2 2
7.科学家发现,食用虾类等水生甲壳类动物的同时服用维生素 C容易中毒。这是因为对人体无害的+5价
砷类化合物在维生素C的作用下,能够转化为有毒的+3价的含砷化合物。通过以上信息填空:
①维生素C具有 (填“氧化性”或“还原性”)。
②3mol+5价砷完全转化为+3价砷,共转移 个电子。
二、拓展提升
8.标出下列氧化还原反应的电子转移数目和方向,并写出氧化剂
(1)2K S+K SO +3H SO ═3K SO +3S↓+3H O 氧化剂: ;
2 2 3 2 4 2 4 2
(2)2KMnO +5H O +3H SO ═K SO +2MnSO +5O ↑+8H O 氧化剂: 。
4 2 2 2 4 2 4 4 2 2
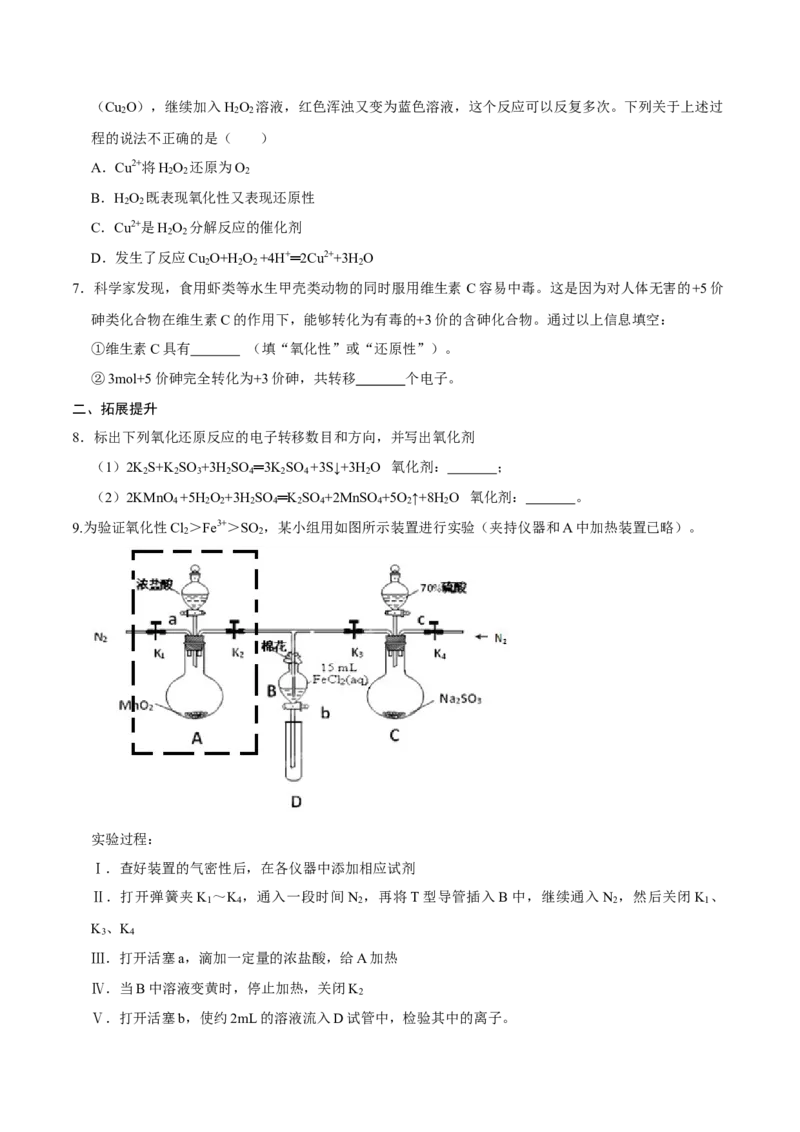
9.为验证氧化性Cl >Fe3+>SO ,某小组用如图所示装置进行实验(夹持仪器和A中加热装置已略)。
2 2
实验过程:
Ⅰ.查好装置的气密性后,在各仪器中添加相应试剂
Ⅱ.打开弹簧夹K ~K ,通入一段时间N ,再将T型导管插入B中,继续通入N ,然后关闭K 、
1 4 2 2 1
K 、K
3 4
Ⅲ.打开活塞a,滴加一定量的浓盐酸,给A加热
Ⅳ.当B中溶液变黄时,停止加热,关闭K
2
Ⅴ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。Ⅵ.打开K 和活塞c,加入70%的硫酸,一段时间后关闭K
3 3
Ⅶ.更换试管D,重复过程V,检验B溶液中的离子
(1)检验虚线框内装置气密性的操作是 。
(2)B棉花中浸润的溶液为 。实验Ⅱ通入N 的作用是 。
2
(3)C中发生反应的化学方程式 。
(4)用70%的硫酸制取SO ,反应速率比用98%的硫酸快,原因是 。
2
(5)若将制取的SO 通入酸性高锰酸钾溶液可使溶液褪色,其离子方程式为 。
2
(6)甲、乙、丙三位同学分别完成了上述实验,结论如表所示。他们的检测结果一定能够证明氧化性
Cl >Fe3+>SO 的是 (填“甲”“乙”“丙”)。
2 2
氢氧化物 Fe(OH) Fe(OH) Cd(OH) Mn(OH)
2 3 2 2
开始沉淀的pH 6.5 1.5 7.2 8.2
沉淀完全的pH 9.9 3.3 9.5 10.6
10.取一定量的酸性硫酸锰(MnSO )溶液,向其中依次加入下列物质,对应现象如表所示:
4
步骤1 步骤2 步骤3
依次加入 适量NaBiO 过量的H O 溶液 适量KI﹣淀粉混合液
3 2 2
实验现象 溶液呈紫红色 紫红色消失,产生气 现象A
泡
已知:
①金属铋(Bi),价态为+3 时较稳定
②铋酸钠(NaBiO )无色,难溶于水,高锰酸根(MnO )呈紫红色
3 4
③I 遇到淀粉溶液变成蓝色
2
(1)步骤 1 氧化产物为 (填序号:①Bi3+②MnO4 )。
(2)补充步骤 2 中的离子反应方程式并配平:
MnO ﹣+ H O + H+= Mn2++ H O+
4 2 2 2
(3)步骤 2 中过量的 H O 可以氧化 KI,则步骤 3 现象 A 为: 。
2 2
(4)由上述现象可以补充下列粒子氧化性由强到弱的顺序为:NaBiO > > >I (填序
3 2
号:①H O ②MnO )。
2 2 4
(5)根据上述结论,推断下列离子反应可能发生且书写正确的是(不定项选择) 。
A.Bi3++H O +H O═BiO ﹣+4H+
2 2 2 3
B.NaBiO +2I﹣+6H+═Na++I +Bi3++3H O
3 2 2
C.5I +2Mn2++16OH﹣═2MnO +10I+8H O
2 4 2D.H O +2I﹣+2H+═I +2H O
2 2 2 2